文档内容
景胜学校 2023-2024 学年度第一学期高三月考(10 月)
化学试题(B 卷) 2023.10
一、选择题(共16题,每题3分,共48分)
1.工业上冶炼金属钠通常采用的方法是( )
A.热分解法 B.电解法 C.结晶法 D.热还原法
2.下列化学反应中电子转移的表示方法正确的是
A. B.
C.
D.
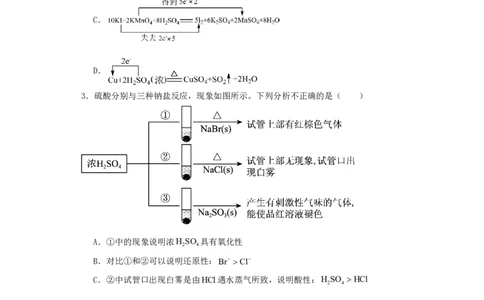
3.硫酸分别与三种钠盐反应,现象如图所示。下列分析不正确的是( )
A.①中的现象说明浓H SO 具有氧化性
2 4
B.对比①和②可以说明还原性:Br Cl
C.②中试管口出现白雾是由HCl遇水蒸气所致,说明酸性:H SO HCl
2 4
D.③中浓H SO 表现酸性
2 4
4.将Mg、Al组成的mg混合物投入一定量稀盐酸中,固体完全溶解,收集到气体为
1.12L(标准状况),向反应后溶液中加入2mol/LNaOH溶液100mL时,金属离子恰好沉
淀完全,则形成沉淀的质量为( )
A.(m+1.7)g B.(m+3.4)g C.(m+5.1)g D.(m+6.8)g
5.下列实验操作与现象及相关结论都正确的是( )
选
实验操作及现象 结论
项
常温下将铁片分别插入稀硝酸和浓硝酸中,前者产生无色气体, 浓硝酸的氧化
A
后者产生红棕色气体 性比稀硝酸强
试卷第1页,共6页
{#{QQABKQQAogggAhBAAQhCQwkACgEQkAECACoGgBAIMAAAQQNABAA=}#}X一定具有强氧
B 向溶有SO 的BaCl 溶液中通入气体X,出现白色沉淀
2 2 化性
溴与苯发生了
C 向溴水中加入苯,振荡后静置,水层颜色变浅
加成反应
将银和AgNO 溶液与铜和Na SO 溶液组成原电池,连通后银 Cu的金属性比
D 3 2 4
Ag强
表面有银白色金属沉积,铜电极附近溶液逐渐变蓝
A.A B.B C.C D.D
6.Na、Mg、Ca、Al是常用作冶炼金属的还原剂,如:工业冶炼金属钾的反应原理是
高温
①NaKCl KNaCl,工业冶炼金属铷的反应原理是
高温
②2RbClCa CaCl 2Rb,下列说法不正确的是( )
2
A.铝作还原剂冶炼金属的反应称之为铝热反应
B.该冶炼方法属于热还原法
C.①反应无法说明钠元素的金属性强于钾元素
D.①反应中可以选KCl水溶液
7.已知反应:①Cl+2KBr=2KCl+Br,②KClO+6HCl=3Cl↑+KCl+3HO,
2 2 3 2 2
③2KBrO+Cl=Br+2KClO,下列说法正确的是( )
3 2 2 3
A.上述三个反应都有单质生成,所以都是置换反应
B.氧化性由强到弱顺序为 KBrO>KClO>Cl>Br
3 3 2 2
C.反应②中氧化剂与还原剂的物质的量之比为1:6
D.③中 1 mol 还原剂反应,则氧化剂得到电子的物质的量为 2 mol
8.实验室以含锌废液(主要成分为ZnSO ,还含有少量的Fe2、Mn2,溶液pH5)
4
为原料制备ZnCO 的实验流程如图甲所示,S O2具有强氧化性,易被还原为SO2,
3 2 8 4
S O2的结构如图乙所示。下列说法正确的是( )
2 8
A.“除锰”反应的离子方程式为S O2Mn2 2H O2SO2MnO 4H
2 8 2 4 2
B.“除锰”反应中每消耗1molS O2,硫元素共得到2mol电子
2 8
C.试剂X可以选用Zn、ZnO等物质
D.滤液中一定大量存在阳离子有Na、NH和Zn2
4
9.在200g8%的NaOH溶液中通入一定量的CO 后,再向溶液中逐滴滴加稀盐酸至150mL
2
时开始产生气体,继续滴加稀盐酸到200mL时,气体质量最大(假设CO 全部逸出)。溶
2
试卷第2页,共6页
{#{QQABKQQAogggAhBAAQhCQwkACgEQkAECACoGgBAIMAAAQQNABAA=}#}液中产生CO 的质量与加入稀盐酸的体积如图所示。下列说法正确的是( )
2
A.B点时所得溶液的溶质为NaHCO B.AB段发生的反应只有CO2-+H+=HCO-
3 3 3
C.最初通入的CO 的物质的量为0.2mol D.加入盐酸的物质的量浓度为2mol·L-1
2
10.下列离子反应方程式正确的是( )
A.将少量SO 通入NaClO溶液:SO+3ClO-+HO=SO2+Cl-+2HClO
2 2 2 4
B.少量Mg(HCO) 溶液与NaOH溶液混合:Mg2++2HCO+2OH-=MgCO↓+2HO+CO2
3 2 3 3 2 3
C.常温下,pH=5的溶液中FeSO 可将KMnO 还原为MnO:3Fe2++MnO+4H+=3Fe3++MnO
4 4 2 4 2
↓+2HO
2
电解
D.用铜电极电解饱和食盐水:2Cl-+2HO Cl↑+H↑+2OH-
2 2 2
11.常温下,下列各组离子在指定溶液中可能大量共存的是( )
c
OH-
A.在 =11012的溶液中:HCO、K、Na、SO2
c H+ 3 4
B.含有大量Fe3+的溶液中:Na、OH、Br、K
C.pH0的溶液中:Na+、K+、SO2-、S O2-
4 2 3
K
D.在
c
OH
w
-
11012molL1 的溶液中:Na、Ba2、Cl、Br
12.设N 表示阿伏加 德罗常数的值,下列说法错误的是
A
A.标准状况下,22.4 L环丙烷和丙烯的混合气体中所含共用电子对数为9N
A
B.56g铁在足量氧气中完全燃烧,转移的电子数小于3N
A
C.16g O 和14CH 的混合物中所含中子数为8N
2 2 4 A
D.常温下,1 L 0.5 mol/L CHCOONH 溶液的pH=7,则溶液中CHCOO-与NH+的数
3 4 3 4
目均为0.5N
A
13.下列离子方程式书写正确的是
A.碳酸钡和稀硫酸反应:BaCO+2H+=Ba2++CO↑+HO
3 2 2
B.CO 通入足量的NaOH溶液:CO+OH-=HCO-
2 2 3
C.向FeCl 溶液中通入Cl 反应生成FeCl 溶液:Fe2++Cl=Fe3++2Cl-
2 2 3 2
D.少量CO 通入澄清石灰水:CO+Ca2++2OH-=CaCO↓+HO
2 2 3 2
14.将含O 和CH 的混合气体充入装有23.4gNaO 的密闭容器中点燃,反应结束后,容
2 4 2 2
器温度为150℃,压强为0pa,将残留物溶于水无气体逸出。下列叙述正确的是( )
A.原混合气体中O 和CH 的体积比为2:1
2 4
B.原混合气体中O 和CH 的体积比为1:2
2 4
试卷第3页,共6页
{#{QQABKQQAogggAhBAAQhCQwkACgEQkAECACoGgBAIMAAAQQNABAA=}#}C.残留固体中有NaCO 和NaO、NaOH D.残留固体中只有NaCO
2 3 2 2 2 3
15.W、X、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Z是非金属元
素,W、X的最高价氧化物对应的水化物可以相互反应生成盐和水,向一定量的W的最
高价氧化物对应的水化物溶液中逐滴加入XZ 溶液,生成的沉淀X(OH) 的质量随XZ 溶
3 3 3
液加入量的变化关系如图所示。则下列离子组在对应的溶液中一定能大量共存的是
A.d点对应的溶液中:K+、NH+、CO2-、I-
4 3
B.c点对应的溶液中:Ag+、Ca2+、NO-、Na+
3
C.b点对应的溶液中:Na+、S2-、SO2-、Cl-
4
D.a点对应的溶液中:Na+、K+、S02-、HCO-
4 3
16.将等物质的量的镁和铝混合,取等质量该混合物四份,分别加
到足量的下列溶液中,充分反应后,放出氢气最多的是( )
A.4 mol·L-1 HNO B.3 mol·L-1HCl C.8 mol·L-1 NaOH D.18mol·L-1HSO
3 2 4
二、填空题(5个大题,共52分)
17.(10分)氮、磷、硫、氯等非金属元素的单质和化合物在工农业生产中有 重要应
用。回答下列问题:
(1)在微生物作用下, 蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO),
2
反应的化学方程式为 。某厂废液中含有 2%5% 的 NaNO , 直接排放会造
2
成污染, 下列试 剂能使 NaNO 转化为 N 的是 (填标号)。
2 2
A. NaCl B.NHCl C. HNO D. 浓硫酸
4 3
(2)H PO 及正盐 NaH PO 均可将溶液中的 Ag还原为银, 从而可用于化学镀银。
3 2 2 2
①H PO 为 元酸(填“一”二”或“三”)。
3 2
②利用 H PO 进行化学镀银, 反应中氧化剂与还原剂的物质的量 之比为 4:1, 则
3 2
氧化产物为 (填化学式)。
(3)硫代硫酸钠晶体(NaSO·5HO), 又名大苏打、海波, 是一种用 途非常广泛的化
2 2 3 2
学试剂, 遇酸立即分解, 生成淡黄色沉淀, 放出的气 体能使品红溶液褪色, 试写
出硫代硫酸钠溶液与稀硫酸反应的离子方程式: 。
(4)氯气与氢氧化钠在 70℃时反应, 生成物中NaClO 和NaClO的物质的量之比为3:1,
3
其离子方程式为 。
18.(10分)(1)含有相同碳原子数的CO和CO,其质量比为 。同温同压下,
2
同质量的CO和CO,它们的密度之比为 。
2
(2)一定质量的Al(SO) 中含有2.7gAl3+,含有 个SO2-;溶于水得100mL
2 4 3 4
溶液,所得溶液的物质的量浓度为 mol·L-1。
(3)已知agA和bgB恰好完全反应生成0.2molC和dgD,则C的摩尔质量为 。
(4)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、SO2-,测得Na+、Mg2+和Cl-的物质的量
4
浓度依次为0.2mol·L-1、0.25mol·L-1、0.4mol·L-1,则c(SO2-)= 。
4
19.(8分)As和P属于同主族元素,中国自古就有“信口雌黄”“雄黄入药”之说。雌
黄(AsS)和雄黄(AsS)早期都曾用作绘画颜料,又都因有抗病毒疗效而用来入药。在一
2 3 4 4
定条件下, 雌黄和雄黄的转化关系如图所示。
试卷第4页,共6页
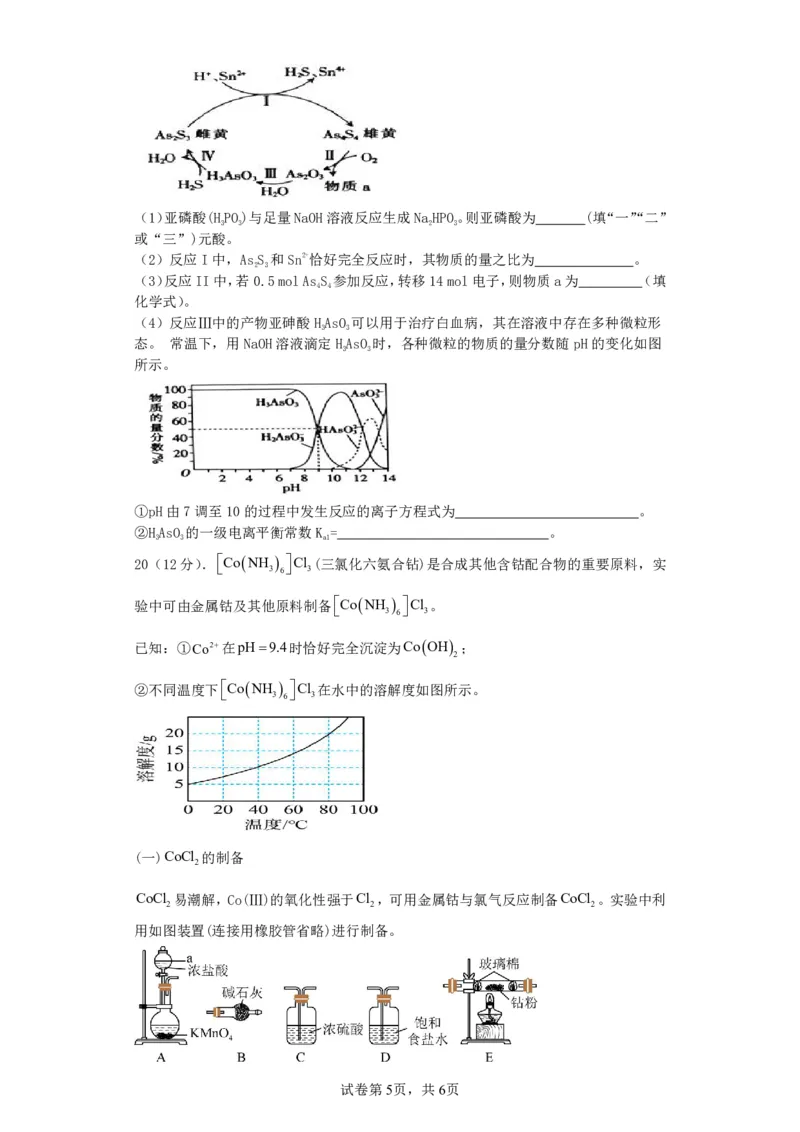
{#{QQABKQQAogggAhBAAQhCQwkACgEQkAECACoGgBAIMAAAQQNABAA=}#}(1)亚磷酸(HPO)与足量NaOH溶液反应生成NaHPO。则亚磷酸为 (填“一”“二”
3 3 2 3
或“三”)元酸。
(2)反应I中,AsS 和Sn2+恰好完全反应时,其物质的量之比为 。
2 3
(3)反应II中,若0.5molAsS 参加反应,转移14mol电子,则物质a为 (填
4 4
化学式)。
(4)反应Ⅲ中的产物亚砷酸HAsO 可以用于治疗白血病,其在溶液中存在多种微粒形
3 3
态。 常温下,用NaOH溶液滴定HAsO 时,各种微粒的物质的量分数随pH的变化如图
3 3
所示。
①pH由7调至10的过程中发生反应的离子方程式为 。
②HAsO 的一级电离平衡常数K = 。
3 3 a1
20(12分).CoNH Cl (三氯化六氨合钻)是合成其他含钴配合物的重要原料,实
3 6 3
验中可由金属钴及其他原料制备CoNH Cl 。
3 6 3
已知:①Co2在pH9.4时恰好完全沉淀为CoOH ;
2
②不同温度下CoNH Cl 在水中的溶解度如图所示。
3 6 3
(一)CoCl 的制备
2
CoCl 易潮解,Co(Ⅲ)的氧化性强于Cl ,可用金属钴与氯气反应制备CoCl 。实验中利
2 2 2
用如图装置(连接用橡胶管省略)进行制备。
试卷第5页,共6页
{#{QQABKQQAogggAhBAAQhCQwkACgEQkAECACoGgBAIMAAAQQNABAA=}#}(1)用图中的装置组合制备CoCl ,连接顺序为 (填标号)。装置B的作用
2
是 。
(2)装置A中发生反应的离子方程式为 。
(二)CoNH Cl 的制备
3 6 3
步骤如下:
Ⅰ.在100mL锥形瓶内加入4.5g研细的CoCl ,3gNH Cl和5mL水,加热溶解后加入
2 4
0.3g活性炭作催化剂。
Ⅱ.冷却后,加入浓氨水混合均匀。控制温度在10℃以下,并缓慢加入10mLH O 溶液。
2 2
Ⅲ.在60℃下反应一段时间后,经过________、________、过滤、洗涤、干燥等操作,
得到CoNH Cl 晶体。
3 6 3
根据以上步骤,回答下列问题:
(3)在步骤Ⅱ加入浓氨水前,需在步骤Ⅰ中加入NH Cl的原因之一是利用NH Cl溶于水
4 4
电离出NH,使NH H O的电离平衡逆向移动,请解释另一原因: 。
4 3 2
(4)步骤Ⅱ中在加入H O 溶液时,控制温度在10℃以下并缓慢加入的目的是控制反应
2 2
速率同时 。
(5)制备CoNH Cl 的总反应的化学方程式为 。
3 6 3
(6)步骤Ⅲ中的操作名称为 、 。
21.(12分)由黄铜矿(主要成分为CuFeS)炼制精铜以及从电解精炼铜的阳极泥(含有
2
TeO、少量Au、Ag等金属及其他化合物)中回收碲的一种工艺流程如图所示:
2
已知:①冰铜也叫铜锍,主要由硫化亚铜和硫化亚铁互相熔解而成的。
②TeO 是两性氧化物,微溶于水,可溶于强酸或强碱;
2
③阳极泥中的少量金属及其他化合物不与碱液反应。
(1)为加快黄铜矿的焙烧速率,可采取的措施为 (任写一种)。
(2)黄铜矿砂焙烧除渣过程中发生反应的化学方程式为 。
(3)在粗铜的电解过程中,粗铜应作 (填“阴极”或“阳极”),阴极的电极
反应式为 。
(4)“碱浸”时,TeO 发生反应的离子方程式为 。
2
(5)阳极泥中含有TeO,经过“碱浸”和 “过滤”后,向溶液中滴加稀HSO 调节pH,
2 2 4
又重新生成TeO,这个过程的目的是 ;如果HSO 过量,将导致碲的回收率
2 2 4
(填“偏高”“偏低”或“无影响”)。防止局部酸度过大的操作方法是 。
(6)向TeO 中加入HCl溶解后,再向溶液中通入SO 即可得到碲。通入SO 时发生反应的
2 2 2
化学方程式为 。
试卷第6页,共6页
{#{QQABKQQAogggAhBAAQhCQwkACgEQkAECACoGgBAIMAAAQQNABAA=}#}答案第1页,共1页
{#{QQABKQQAogggAhBAAQhCQwkACgEQkAECACoGgBAIMAAAQQNABAA=}#}