文档内容
专题26 硫及其化合物
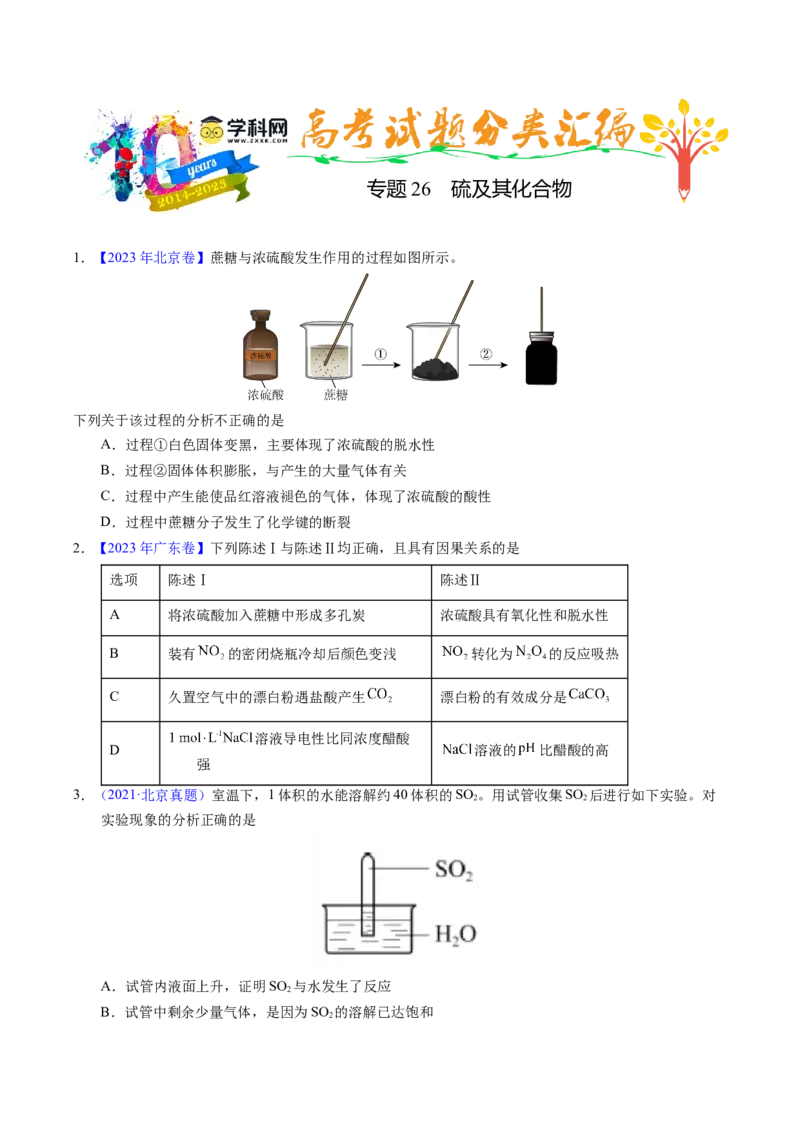
1.【2023年北京卷】蔗糖与浓硫酸发生作用的过程如图所示。
下列关于该过程的分析不正确的是
A.过程①白色固体变黑,主要体现了浓硫酸的脱水性
B.过程②固体体积膨胀,与产生的大量气体有关
C.过程中产生能使品红溶液褪色的气体,体现了浓硫酸的酸性
D.过程中蔗糖分子发生了化学键的断裂
2.【2023年广东卷】下列陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是
选项 陈述Ⅰ 陈述Ⅱ
A 将浓硫酸加入蔗糖中形成多孔炭 浓硫酸具有氧化性和脱水性
B 装有 的密闭烧瓶冷却后颜色变浅 转化为 的反应吸热
C 久置空气中的漂白粉遇盐酸产生 漂白粉的有效成分是
溶液导电性比同浓度醋酸
D 溶液的 比醋酸的高
强
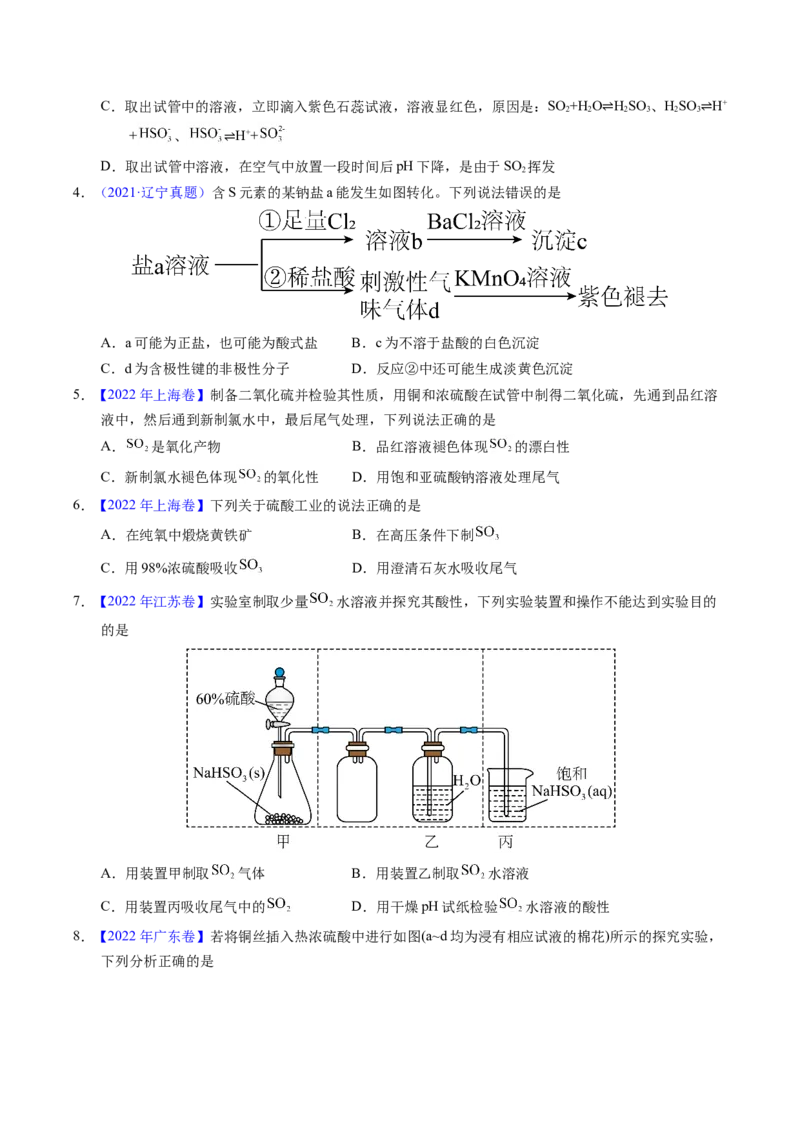
3.(2021·北京真题)室温下,1体积的水能溶解约40体积的SO 。用试管收集SO 后进行如下实验。对
2 2
实验现象的分析正确的是
A.试管内液面上升,证明SO 与水发生了反应
2
B.试管中剩余少量气体,是因为SO 的溶解已达饱和
2C.取出试管中的溶液,立即滴入紫色石蕊试液,溶液显红色,原因是:SO +H O HSO 、HSO H+
2 2 2 3 2 3
+ 、 H++ ⇌ ⇌
D.取出试管中溶液⇌,在空气中放置一段时间后pH下降,是由于SO 挥发
2
4.(2021·辽宁真题)含S元素的某钠盐a能发生如图转化。下列说法错误的是
A.a可能为正盐,也可能为酸式盐 B.c为不溶于盐酸的白色沉淀
C.d为含极性键的非极性分子 D.反应②中还可能生成淡黄色沉淀
5.【2022年上海卷】制备二氧化硫并检验其性质,用铜和浓硫酸在试管中制得二氧化硫,先通到品红溶
液中,然后通到新制氯水中,最后尾气处理,下列说法正确的是
A. 是氧化产物 B.品红溶液褪色体现 的漂白性
C.新制氯水褪色体现 的氧化性 D.用饱和亚硫酸钠溶液处理尾气
6.【2022年上海卷】下列关于硫酸工业的说法正确的是
A.在纯氧中煅烧黄铁矿 B.在高压条件下制
C.用98%浓硫酸吸收 D.用澄清石灰水吸收尾气
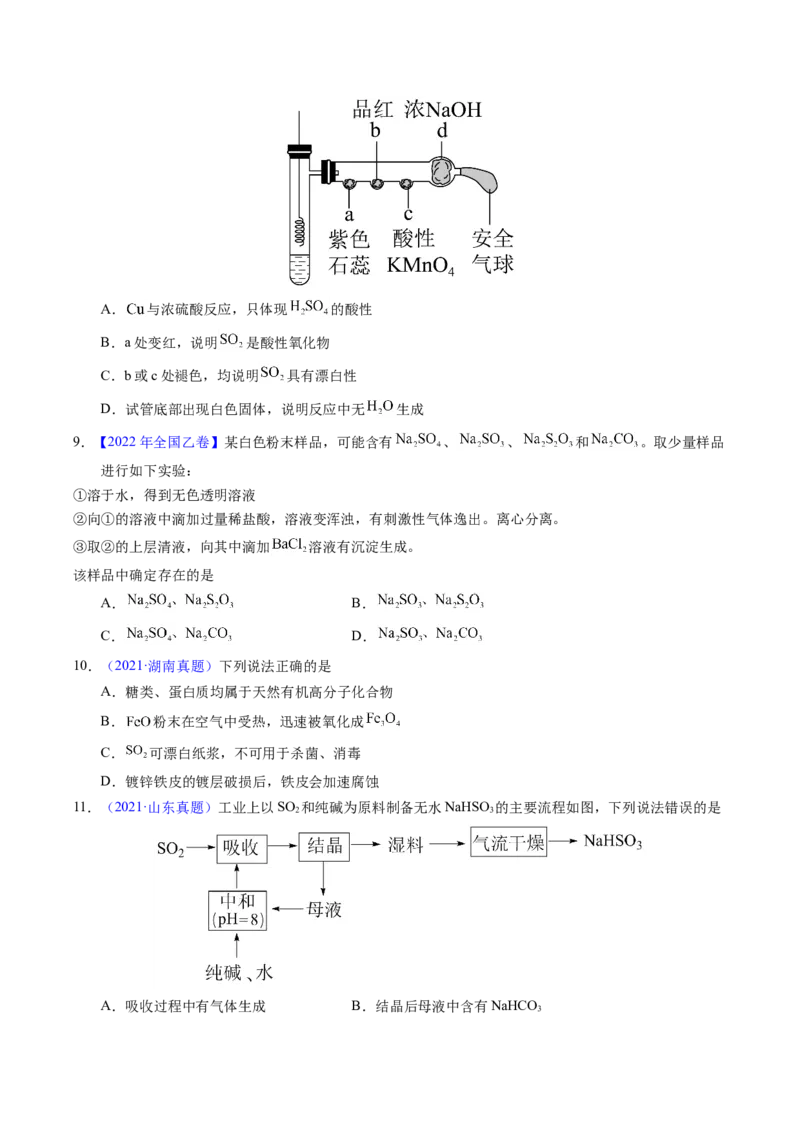
7.【2022年江苏卷】实验室制取少量 水溶液并探究其酸性,下列实验装置和操作不能达到实验目的
的是
A.用装置甲制取 气体 B.用装置乙制取 水溶液
C.用装置丙吸收尾气中的 D.用干燥pH试纸检验 水溶液的酸性
8.【2022年广东卷】若将铜丝插入热浓硫酸中进行如图(a~d均为浸有相应试液的棉花)所示的探究实验,
下列分析正确的是A. 与浓硫酸反应,只体现 的酸性
B.a处变红,说明 是酸性氧化物
C.b或c处褪色,均说明 具有漂白性
D.试管底部出现白色固体,说明反应中无 生成
9.【2022年全国乙卷】某白色粉末样品,可能含有 、 、 和 。取少量样品
进行如下实验:
①溶于水,得到无色透明溶液
②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体逸出。离心分离。
③取②的上层清液,向其中滴加 溶液有沉淀生成。
该样品中确定存在的是
A. B.
C. D.
10.(2021·湖南真题)下列说法正确的是
A.糖类、蛋白质均属于天然有机高分子化合物
B. 粉末在空气中受热,迅速被氧化成
C. 可漂白纸浆,不可用于杀菌、消毒
D.镀锌铁皮的镀层破损后,铁皮会加速腐蚀
11.(2021·山东真题)工业上以SO 和纯碱为原料制备无水NaHSO 的主要流程如图,下列说法错误的是
2 3
A.吸收过程中有气体生成 B.结晶后母液中含有NaHCO
3C.气流干燥湿料时温度不宜过高 D.中和后溶液中含NaSO 和NaHCO
2 3 3
12.(2017·江苏高考真题)下列制取SO 、验证其漂白性、收集并进行尾气处理的装置和原理能达到实验
2
目的的是( )
A.制取SO B.验证漂白性 C.收集SO D.尾气处理
2 2
13.(2017·全国高考真题)化学与生活密切相关。下列说法错误的是( )
A.PM2.5是指粒径不大于2.5 μm的可吸入悬浮颗粒物
B.绿色化学要求从源头上消除或减少生产活动对环境的污染
C.燃煤中加入CaO可以减少酸雨的形成及温室气体的排放
D.天然气和液化石油气是我国目前推广使用的清洁燃料
14.(2017·海南高考真题)分别将足量下列气体通入稀NaS溶液中,可以使溶液变浑浊的是
2
A.CO B.SO C.HCl D.CO
2 2
15.(2018·浙江高考真题)下列反应中能产生二氧化硫的是
A.氧化铜和稀硫酸反应 B.亚硫酸钠和氧气反应
C.三氧化硫和水反应 D.铜和热的浓硫酸反应
16.(2020·北京高考真题)硫酸盐(含SO 、HSO )气溶胶是PM 的成分之一。近期科研人员提出了雾
2.5
霾微颗粒中硫酸盐生成的转化机理,其主要过程示意图如图:
下列说法不正确的是
A.该过程有HO参与 B.NO 是生成硫酸盐的氧化剂
2 2
C.硫酸盐气溶胶呈酸性 D.该过程没有生成硫氧键
17.(2020·天津高考真题)检验下列物所选用的试剂正确的是待检验物质 所用试剂
A 海水中的碘元素 淀粉溶液
B SO 气体 澄清石灰水
2
C 溶液中的Cu2+ 氨水
D 溶液中的 NaOH溶液,湿润的蓝色石蕊试纸
18.(2015·上海高考真题)二氧化硫能使溴水褪色,说明二氧化硫具有( )
A.还原性 B.氧化性 C.漂白性 D.酸性
19.(2015·上海高考真题)与氢硫酸反应有沉淀生成的电解质是( )
A.硫酸铜 B.氢氧化钠 C.硫酸亚铁 D.二氧化硫
20.(2018·上海高考真题)关于硫酸工业中的催化氧化反应,叙述正确的是( )
A.是吸热反应 B.在常压下进行
C.在沸腾炉中进行 D.使用铁触媒作催化剂
21.(2018·上海高考真题)下列转化不能通过一步反应实现的是( )
A.HS+O→SO
2 2 2
B.SO +H O→H SO
2 2 2 3
C.S+O→SO
2 3
D.SO +H O→H SO
3 2 2 4
22.(2018·上海高考真题)下列变化说明浓硫酸具有脱水性的是( )
A.铁遇浓硫酸发生钝化 B.蔗糖遇浓硫酸变黑
C.加热时碳与浓硫酸反应 D.加热时铜与浓硫酸反应
23.(2020·浙江高考真题)100%硫酸吸收 可生成焦硫酸(分子式为 或 )。下
列说法不正确的是( )
A.焦硫酸具有强氧化性
B. 水溶液呈中性
C. 可与碱性氧化物反应生成新盐
D.100%硫酸吸收 生成焦硫酸的变化是化学变化
24.(2019·上海高考真题)能证明亚硫酸钠样品部分变质的试剂是
A.硝酸钡,稀硫酸 B.稀盐酸,氯化钡
C.稀硫酸,氯化钡 D.稀硝酸,氯化钡
25.(2019·海南高考真题)我国古代典籍中有“石胆……浅碧色,烧之变白色者真”的记载,其中石胆是
指( )
A. B.C. D.
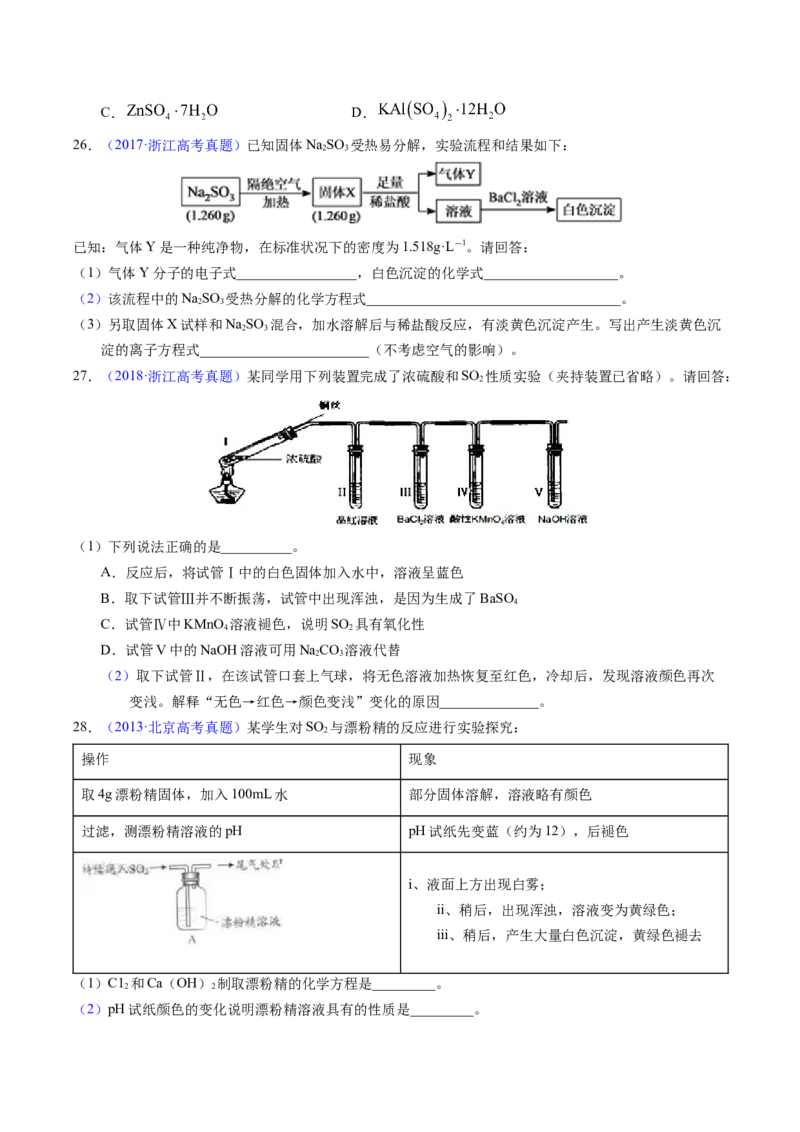
26.(2017·浙江高考真题)已知固体NaSO 受热易分解,实验流程和结果如下:
2 3
已知:气体Y是一种纯净物,在标准状况下的密度为1.518g·L-1。请回答:
(1)气体Y分子的电子式_________________,白色沉淀的化学式___________________。
(2)该流程中的NaSO 受热分解的化学方程式____________________________________。
2 3
(3)另取固体X试样和NaSO 混合,加水溶解后与稀盐酸反应,有淡黄色沉淀产生。写出产生淡黄色沉
2 3
淀的离子方程式________________________(不考虑空气的影响)。
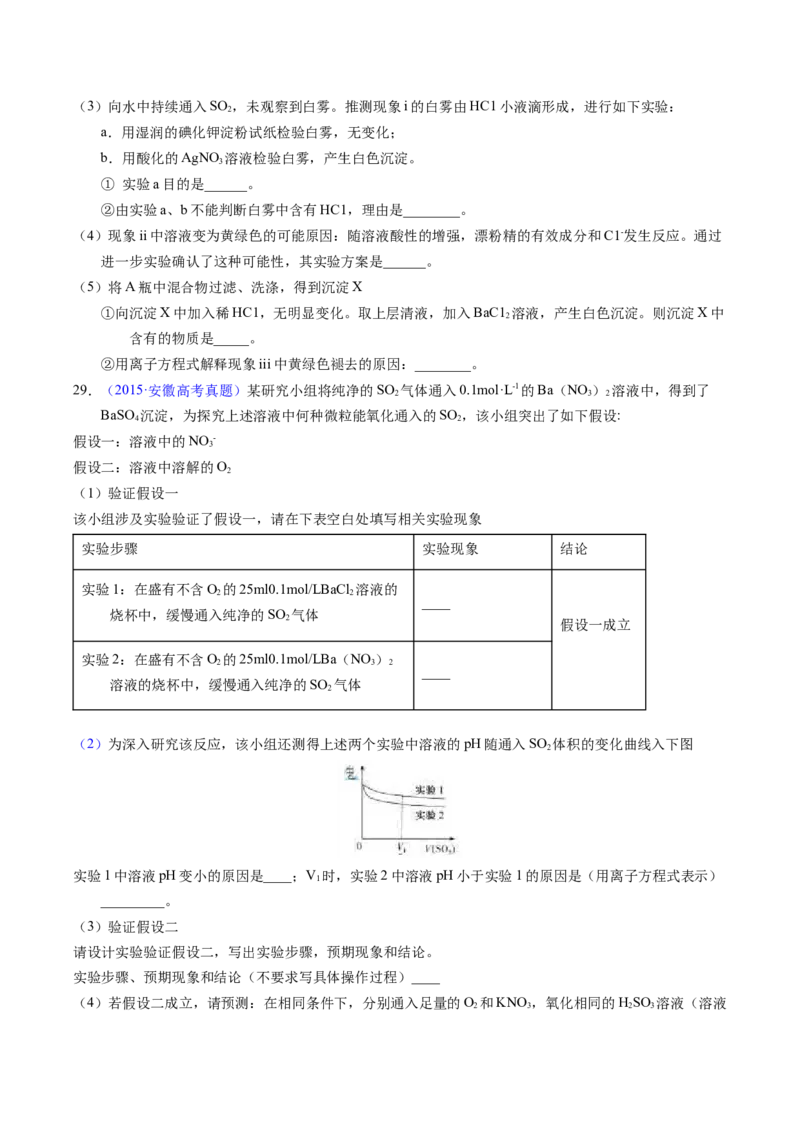
27.(2018·浙江高考真题)某同学用下列装置完成了浓硫酸和SO 性质实验(夹持装置已省略)。请回答:
2
(1)下列说法正确的是__________。
A.反应后,将试管Ⅰ中的白色固体加入水中,溶液呈蓝色
B.取下试管Ⅲ并不断振荡,试管中出现浑浊,是因为生成了BaSO
4
C.试管Ⅳ中KMnO 溶液褪色,说明SO 具有氧化性
4 2
D.试管V中的NaOH溶液可用NaCO 溶液代替
2 3
(2)取下试管Ⅱ,在该试管口套上气球,将无色溶液加热恢复至红色,冷却后,发现溶液颜色再次
变浅。解释“无色→红色→颜色变浅”变化的原因______________。
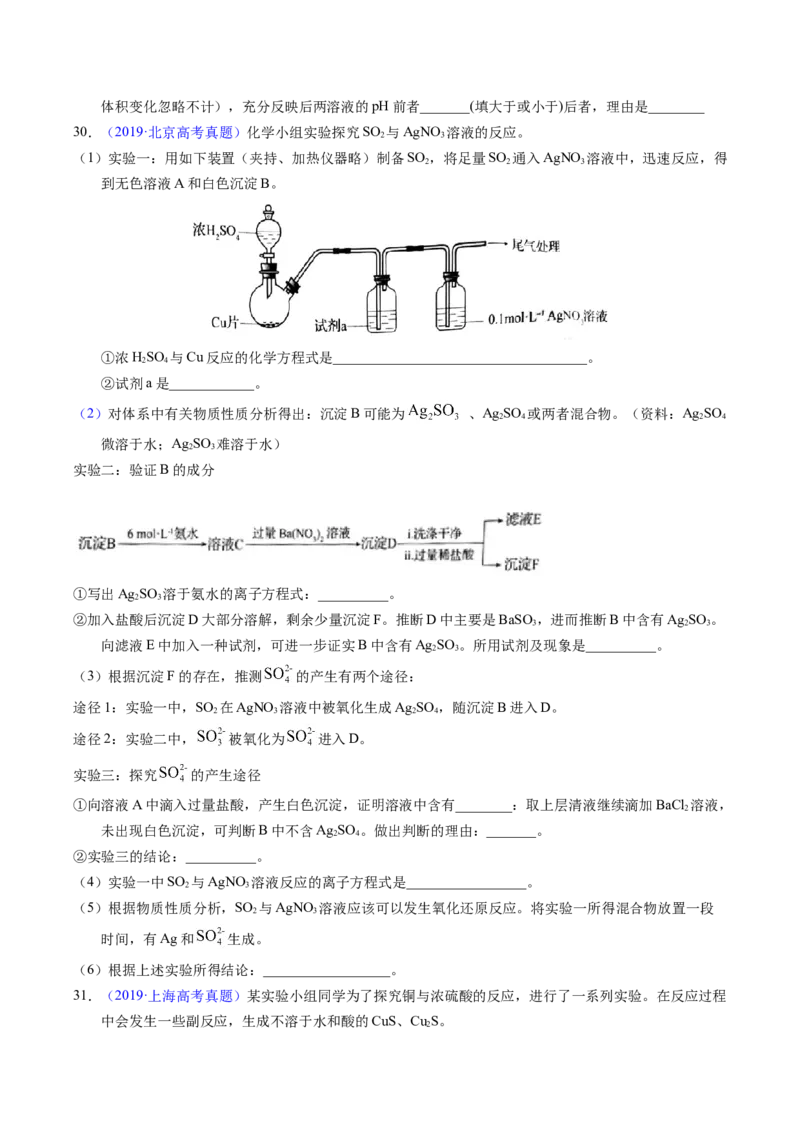
28.(2013·北京高考真题)某学生对SO 与漂粉精的反应进行实验探究:
2
操作 现象
取4g漂粉精固体,加入100mL水 部分固体溶解,溶液略有颜色
过滤,测漂粉精溶液的pH pH试纸先变蓝(约为12),后褪色
i、液面上方出现白雾;
ii、稍后,出现浑浊,溶液变为黄绿色;
iii、稍后,产生大量白色沉淀,黄绿色褪去
(1)C1 和Ca(OH) 制取漂粉精的化学方程是_________。
2 2
(2)pH试纸颜色的变化说明漂粉精溶液具有的性质是_________。(3)向水中持续通入SO ,未观察到白雾。推测现象i的白雾由HC1小液滴形成,进行如下实验:
2
a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用酸化的AgNO 溶液检验白雾,产生白色沉淀。
3
① 实验a目的是______。
②由实验a、b不能判断白雾中含有HC1,理由是________。
(4)现象ii中溶液变为黄绿色的可能原因:随溶液酸性的增强,漂粉精的有效成分和C1-发生反应。通过
进一步实验确认了这种可能性,其实验方案是______。
(5)将A瓶中混合物过滤、洗涤,得到沉淀X
①向沉淀X中加入稀HC1,无明显变化。取上层清液,加入BaC1 溶液,产生白色沉淀。则沉淀X中
2
含有的物质是_____。
②用离子方程式解释现象iii中黄绿色褪去的原因:________。
29.(2015·安徽高考真题)某研究小组将纯净的SO 气体通入0.1mol·L-1的Ba(NO ) 溶液中,得到了
2 3 2
BaSO 沉淀,为探究上述溶液中何种微粒能氧化通入的SO ,该小组突出了如下假设:
4 2
假设一:溶液中的NO -
3
假设二:溶液中溶解的O
2
(1)验证假设一
该小组涉及实验验证了假设一,请在下表空白处填写相关实验现象
实验步骤 实验现象 结论
实验1:在盛有不含O 的25ml0.1mol/LBaCl 溶液的
2 2
____
烧杯中,缓慢通入纯净的SO 气体
2 假设一成立
实验2:在盛有不含O 的25ml0.1mol/LBa(NO )
2 3 2
____
溶液的烧杯中,缓慢通入纯净的SO 气体
2
(2)为深入研究该反应,该小组还测得上述两个实验中溶液的pH随通入SO 体积的变化曲线入下图
2
实验1中溶液pH变小的原因是____;V 时,实验2中溶液pH小于实验1的原因是(用离子方程式表示)
1
_________。
(3)验证假设二
请设计实验验证假设二,写出实验步骤,预期现象和结论。
实验步骤、预期现象和结论(不要求写具体操作过程)____
(4)若假设二成立,请预测:在相同条件下,分别通入足量的O 和KNO,氧化相同的HSO 溶液(溶液
2 3 2 3体积变化忽略不计),充分反映后两溶液的pH前者_______(填大于或小于)后者,理由是________
30.(2019·北京高考真题)化学小组实验探究SO 与AgNO 溶液的反应。
2 3
(1)实验一:用如下装置(夹持、加热仪器略)制备SO ,将足量SO 通入AgNO 溶液中,迅速反应,得
2 2 3
到无色溶液A和白色沉淀B。
①浓HSO 与Cu反应的化学方程式是____________________________________。
2 4
②试剂a是____________。
(2)对体系中有关物质性质分析得出:沉淀B可能为 、Ag SO 或两者混合物。(资料:Ag SO
2 4 2 4
微溶于水;Ag SO 难溶于水)
2 3
实验二:验证B的成分
①写出Ag SO 溶于氨水的离子方程式:__________。
2 3
②加入盐酸后沉淀D大部分溶解,剩余少量沉淀F。推断D中主要是BaSO,进而推断B中含有Ag SO 。
3 2 3
向滤液E中加入一种试剂,可进一步证实B中含有Ag SO 。所用试剂及现象是__________。
2 3
(3)根据沉淀F的存在,推测 的产生有两个途径:
途径1:实验一中,SO 在AgNO 溶液中被氧化生成Ag SO ,随沉淀B进入D。
2 3 2 4
途径2:实验二中, 被氧化为 进入D。
实验三:探究 的产生途径
①向溶液A中滴入过量盐酸,产生白色沉淀,证明溶液中含有________:取上层清液继续滴加BaCl 溶液,
2
未出现白色沉淀,可判断B中不含Ag SO 。做出判断的理由:_______。
2 4
②实验三的结论:__________。
(4)实验一中SO 与AgNO 溶液反应的离子方程式是_________________。
2 3
(5)根据物质性质分析,SO 与AgNO 溶液应该可以发生氧化还原反应。将实验一所得混合物放置一段
2 3
时间,有Ag和 生成。
(6)根据上述实验所得结论:__________________。
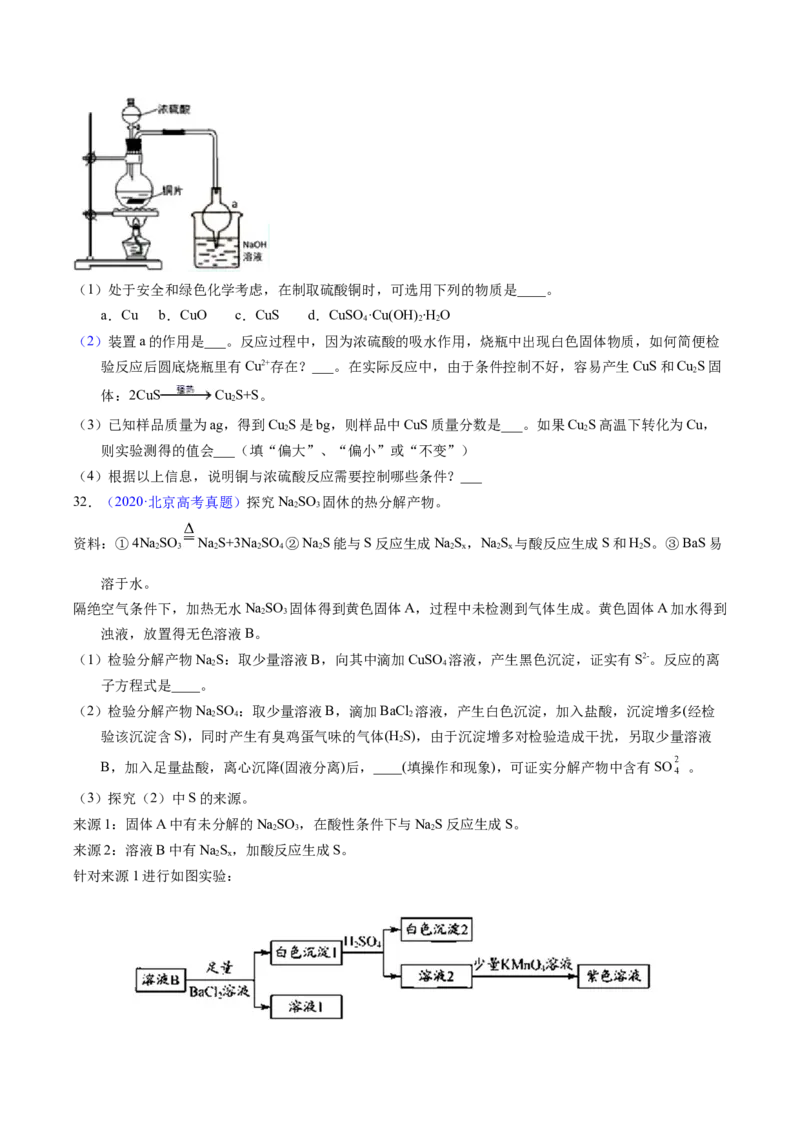
31.(2019·上海高考真题)某实验小组同学为了探究铜与浓硫酸的反应,进行了一系列实验。在反应过程
中会发生一些副反应,生成不溶于水和酸的CuS、Cu S。
2(1)处于安全和绿色化学考虑,在制取硫酸铜时,可选用下列的物质是____。
a.Cu b.CuO c.CuS d.CuSO ·Cu(OH) ∙HO
4 2 2
(2)装置a的作用是___。反应过程中,因为浓硫酸的吸水作用,烧瓶中出现白色固体物质,如何简便检
验反应后圆底烧瓶里有Cu2+存在?___。在实际反应中,由于条件控制不好,容易产生CuS和Cu S固
2
体:2CuS Cu S+S。
2
(3)已知样品质量为ag,得到Cu S是bg,则样品中CuS质量分数是___。如果Cu S高温下转化为Cu,
2 2
则实验测得的值会___(填“偏大”、“偏小”或“不变”)
(4)根据以上信息,说明铜与浓硫酸反应需要控制哪些条件?___
32.(2020·北京高考真题)探究NaSO 固休的热分解产物。
2 3
资料:①4NaSO NaS+3Na SO ②NaS能与S反应生成NaS,NaS 与酸反应生成S和HS。③BaS易
2 3 2 2 4 2 2 x 2 x 2
溶于水。
隔绝空气条件下,加热无水NaSO 固体得到黄色固体A,过程中未检测到气体生成。黄色固体A加水得到
2 3
浊液,放置得无色溶液B。
(1)检验分解产物NaS:取少量溶液B,向其中滴加CuSO 溶液,产生黑色沉淀,证实有S2-。反应的离
2 4
子方程式是____。
(2)检验分解产物NaSO :取少量溶液B,滴加BaCl 溶液,产生白色沉淀,加入盐酸,沉淀增多(经检
2 4 2
验该沉淀含S),同时产生有臭鸡蛋气味的气体(H S),由于沉淀增多对检验造成干扰,另取少量溶液
2
B,加入足量盐酸,离心沉降(固液分离)后,____(填操作和现象),可证实分解产物中含有SO 。
(3)探究(2)中S的来源。
来源1:固体A中有未分解的NaSO ,在酸性条件下与NaS反应生成S。
2 3 2
来源2:溶液B中有NaS,加酸反应生成S。
2 x
针对来源1进行如图实验:①实验可证实来源1不成立。实验证据是____。
②不能用盐酸代替硫酸的原因是____。
③写出来源2产生S的反应的离子方程式:____。
(4)实验证明NaSO 固体热分解有NaS,NaSO 和S产生。运用氧化还原反应规律分析产物中S产生的
2 3 2 2 4
合理性:____。