文档内容
专题47 电解应用
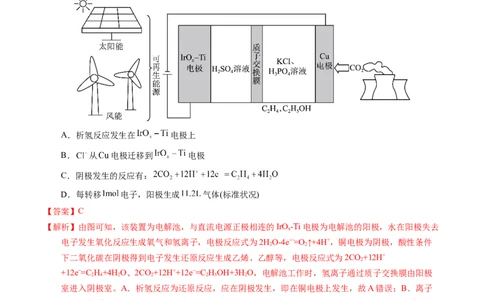
1.【2023年全国甲卷】用可再生能源电还原 时,采用高浓度的 抑制酸性电解液中的析氢反应来提
高多碳产物(乙烯、乙醇等)的生成率,装置如下图所示。下列说法正确的是
A.析氢反应发生在 电极上
B. 从 电极迁移到 电极
C.阴极发生的反应有:
D.每转移 电子,阳极生成 气体(标准状况)
【答案】C
【解析】由图可知,该装置为电解池,与直流电源正极相连的IrO -Ti电极为电解池的阳极,水在阳极失去
x
电子发生氧化反应生成氧气和氢离子,电极反应式为2HO-4e—=O ↑+4H+,铜电极为阴极,酸性条件
2 2
下二氧化碳在阴极得到电子发生还原反应生成乙烯、乙醇等,电极反应式为2CO+12H+
2
+12e−=C H+4H O、2CO+12H++12e−=C HOH+3H O,电解池工作时,氢离子通过质子交换膜由阳极
2 4 2 2 2 5 2
室进入阴极室。A.析氢反应为还原反应,应在阴极发生,即在铜电极上发生,故A错误;B.离子
交换膜为质子交换膜,只允许氢离子通过,Cl-不能通过,故B错误;C.由分析可知,铜电极为阴极,
酸性条件下二氧化碳在阴极得到电子发生还原反应生成乙烯、乙醇等,电极反应式有2CO+12H+
2
+12e−=C H+4H O,故C正确;D.水在阳极失去电子发生氧化反应生成氧气和氢离子,电极反应式
2 4 2
为2HO-4e—=O ↑+4H+,每转移1mol电子,生成0.25molO,在标况下体积为5.6L,故D错误;答案
2 2 2
选C。
2.【2023年北京卷】回收利用工业废气中的 和 ,实验原理示意图如下。下列说法不正确的是
A.废气中 排放到大气中会形成酸雨
B.装置a中溶液显碱性的原因是 的水解程度大于 的电离程度
C.装置a中溶液的作用是吸收废气中的 和
D.装置 中的总反应为
【答案】C
【解析】A. 是酸性氧化物,废气中 排放到空气中会形成硫酸型酸雨,故A正确;B.装置a中溶
液的溶质为 ,溶液显碱性,说明 的水解程度大于电离程度,故B正确;C.装置a中
溶液的作用是吸收 气体, 与 溶液不反应,不能吸收 ,故C错误;D.
由电解池阴极和阳极反应式可知,装置b中总反应为 ,故D正
确;选C。
3.(2021·湖北真题)NaCr O 的酸性水溶液随着H+浓度的增大会转化为CrO。电解法制备CrO 的原理
2 2 7 3 3
如图所示。下列说法错误的是
A.电解时只允许H+通过离子交换膜
B.生成O 和H 的质量比为8∶1
2 2
C.电解一段时间后阴极区溶液OH-的浓度增大
D.CrO 的生成反应为:Cr O +2H+=2CrO +H O
3 2 3 2
【答案】A【解析】根据左侧电极上生成 ,右侧电极上生成 ,知左侧电极为阳极,发生反应:
,右侧电极为阴极,发生反应: ;由题意知,左室
中 随着 浓度增大转化为 ,因此阳极生成的 不能通过
离子交换膜。A.由以上分析知,电解时通过离子交换膜的是 ,A项错误;B.根据各电极上转移
电子数相同,由阳极反应和阴极反应,知生成 和 的物质的量之比为1∶2,其质量比为8∶1,B
项正确;C.根据阴极反应知,电解一段时间后阴极区溶液 的浓度增大,C项正确:D.电解过
程中阳极区 的浓度增大, 转化为 ,D项正确。故选A。
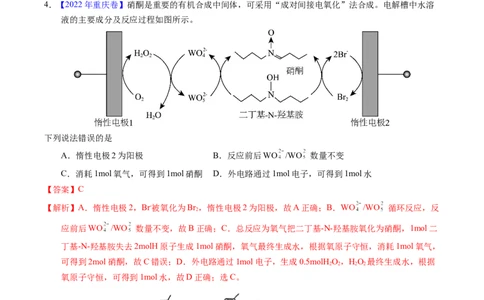
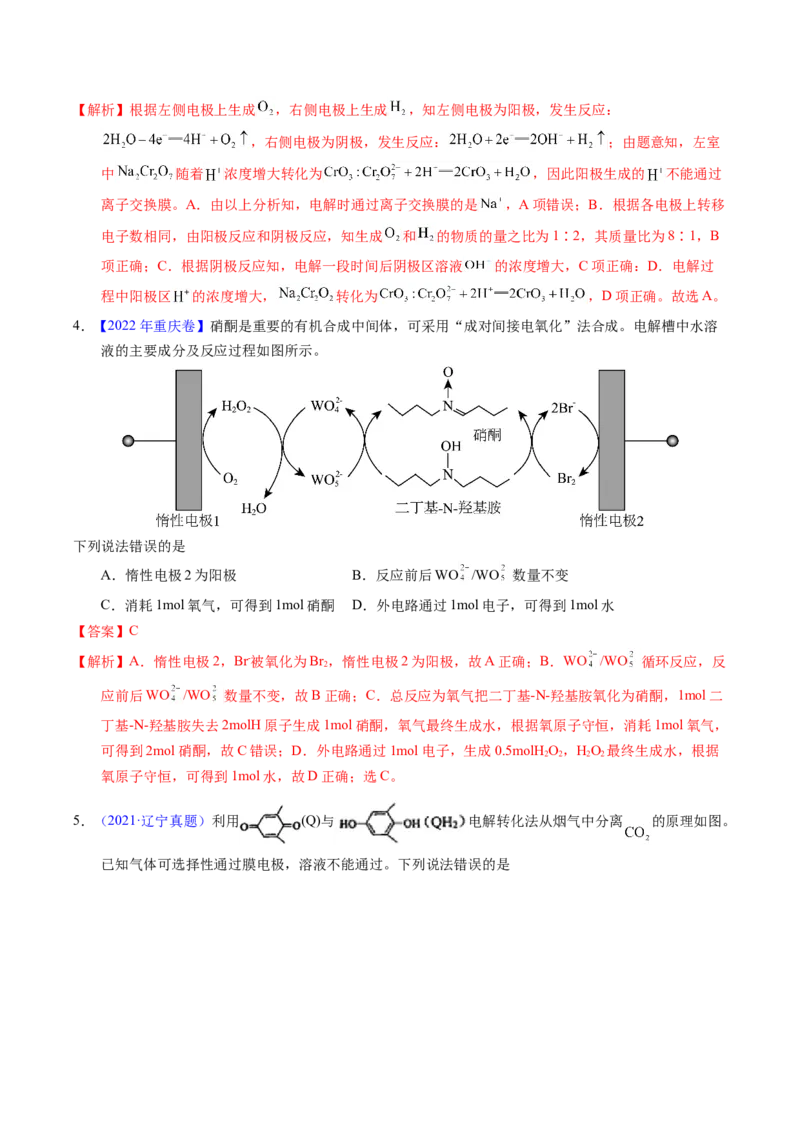
4.【2022年重庆卷】硝酮是重要的有机合成中间体,可采用“成对间接电氧化”法合成。电解槽中水溶
液的主要成分及反应过程如图所示。
下列说法错误的是
A.惰性电极2为阳极 B.反应前后WO /WO 数量不变
C.消耗1mol氧气,可得到1mol硝酮 D.外电路通过1mol电子,可得到1mol水
【答案】C
【解析】A.惰性电极2,Br-被氧化为Br ,惰性电极2为阳极,故A正确;B.WO /WO 循环反应,反
2
应前后WO /WO 数量不变,故B正确;C.总反应为氧气把二丁基-N-羟基胺氧化为硝酮,1mol二
丁基-N-羟基胺失去2molH原子生成1mol硝酮,氧气最终生成水,根据氧原子守恒,消耗1mol氧气,
可得到2mol硝酮,故C错误;D.外电路通过1mol电子,生成0.5molHO,HO 最终生成水,根据
2 2 2 2
氧原子守恒,可得到1mol水,故D正确;选C。
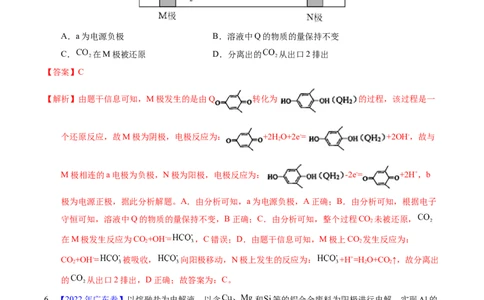
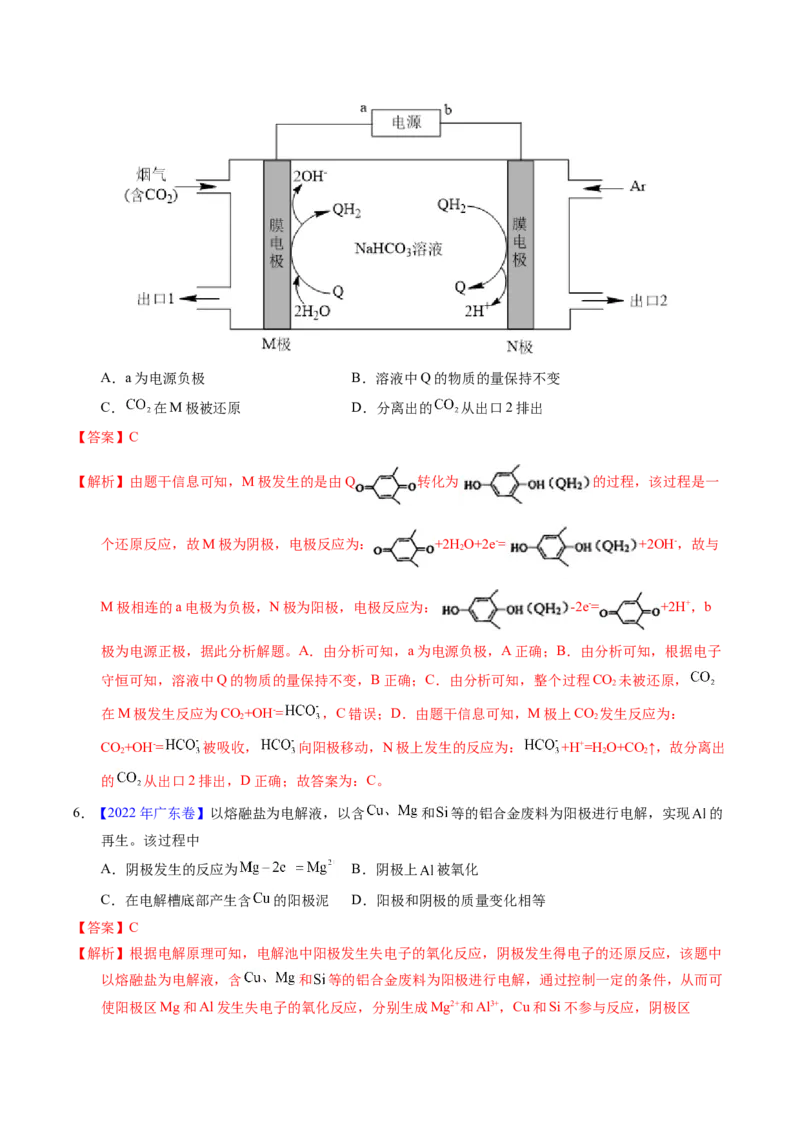
5.(2021·辽宁真题)利用 (Q)与 电解转化法从烟气中分离 的原理如图。
已知气体可选择性通过膜电极,溶液不能通过。下列说法错误的是A.a为电源负极 B.溶液中Q的物质的量保持不变
C. 在M极被还原 D.分离出的 从出口2排出
【答案】C
【解析】由题干信息可知,M极发生的是由Q 转化为 的过程,该过程是一
个还原反应,故M极为阴极,电极反应为: +2H O+2e-= +2OH-,故与
2
M极相连的a电极为负极,N极为阳极,电极反应为: -2e-= +2H+,b
极为电源正极,据此分析解题。A.由分析可知,a为电源负极,A正确;B.由分析可知,根据电子
守恒可知,溶液中Q的物质的量保持不变,B正确;C.由分析可知,整个过程CO 未被还原,
2
在M极发生反应为CO+OH-= ,C错误;D.由题干信息可知,M极上CO 发生反应为:
2 2
CO+OH-= 被吸收, 向阳极移动,N极上发生的反应为: +H+=H O+CO↑,故分离出
2 2 2
的 从出口2排出,D正确;故答案为:C。
6.【2022年广东卷】以熔融盐为电解液,以含 和 等的铝合金废料为阳极进行电解,实现 的
再生。该过程中
A.阴极发生的反应为 B.阴极上 被氧化
C.在电解槽底部产生含 的阳极泥 D.阳极和阴极的质量变化相等
【答案】C
【解析】根据电解原理可知,电解池中阳极发生失电子的氧化反应,阴极发生得电子的还原反应,该题中
以熔融盐为电解液,含 和 等的铝合金废料为阳极进行电解,通过控制一定的条件,从而可
使阳极区Mg和Al发生失电子的氧化反应,分别生成Mg2+和Al3+,Cu和Si不参与反应,阴极区Al3+得电子生成Al单质,从而实现Al的再生,据此分析解答。A.阴极应该发生得电子的还原反应,
实际上Mg在阳极失电子生成Mg2+,A错误;B.Al在阳极上被氧化生成Al3+,B错误;C.阳极材料
中Cu和Si不参与氧化反应,在电解槽底部可形成阳极泥,C正确;D.因为阳极除了铝参与电子转移,
镁也参与了电子转移,且还会形成阳极泥,而阴极只有铝离子得电子生成铝单质,根据电子转移数守
恒及元素守恒可知,阳极与阴极的质量变化不相等,D错误;故选C。
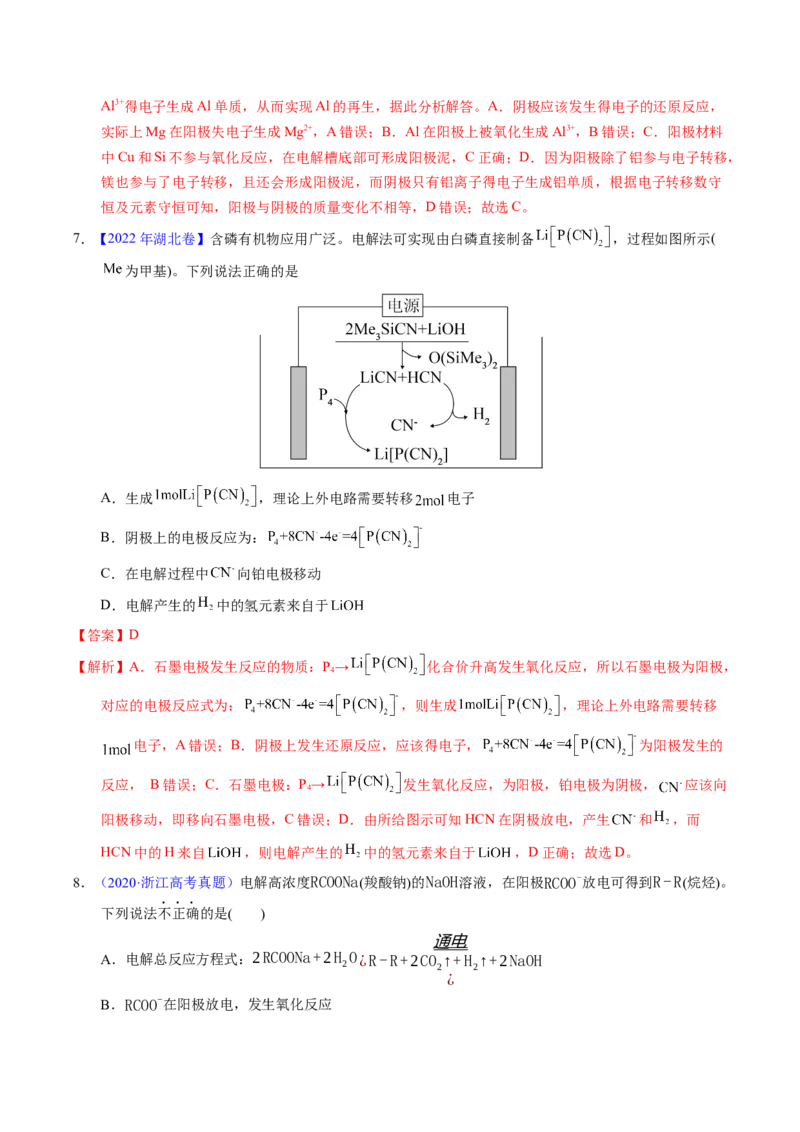
7.【2022年湖北卷】含磷有机物应用广泛。电解法可实现由白磷直接制备 ,过程如图所示(
为甲基)。下列说法正确的是
A.生成 ,理论上外电路需要转移 电子
B.阴极上的电极反应为:
C.在电解过程中 向铂电极移动
D.电解产生的 中的氢元素来自于
【答案】D
【解析】A.石墨电极发生反应的物质:P→ 化合价升高发生氧化反应,所以石墨电极为阳极,
4
对应的电极反应式为: ,则生成 ,理论上外电路需要转移
电子,A错误;B.阴极上发生还原反应,应该得电子, 为阳极发生的
反应, B错误;C.石墨电极:P→ 发生氧化反应,为阳极,铂电极为阴极, 应该向
4
阳极移动,即移向石墨电极,C错误;D.由所给图示可知HCN在阴极放电,产生 和 ,而
HCN中的H来自 ,则电解产生的 中的氢元素来自于 ,D正确;故选D。
8.(2020·浙江高考真题)电解高浓度RCOONa(羧酸钠)的NaOH溶液,在阳极RCOO-放电可得到R-R(烷烃)。
下列说法不正确的是( )
通电
A.电解总反应方程式:2RCOONa+2H O ¿R-R+2CO ↑+H ↑+2NaOH
2 2 2
¿
B.RCOO-在阳极放电,发生氧化反应C.阴极的电极反应:2H O+2e-=2OH-+H ↑
2 2
D.电解CH COONa、CH CH COONa和NaOH混合溶液可得到乙烷、丙烷和丁烷
3 3 2
【答案】A
【解析】A.因为阳极RCOO-放电可得到R-R(烷烃)和产生CO,在强碱性环境中,CO 会与OH-反应生成
2 2
CO2-和HO,故阳极的电极反应式为2RCOO--2e-+4OH-=R-R+2CO2-+2H O,阴极上HO电离产生的
3 2 3 2 2
H+放电生成H,同时生成OH-,阴极的电极反应式为2HO+2e-=2OH-+H ↑,因而电解总反应方程式为
2 2 2
通电
2RCOONa+2NaOH = R-R+2Na 2 CO 3 +H 2 ↑,不正确;B.RCOO-在阳极放电,电极反应式为2RCOO--2e-
+4OH-=R-R+2CO2-+2H O, -COO-中碳元素的化合价由+3价升高为+4价,发生氧化反应,烃基-R中
3 2
元素的化合价没有发生变化,正确;C.阴极上HO电离产生的H+放电生成H,同时生成OH-,阴极
2 2
的电极反应为2HO+2e-=2OH-+H ↑,正确;D.根据题中信息,由上述电解总反应方程式可以确定下
2 2
通电 通电
列反应能够发生:2CH 3 COONa+2NaOH = CH 3 -CH 3 +2Na 2 CO 3 +H 2 ↑,2CH 3 CH 2 COONa+2NaOH =
通电
CH 3 CH 2 -CH 2 CH 3 +2Na 2 CO 3 +H 2 ↑,CH 3 COONa+CH 3 CH 2 COONa+2NaOH = CH 3 -CH 2 CH 3 +2Na 2 CO 3 +H 2 ↑。
因此,电解CHCOONa、CHCHCOONa和NaOH 的混合溶液可得到乙烷、丙烷和丁烷,正确。答案
3 3 2
为A。
9.(2017·全国高考真题)用电解氧化法可以在铝制品表面形成致密、耐腐蚀的氧化膜,电解质溶液一般
为 混合溶液。下列叙述错误的是
A.待加工铝质工件为阳极
B.可选用不锈钢网作为阴极
C.阴极的电极反应式为:
D.硫酸根离子在电解过程中向阳极移动
【答案】C
【解析】A、根据原理可知,Al要形成氧化膜,化合价升高失电子,因此铝为阳极,说法正确;B、不锈
钢网接触面积大,能增加电解效率,说法正确;C、阴极应为阳离子得电子,根据离子放电顺序应是
H+放电,即2H++2e-=H ↑,说法错误;D、根据电解原理,电解时,阴离子移向阳极,说法正确。
2
10.(2015·四川高考真题)用下图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液PH为9~10,阳
极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是
A.用石墨作阳极,铁作阴极
B.阳极的电极反应式为:Cl- + 2OH--2e-= ClO- + H O
2
C.阴极的电极反应式为:2HO + 2e- = H ↑ + 2OH-
2 2
D.除去CN-的反应:2CN-+ 5ClO- + 2H+ = N ↑ + 2CO ↑ + 5Cl-+ H O
2 2 2【答案】D
【解析】A、根据电解的原理,铁作阳极时,铁失电子,参与反应,但根据题中信息,铁不参与反应,因
此铁作阴极,正确;B、根据信息,环境是碱性,利用ClO-氧化CN-,因此阳极反应式为Cl-+2OH
--2e-=ClO-+HO,正确;C、根据电解原理,阴极上是阳离子放电,即2H++2e-=H ↑,正确;
2 2
D、CN-被ClO-氧化成两种无毒的气体,即为N 和CO,环境是碱性,不能生成H+,错误。
2 2
11.(2017·海南高考真题)一种电化学制备NH 的装置如图所示,图中陶瓷在高温时可以传输H+。下列
3
叙述错误的是
A.Pd电极b为阴极
B.阴极的反应式为:N+6H++6e− 2NH
2 3
C.H+由阳极向阴极迁移
D.陶瓷可以隔离N 和H
2 2
【答案】A
【解析】A、此装置为电解池,总反应是N+3H=2NH,Pd电极b上是氢气发生反应,即氢气失去电子化
2 2 3
合价升高,Pd电极b为阳极,说法错误;B、根据A选项分析,Pd电极a为阴极,反应式为N+6H+
2
+6e-=2NH,说法正确;C、根据电解的原理,阴极上发生还原反应,即有阳极移向阴极,说法正确;
3
D、根据装置图,陶瓷隔离N 和H,说法正确。
2 2
12.(2012·浙江高考真题)以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如下:
下列说法不正确的是
A.在阴极式,发生的电极反应为:2HO+2e- 2OH―+H↑
2 2
B.在阳极室,通电后溶液逐渐由黄色变为橙色,是因为阳极区H+浓度增大,使平衡2 +2H+
+HO向右移动
2
C.该制备过程总反应的化学方程式为:4KCrO+4HO 2KCr O+4KOH+2H↑+2O↑
2 4 2 2 2 7 2 2D.测定阳极液中K和Cr的含量,若K与Cr的物质的量之比为d,则此时铬酸钾的转化率为α=
【答案】D
【解析】A、根据装置图可知,左侧是阴极室,阴极是氢离子放电,腐蚀还原反应生成氢气,正确;B、阳
极发生氧化反应,氢氧根离子放电生成氧气,导致阳极区氢离子浓度增大,2CrO2-+2H+ Cr O2-
4 2 7
+H O向右移动,正确;C、电解时,铬酸钾和水放电生成重铬酸钾、氢气、氧气和氢氧化钠,所以总
2
反应的化学方程式为4KCrO+4H O 2KCr O+4KOH+2H ↑+O ↑,正确;D、设加入反应容器内的
2 4 2 2 2 7 2 2
KCrO 为1mol,则n(K)="2mol," n(Cr)=1mol,反应过程中有xmol KCrO 转化为KCr O,由于阴
2 4 2 4 2 2 7
极是氢离子放电,造成阴极区氢氧根离子增多,所以K+向阴极区移动,补充氢离子,根据化学方程式
可知,xmol KCrO 转化为KCr O,则阴极区生成KOH的物质的量是xmol,则阳极区剩余n(K)=
2 4 2 2 7
(2-x)mol,Cr元素不变,仍是1mol,根据:K与Cr的物质的量之比为d,解得(2-x)/1=d,x=2-d,
转化率为(2-d)/1×100%=2-d,错误,答案选D。
13.(2013·海南高考真题)下列叙述正确的是
A.合成氨的“造气”阶段会产生废气
B.电镀的酸性废液用碱中和后就可以排放
C.电解制铝的过程中,作为阳极材料的无烟煤不会消耗
D.使用煤炭转化的管道煤气比直接燃煤可减少环境污染
【答案】AD
【解析】氨的造气用天燃气或煤,必产生二氧化碳,A对;电镀液含重金属离子,应处理后排放,B错;
铝的生产中阳极放电,煤有消耗,C错;煤的气化后作了脱硫处理,污染减少,D对。
14.(2013·全国高考真题)电解法处理酸性含铬废水(主要含有Cr O2-)时,以铁板作阴、阳极,处理过
2 7
程中存在反应Cr O2-+6Fe2++14H+=2Cr3++6Fe3++7HO,最后Cr3+以Cr(OH) 形式除去,下列说法
2 7 2 3
不正确的是
A.阳极反应为Fe-2e-=Fe2+
B.电解过程中溶液pH不会变化
C.过程中有Fe(OH) 沉淀生成
3
D.电路中每转移12 mol电子,最多有1 mol Cr O2-被还原
2 7
【答案】B
【解析】A、铁为活泼电极,铁板作阳极时电解过程中电极本身失电子,电极反应式为: Fe-2e-=Fe2+,正
确;B、阴极是氢离子得到电子生成氢气,氢离子被消耗,在反应Cr O2+6Fe2++14H+=2Cr3++6Fe3+
2 7
+7H O中,也消耗氢离子,所以反应过程中溶液中的氢离子浓度减小,溶液pH增大,错误;C、反应
2
过程中消耗了大量H+,使得Cr3+和Fe3+都转化为氢氧化物沉淀,正确;D、电路中每转移12 mol电子,
有6mol Fe2+生成,根据反应Cr O2+6Fe2++14H+=2Cr3++6Fe3++7H O可知,最多有1 mol Cr O2-被还原,
2 7 2 2 7
正确。
15.(2013·北京高考真题)用石墨电极电解CuCl 溶液(见右图)。下列分析正确的是
2A.a端是直流电源的负极
B.通电使CuCl 发生电离
2
C.阳极上发生的反应:Cu2++2e-=Cu
D.通电一段时间后,在阴极附近观察到黄绿色气体
【答案】A
【解析】A、依据装置图可知,铜离子移向的电极为阴极,阴极和电源负极相连,a为负极,正确;B、通
电氯化铜发生氧化还原反应生成氯气和铜,电离是氯化铜离解为阴阳离子,错误;C、与b连接的电
极是阳极,氯离子失电子发生氧化反应,电极反应式为:2Cl﹣﹣2e﹣=Cl↑,错误;D、通电一段时间
2
后,氯离子在阳极失电子发生氧化反应,在阳极附近观察到黄绿色气体,错误;故选A.
16.(2010·海南高考真题)利用电解法可将含有Fe、Zn、Ag、Au等杂质的粗铜提纯,下列叙述正确的是
A.电解时以纯铜作阳极
B.电解时阴极发生氧化反应
C.粗铜连接电源负极,电极反应是Cu -2e-=Cu2+
D.电解结束,电解槽底部会形成含少量Ag、Au等阳极泥
【答案】D
【解析】A.电解精炼Cu时,以粗铜作阳极,纯铜作阴极,A错误;B.电解时阴极发生得电子的还原反
应,B错误;C.粗铜作阳极,连接电源的正极,电极反应有Zn-2e-=Zn2+、Fe-2e-=Fe2+、Cu-2e-=Cu2+,
C错误;D.粗铜作阳极,电极反应有Zn-2e-=Zn2+、Fe-2e-=Fe2+、Cu-2e-=Cu2+,粗铜中活泼性不如Cu
的Ag、Au不会放电,以阳极泥的形式沉积在电解槽底部,D正确;答案选D。
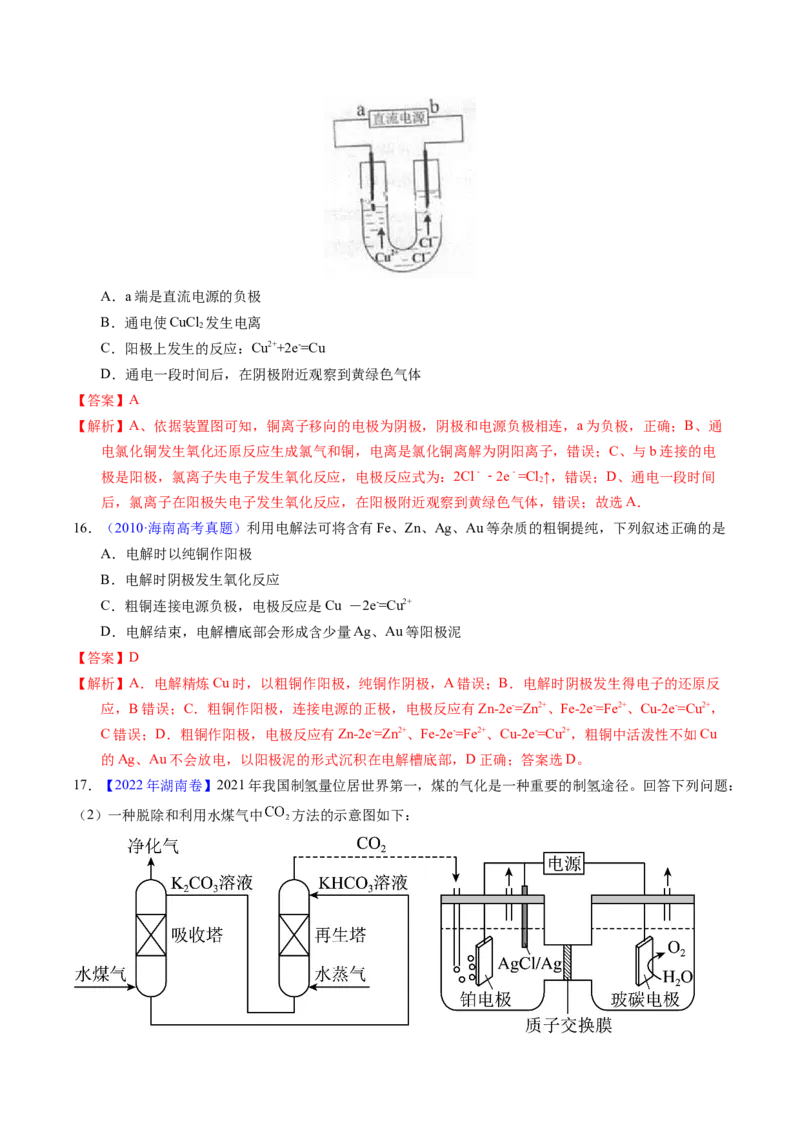
17.【2022年湖南卷】2021年我国制氢量位居世界第一,煤的气化是一种重要的制氢途径。回答下列问题:
(2)一种脱除和利用水煤气中 方法的示意图如下:①某温度下,吸收塔中 溶液吸收一定量的 后, ,则该溶液的
_______(该温度下 的 );
②再生塔中产生 的离子方程式为_______;
③利用电化学原理,将 电催化还原为 ,阴极反应式为_______。
【答案】
(2) 10 2 CO↑+ +H O 2CO+12e-+12H+=C H+4H O、AgCl+e-=Ag+Cl-
2 2 2 2 4 2
【解析】
(2)①某温度下,吸收塔中KCO 溶液吸收一定量的CO 后,c( ):c( )=1:2,由
2 3 2
可知, = ,则该溶液的
pH=10;
②再生塔中KHCO 受热分解生成KCO、HO和CO,该反应的离子方程式为2 CO↑+
3 2 3 2 2 2
+H O;
2
③利用电化学原理,将CO 电催化还原为C H,阴极上发生还原反应,阳极上水放电生成氧气和H+,
2 2 4
H+通过质子交换膜迁移到阴极区参与反应生成乙烯,铂电极和Ag/AgCl电极均为阴极,在电解过程中
AgCl可以转化为Ag,则阴极的电极反应式为2CO+12e-+12H+=C H+4H O、AgCl+e-=Ag+Cl-。
2 2 4 2
18.(2021·湖南真题)氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过下面两
种方法由氨气得到氢气。
方法Ⅱ:氨电解法制氢气
利用电解原理,将氨转化为高纯氢气,其装置如图所示。
(4)电解过程中 的移动方向为_______(填“从左往右”或“从右往左”);
(5)阳极的电极反应式为_______。
【答案】
(4)从右往左(5)2NH -6e-+6OH-= N +6H O
3 2 2
【解析】
(4)由图可知,通NH 的一极氮元素化合价升高,发生氧化反应,为电解池的阳极,则另一电极为阴极,
3
电解过程中OH-移向阳极,则从右往左移动,故答案为:从右往左;
(5)阳极NH 失电子发生氧化反应生成N,结合碱性条件,电极反应式为:2NH -6e-+6OH-= N +6H O,
3 2 3 2 2
故答案为:2NH -6e-+6OH-= N +6H O。
3 2 2
19.(2020·北京高考真题)HO 是一种重要的化学品,其合成方法不断发展。
2 2
(2)电化学制备方法:已知反应2HO=2H O+O↑能自发进行,反向不能自发进行,通过电解可以实现由
2 2 2 2
HO和O 为原料制备HO,如图为制备装置示意图。
2 2 2 2
①a极的电极反应式是____。
②下列说法正确的是____。
A.该装置可以实现电能转化为化学能
B.电极b连接电源负极
C.该方法相较于早期剂备方法具有原料廉价,对环境友好等优点
【答案】(2)① O+2H++2e-= H O ②AC
2 2 2
【解析】
(2)①根据分析,a极的电极反应式是O+2H++2e-= H O;
2 2 2
②A.2HO=2H O+O↑能自发进行,反向不能自发进行,根据图示,该装置有电源,属于电解池,电解池
2 2 2 2
是将电能转化为化学能的装置,正确;
B.根据分析,电极b为阳极,电解池阳极与电源正极连接,错误;
C.根据分析,该装置的总反应为2HO+O 2HO,根据反应可知,制取双氧水的原料为氧气和水,来
2 2 2 2
源广泛,原料廉价,对环境友好等优点,正确;
答案选AC。
20.(2019·北京高考真题)氢能源是最具应用前景的能源之一,高纯氢的制备是目前的研究热点。
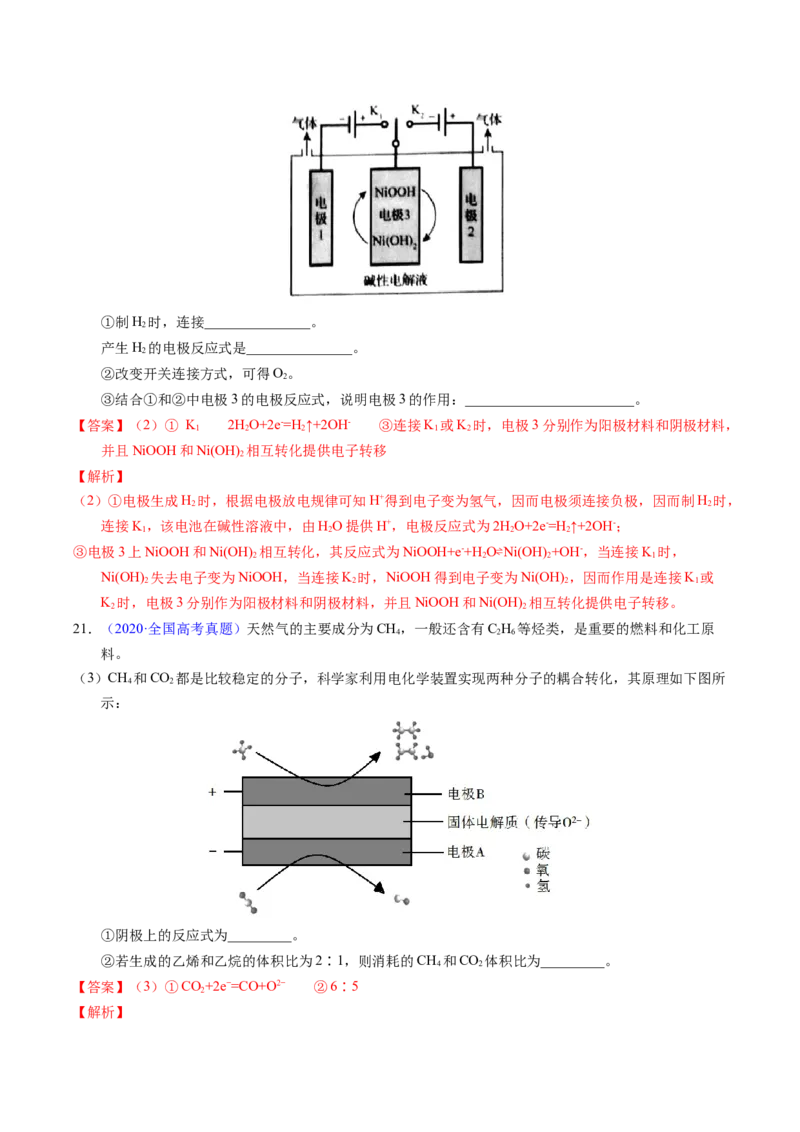
(2)可利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接K 或K,可交替得到
1 2
H 和O。
2 2①制H 时,连接_______________。
2
产生H 的电极反应式是_______________。
2
②改变开关连接方式,可得O。
2
③结合①和②中电极3的电极反应式,说明电极3的作用:________________________。
【答案】(2)① K 2H O+2e-=H ↑+2OH- ③连接K 或K 时,电极3分别作为阳极材料和阴极材料,
1 2 2 1 2
并且NiOOH和Ni(OH) 相互转化提供电子转移
2
【解析】
(2)①电极生成H 时,根据电极放电规律可知H+得到电子变为氢气,因而电极须连接负极,因而制H 时,
2 2
连接K,该电池在碱性溶液中,由HO提供H+,电极反应式为2HO+2e-=H ↑+2OH-;
1 2 2 2
③电极3上NiOOH和Ni(OH) 相互转化,其反应式为NiOOH+e-+H O⇌Ni(OH) +OH-,当连接K 时,
2 2 2 1
Ni(OH) 失去电子变为NiOOH,当连接K 时,NiOOH得到电子变为Ni(OH) ,因而作用是连接K 或
2 2 2 1
K 时,电极3分别作为阳极材料和阴极材料,并且NiOOH和Ni(OH) 相互转化提供电子转移。
2 2
21.(2020·全国高考真题)天然气的主要成分为CH,一般还含有C H 等烃类,是重要的燃料和化工原
4 2 6
料。
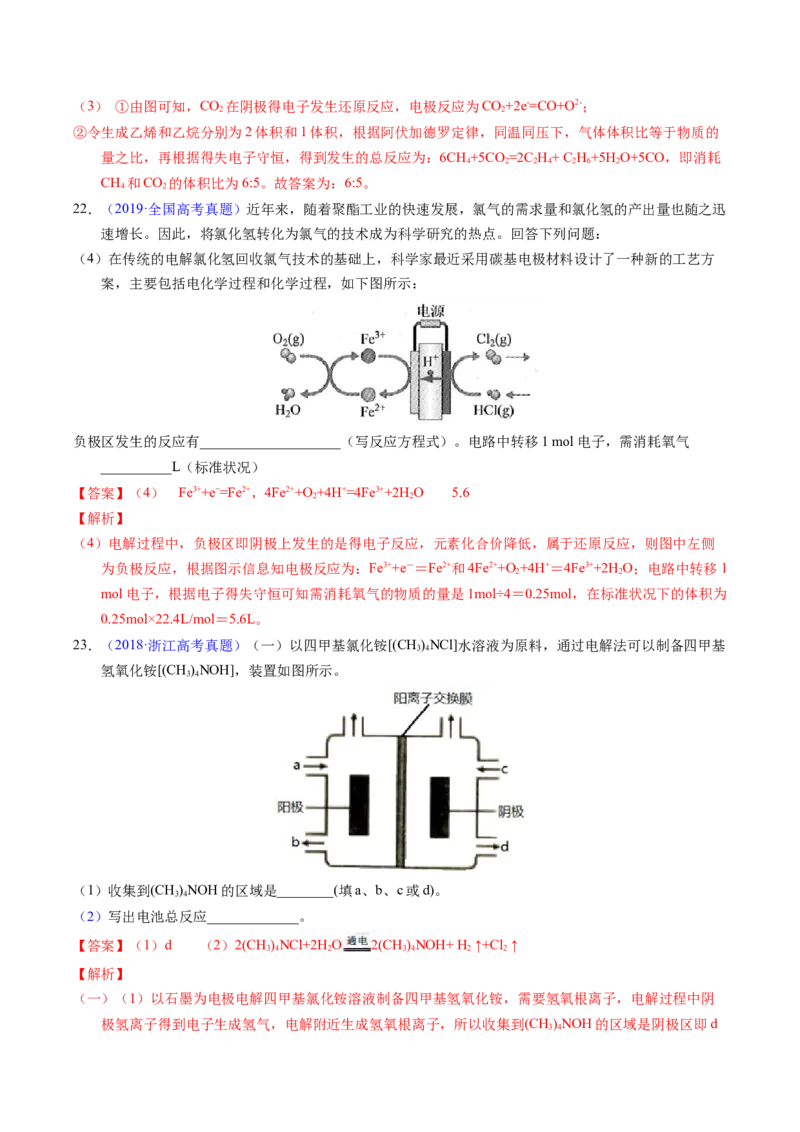
(3)CH 和CO 都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如下图所
4 2
示:
①阴极上的反应式为_________。
②若生成的乙烯和乙烷的体积比为2∶1,则消耗的CH 和CO 体积比为_________。
4 2
【答案】(3)①CO+2e−=CO+O2− ②6∶5
2
【解析】(3) ①由图可知,CO 在阴极得电子发生还原反应,电极反应为CO+2e-=CO+O2-;
2 2
②令生成乙烯和乙烷分别为2体积和1体积,根据阿伏加德罗定律,同温同压下,气体体积比等于物质的
量之比,再根据得失电子守恒,得到发生的总反应为:6CH+5CO =2C H+ C H+5H O+5CO,即消耗
4 2 2 4 2 6 2
CH 和CO 的体积比为6:5。故答案为:6:5。
4 2
22.(2019·全国高考真题)近年来,随着聚酯工业的快速发展,氯气的需求量和氯化氢的产出量也随之迅
速增长。因此,将氯化氢转化为氯气的技术成为科学研究的热点。回答下列问题:
(4)在传统的电解氯化氢回收氯气技术的基础上,科学家最近采用碳基电极材料设计了一种新的工艺方
案,主要包括电化学过程和化学过程,如下图所示:
负极区发生的反应有____________________(写反应方程式)。电路中转移1 mol电子,需消耗氧气
__________L(标准状况)
【答案】(4) Fe3++e−=Fe2+,4Fe2++O +4H+=4Fe3++2H O 5.6
2 2
【解析】
(4)电解过程中,负极区即阴极上发生的是得电子反应,元素化合价降低,属于还原反应,则图中左侧
为负极反应,根据图示信息知电极反应为:Fe3++e-=Fe2+和4Fe2++O +4H+=4Fe3++2H O;电路中转移1
2 2
mol电子,根据电子得失守恒可知需消耗氧气的物质的量是1mol÷4=0.25mol,在标准状况下的体积为
0.25mol×22.4L/mol=5.6L。
23.(2018·浙江高考真题)(一)以四甲基氯化铵[(CH )NCl]水溶液为原料,通过电解法可以制备四甲基
3 4
氢氧化铵[(CH )NOH],装置如图所示。
3 4
(1)收集到(CH)NOH的区域是________(填a、b、c或d)。
3 4
(2)写出电池总反应_____________。
【答案】(1)d (2)2(CH)NCl+2H O 2(CH)NOH+ H ↑+Cl ↑
3 4 2 3 4 2 2
【解析】
(一)(1)以石墨为电极电解四甲基氯化铵溶液制备四甲基氢氧化铵,需要氢氧根离子,电解过程中阴
极氢离子得到电子生成氢气,电解附近生成氢氧根离子,所以收集到(CH)NOH的区域是阴极区即d
3 4口。
故答案为d;
(2)结合反应为和生成物的关系可知电解过程中生成产物为四甲基氢氧化铵、氢气和氯气,据此写出电
解反应的化学方程式:2(CH)NCl+2H O 2(CH)NOH+ H ↑+Cl ↑。
3 4 2 3 4 2 2
故答案为2(CH)NCl+2H O 2(CH)NOH+ H ↑+Cl ↑。
3 4 2 3 4 2 2
24.(2015·山东高考真题)(15分)利用LiOH和钴氧化物可制备锂离子电池正极材料。LiOH可由电解法
制备,钴氧化物可通过处理钴渣获得。
(1)利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。B极区电解液为________
溶液(填化学式),阳极电极反应式为_________,电解过程中Li+向_____电极迁移(填“A”或
“B”)。
【答案】(1)LiOH;2Cl‾—2e‾=Cl↑;B
2
【解析】
(1)根据示意图,B极区生产H,同时生成LiOH,则B极区电解液不能是LiCl溶液,如果是LiCl溶液
2
则无法得到纯净的LiOH,则B极区电解液为LiOH溶液;电极A为阳极,阳极区电解液为LiCl溶液,
根据放电顺序,阳极上Cl‾失去电子,则阳极电极反应式为:2Cl‾—2e‾=Cl↑;根据电流方向,电解过
2
程中Li+向B电极迁移。
25.(2014·北京高考真题)NH 经一系列反应可以得到HNO,如下图所示。
3 3
(4)IV中,电解NO制备 NH NO ,其工作原理如右图所示,为使电解产物全部转化为NH NO ,需补充
4 3 4 3
物质A,A是_____________,说明理由:________________。【答案】
(4)氨气;根据反应8NO+7H O 3NH NO +2HNO ,电解产生的HNO 多
2 4 3 3 3
【解析】
(4)电解 NO 制备硝酸铵,阳极反应为:NO-3e-+2H O=NO -+4H+,阴极反应为:NO+5e-+6H+=NH+
2 3 4
+H O,从两极反应可看出若要使电子得失守恒,阳极产生的NO -的量大于阴极产生的NH +的量,总
2 3 4
反应为8NO+7H O 3NH NO +2HNO ,故应补充适量的氨气。
2 4 3 3