文档内容
五年(2019-2023)年高考真题分项汇编
专题 05 常见无机物的性质、用途与转化
〖2023年高考真题〗
考点一 常见无机物的性质与用途
1.(2023·山东卷)实验室中使用盐酸、硫酸和硝酸时,对应关系错误的是
A.稀盐酸:配制 溶液
B.稀硫酸:蔗糖和淀粉的水解
C.稀硝酸:清洗附有银镜的试管
D.浓硫酸和浓硝酸的混合溶液:苯的磺化
2.(2023·浙江卷)氯化铁是一种重要的盐,下列说法不正确的是
A.氯化铁属于弱电解质 B.氯化铁溶液可腐蚀覆铜板
C.氯化铁可由铁与氯气反应制得 D.氯化铁溶液可制备氢氧化铁胶体
3.(2023·湖北卷)下列化学事实不符合“事物的双方既相互对立又相互统一”的哲学观点的是
A.石灰乳中存在沉淀溶解平衡
B.氯气与强碱反应时既是氧化剂又是还原剂
C.铜锌原电池工作时,正极和负极同时发生反应
D.Li、Na、K的金属性随其核外电子层数增多而增强
4.(2023·浙江卷)物质的性质决定用途,下列两者对应关系不正确的是
A.铝有强还原性,可用于制作门窗框架
B.氧化钙易吸水,可用作干燥剂
C.维生素C具有还原性,可用作食品抗氧化剂
D.过氧化钠能与二氧化碳反应生成氧气,可作潜水艇中的供氧剂
5.(2023·北京卷)蔗糖与浓硫酸发生作用的过程如图所示。
下列关于该过程的分析不正确的是
A.过程①白色固体变黑,主要体现了浓硫酸的脱水性
B.过程②固体体积膨胀,与产生的大量气体有关
C.过程中产生能使品红溶液褪色的气体,体现了浓硫酸的酸性
D.过程中蔗糖分子发生了化学键的断裂考点二 无机物的转化
6.(2023·辽宁卷)下列有关物质的工业制备反应错误的是
A.合成氨:N+3H 2NH B.制HCl:H+Cl 2HCl
2 2 3 2 2
C.制粗硅:SiO+2C Si+2CO D.冶炼镁:2MgO(熔融) 2Mg+O↑
2 2
7.(2023·全国乙卷)一些化学试剂久置后易发生化学变化。下列化学方程式可正确解释相应变化的是
A 硫酸亚铁溶液出现棕黄色沉淀
B 硫化钠溶液出现浑浊颜色变深
C 溴水颜色逐渐褪去
D 胆矾表面出现白色粉末
8.(2023·湖北卷)工业制备高纯硅的主要过程如下:
石英砂 粗硅 高纯硅
下列说法错误的是
A.制备粗硅的反应方程式为
B.1molSi含Si-Si键的数目约为
C.原料气HCl和 应充分去除水和氧气
D.生成 的反应为熵减过程
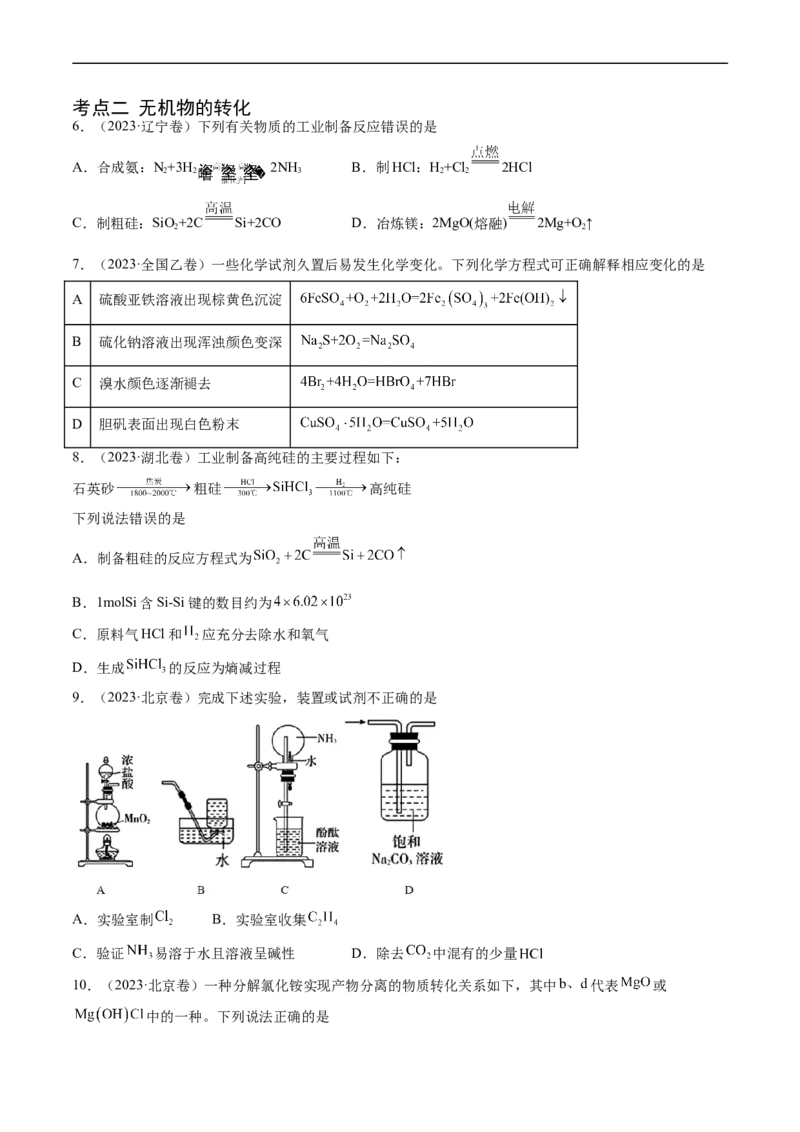
9.(2023·北京卷)完成下述实验,装置或试剂不正确的是
A.实验室制 B.实验室收集
C.验证 易溶于水且溶液呈碱性 D.除去 中混有的少量
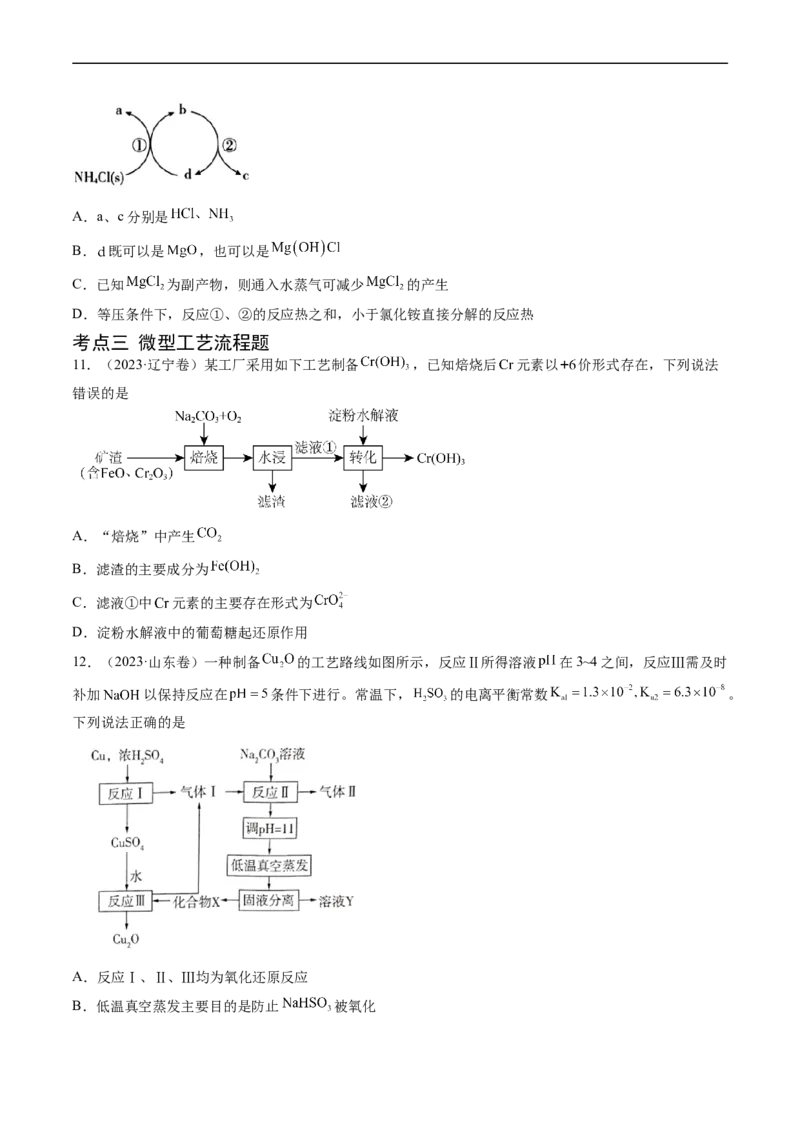
10.(2023·北京卷)一种分解氯化铵实现产物分离的物质转化关系如下,其中 代表 或
中的一种。下列说法正确的是A.a、c分别是
B. 既可以是 ,也可以是
C.已知 为副产物,则通入水蒸气可减少 的产生
D.等压条件下,反应①、②的反应热之和,小于氯化铵直接分解的反应热
考点三 微型工艺流程题
11.(2023·辽宁卷)某工厂采用如下工艺制备 ,已知焙烧后 元素以 价形式存在,下列说法
错误的是
A.“焙烧”中产生
B.滤渣的主要成分为
C.滤液①中 元素的主要存在形式为
D.淀粉水解液中的葡萄糖起还原作用
12.(2023·山东卷)一种制备 的工艺路线如图所示,反应Ⅱ所得溶液 在3~4之间,反应Ⅲ需及时
补加 以保持反应在 条件下进行。常温下, 的电离平衡常数 。
下列说法正确的是
A.反应Ⅰ、Ⅱ、Ⅲ均为氧化还原反应
B.低温真空蒸发主要目的是防止 被氧化C.溶液Y可循环用于反应Ⅱ所在操作单元吸收气体Ⅰ
D.若 产量不变,参与反应Ⅲ的 与 物质的量之比 增大时,需补加 的量减少
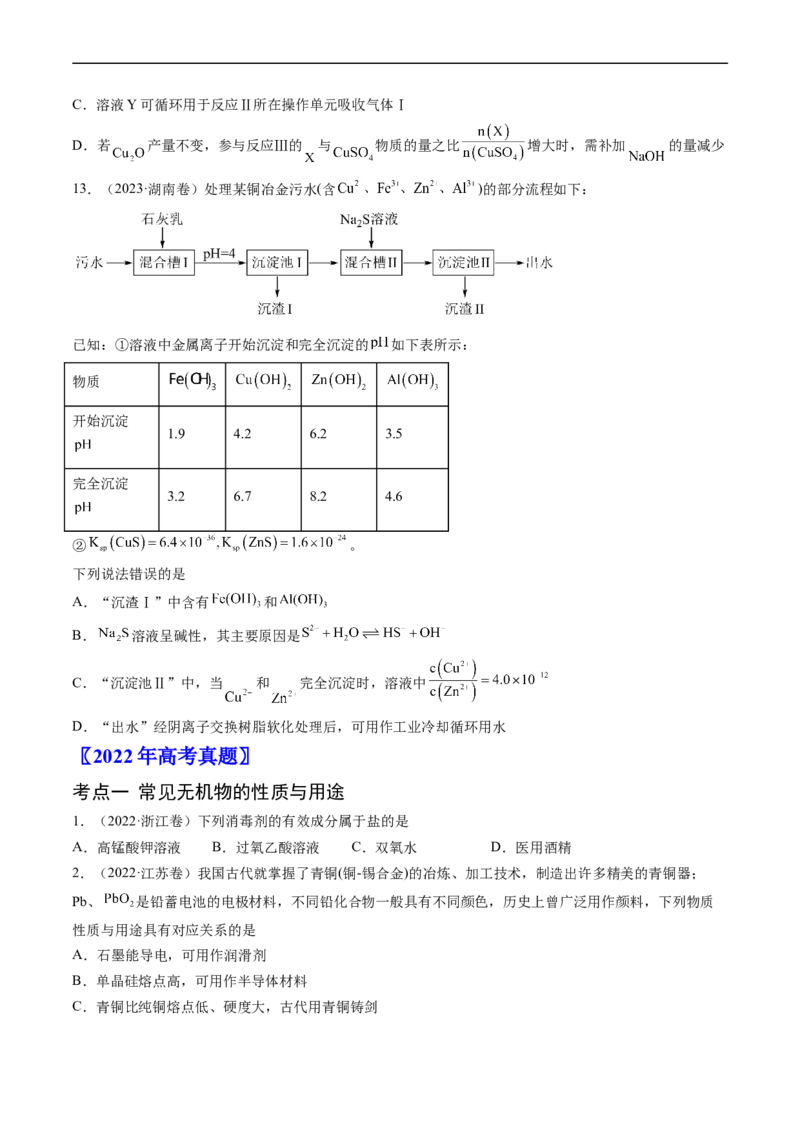
13.(2023·湖南卷)处理某铜冶金污水(含 )的部分流程如下:
已知:①溶液中金属离子开始沉淀和完全沉淀的 如下表所示:
物质
开始沉淀
1.9 4.2 6.2 3.5
完全沉淀
3.2 6.7 8.2 4.6
② 。
下列说法错误的是
A.“沉渣Ⅰ”中含有 和
B. 溶液呈碱性,其主要原因是
C.“沉淀池Ⅱ”中,当 和 完全沉淀时,溶液中
D.“出水”经阴离子交换树脂软化处理后,可用作工业冷却循环用水
〖2022年高考真题〗
考点一 常见无机物的性质与用途
1.(2022·浙江卷)下列消毒剂的有效成分属于盐的是
A.高锰酸钾溶液 B.过氧乙酸溶液 C.双氧水 D.医用酒精
2.(2022·江苏卷)我国古代就掌握了青铜(铜-锡合金)的冶炼、加工技术,制造出许多精美的青铜器;
Pb、 是铅蓄电池的电极材料,不同铅化合物一般具有不同颜色,历史上曾广泛用作颜料,下列物质
性质与用途具有对应关系的是
A.石墨能导电,可用作润滑剂
B.单晶硅熔点高,可用作半导体材料
C.青铜比纯铜熔点低、硬度大,古代用青铜铸剑D.含铅化合物颜色丰富,可用作电极材料
3.(2022·福建卷)福建多个科研机构经过长期联合研究发现,使用 和改性的 基催化剂,可打通从
合成气经草酸二甲酯常压催化加氢制备乙二醇的技术难关。下列说法正确的是
A.草酸属于无机物 B. 与石墨互为同分异构体
C. 属于过渡元素 D.催化剂通过降低焓变加快反应速率
4.(2022·海南卷)化学与日常生活息息相关。下列说法错误的是
A.使用含氟牙膏能预防龋齿 B.小苏打的主要成分是
C.可用食醋除去水垢中的碳酸钙 D.使用食品添加剂不应降低食品本身营养价值
5.(2022·江苏卷)氮及其化合物的转化具有重要应用。下列说法不正确的是
A.自然固氮、人工固氮都是将 转化为
B.侯氏制碱法以 、 、 、 为原料制备 和
C.工业上通过 催化氧化等反应过程生产
D.多种形态的氮及其化合物间的转化形成了自然界的“氮循环”
6.(2022·北京卷)2022年3月神舟十三号航天员在中国空间站进行了“天宫课堂”授课活动。其中太空
“冰雪实验”演示了过饱和醋酸钠溶液的结晶现象。下列说法不正确的是
A.醋酸钠是强电解质
B.醋酸钠晶体与冰都是离子晶体
C.常温下,醋酸钠溶液的
D.该溶液中加入少量醋酸钠固体可以促进醋酸钠晶体析出
7.(2022·浙江卷)下列说法不正确的是
A.晶体硅的导电性介于导体和绝缘体之间,常用于制造光导纤维
B.高压钠灯发出的黄光透雾能力强、射程远,可用于道路照明
C.氧化铝熔点高,常用于制造耐高温材料
D.用石灰右-石膏法对燃煤烟气进行脱硫,同时可得到石膏
8.(2022·浙江卷)下列说法正确的是
A.工业上通过电解六水合氯化镁制取金属镁
B.接触法制硫酸时,煅烧黄铁矿以得到三氧化硫
C.浓硝酸与铁在常温下不能反应,所以可用铁质容器贮运浓硝酸
D.“洁厕灵”(主要成分为盐酸)和“84消毒液”(主要成分为次氯酸钠)不能混用
9.(2022·北京卷)已知: 。下列说法不正确的是A. 分子的共价键是 键, 分子的共价键是 键
B.燃烧生成的 气体与空气中的水蒸气结合呈雾状
C.停止反应后,用蘸有浓氨水的玻璃棒靠近集气瓶口产生白烟
D.可通过原电池将 与 反应的化学能转化为电能
10.(2022·辽宁卷)下列类比或推理合理的是
已知 方法 结论
A 沸点: 类比 沸点:
B 酸性: 类比 酸性:
C 金属性: 推理 氧化性:
D : 推理 溶解度:
考点二 无机物的转化
11.(2022·浙江卷)关于化合物 的性质,下列推测不合理的是
A.与稀盐酸反应生成 、 、
B.隔绝空气加热分解生成FeO、 、
C.溶于氢碘酸(HI),再加 萃取,有机层呈紫红色
D.在空气中,与 高温反应能生成
12.(2022·广东卷)劳动开创未来。下列劳动项目与所述的化学知识没有关联的是
选
劳动项目 化学知识
项
A 面包师用小苏打作发泡剂烘焙面包 Na 2 CO 3可与酸反应
B 环保工程师用熟石灰处理酸性废水 熟石灰具有碱性
C 工人将模具干燥后再注入熔融钢水 铁与 H 2 O 高温下会反应D 技术人员开发高端耐腐蚀镀铝钢板 铝能形成致密氧化膜
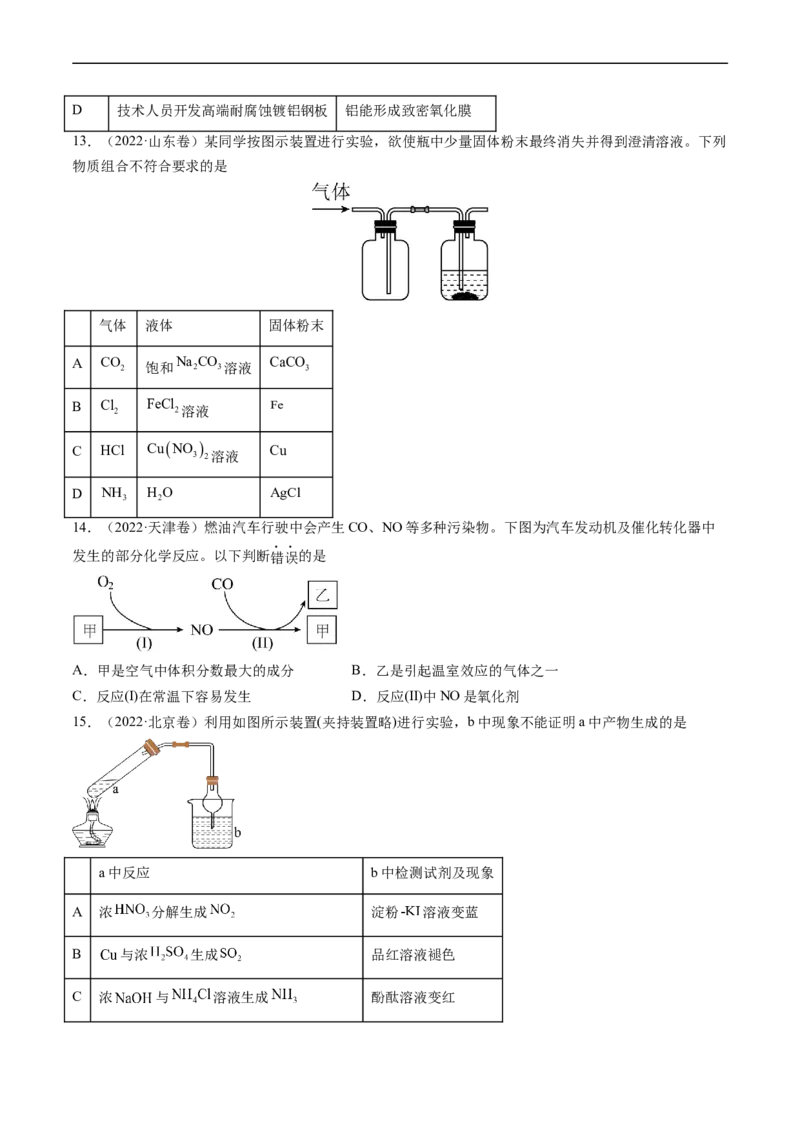
13.(2022·山东卷)某同学按图示装置进行实验,欲使瓶中少量固体粉末最终消失并得到澄清溶液。下列
物质组合不符合要求的是
气体 液体 固体粉末
A CO 2 饱和 Na 2 CO 3溶液 CaCO 3
B Cl FeCl Fe
2 2溶液
C HCl
CuNO
Cu
3 2溶液
D NH H O AgCl
3 2
14.(2022·天津卷)燃油汽车行驶中会产生CO、NO等多种污染物。下图为汽车发动机及催化转化器中
发生的部分化学反应。以下判断错误的是
A.甲是空气中体积分数最大的成分 B.乙是引起温室效应的气体之一
C.反应(Ⅰ)在常温下容易发生 D.反应(Ⅱ)中NO是氧化剂
15.(2022·北京卷)利用如图所示装置(夹持装置略)进行实验,b中现象不能证明a中产物生成的是
a中反应 b中检测试剂及现象
A 浓 分解生成 淀粉 溶液变蓝
B 与浓 生成 品红溶液褪色
C 浓 与 溶液生成 酚酞溶液变红D 与 乙醇溶液生成丙烯 溴水褪色
16.(2022·广东卷)若将铜丝插入热浓硫酸中进行如图(a~d均为浸有相应试液的棉花)所示的探究实验,
下列分析正确的是
A. 与浓硫酸反应,只体现 的酸性
B.a处变红,说明 是酸性氧化物
C.b或c处褪色,均说明 具有漂白性
D.试管底部出现白色固体,说明反应中无 生成
17.(2022·广东卷)陈述Ⅰ和Ⅱ均正确但不具有因果关系的是
选
陈述Ⅰ 陈述Ⅱ
项
A 用焦炭和石英砂制取粗硅 SiO 2可制作光导纤维
B 利用海水制取溴和镁单质 Br可被氧化, Mg2 可被还原
C 石油裂解气能使溴的 CCl 4溶液褪色 石油裂解可得到乙烯等不饱和烃
D FeCl 3水解可生成 FeOH 3胶体 FeCl 3可用作净水剂
18.(2022·重庆卷)下列叙述正确的是
A.Cl 和Br 分别与Fe2+反应得到Cl-和Br-
2 2
B.Na和Li分别在O 中燃烧得到NaO和LiO
2 2 2
C.1molSO 与1molNO 分别通入1L水中可产生相同浓度的HSO 和HNO
3 2 2 4 3
D.0.1mol•L-1醋酸和0.1mol•L-1硼酸分别加入适量NaCO 中均可得到CO 和HO
2 3 2 2
考点三 微型工艺流程题
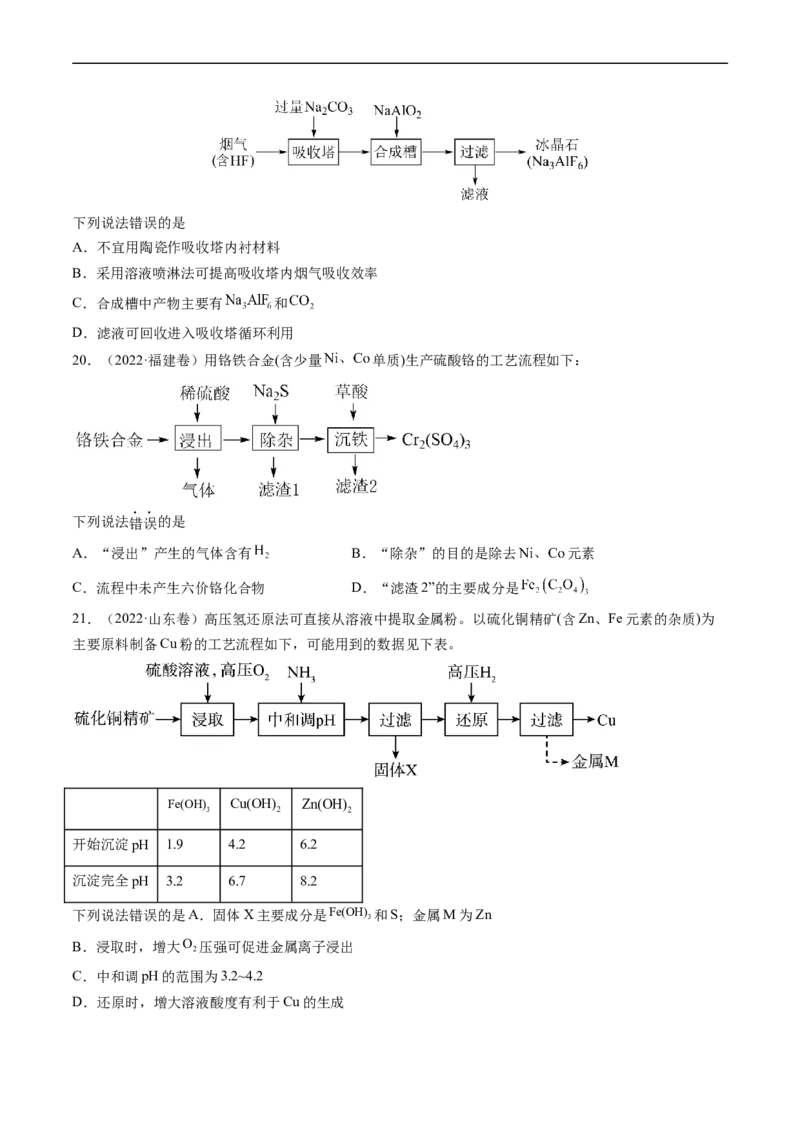
19.(2022·湖南卷)铝电解厂烟气净化的一种简单流程如下:下列说法错误的是
A.不宜用陶瓷作吸收塔内衬材料
B.采用溶液喷淋法可提高吸收塔内烟气吸收效率
C.合成槽中产物主要有 和
D.滤液可回收进入吸收塔循环利用
20.(2022·福建卷)用铬铁合金(含少量 单质)生产硫酸铬的工艺流程如下:
下列说法错误的是
A.“浸出”产生的气体含有 B.“除杂”的目的是除去 元素
C.流程中未产生六价铬化合物 D.“滤渣2”的主要成分是
21.(2022·山东卷)高压氢还原法可直接从溶液中提取金属粉。以硫化铜精矿(含Zn、Fe元素的杂质)为
主要原料制备Cu粉的工艺流程如下,可能用到的数据见下表。
Fe(OH) Cu(OH) Zn(OH)
3 2 2
开始沉淀pH 1.9 4.2 6.2
沉淀完全pH 3.2 6.7 8.2
下列说法错误的是A.固体X主要成分是Fe(OH) 和S;金属M为Zn
3
B.浸取时,增大O 压强可促进金属离子浸出
2
C.中和调pH的范围为3.2~4.2
D.还原时,增大溶液酸度有利于Cu的生成〖2021年高考真题〗
考点一 常见无机物的性质与用途
22.(2021·浙江)下列说法不正确的是
A.硅酸钠是一种难溶于水的硅酸盐
B.镁在空气中燃烧可生成氧化镁和氮化镁
C.钠与水反应生成氢氧化钠和氢气
D.常温下,铝遇浓硝酸或浓硫酸时会发生钝化
23.(2021·河北)“灌钢法”是我国古代劳动人民对钢铁冶炼技术的重大贡献,陶弘景在其《本草经集注》
中提到“钢铁是杂炼生鍒作刀镰者”。“灌钢法”主要是将生铁和熟铁(含碳量约0.1%)混合加热,生铁熔化灌
入熟铁,再锻打成钢。下列说法错误的是
A.钢是以铁为主的含碳合金
B.钢的含碳量越高,硬度和脆性越大
C.生铁由于含碳量高,熔点比熟铁高
D.冶炼铁的原料之一赤铁矿的主要成分为Fe O
2 3
24.(2021·河北)硫和氮及其化合物对人类生存和社会发展意义重大,但硫氧化物和氮氧化物造成的环境
问题也日益受到关注,下列说法正确的是
A.NO 和SO 均为红棕色且有刺激性气味的气体,是酸雨的主要成因
2 2
B.汽车尾气中的主要大气污染物为NO、SO 和PM2.5
2
C.植物直接吸收利用空气中的NO和NO 作为肥料,实现氮的固定
2
D.工业废气中的SO 可采用石灰法进行脱除
2
25.(2021·河北)关于非金属含氧酸及其盐的性质,下列说法正确的是
A.浓HSO 具有强吸水性,能吸收糖类化合物中的水分并使其炭化
2 4
B.NaClO、KClO 等氯的含氧酸盐的氧化性会随溶液的pH减小而增强
3
C.加热NaI与浓HPO 混合物可制备HI,说明HPO 比HI酸性强
3 4 3 4
D.浓HNO 和稀HNO 与Cu反应的还原产物分别为NO 和NO,故稀HNO 氧化性更强
3 3 2 3
26.(2021·山东)下列由实验现象所得结论错误的是
A.向NaHSO 溶液中滴加氢硫酸,产生淡黄色沉淀,证明HSO 具有氧化性
3
B.向酸性KMnO 溶液中加入Fe O 粉末,紫色褪去,证明Fe O 中含Fe(Ⅱ)
4 3 4 3 4
C.向浓HNO 中插入红热的炭,产生红棕色气体,证明炭可与浓HNO 反应生成NO
3 3 2
D.向NaClO溶液中滴加酚酞试剂,先变红后褪色,证明NaClO在溶液中发生了水解反应
考点二 无机物的转化
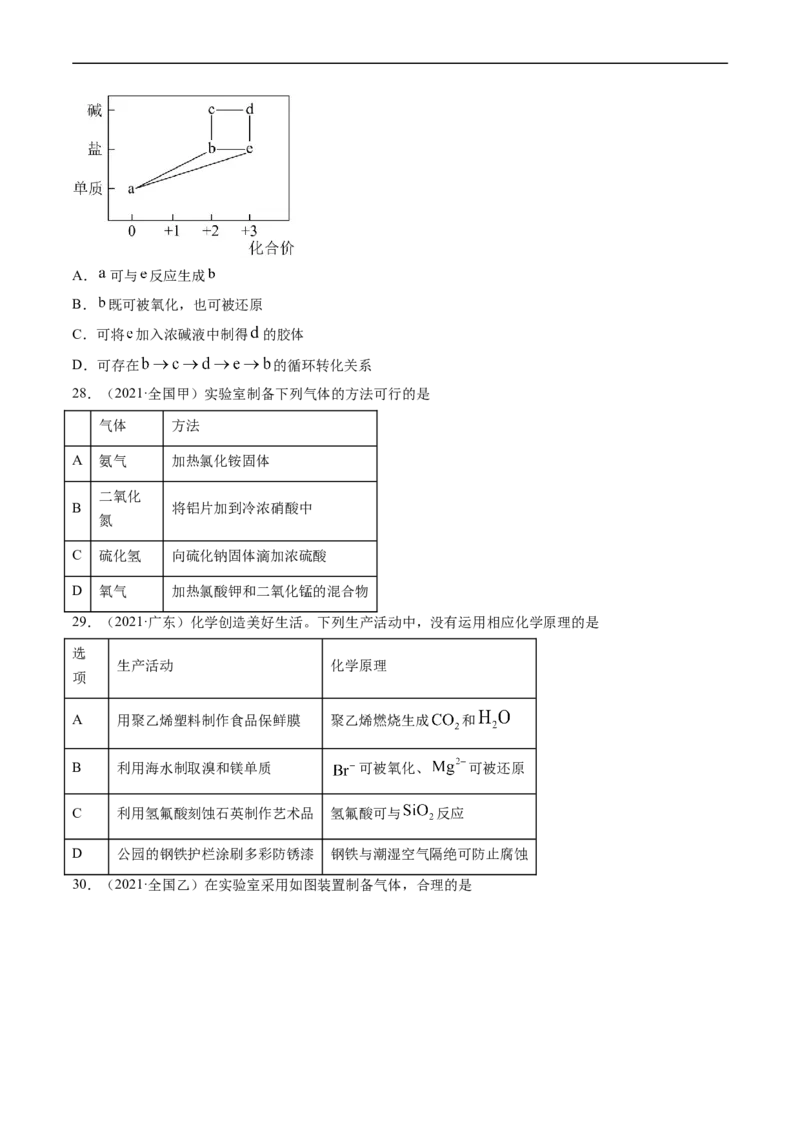
27.(2021·广东)部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的是A. 可与 反应生成
B. 既可被氧化,也可被还原
C.可将 加入浓碱液中制得 的胶体
D.可存在 的循环转化关系
28.(2021·全国甲)实验室制备下列气体的方法可行的是
气体 方法
A 氨气 加热氯化铵固体
二氧化
B 将铝片加到冷浓硝酸中
氮
C 硫化氢 向硫化钠固体滴加浓硫酸
D 氧气 加热氯酸钾和二氧化锰的混合物
29.(2021·广东)化学创造美好生活。下列生产活动中,没有运用相应化学原理的是
选
生产活动 化学原理
项
A 用聚乙烯塑料制作食品保鲜膜 聚乙烯燃烧生成 和
B 利用海水制取溴和镁单质 可被氧化、 可被还原
C 利用氢氟酸刻蚀石英制作艺术品 氢氟酸可与 反应
D 公园的钢铁护栏涂刷多彩防锈漆 钢铁与潮湿空气隔绝可防止腐蚀
30.(2021·全国乙)在实验室采用如图装置制备气体,合理的是化学试剂 制备的气体
A
B (浓)
C
D (浓)
考点三 微型工艺流程题
31.(2021·山东)工业上以SO 和纯碱为原料制备无水NaHSO 的主要流程如图,下列说法错误的是
2 3
A.吸收过程中有气体生成 B.结晶后母液中含有NaHCO
3
C.气流干燥湿料时温度不宜过高 D.中和后溶液中含NaSO 和NaHCO
2 3 3
〖2020年高考真题〗
考点一 常见无机物的性质与用途
32.(2020·新课标Ⅰ)国家卫健委公布的新型冠状病毒肺炎诊疗方案指出,乙醚、75%乙醇、含氯消毒剂、
过氧乙酸(CHCOOOH)、氯仿等均可有效灭活病毒。对于上述化学药品,下列说法错误的是
3
A.CHCHOH能与水互溶
3 2
B.NaClO通过氧化灭活病毒
C.过氧乙酸相对分子质量为76
D.氯仿的化学名称是四氯化碳
33.(2020·江苏卷)下列有关物质的性质与用途具有对应关系的是
A.铝的金属活泼性强,可用于制作铝金属制品
B.氧化铝熔点高,可用作电解冶炼铝的原料
C.氢氧化铝受热分解,可用于中和过多的胃酸D.明矾溶于水并水解形成胶体,可用于净水
34.(2020·浙江卷)水溶液呈酸性的是( )
A.NaCl B.NaHSO C.HCOONa D.NaHCO
4 3
35.(2020·浙江卷)下列说法不正确的是( )
A.天然气是不可再生能源
B.用水煤气可合成液态碳氢化合物和含氧有机物
C.煤的液化属于物理变化
D.火棉是含氮量高的硝化纤维
36.(2020·浙江卷)下列说法不正确的是( )
A.Cl−会破坏铝表面的氧化膜
B.NaHCO 的热稳定性比NaCO 强
3 2 3
C.KMnO 具有氧化性,其稀溶液可用于消毒
4
D.钢铁在潮湿空气中生锈主要是发生了电化学腐蚀
37.(2020·浙江卷)下列说法不正确的是( )
A.高压钠灯可用于道路照明
B.二氧化硅可用来制造光导纤维
C.工业上可采用高温冶炼黄铜矿的方法获得粗铜
D.碳酸钡不溶于水,可用作医疗上检查肠胃的钡餐
38.(2020·浙江卷)下列说法正确的是( )
A. 在空气中加热可得固体
B. 加入到过量 溶液中可得
C. 在沸腾炉中与 反应主要生成
D. 溶液中加入少量 粉末生成 和
39.(2020·浙江卷)Ca SiO 是硅酸盐水泥的重要成分之一,其相关性质的说法不正确的是( )
3 5
A.可发生反应:
B.具有吸水性,需要密封保存
C.能与SO ,反应生成新盐
2
D.与足量盐酸作用,所得固体产物主要为SiO
2
考点二 无机物的转化
40.(2020·新课标Ⅱ)某白色固体混合物由NaCl、KCl、MgSO 、CaCO 中的两种组成,进行如下实验:①
4 3
混合物溶于水,得到澄清透明溶液;② 做焰色反应,通过钴玻璃可观察到紫色;③ 向溶液中加碱,产生
白色沉淀。根据实验现象可判断其组成为
A.KCl、NaCl B.KCl、MgSO
4
C.KCl、CaCO D.MgSO 、NaCl
3 441.(2020·江苏卷)下列有关化学反应的叙述正确的是
A.室温下,Na在空气中反应生成NaO
2 2
B.室温下,Al与4.0 mol﹒L−1NaOH溶液反应生成NaAlO
2
C.室温下,Cu与浓HNO 反应放出NO气体
3
D.室温下,Fe与浓HSO 反应生成FeSO
2 4 4
42.(2020·江苏卷)下列选项所示的物质间转化均能实现的是
A. (aq) (g) 漂白粉(s)
B. (aq) (s) (s)
C. (aq) (aq) (aq)
D. (s) (aq) (s)
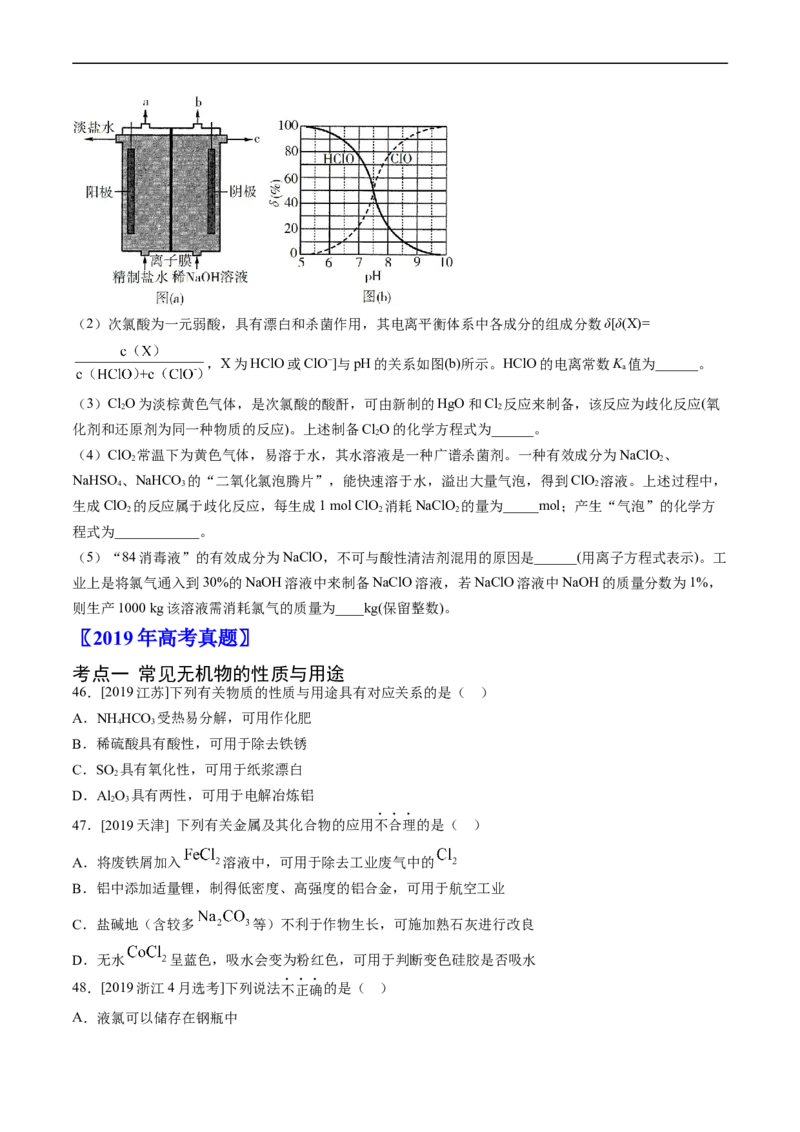
43.(2020·新课标Ⅱ)据文献报道:Fe(CO) 催化某反应的一种反应机理如下图所示。下列叙述错误的是
5
A.OH−参与了该催化循环 B.该反应可产生清洁燃料H
2
C.该反应可消耗温室气体CO D.该催化循环中Fe的成键数目发生变化
2
44.(2020·浙江卷)黄色固体X,可能含有漂白粉、FeSO 、Fe (SO )、CuCl 、KI之中的几种或全部。将X
4 2 4 3 2
与足量的水作用,得到深棕色固体混合物Y和无色碱性溶液Z。下列结论合理的是( )
A.X中含KI,可能含有CuCl
2
B.X中含有漂白粉和FeSO
4
C.X中含有CuCl ,Y中含有Fe(OH)
2 3
D.用HSO 酸化溶液Z,若有黄绿色气体放出,说明X中含有CuCl
2 4 2
45.(2020·新课标Ⅱ)化学工业为疫情防控提供了强有力的物质支撑。氯的许多化合物既是重要化工原料,
又是高效、广谱的灭菌消毒剂。回答下列问题:
(1)氯气是制备系列含氯化合物的主要原料,可采用如图(a)所示的装置来制取。装置中的离子膜只允许
______离子通过,氯气的逸出口是_______(填标号)。(2)次氯酸为一元弱酸,具有漂白和杀菌作用,其电离平衡体系中各成分的组成分数δ[δ(X)=
,X为HClO或ClO−]与pH的关系如图(b)所示。HClO的电离常数K 值为______。
a
(3)ClO为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl 反应来制备,该反应为歧化反应(氧
2 2
化剂和还原剂为同一种物质的反应)。上述制备ClO的化学方程式为______。
2
(4)ClO 常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO、
2 2
NaHSO、NaHCO 的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO 溶液。上述过程中,
4 3 2
生成ClO 的反应属于歧化反应,每生成1 mol ClO 消耗NaClO 的量为_____mol;产生“气泡”的化学方
2 2 2
程式为____________。
(5)“84消毒液”的有效成分为NaClO,不可与酸性清洁剂混用的原因是______(用离子方程式表示)。工
业上是将氯气通入到30%的NaOH溶液中来制备NaClO溶液,若NaClO溶液中NaOH的质量分数为1%,
则生产1000 kg该溶液需消耗氯气的质量为____kg(保留整数)。
〖2019年高考真题〗
考点一 常见无机物的性质与用途
46.[2019江苏]下列有关物质的性质与用途具有对应关系的是( )
A.NH HCO 受热易分解,可用作化肥
4 3
B.稀硫酸具有酸性,可用于除去铁锈
C.SO 具有氧化性,可用于纸浆漂白
2
D.Al O 具有两性,可用于电解冶炼铝
2 3
47.[2019天津] 下列有关金属及其化合物的应用不合理的是( )
A.将废铁屑加入 溶液中,可用于除去工业废气中的
B.铝中添加适量锂,制得低密度、高强度的铝合金,可用于航空工业
C.盐碱地(含较多 等)不利于作物生长,可施加熟石灰进行改良
D.无水 呈蓝色,吸水会变为粉红色,可用于判断变色硅胶是否吸水
48.[2019浙江4月选考]下列说法不正确的是( )
A.液氯可以储存在钢瓶中B.天然气的主要成分是甲烷的水合物
C.天然石英和水晶的主要成分都是二氧化硅
D.硫元素在自然界的存在形式有硫单质、硫化物和硫酸盐等
49.[2019浙江4月选考] 18.下列说法不正确的是( )
A.纯碱和烧碱熔化时克服的化学键类型相同
B.加热蒸发氯化钾水溶液的过程中有分子间作用力的破坏
C.CO 溶于水和干冰升华都只有分子间作用力改变
2
D.石墨转化为金刚石既有共价键的断裂和生成,也有分子间作用力的破坏
考点二 无机物的转化
50.[2019江苏] 下列有关化学反应的叙述正确的是( )
A.Fe在稀硝酸中发生钝化
B.MnO 和稀盐酸反应制取Cl
2 2
C.SO 与过量氨水反应生成(NH )SO D.室温下Na与空气中O
2 4 2 3 2
反应制取NaO
2 2
51.[2019江苏] 在给定条件下,下列选项所示的物质间转化均能实现的是( )
A.NaCl(aq) Cl(g) FeCl (s)
2 2
(aq) Mg(OH) (s) MgO (s)
B.MgCl2 2
C.S(s) SO (g) HSO (aq)
3 2 4
(g) NH (g) NaCO(s)
D.N2 3 2 3