文档内容
3.2.1 水的电离 溶液的酸碱性与 pH 练习(原卷版)
1.最近《科学》杂志评出“十大科技突破”,其中“火星上‘找’到水的影子”名列第一。下列
关于水的说法中正确的是( )
A.水的离子积不仅只适用于纯水,升高温度一定使水的离子积增大
B.水的电离和电解都需要电,常温下都是非自发过程
C.水中氢键的存在既增强了水分子的稳定性,也增大了水的沸点
D.加入电解质一定会破坏水的电离平衡,其中酸和碱通常都会抑制水的电离
2.下列操作可以使水的离子积常数K 增大的是( )
w
A.加热 B.通入少量氯化氢气体
C.通入少量氨气 D.加入少量醋酸钠固体
3.室温时纯水中存在电离平衡:H O H++OH﹣.下列叙述正确的是( )
2
A.升高温度,水的电离程度增大,⇌c(H+)增大,pH<7,溶液显酸性
B.向水中加入少量氨水,平衡逆向移动,抑制水的电离,c(OH﹣)降低
C.向水中加入少量硫酸,c(H+)增大,由水电离出的c(H+)>1×10﹣7mol/L
D.向水中加入少量NH Cl固体,NH +结合水电离出的OH﹣,由水电离出的c(H+)>1×10﹣
4 4
7mol/L
4.下列操作中,能使电离平衡H O H++OH﹣,向逆反应反向移动的是( )
2
A.向水中加入2.0mol/L碳酸钠溶⇌液 B.向水中加入2.0mol/L氢氧化钠溶液
C.向水中加入2.0mol/L氯化钠溶液 D.将水加热到100℃,使pH=6
5.60℃时水的离子积K =3.2×10﹣14,则在60℃时,c(H+)=2×10﹣7mol•L﹣1的溶液( )
w
A.呈酸性 B.呈碱性 C.呈中性 D.无法判断
6.T℃时,NaCl溶液中c(H+)=1×10﹣6mol/L.下列说法正确的是( )
A.该NaCl溶液显酸性 B.该NaCl溶液中K =1×10﹣12
W
C.该NaCl溶液中c(OH﹣)>c(H+) D.该NaCl溶液pH=7
7.100℃时,水的离子积为1×10﹣12,若该温度下某溶液中的H+浓度为1×10﹣7mol/L则该溶液是(
)
A.酸性 B.碱性 C.中性 D.无法判断
8.酸碱度影响鱼类生长发育,饲养罗汉鱼理想pH是6.8~7.2.山西某些地区水的pH低于6.8,饲
养罗汉鱼时可向水中添加少量( )
A.NaCl B.H PO C.NH Cl D.NaHCO
3 4 4 3
9.常温下,某地土壤的pH约为8,则土壤中的c(OH﹣)最接近于多少mol/L( )A.1×10﹣5 B.1×10﹣6 C.1×10﹣8 D.1×10﹣9
10.常温下, pH=3的醋酸和 0.01 mol•L﹣1 NaOH溶液两种溶液中,由水电离产生的氢离子
① ②
浓度之比( : )是( )
① ②
A.1:10 B.1:4 C.10:1 D.无法计算
11.室温下,下列叙述正确的是( )
A.pH=2的盐酸与pH=12的氨水等体积混合后pH>7
B.pH=4的盐酸溶液,稀释至10倍后pH>5
C.0.2mol•L﹣1的醋酸,与等体积水混合后pH=1
D.100℃纯水的pH=6,所以水在100℃时呈酸性
12.常温下,某酸溶液中由水电离出的离子浓度关系为c(H+)•c(OH﹣)=1×10﹣20,该溶液的
pH等于( )
A.1 B.2 C.3 D.4
13.25℃时,pH=2的硫酸中和由水电离出的H+的浓度是( )
A.1×10﹣14mol•L﹣1 B.1×10﹣2mol•L﹣1
C.1×10﹣7mol•L﹣1 D.1×10﹣12mol•L﹣1
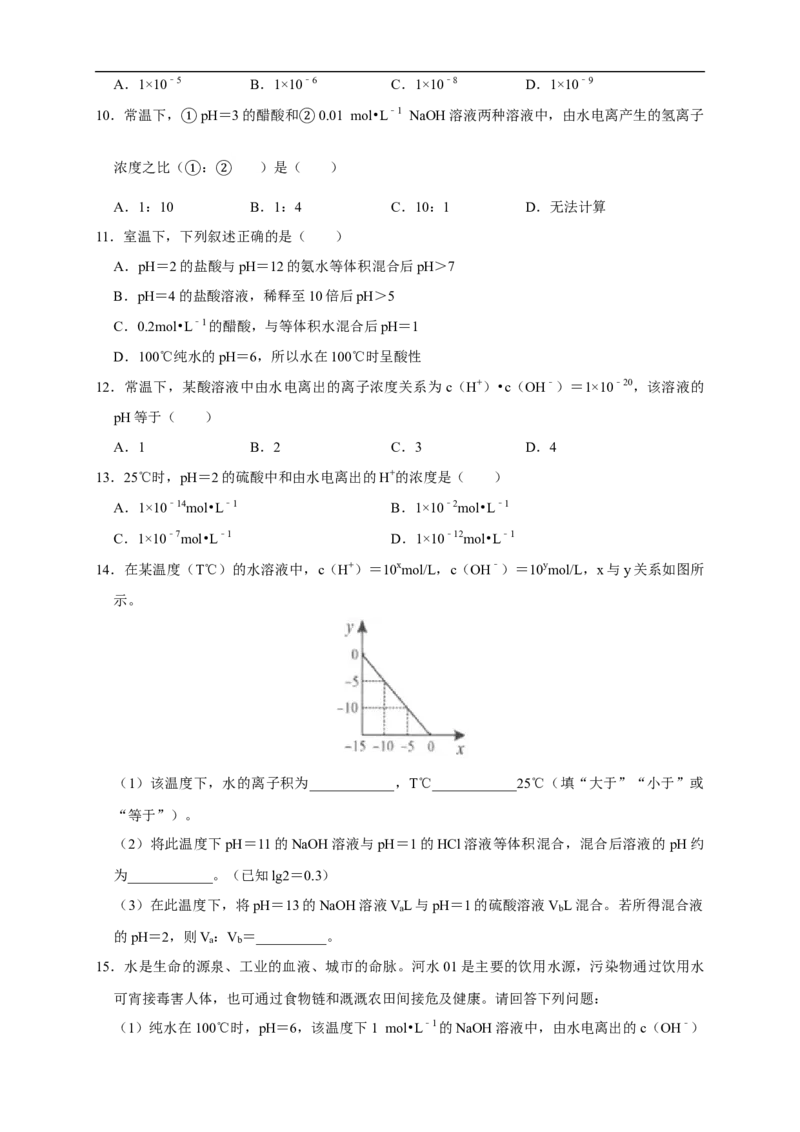
14.在某温度(T℃)的水溶液中,c(H+)=10xmol/L,c(OH﹣)=10ymol/L,x与y关系如图所
示。
(1)该温度下,水的离子积为____________,T℃____________25℃(填“大于”“小于”或
“等于”)。
(2)将此温度下pH=11的NaOH溶液与pH=1的HCl溶液等体积混合,混合后溶液的 pH约
为____________。(已知lg2=0.3)
(3)在此温度下,将pH=13的NaOH溶液VL与pH=1的硫酸溶液V L混合。若所得混合液
a b
的pH=2,则V:V =__________。
a b
15.水是生命的源泉、工业的血液、城市的命脉。河水01是主要的饮用水源,污染物通过饮用水
可宵接毒害人体,也可通过食物链和溉溉农田间接危及健康。请回答下列问题:
(1)纯水在100℃时,pH=6,该温度下1 mol•L﹣1的NaOH溶液中,由水电离出的c(OH﹣)=______________mol•L﹣1。
(2)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解的离
子方程式为_____________。
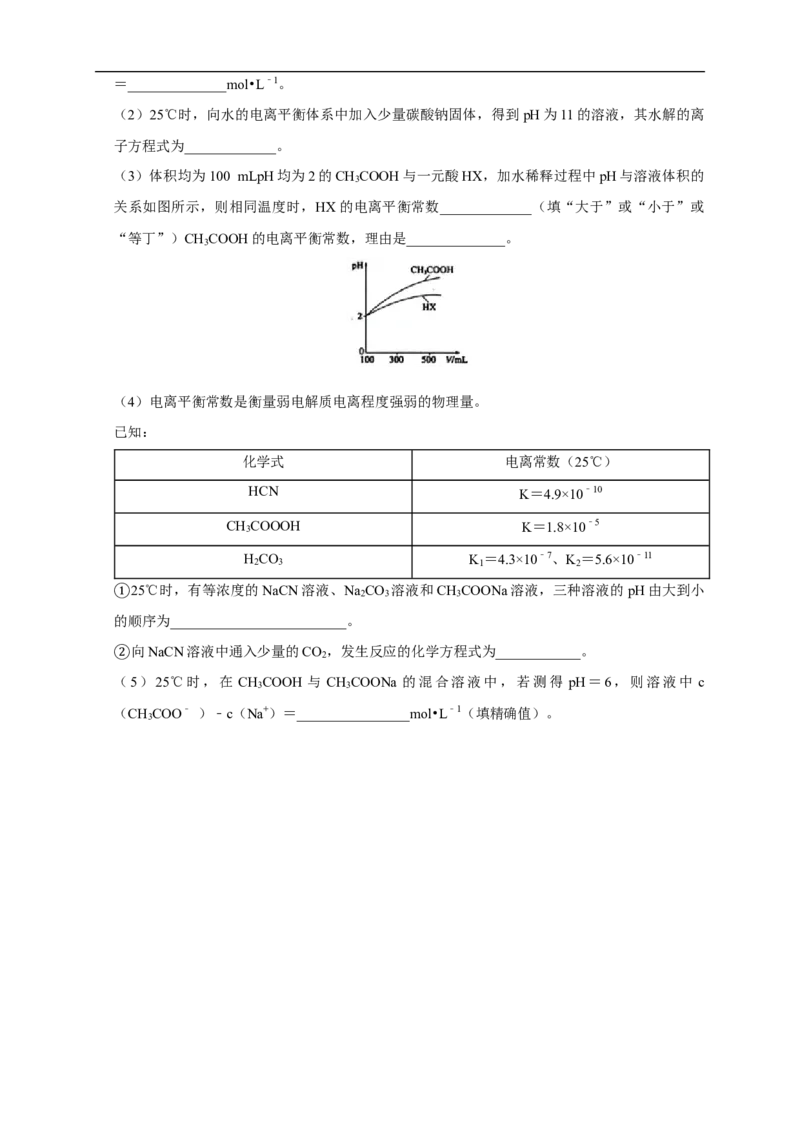
(3)体积均为100 mLpH均为2的CH COOH与一元酸HX,加水稀释过程中pH与溶液体积的
3
关系如图所示,则相同温度时,HX的电离平衡常数_____________(填“大于”或“小于”或
“等丁”)CH COOH的电离平衡常数,理由是______________。
3
(4)电离平衡常数是衡量弱电解质电离程度强弱的物理量。
已知:
化学式 电离常数(25℃)
HCN K=4.9×10﹣10
CH COOOH K=1.8×10﹣5
3
H CO K =4.3×10﹣7、K =5.6×10﹣11
2 3 1 2
25℃时,有等浓度的NaCN溶液、Na CO 溶液和CH COONa溶液,三种溶液的pH由大到小
2 3 3
①的顺序为_________________________。
向NaCN溶液中通入少量的CO ,发生反应的化学方程式为____________。
2
②(5)25℃时,在 CH
3
COOH 与 CH
3
COONa 的混合溶液中,若测得 pH=6,则溶液中 c
(CH COO﹣ )﹣c(Na+)=________________mol•L﹣1(填精确值)。
3