文档内容
更多全科试卷,请关注公众号:高中试卷君
2024 年 1 月“九省联考”考后提升卷(广西卷)
高三化学
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮
擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 O 16 Ca 40 Zn 65
第Ⅰ卷
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.广西新增了一批国家级非物质文化遗产代表性项目,如瑶族祝著节、柳州螺蛳粉制作技艺、北海贝雕、
桂林米粉制作技艺等,下列说法错误的是
A.瑶族祝著节时制甜酒过程发生了化学反应
B.螺蛳粉的螺蛳汤香气四溢,体现了分子是运动的
C.贝雕所用贝壳的主要成分碳酸钙属于有机物
D.桂林米粉中含有的淀粉是一种天然高分子化合物
2.反应 是我国科学家发明的低压高效电催化还原 的新方法。下列有关说法
正确的是
A.氯离子的结构示意图为
B.NaClO的电子式为
C.CO是非极性分子
D. 的结构式为
3.物质结构决定物质性质。下列性质总异与结构因素匹配错误的是更多全科试卷,请关注公众号:高中试卷君
选项 性质差异 结构因素
A 的沸点低于 的沸点 晶体类型
与水互溶, 难溶于
B 分子间氢键
水
C 的沸点低于 分子间作用力
D 的熔点高于 离子半径
4.实验室利用 制备 晶体,下列实验装置和操作能达到实验目的的是
A.利用装置甲制备 B.利用装置乙制备
C.利用装置丙制备 溶液 D.利用装置丁蒸发获得 晶体
5.X、Y、Z、W为原子序数依次增大的短周期主族元素,X的原子半径在短周期主族元素中最小,Y的
单质在空气中含量最大,Z原子的最外层电子数是次外层电子数的3倍。W与Z同主族。下列说法正确的
是
A.第一电离能:
B.分子的极性:
C.同温下,同物质的量浓度水溶液的酸性:
D.键能:
6.有机物M具有优良的生理活性,其结构简式如图所示。下列有关M的说法正确的是更多全科试卷,请关注公众号:高中试卷君
A.属于芳香烃 B.可发生取代反应和加成反应
C.1个M分子中有1个手性碳原子 D.1molM最多消耗4molNaOH
7.HO 在纸张漂白和废水处理等领域有重要应用。一定条件下用H 和O 合成HO 的反应过程如图所示。
2 2 2 2 2 2
设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.1molH O 中含2N σ键,不含π键
2 2 A
B.合成1molH O,电子转移数为4N
2 2 A
C.lmol的HO 含18N 电子
2 2 A
D.标准状况下,4.48LH O 中含有0.2N HO 分子
2 2 A 2 2
8.高铁酸钠 是一种新型绿色消毒剂,主要用于饮用水处理。某化学兴趣小组用废铁屑(主要成
分为 ,杂质有 及油脂)制备高铁酸钠的主要流程如下。下列说法错误的是
A.“碱浸”可以除去废铁屑中的油脂
B.“滤渣”的主要成分是 和
C.“操作Ⅰ”通入的空气可以用 溶液代替
D.若流程改为先“氧化”后“调 ”,可能会生成
9.下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
实验 现象 结论更多全科试卷,请关注公众号:高中试卷君
白色粉末变成了 与 发生化
A 向碳酸钠固体中加入少量水
晶体
学反应
B 某粉末用酒精润湿后,用玻璃棒蘸取做焰色试验 火焰呈黄色 该粉末一定含钠元素
C 将 固体溶于水,进行导电性实验 溶液可导电 中含有离子键
向 溶液中滴入2滴
先产生白色沉淀
D 溶液,再滴加2滴 后再产生红褐色
沉淀
溶液
10.环氧乙烷( ,简称EO)是一种重要的工业原料和消毒剂。由乙烯经电解制备EO的原理
示意图如下,下列说法中错误的是
A.电极1连接外接电源的正极 B.电极2的电极反应式为:
C.溶液a可能含有两种溶质,溶液b可循环使用D.离子膜可选择性的透过 和
11.下列实验对应的离子方程式不正确的是
A.将碳酸氢钙溶液与过量的澄清石灰水混合:HCO +Ca2++OH﹣=CaCO ↓+H O
3 2
B.将少量SO 通入NaClO溶液:SO +H O+2ClO﹣=SO +2HClO
2 2 2
C.用过量氨水吸收工业尾气中的SO :
2
D.向氨水中滴入少量硝酸银溶液:Ag++2NH•H O=[Ag(NH)]++2H O
3 2 3 2 2
12.砷化镉晶胞结构如图,图1中“①”和“②”位是“真空”,晶胞参数为apm,建立如图2,①号位
的坐标为( , , )。已知:砷化镉的摩尔质量为Mg·mol-1,N 为阿伏加德罗常数的值,下列说法错误
A更多全科试卷,请关注公众号:高中试卷君
的是
A.砷化镉中Cd与As原子个数比为3:2 B.两个Cd原子间最短距离为0.5a pm
C.③号位原子坐标参数为( ,1, ) D.该晶胞的密度为N (a×10—10)3g·cm-3
A
13.工业上用乙苯与 生产苯乙烯,主要反应:
① (g) (g)+H(g)
2
②
在一定压强和催化剂作用下,向恒容容器中充入等物质的量的乙苯和 。达到平衡时,各物质的体积分
数随温度的变化如图所示。
下列说法不正确的是
A.当反应混合气体的平均相对分子质量不再变化时,反应达到化学平衡状态
B.苯乙烯和 的体积分数变化差异的主要原因是 消耗
C.乙苯的平衡转化率随温度升高而升高,宜采用700℃获得更多的苯乙烯
D.温度越高,乙苯脱氢生成苯乙烯的反应的K越大
14.乙二胺(H NCH CHNH )有类似于NH 的性质。25℃时,向0.01mol/L乙二胺溶液中通入HCl气体,所
2 2 2 2 3更多全科试卷,请关注公众号:高中试卷君
得溶液(忽略溶液体积的变化)的pH与体系中含N微粒浓度的对数值( )、反应物的物质的量之比
关系如下图所示。下列有关说法正确的是
A.图中曲线Y表示 B.P 所示溶液:
3
C.P 所示溶液: D.图中M点对应的
4
第Ⅱ卷
二、非选择题:本题共4小题,共58分。
15.(14分)《自然》杂志公布最新科学研究成果:碘化镍(NiI )在二维形式上具有多铁性。某小组以废
2
镍催化剂(主要成分是Ni,含少量Zn、Fe、CaO、SiO 等杂质)为原料制备碘化镍的流程如下:
2
请回答下列问题:
(1)滤渣1的成分是CaSO、 (填化学式)。滤渣2经过洗涤、干燥、 (填操作名称)可制铁红。
4
(2)“除铁"中可通过先加入HO 溶液再加入NiO替代NaClO溶液, HO 的作用是 (用离子方程式表
2 2 2 2
示)。
(3)“萃取"中,萃取剂的密度小于1 g·cm-3,若在实验室中分离萃取液,操作是 (填操作名称)。
(4)“分解”过程中通入N 的作用是 。
2
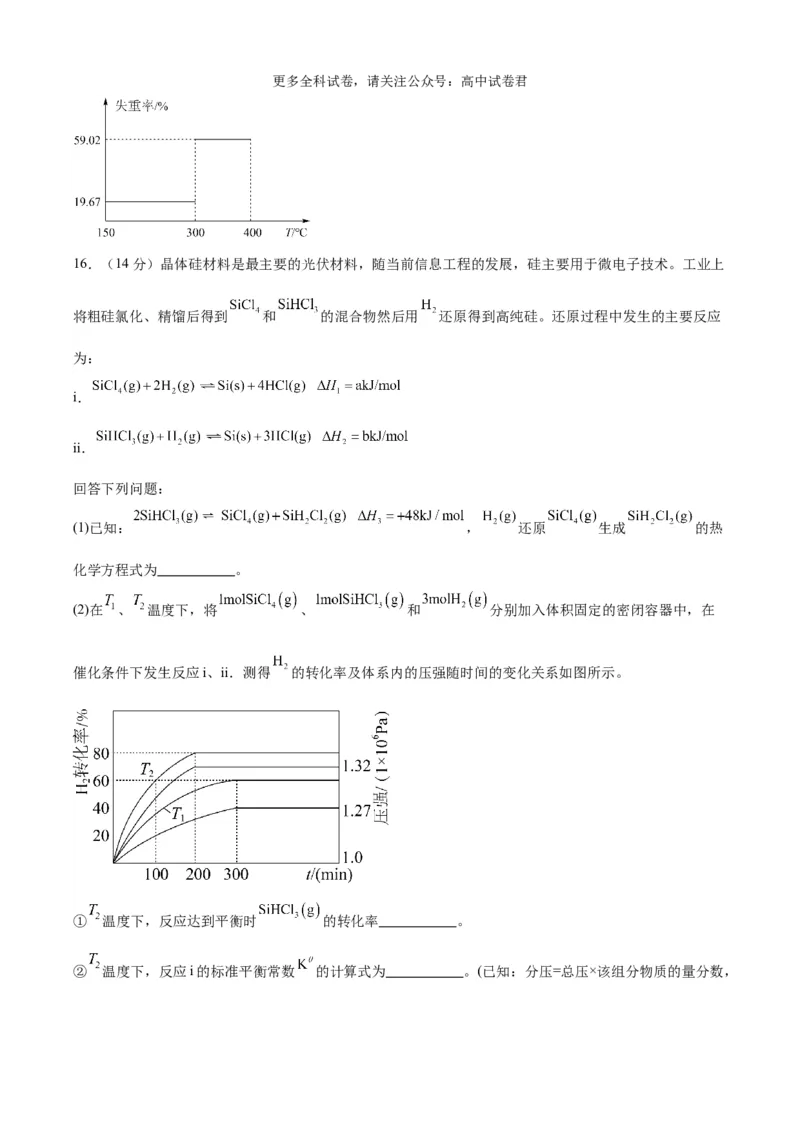
(5)在空气中加热一定量的 NiC O·2H O晶体,测得固体失重率(固体失重率=
2 4 2
×100%)与温度的关系如图所示,300℃发生反应的化学方程式为 。更多全科试卷,请关注公众号:高中试卷君
16.(14分)晶体硅材料是最主要的光伏材料,随当前信息工程的发展,硅主要用于微电子技术。工业上
将粗硅氯化、精馏后得到 和 的混合物然后用 还原得到高纯硅。还原过程中发生的主要反应
为:
i.
ii.
回答下列问题:
(1)已知: , 还原 生成 的热
化学方程式为 。
(2)在 、 温度下,将 、 和 分别加入体积固定的密闭容器中,在
催化条件下发生反应i、ii.测得 的转化率及体系内的压强随时间的变化关系如图所示。
① 温度下,反应达到平衡时 的转化率 。
② 温度下,反应i的标准平衡常数 的计算式为 。(已知:分压=总压×该组分物质的量分数,更多全科试卷,请关注公众号:高中试卷君
对于反应 的 ,其中 , 、 、 、 为各
组分的平衡分压)。
③ 0(填“>”或“<”),写出推理过程 。
(3)研究发现,反应 的活化能 。反应的活化能 、速率
常数k、温度T满足关系: 。
已知: ;ln10=2.3
①若 ,通过升高温度到595K,才能满足 以加快反应速率;
②若T=300K,使用催化剂使活化能降低,满足 以加快反应速率, 应减小。
上述②中 应减小 kJ/mol(保留1位小数);对比①和②你得到的结论是 。
17.(15分)一水硫酸四氨合铜 是一种易溶于水的晶体,可作高效安全的广谱杀菌
剂。回答下列问题
Ⅰ.制备少量晶体 ,设计实验方案如下:
(1)仪器A的名称为 ,对比铜和浓硫酸加热制备硫酸铜,该方案的优点是 。
(2)利用溶液C制备“产物晶体”时,需用玻璃棒摩擦试管内壁的目的是 。
Ⅱ.氨含量的测定。精确称取 g晶体,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入V更多全科试卷,请关注公众号:高中试卷君
10% 溶液,通入水蒸气,将样品液中的氨全部蒸出,并用蒸馏水冲洗导管内壁,用
的盐酸标准溶液完全吸收。取下接收瓶,用 标准溶液滴定过剩的 ,到终点时消耗
溶液。
(3)“玻璃管2”的作用 ,样品中氨的质量分数的表达式 。
Ⅲ.探究四氨合铜离子的性质
用所得晶体配成水溶液,取三份1 试样,分别加入0.5 的水、稀硫酸、氢氧化钠溶液,实验现象记
录如下:
加入试
水 稀硫酸 氢氧化钠
剂
现象 几乎无变化 溶液颜色变成浅蓝色,与同浓度硫酸铜颜色相当
(4)上述实验现象与配位离子的解离平衡有关,请用适当的化学用语表示该配位离子的解离平衡 ,则
加入氢氧化钠溶液后的现象为 。
18.(14分)多环化合物是合成很多药物的中间体,下面是一种多环化合物G的合成路线:
已知:RNH + +2HO
2 2更多全科试卷,请关注公众号:高中试卷君
回答下列问题:
(1)A的分子式为 ,A侧链上的碳原子的杂化类型有 。
(2)由B生成D的反应类型为 。
(3)E中含氧官能团的名称为 ,E→F反应的方程式为 。
(4)C的同分异构体中,同时满足以下两个条件的有 种(考虑碳碳双键的顺反异构)。
ⅰ.除苯环外不含其他的环状结构;
ⅱ.能发生银镜反应。
(5)G的结构简式为 。
(6)结合题中相关信息,设计以 和 为原料制备 的合成路线 (其
他无机试剂任选)。