文档内容
第一章 物质及其变化
第三节 氧化还原反应
第3课时 氧化还原反应的应用
一、选择题
1.飞船以铝粉与高氯酸铵的混合物为固体燃料,其中高氯酸铵的反应为2NH ClO =N ↑+Cl↑+2O↑+
4 4 2 2 2
4HO。下列有关叙述不正确的是( )
2
A.该反应属于分解反应、氧化还原反应
B.上述反应瞬间能产生大量高温气体,推动飞船飞行
C.铝粉的作用是点燃时氧化放热引发高氯酸铵反应
D.在反应中NH ClO 只作氧化剂
4 4
2.关于物质氧化性及还原性的强弱,下列说法中正确的是( )
A.物质越易失电子,还原性越强
B.原子失电子越多,还原性越强
C.元素化合价降低越多,氧化性越强
D.物质越易被氧化,氧化性越强
3.对于反应3Cl+6NaOH5NaCl+NaClO +3H O,以下叙述正确的是( )
2 3 2
A.Cl 是氧化剂,NaOH是还原剂
2
B.被氧化的氯原子和被还原的氯原子的个数之比为5∶1
C.Cl 既做氧化剂又做还原剂
2
D.氧化剂得电子数与还原剂失电子数之比为5∶1
4.ClO 是一种杀菌消毒效率高、二次污染小的水处理剂,实验室中可通过以下反应制得2KClO+HC O
2 3 2 2 4
+HSO 2ClO ↑+KSO +2CO↑+2HO。据此,下列说法不正确的( )
2 4 2 2 4 2 2
A.KClO 发生还原反应
3
B.HC O 在反应中被氧化
2 2 4
C.HC O 的氧化性强于ClO 的氧化性
2 2 4 2
D.ClO 作水处理剂时,利用了其强氧化性
2
5.研究表明:多种海产品体内含有+5价的砷(As)元素,对人体无毒,而砒霜的成分是As O,有剧毒;
2 3
青菜中含有维生素C.专家忠告:不要同时大量食用海鲜和青菜,否则容易中毒。下面有关解释不正确的
是( )
A.As O 中As元素为+3价
2 3B.致人中毒过程中砷元素发生氧化反应
C.维生素C能将+5价砷还原成As O
2 3
D.维生素C具有还原性
6.(2020·元氏县第四中学高一期中)反应2FeCl +2KI═2FeCl +2KCl+I 中氧化产物是( )
3 2 2
A.FeCl B.KCl、I C.I D.KCl
2 2 2
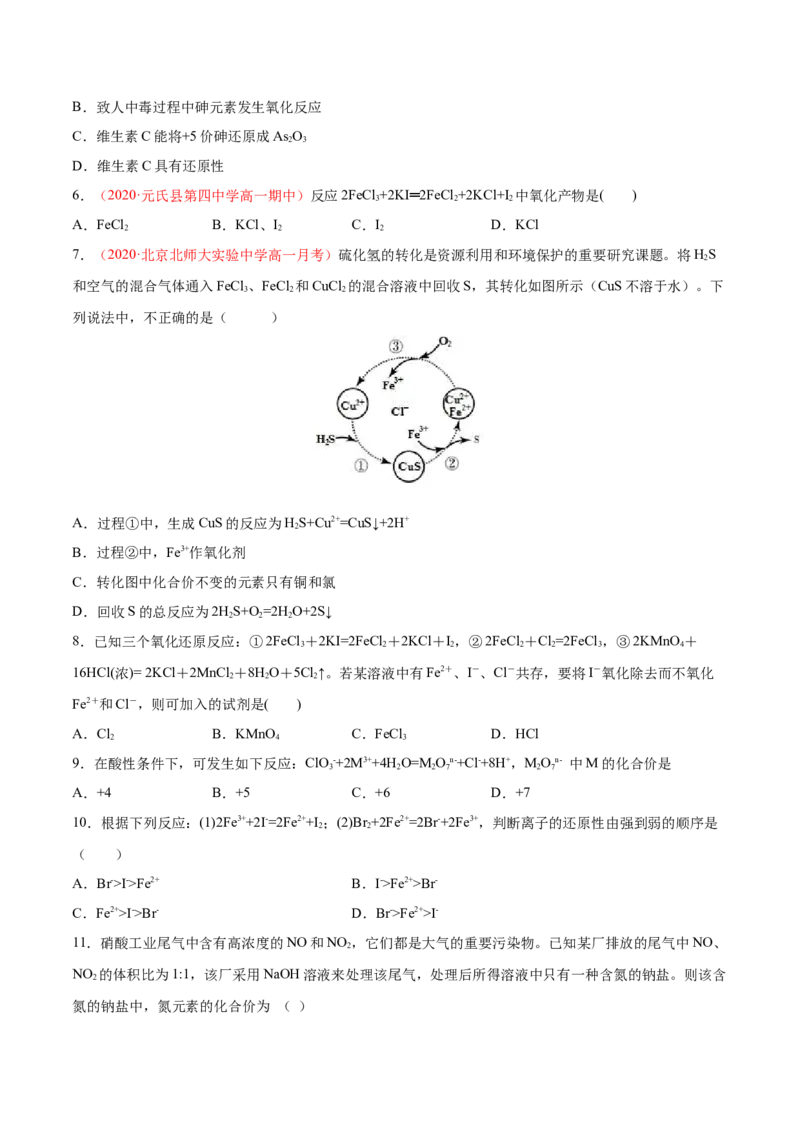
7.(2020·北京北师大实验中学高一月考)硫化氢的转化是资源利用和环境保护的重要研究课题。将HS
2
和空气的混合气体通入FeCl 、FeCl 和CuCl 的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下
3 2 2
列说法中,不正确的是( )
A.过程①中,生成CuS的反应为HS+Cu2+=CuS↓+2H+
2
B.过程②中,Fe3+作氧化剂
C.转化图中化合价不变的元素只有铜和氯
D.回收S的总反应为2HS+O=2H O+2S↓
2 2 2
8.已知三个氧化还原反应:①2FeCl +2KI=2FeCl +2KCl+I,②2FeCl +Cl=2FeCl ,③2KMnO +
3 2 2 2 2 3 4
16HCl(浓)= 2KCl+2MnCl +8HO+5Cl↑。若某溶液中有Fe2+、I-、Cl-共存,要将I-氧化除去而不氧化
2 2 2
Fe2+和Cl-,则可加入的试剂是( )
A.Cl B.KMnO C.FeCl D.HCl
2 4 3
9.在酸性条件下,可发生如下反应:ClO -+2M3++4H O=MOn-+Cl-+8H+,MOn- 中M的化合价是
3 2 2 7 2 7
A.+4 B.+5 C.+6 D.+7
10.根据下列反应:(1)2Fe3++2I-=2Fe2++I ;(2)Br +2Fe2+=2Br-+2Fe3+,判断离子的还原性由强到弱的顺序是
2 2
( )
A.Br->I->Fe2+ B.I->Fe2+>Br-
C.Fe2+>I->Br- D.Br->Fe2+>I-
11.硝酸工业尾气中含有高浓度的NO和NO ,它们都是大气的重要污染物。已知某厂排放的尾气中NO、
2
NO 的体积比为1:1,该厂采用NaOH溶液来处理该尾气,处理后所得溶液中只有一种含氮的钠盐。则该含
2
氮的钠盐中,氮元素的化合价为 ( )A.-3 B.+1 C.+3 D.+5
12.已知Co O 在酸性溶液中易被还原成Co2+,而Co O、Cl、FeCl 、I 的氧化性依次减弱。下列反应在
2 3 2 3 2 3 2
水溶液中不可能发生的是( )
A.Cl+FeI =FeCl +I B.3Cl+6FeI =2FeCl +4FeI
2 2 2 2 2 2 3 3
C.Co O+6HCl=2CoCl +Cl↑+3H O D.2Fe3++2I-=2Fe2++I
2 3 2 2 2 2
13.(2020·全国高一单元测试)在8NH +3Cl=N +6NHCl反应中,被氧化的原子与被还原的原子物质的
3 2 2 4
量之比为
A.8︰3 B.1︰3 C.3︰8 D.3︰1
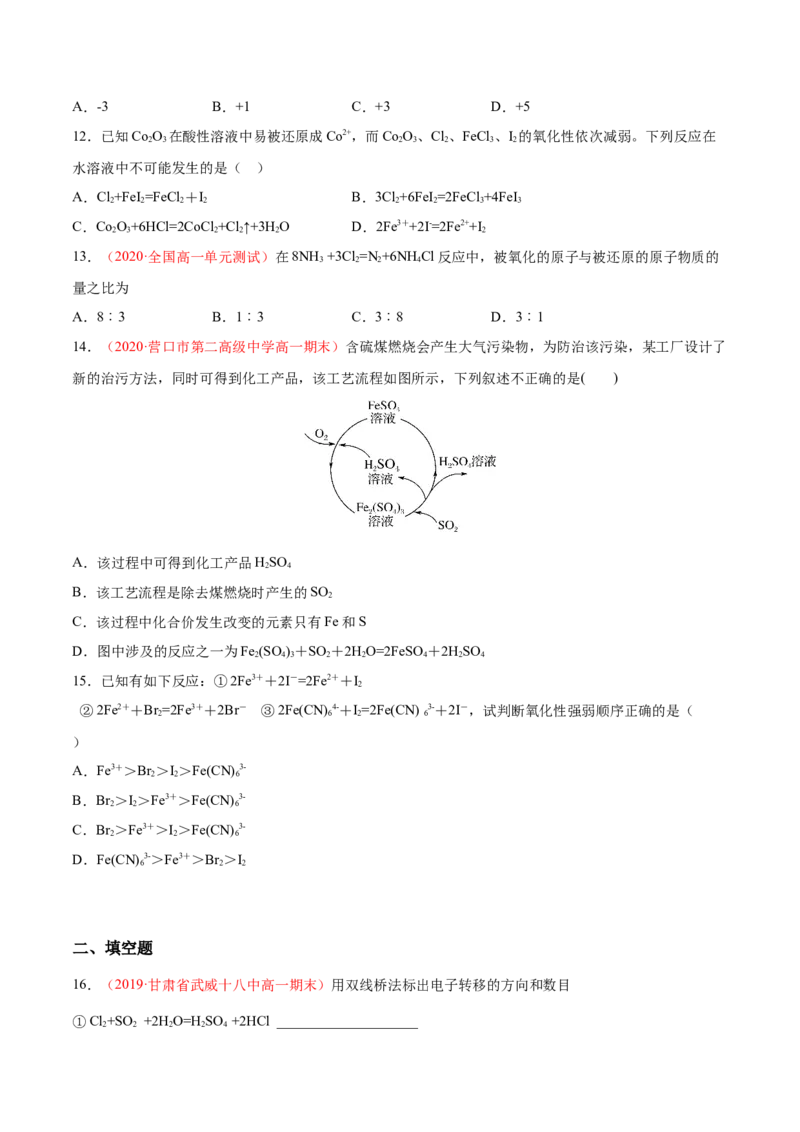
14.(2020·营口市第二高级中学高一期末)含硫煤燃烧会产生大气污染物,为防治该污染,某工厂设计了
新的治污方法,同时可得到化工产品,该工艺流程如图所示,下列叙述不正确的是( )
A.该过程中可得到化工产品HSO
2 4
B.该工艺流程是除去煤燃烧时产生的SO
2
C.该过程中化合价发生改变的元素只有Fe和S
D.图中涉及的反应之一为Fe (SO )+SO +2HO=2FeSO +2HSO
2 4 3 2 2 4 2 4
15.已知有如下反应:①2Fe3++2I-=2Fe2++I
2
②2Fe2++Br =2Fe3++2Br- ③2Fe(CN) 4-+I=2Fe(CN) 3-+2I-,试判断氧化性强弱顺序正确的是(
2 6 2 6
)
A.Fe3+>Br >I>Fe(CN) 3-
2 2 6
B.Br >I>Fe3+>Fe(CN) 3-
2 2 6
C.Br >Fe3+>I>Fe(CN) 3-
2 2 6
D.Fe(CN) 3->Fe3+>Br >I
6 2 2
二、填空题
16.(2019·甘肃省武威十八中高一期末)用双线桥法标出电子转移的方向和数目
①Cl+SO +2H O=HSO +2HCl ____________________
2 2 2 2 4②2NaO+2HO=4NaOH+O↑____________________
2 2 2 2
17.(2020·甘肃省灵台一中高一期中)已知下列反应
①2FeCl +Cl=2FeCl ②Zn+2FeCl =ZnCl +2FeCl ③PbO +4HCl=PbCl +Cl↑+2H O。据此可判断:Cl、
2 2 3 3 2 2 2 2 2 2 2
FeCl 、PbO 、ZnCl 的氧化性由强到弱顺序为_____________(用﹥表示)。
3 2 2
18.利用氧化还原反应原理配平
(1)__NH +___O ____NO +____HO
3 2 2
(2)____FeSO +____KNO+____HSO =____KSO +____Fe (SO )+____NO↑+____HO
4 3 2 4 2 4 2 4 3 2