文档内容
3.1.2 铁的氢氧化物,铁盐亚铁盐 练习(解析版)
1.实验室制取氢氧化铁的一组试剂是( )
A.氯化铁溶液和烧碱溶液 B.氧化铁和烧碱溶液
C.氧化铁和水 D.铁和水蒸气
【答案】A
【详解】
A. 氯化铁溶液和烧碱溶液反应生成氢氧化铁沉淀和氯化钠,A正确;
B. 氧化铁和烧碱溶液不反应,B错误;
C. 氧化铁不溶于水,也不和水反应,C错误;
D. 铁和水蒸气常温下不反应,高温时生成四氧化三铁,D错误;
答案为A。
2.在空气中氢氧化亚铁白色沉淀可转化为红褐色沉淀。关于该反应的下列叙述中不正确的是
A.生成物为氢氧化铁 B.该反应是化合反应
C.该反应是氧化还原反应 D.氢氧化亚铁作氧化剂
【答案】D
【详解】
A.由上述分析知道,氢氧化亚铁白色沉淀转化为红褐色沉淀,生成物是氢氧化铁,故A正确;
B.上述反应符合化合反应的特征,该反应是化合反应,故B正确;
C.该反应中有化合价变化,是氧化还原反应,故C正确;
D.在4Fe(OH) 2HO O=4Fe(OH) 中,氢氧化亚铁作还原剂,O 作氧化剂,故D错误;
2 2 2 3 2
本题答案为D。
3.把一定量铁粉放入FeCl 溶液中,过滤,除去杂质,在滤液中加入适量硝酸,再加入过量氨水,有红褐
3
色沉淀生成。过滤,加热沉淀物至质量不再发生变化,得到红棕色的残渣。上述沉淀和残渣分别为
A.Fe(OH) ;FeO B.Fe(OH) ; Fe O
2 3 2 3
C.Fe O ;Fe(OH) D.Fe(OH) Fe(OH) ; Fe O
2 3 3 3 2 3 4
【答案】B
【详解】
铁粉放入FeCl 溶液中,生成氯化亚铁,加入适量硝酸,把二价铁氧化成三价铁,再加入过量氨水,有红
3
褐色氧氢化铁沉淀生成,氢氧化铁不稳定,加热时分解得到红棕色的残渣是氧化铁,故B正确。
故选B。
4.将过氧化钠投入到氯化亚铁溶液中,可观察到的现象是( )A.最终生成白色沉淀 B.最终生成红褐色沉淀
C.有黄绿色气体产生 D.无明显变化
【答案】B
【详解】
NaO 具有强氧化性,能将氧化成 Fe3+,可与NaO 和水反应生成的 OH-生成红褐色的Fe(OH) 沉淀,
2 2 2 2 3
NaO 与水反应产生O ,不放出黄绿色的Cl ;A.最终生成白色沉淀不符合题意;B.最终生成红褐色沉淀符
2 2 2 2
合题意;C. 有黄绿色气体产生不符合题意;D.无明显变化不符合题意;答案:B。
5.下列有关铁及其化合物的说法正确的是( )
A.铁的氧化物有FeO、Fe O、Fe O,它们都是黑色的固体
2 3 3 4
B.铁的氢氧化物Fe(OH) 、Fe(OH) 的混合物可能是灰绿色
2 3
C.鉴别Fe2+中混有Fe3+,可先加入Cl 水,再加入KSCN溶液
2
D.铁的合金生铁比纯铁硬度大,熔点高。
【答案】B
【详解】
A、FeO为黑色,Fe O 为红棕色,Fe O 为黑色晶体,故A错误;
2 3 3 4
B、氢氧化亚铁为白色絮状沉淀,氢氧化铁为红褐色沉淀,两者混合有可能是灰绿色,故B说法正确;
C、先加入Cl ,将Fe2+氧化成Fe3+,Fe2+对实验产生干扰,应先加KSCN溶液,如果溶液显红色,说明含
2
有Fe3+,故C错误;
D、生铁是合金,其硬度比纯铁大,但熔点比纯铁低,故D错误;
答案选B。
6.为了检验某FeCl 溶液是否变质,可向溶液中加入( )
2
A.KSCN溶液 B.铁片 C.NaOH溶液 D.石蕊溶液
【答案】A
【详解】
A.Fe2+与KSCN不反应,而Fe3+与KSCN溶液反应生成血红色络合物,反应现象明显,因此可以用 KSCN
溶液检验溶液是否变质,A合理;
B.铁片与Fe2+不能反应,而与 Fe3+反应产生Fe2+,反应现象不明显,因此铁片只能使变质的 Fe3+转化为
Fe2+,不能用于检验溶液是否变质,B不合理;
C.Fe2+与OH-反应产生Fe(OH) 白色沉淀,Fe(OH) 不稳定,容易被溶解在溶液中的空气氧化产生红褐色的
2 2
Fe(OH) 沉淀,因此看到的现象是沉淀由白色迅速变为灰绿色,最后变为红褐色,因此不容易观察到 FeCl
3 2
溶液是否变质,C不合理;D.FeCl 、FeCl 都是强酸弱碱盐,金属阳离子发生水解反应使溶液显酸性,因此都可以使石蕊溶液变为红
2 3
色,因此不能检验是否变质,D不合理;
故合理选项是A。
7.往FeCl 溶液中滴加溴水,溶液变为黄色,下列说法正确的是
2
A.由于溶液存在Br ,所以溶液为黄色
2
B.往所得溶液中加入硫氰化钾溶液,可判断是否生成了Fe3+
C.往所得溶液中加入足量氢氧化钾溶液,不能判断是否生成了Fe3+
D.往所得溶液中加入淀粉碘化钾溶液,可判断是否生成了Fe3+
【答案】B
【详解】
A. 溶液为黄色是亚铁离子被氧化为铁离子,即使溴水不过量,溶液也是黄色的,A错误;
B. 往所得溶液中加入硫氰化钾溶液,溶液变血红色,可判断生成了Fe3+,B正确;
C. 往所得溶液中加入足量氢氧化钾溶液,如果立即生成红褐色沉淀,能判断生成了Fe3+,C错误;
D. 往所得溶液中加入淀粉碘化钾溶液,由于铁离子和单质溴都能把碘化钾氧化为单质,因此不能据此判
断是否生成了Fe3+,D错误;
答案选B。
8.对铁及其化合物的叙述不正确的是( )
A.可用KSCN溶液检验Fe3+ B.Fe(OH) 能在空气中稳定存在
2
C.Fe能从CuSO 溶液中置换出Cu D.Fe O 与Al可发生铝热反应
4 2 3
【答案】B
【详解】
A.加入KSCN溶液,溶液呈血红色,证明有铁离子,故A正确;
B.氢氧化亚铁为白色固体,不稳定,易被空气中氧气氧化生成红褐色氢氧化铁,不能稳定存在,故 B错
误;
C.铁的活动性大于铜,所以铁可以从CuSO 溶液中置换出铜,故C正确;
4
D.在金属活动顺序表中,铝排在铁的前面,铝比铁的活泼性强,铁的氧化物能在高温下与 Al发生铝热反
应,故D正确;
故选B。
9.阅读下面科普信息,回答问题:
一个体重50kg的健康人含铁2 g,这2g铁在人体中以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血
者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是____。
A.Fe B.Fe2+ C.Fe3+
(2)工业盐的主要成分是NaNO ,曾多次发生过因误食NaNO 而中毒的事件,其原因是NaNO 把人体内
2 2 2
的Fe2+转化为Fe3+而失去与O 结合的能力,这说明NaNO 具有___性。下列不能实现上述转化的物质是
2 2
____。
A.Cl B.O C.FeCl D.KMnO (H+)
2 2 3 4
(3)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有_____性。
(4)在Fe+4HNO(稀)===Fe(NO ) +NO↑+2HO的反应中,HNO 表现了____性和_____性,则56g Fe参
3 3 3 2 3
加反应时,被还原的HNO 为____g。
3
【答案】B 氧化 C 还原 酸 氧化 63
【详解】
(1)最高价态的粒子只有氧化性,最低价态的粒子只有还原性,中间价态的粒子既有氧化性又有还原性,
故选B;
(2)Fe2+→Fe3+发生了氧化反应,故NaNO 具有氧化性,所以实现此转化也应选择具有强氧化性的物质,
2
而FeCl 与Fe2+不能反应,故FeCl 不能实现上述转化;
3 3
(3)缓解中毒,则应能使Fe3+→Fe2+,所以维生素C具有还原性;
(4)Fe和HNO 的反应中,一部分HNO 起氧化作用,生成NO,另一部分则起酸性作用生成Fe(NO ) ,
3 3 3 3
由化学方程式可知,1molFe还原1molHNO,所以56g Fe参加反应时,被还原的HNO 为63g。
3 3
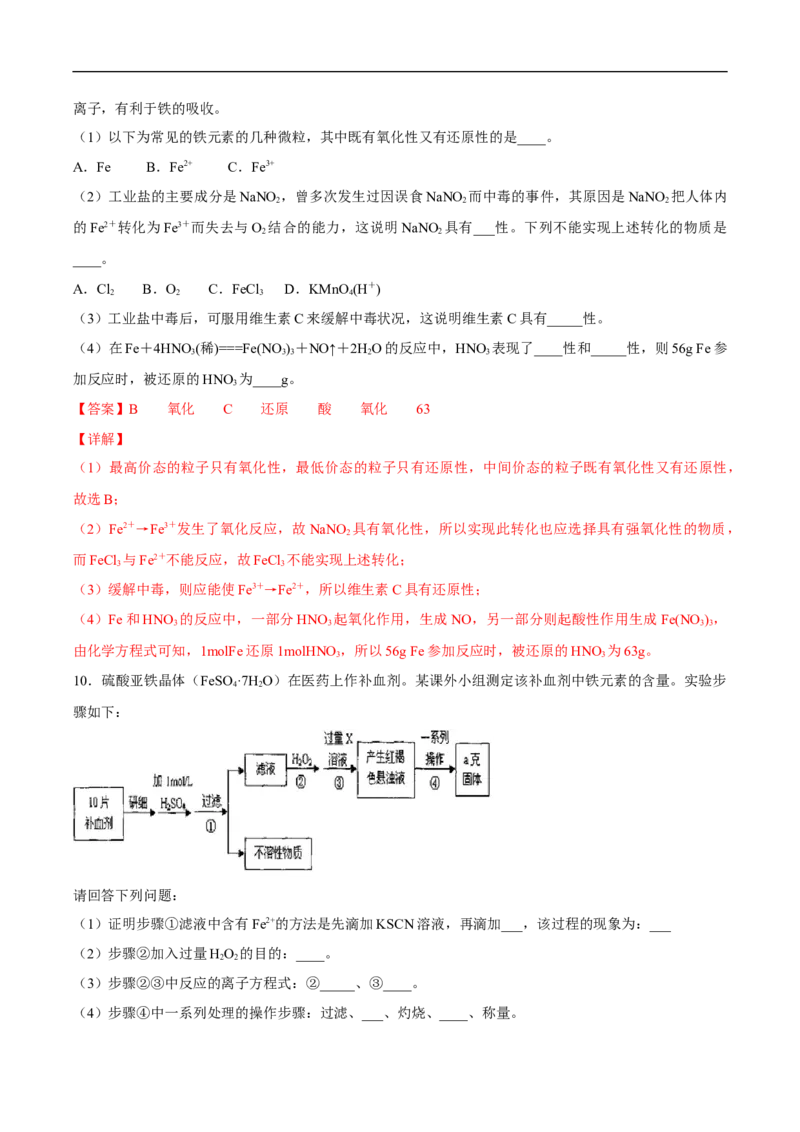
10.硫酸亚铁晶体(FeSO ·7H O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量。实验步
4 2
骤如下:
请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是先滴加KSCN溶液,再滴加___,该过程的现象为:___
(2)步骤②加入过量HO 的目的:____。
2 2
(3)步骤②③中反应的离子方程式:②_____、③____。
(4)步骤④中一系列处理的操作步骤:过滤、___、灼烧、____、称量。(5)若实验无损耗,则每片补血剂含铁元素的质量___g。
【答案】氯水或双氧水 溶液由浅绿色变为血红色 将亚铁离子氧化为三价铁离子 HO+2Fe2+
2 2
+2H+=2Fe3++2H O = ↓或 = ↓ 洗涤 冷
2
却
【详解】
(1) 遇KSCN溶液显红色,该现象用于检验 存在,可以加入氧化剂将 氧化为 。检验
可以先滴加KSCN溶液,溶液不变色,再滴加氯水或双氧水,溶液变为血红色,说明含有 ;
(2)双氧水具有氧化性,酸性条件下能将 全部氧化为 ;
(3)步骤②是使用双氧水氧化二价铁离子,方程式为HO+2Fe2++2H+=2Fe3++2H O,步骤③是调节溶液
2 2 2
pH使三价铁离子沉淀,方程式为 = ↓或 = ↓ ;
(4)步骤④中一系列处理的操作步骤为过滤、洗涤、灼烧、冷却、称量;
(5)ag 氧化铁中铁元素的质量即为 10 片补血剂中铁的质量,所以每片补血剂含铁元素的质量
。