文档内容
第七章第一节认识有机化合物小题训练--人教版(2019)必
修第二册
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.关于CH=CH-CH=CH 的说法错误的是
2 2
A.与2-丁炔互为同分异构体 B.是乙烯的同系物
C.可使酸性高锰酸钾溶液褪色 D.与氢气反应,可能生成三种产物
2.有关CHCOOH及其组成元素的说法错误的是
3
A.中子数为8的碳原子可表示为:
B.O2-的结构示意图:
C. 、 、 互为同位素
D.CHCOOH的电离方程式:CHCOOH CHCOO-+H+
3 3 3
3.化学与生活、生产及科技密切相关,下列有关说法正确的是
A.为防控新冠病毒,将“84”消毒液与酒精1∶1混合,消毒效果更好
B.“天宫二号”空间实验室的硅电池板将光能直接转化为电能
C.利用明矾净水,可以达到杀菌消毒和沉淀悬浮物的目的
D.“天宫”空间站使用石墨烯存储器,石墨烯与金刚石互为同分异构体
4.短周期主族元素X、Y、Z的原子序数依次增大,X元素最外层电子数是电子层数
的2倍,Y元素在元素周期表中的周期数等于族序数,Y能溶于Z的最高价氧化物对
应水化物的稀溶液,而不溶于其浓溶液。下列说法不正确的是
A.原子半径:Z>Y>X B.X是形成化合物种类最多的元素
C.Y最高价氧化物具有很高的熔点 D.实验室可用XZ 清洗装有硫磺的试管
2
5.认识和掌握物质结构研究的范式与方法,具有极为重要的意义。下列有关说法正确
的是
A.由元素周期表发现新的元素属于归纳范式
B.通过甲烷(CH)乙烷(C H)、丙烷(C H)、丁烷(C H )的分子式,总结出饱和烷烃的
4 2 6 3 8 4 10
通式为C H ,属于演绎范式
n 2n+2
C.实验方法只能通过化学实验才能实现
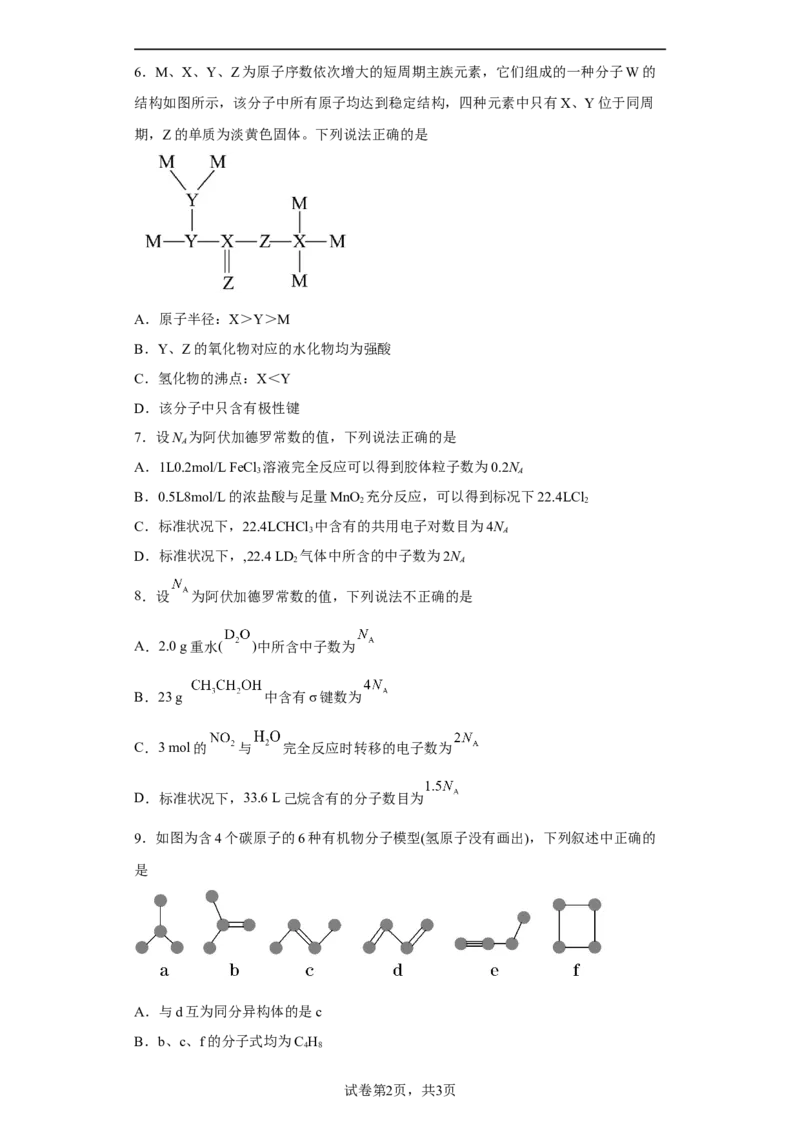
D.归纳范式和演绎范式两者相互联系、互为前提6.M、X、Y、Z为原子序数依次增大的短周期主族元素,它们组成的一种分子W的
结构如图所示,该分子中所有原子均达到稳定结构,四种元素中只有X、Y位于同周
期,Z的单质为淡黄色固体。下列说法正确的是
A.原子半径:X>Y>M
B.Y、Z的氧化物对应的水化物均为强酸
C.氢化物的沸点:X<Y
D.该分子中只含有极性键
7.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.1L0.2mol/L FeCl 溶液完全反应可以得到胶体粒子数为0.2N
3 A
B.0.5L8mol/L的浓盐酸与足量MnO 充分反应,可以得到标况下22.4LCl
2 2
C.标准状况下,22.4LCHCl 中含有的共用电子对数目为4N
3 A
D.标准状况下,,22.4 LD 气体中所含的中子数为2N
2 A
8.设 为阿伏加德罗常数的值,下列说法不正确的是
A.2.0 g重水( )中所含中子数为
B.23 g 中含有σ键数为
C.3 mol的 与 完全反应时转移的电子数为
D.标准状况下,33.6 L己烷含有的分子数目为
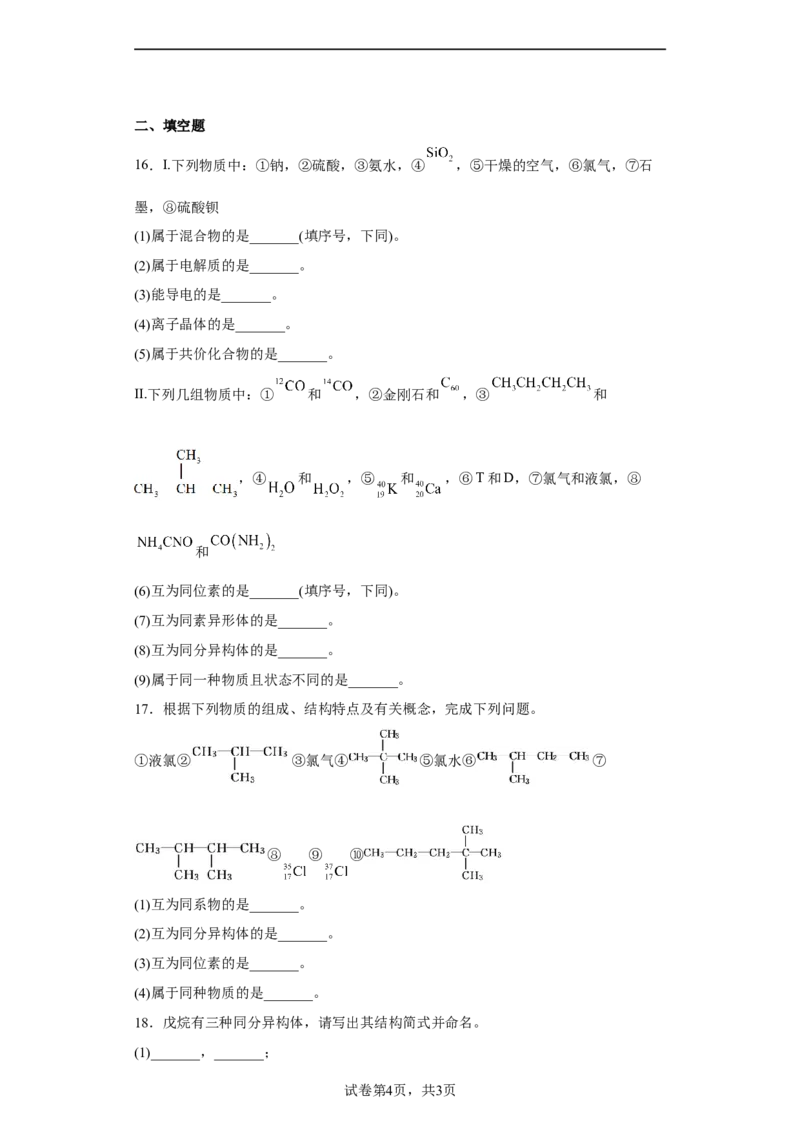
9.如图为含4个碳原子的6种有机物分子模型(氢原子没有画出),下列叙述中正确的
是
A.与d互为同分异构体的是c
B.b、c、f的分子式均为C H
4 8
试卷第2页,共3页C.a和f均为链状烷烃
D.同种物质中只能含碳链或碳环
10.下列“类比”合理的是
A.CH 是正四面体型分子,则 CCl 也是正四面体型分子
4 4
B.Cl 和HO反应是氧化还原反应,则 BrCl和HO反应生成 HBrO和 HCl也是氧化
2 2 2
还原反应
C.ClO 中Cl 的化合价为+1价,则 OF 中F的化合价为+1价
2 2
D.Na在空气中燃烧生成 NaO,则 Li 在空气中燃烧生成 LiO
2 2 2 2
11.下列烷烃在光照下与氯气反应,生成的一氯代烃只有一种的是
A.CHCHCH B.CHCHCHCHCH
3 2 3 3 2 2 2 3
C. D.
12.以下结构表示的物质中是烷烃的是
①CHOH ②CH =CH ③ ④CH CH
3 2 2 3 3
A.①和② B.①和③ C.①和④ D.③和④
13.有机物种类繁多的原因是
A.碳元素在地壳中的含量大,且属于非金属
B.碳原子间能以共价键结合,形成多种链状和环状结构
C.碳元素所形成的化合物性质稳定,且共价键键能大
D.碳原子中质子数和中子数相等
14.下列叙述正确的是
A.分子式相同,各元素质量分数也相同的物质是同种物质
B.通式相同的不同物质一定属于同系物
C.分子式相同的不同物质一定是同分异构体
D.同系物的性质完全相同
15.下列各组物质中,互为同分异构体的是
A. 和 B. 和
C. 和 D. 和二、填空题
16.I.下列物质中:①钠,②硫酸,③氨水,④ ,⑤干燥的空气,⑥氯气,⑦石
墨,⑧硫酸钡
(1)属于混合物的是_______(填序号,下同)。
(2)属于电解质的是_______。
(3)能导电的是_______。
(4)离子晶体的是_______。
(5)属于共价化合物的是_______。
II.下列几组物质中:① 和 ,②金刚石和 ,③ 和
,④ 和 ,⑤ 和 ,⑥T和D,⑦氯气和液氯,⑧
和
(6)互为同位素的是_______(填序号,下同)。
(7)互为同素异形体的是_______。
(8)互为同分异构体的是_______。
(9)属于同一种物质且状态不同的是_______。
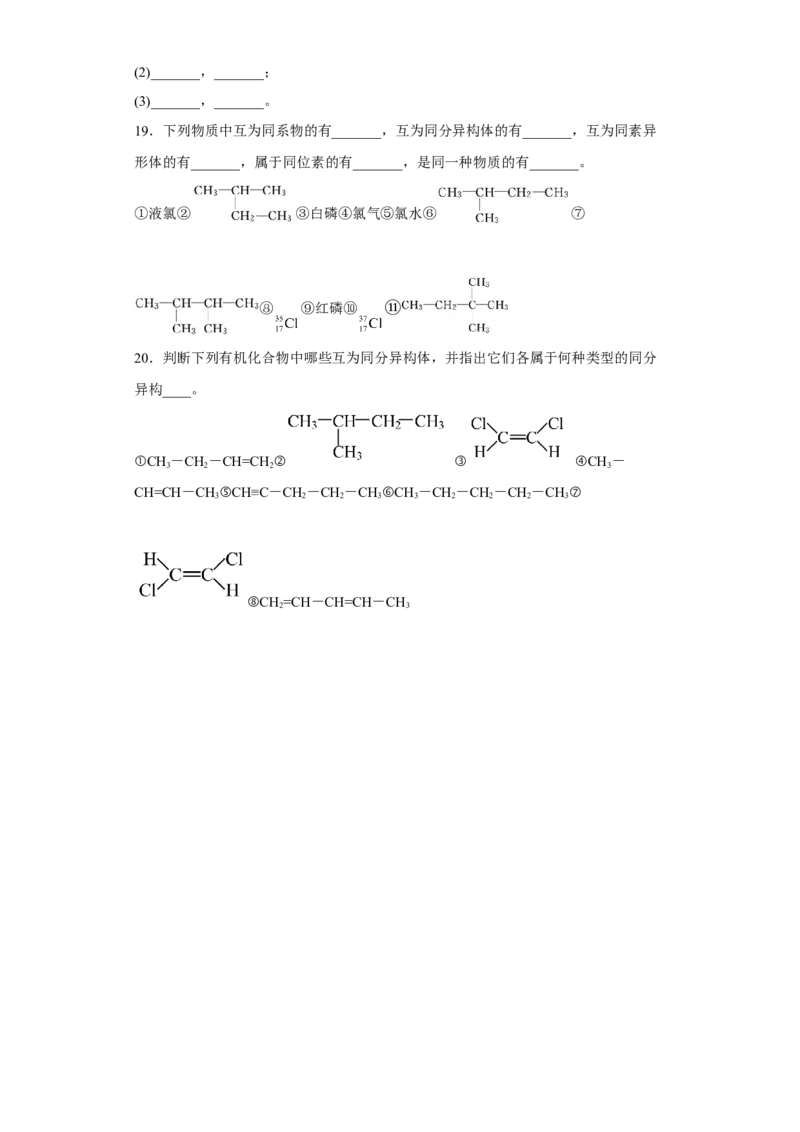
17.根据下列物质的组成、结构特点及有关概念,完成下列问题。
①液氯② ③氯气④ ⑤氯水⑥ ⑦
⑧ ⑨ ⑩
(1)互为同系物的是_______。
(2)互为同分异构体的是_______。
(3)互为同位素的是_______。
(4)属于同种物质的是_______。
18.戊烷有三种同分异构体,请写出其结构简式并命名。
(1)_______,_______;
试卷第4页,共3页(2)_______,_______;
(3)_______,_______。
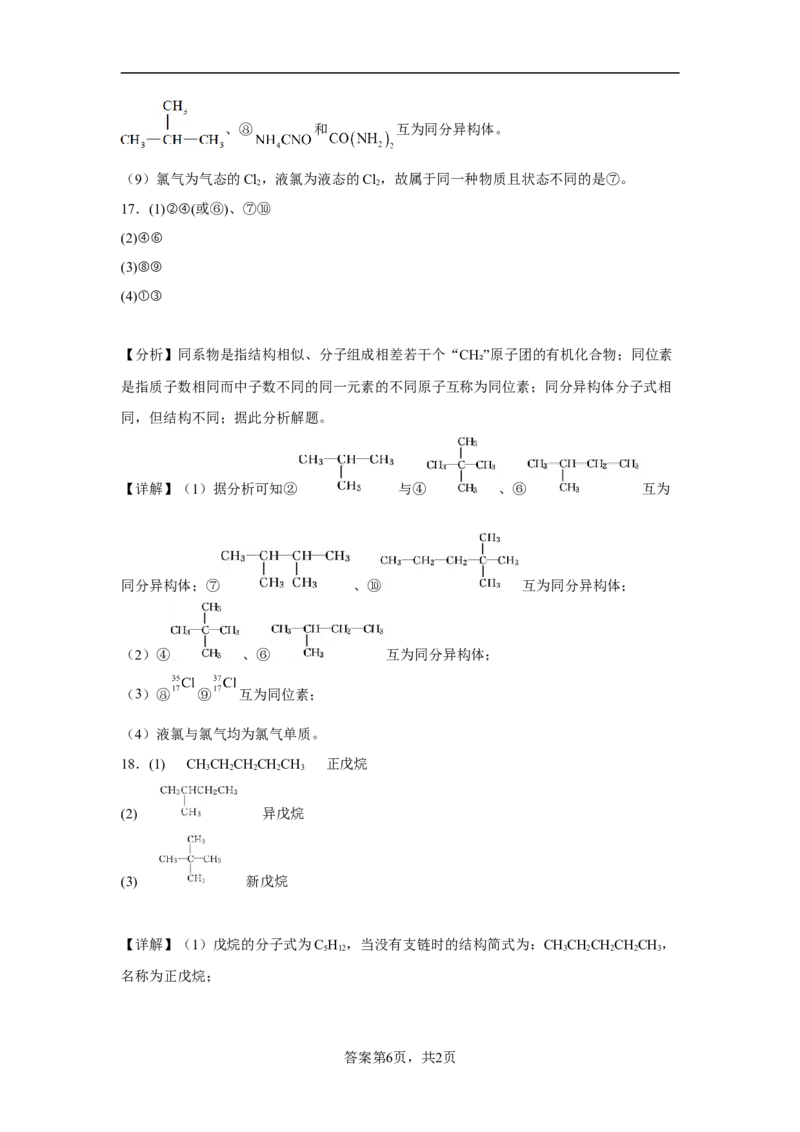
19.下列物质中互为同系物的有_______,互为同分异构体的有_______,互为同素异
形体的有_______,属于同位素的有_______,是同一种物质的有_______。
①液氯② ③白磷④氯气⑤氯水⑥ ⑦
⑧ ⑨红磷⑩
⑪
20.判断下列有机化合物中哪些互为同分异构体,并指出它们各属于何种类型的同分
异构____。
①CH-CH-CH=CH② ③ ④CH -
3 2 2 3
CH=CH-CH⑤CH≡C-CH-CH-CH⑥CH -CH-CH-CH-CH⑦
3 2 2 3 3 2 2 2 3
⑧CH=CH-CH=CH-CH
2 3参考答案:
1.B
【详解】A.与2-丁炔分子式为C H,互为同分异构体,A正确;
4 6
B.与乙烯官能团相同,但官能团数目不同,不是同系物,B错误;
C.分子含C=C可使酸性高锰酸钾溶液褪色,C正确;
D.与氢气反应,可以1、2加成生成1-丁烯,1、4加成生成2-丁烯,全部加成生成丁烷,
可能生成三种产物,D正确;
故选B。
2.A
【详解】A.中子数为8的碳原子质量数为14,可表示为: ,选项A错误;
B.氧离子的核电荷数为8,核外电子总数为10,正确的离子结构示意图为: ,
选项B正确;
C.质子数相同,中子数不同的原子互称为同位素,因此 、 、 互为同位素,选项
C正确;
D.CHCOOH是弱电解质,不完全电离,电离方程式为:CHCOOH CHCOO-+H+,选
3 3 3
项D正确;
答案选A。
3.B
【详解】A.“84”消毒液的有效成分是NaClO,属于一种强氧化剂,而酒精( )具
有还原性,二者混合会发生化学反应,不能使消毒效果更好,选项A错误;
B.太阳能电池可以将光能转化为电能,其主要成分是硅单质,选项B正确;
C.明矾与水反应可以形成氢氧化铝胶体,从而达到沉淀悬浮物的目的,但是明矾不具有
杀菌消毒的功能,选项C错误;
D.石墨烯与金刚石都是由碳元素构成的不同单质,属于同素异形体,选项D错误;
答案选B。
4.A
【分析】短周期主族元素X、Y、Z的原子序数依次增大,X元素最外层电子数是电子层数
的2倍,则X为C,Y元素在元素周期表中的周期数等于族序数,Y能溶于Z的最高价氧化物对应水化物的稀溶液,而不溶于其浓溶液,则Y为Al,Z为S。
【详解】A.同周期从左到右元素原子半径递减,同主族时,核电荷数越大,原子半径越
大,原子半径:Y(Al)>Z(S)>X(C),A不正确;
B. 有机化合物数量庞大、种类繁多,X(C)是形成化合物种类最多的元素,B正确;
C. Y最高价氧化物即氧化铝具有很高的熔点,是一种优良的耐火材料,C正确;
D. 硫难溶于水、易溶于二硫化碳,实验室可用XZ 即二硫化碳清洗装有硫磺的试管,D
2
正确;
答案选A。
5.D
【详解】A.由元素周期表提供了元素之间联系的一般理论,发现新元素是个别,属于一
般到个别,故发现新的元素属于演绎范式,故A错误;
B.通过甲烷(CH)、乙烷(C H)、丙烷(C H)、丁烷(C H )的分子式,总结出饱和烷烃的通
4 2 6 3 8 4 10
式为C H ,属于归纳,故B错误;
n 2n+2
C.实验方法多种多样,可以是调查归纳,也可以是实践,也可以通过化学实验验证,故C
错误;
D.归纳范式和演绎范式作为一对普遍适用的逻辑方法,在化学研究中得到了广泛应用。
两者不是孤立使用的,在实际研究中常常融合在一起,相互联系、互为前提,故D正确;
故答案为D。
6.A
【分析】Z的单质为淡黄色固体,推出Z为S,只有X、Y位于同周期,则X、Y位于第二
周期,则M位于第一周期,即M为H,根据结构式,以及所有原子均达到稳定结构可知,
Y形成3个共价键,即Y为N,X形成四个共价键,X为C,据此分析;
【详解】A.一般电子层数越多,半径越大,同周期从左向右,原子半径依次减小,因此
三种元素原子半径大小顺序是C>N>H,故A正确;
B.Y为N,N的氧化物对应水化物有HNO、HNO,HNO 为弱酸,硝酸为强酸,Z为
2 3 2
S,S的氧化物对应水化物有HSO 、HSO 等,前者为中强酸,后者为强酸,故B错误;
2 3 2 4
C.C的氢化物属于烃,有固、液、气三种状态,因此C的氢化物沸点不一定小于N的氢
化物,故C错误;
D.根据结构中,N-N之间存在非极性键,故D错误;
答案为A。
7.D
答案第2页,共2页【详解】A.胶粒是粒子的聚集体,所以1L0.2mol/L氯化铁溶液完全反应得到氢氧化铁胶
体粒子数小于0.2N ,故A错误;
A
B.浓盐酸与二氧化锰共热反应生成氯化锰、氯气和水,稀盐酸与二氧化锰共热不反应,
所以无法计算0.5L8mol/L的浓盐酸与足量二氧化锰充分反应制得标况下氯气的体积,故B
错误;
C.标准状况下,三氯甲烷为液态,所以无法计算22.4L三氯甲烷的物质的量和含有的共用
电子对数目,故C错误;
D.标准状况下,22.4LD 气体中所含的中子数为 ×2×N mol—1=2N ,故D正确;
2 A A
故选D。
8.D
【详解】A.2.0g重水的物质的量为0.1mol,而1个重水分子中含10个中子,故0.1mol重
水中含N 个中子,故A正确;
A
B.23 g 的物质的量为 =0.5mol,1个 分子中含有8个σ键,
则0.5mol 中含有σ键数为 ,故B正确;
C.NO 与HO反应的化学方程式为3NO +H O=2HNO +NO,该反应消耗3个NO 分子转
2 2 2 2 3 2
移电子数为2个,则有3mol的NO 参与反应时,转移电子数为2N ,故C正确;
2 A
D.己烷在标况下不是气体,33.6 L己烷的物质的量不是1.5mol,故D错误;
故选D。
9.B
【详解】A.d和c的分子式不同,不互为同分异构体,A错误;
B.b、c、f的分子式均为C H,互为同分异构体,B正确;
4 8
C.f为环烷烃,C错误;
D.同种物质中可能同时含有碳链和碳环,D错误;
故选B。
10.A
【详解】A.CCl 是把CH 上的H都用Cl取代,故CCl 仍是正四面体,A正确;
4 4 4
B.因BrCl中的+1价的Br与OH-结合成HBrO,-1价的Cl与H+结合成HCl,故BrCl与
HO的反应为非氧化还原反应,B错误;
2
C.ClO 中Cl 的化合价为+1价,由于F没有正价,OF 中F的化合价为-1价O为+2价,
2 2C错误;
D.Na在空气中燃烧生成 NaO,但Li没有Na活泼,在空气中燃烧生成的是LiO,D错
2 2 2
误;
答案选A。
11.C
【详解】A.有两种不同位置的H原子,与氯气反应生成的一氯代烃有两种,A错误;
B.有三种不同位置的H原子,与氯气反应生成的一氯代烃有三种,B错误;
C.只有一种H原子,与氯气反应生成的一氯代烃只有一种,C正确;
D.有四种不同位置的H原子,与氯气反应生成的一氯代烃有四种,D错误;
故选C。
12.D
【详解】①CHOH含有羟基为醇类, ②CH=CH 为乙烯是烯烃,③ 为异丁
3 2 2
烷, ④CHCH 为乙烷,是烷烃,综上所述故选D。
3 3
13.B
【详解】有机物分子中碳原子间能以共价键结合形成4个共价键,而且可以形成链状或环
状等结构,是导致有机物种类繁多的原因,综上所述故B正确。
14.C
【详解】A.分子式相同的物质,结构不一定相同,所以不一定是同种物质,可能是同分
异构体,A错误;
B.通式相同的物质不一定是同系物,也可能是同分异构体或其他关系,B错误;
C.分子式相同,结构不同,则为同分异构体,C正确;
D.同系物的化学性质相似,物理性质不同,D错误;
故选C。
15.D
【详解】A. 和 是同种元素组成的不同单质,属于同素异形体,故A错误;
B. 和 分子式不同,不属于同分异构体,故B错误;
C. 和 是质子数相同中子数不同的同种元素的不同核素,属于同位素,故C错误;
答案第4页,共2页D. 和 是分子式相同,结构不同的化合物,
属于同分异构体,故D正确;
故答案为D。
16.(1)③⑤
(2)②⑧
(3)①③⑦
(4)⑧
(5)②④
(6)⑥
(7)②
(8)③⑧
(9)⑦
【详解】(1)③氨水为氨气溶于水形成的物质,属于混合物;⑤干燥的空气含有氮气、氧
气等,属于混合物;故属于混合物的是③⑤。
(2)电解质为溶于水或熔融态可以导电的化合物,单质、混合物既不是电解质,也不是非
电解质,②硫酸溶于水可以电离出离子导电,属于电解质;⑧硫酸钡属于盐,虽然难溶于
水,单质熔融态可以导电,属于电解质,故属于电解质的是②⑧。
(3)①钠为金属,存在自由移动的电子,可以导电;③氨水中氨气与水反应生成的一水合
氨电离出铵根离子和氢氧根离子可以导电;⑦石墨存在自由移动的电子,也可以导电,故
能导电的是①③⑦。
(4)⑧硫酸钡由钡离子和硫酸根离子构成,属于离子晶体,故离子晶体的是⑧。
(5)硫酸、 均为由非金属元素通过共用电子对形成的化合物,故属于共价化合物的
是②④。
(6)同种元素的不同核素互为同位素,同位素的质子数相同,中子数不同,故⑥T和D
互为同位素。
(7)同种元素组成的不同单质互为同素异形体,故②金刚石和 互为同素异形体。
(8)分子式相同、结构不同的物质互为同分异构体,故③ 和、⑧ 和 互为同分异构体。
(9)氯气为气态的Cl,液氯为液态的Cl,故属于同一种物质且状态不同的是⑦。
2 2
17.(1)②④(或⑥)、⑦⑩
(2)④⑥
(3)⑧⑨
(4)①③
【分析】同系物是指结构相似、分子组成相差若干个“CH₂”原子团的有机化合物;同位素
是指质子数相同而中子数不同的同一元素的不同原子互称为同位素;同分异构体分子式相
同,但结构不同;据此分析解题。
【详解】(1)据分析可知② 与④ 、⑥ 互为
同分异构体;⑦ 、⑩ 互为同分异构体;
(2)④ 、⑥ 互为同分异构体;
(3)⑧ ⑨ 互为同位素;
(4)液氯与氯气均为氯气单质。
18.(1) CHCHCHCHCH 正戊烷
3 2 2 2 3
(2) 异戊烷
(3) 新戊烷
【详解】(1)戊烷的分子式为C H ,当没有支链时的结构简式为:CHCHCHCHCH,
5 12 3 2 2 2 3
名称为正戊烷;
答案第6页,共2页(2)含有一个支链时,结构简式为: ,名称为异戊烷;
(3)含有两个支链时,结构简式为: ,名称为新戊烷。
19. ②与⑦、 ;⑥与⑦、 ⑦ ③⑨
⑧⑩ ①④、②⑪⑥ ⑪ ⑪
【分析】同系物是指结构相似、分子组成相差若干个“CH₂”原子团的有机化合物;同位素
是指质子数相同而中子数不同的同一元素的不同原子互称为同位素;同素异形体是指由同
样的单一化学元素组成,因排列方式不同,而具有不同性质的单质;同分异构体分子式相
同,但结构不同;据此分析解题。
【详解】先将比较容易找到的找出:①④、②⑥分别为同一种物质,⑧⑩互为同位素,
③⑨互为同素异形体;再找同分异构体,⑦⑪分子式相同,但结构不同,因此互为同分异
构体;最后找出同系物:②与⑦、⑪互为同系物或⑥与⑦、⑪互为同系物。
20.①与④,为官能团位置异构;②与⑥,为碳链异构;③与⑦,为顺反异构;⑤与⑧,
为官能团异构
【分析】分子式相同,结构不同的两种物质互为同分异构体;可分为碳链异构;官能团异
构;位置异构;顺反异构;立体异构等;
【详解】由题中所给结构简式,可得①②③④⑤⑥⑦⑧的分子式分别为 、 、
、 、 、 、 、 ;所以互为同分异构的有:①与④,为
官能团位置异构;②与⑥,为碳链异构;③与⑦,为顺反异构;⑤与⑧,为官能团异构,
故填①与④,为官能团位置异构;②与⑥,为碳链异构;③与⑦,为顺反异构;⑤与⑧,
为官能团异构。答案第8页,共2页