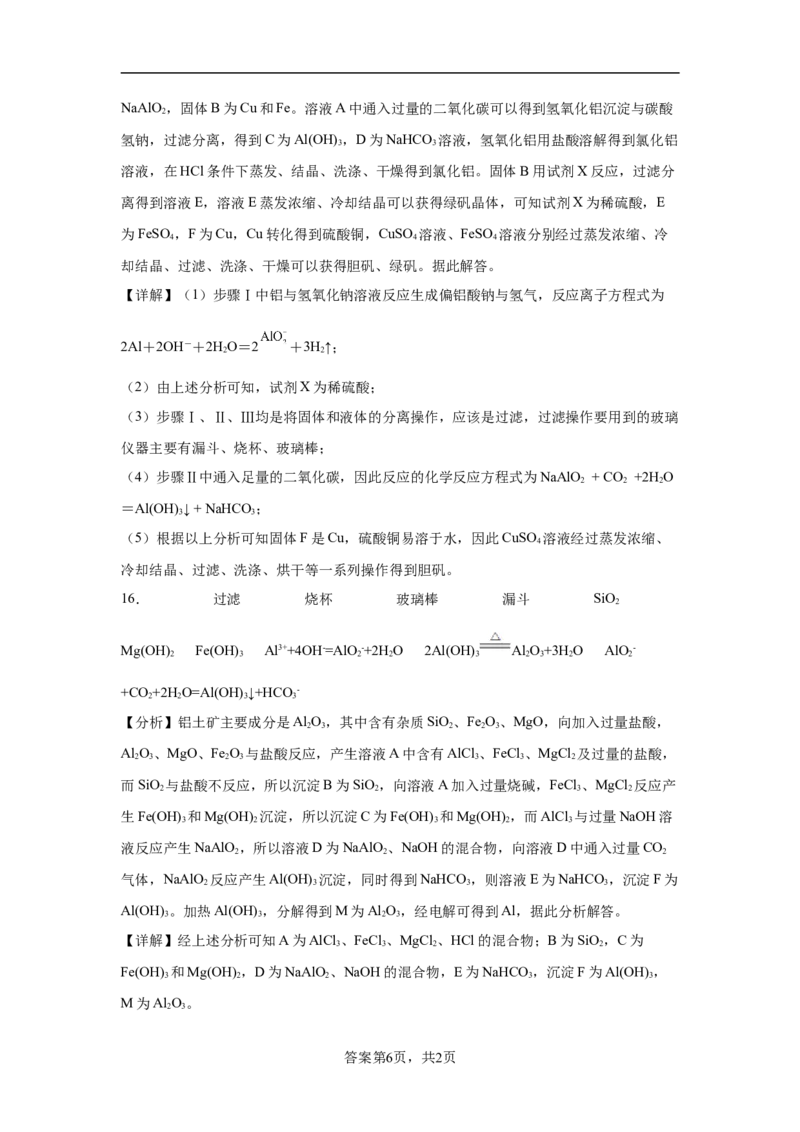文档内容
第三章� 第 2节 金属材料课时作业2022-2023学年高中化
学人教版(2019)必修第一册
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列有关物质用途的说法正确的是
A.氯气可用于自来水消毒 B.甲醛可用作食品防腐剂
C.碳酸钠可用来治疗胃酸过多 D.铝制容器可长期存放碱性物质
2.下列说法正确的是
A.高碳钢的含碳量大于2% B.生铁既可铸造也可锻造
C.生铁和钢都属于铁合金 D.生铁是用途最广的合金
3.许多成语蕴含了化学知识。下列成语违背化学理论或化学观念的是
A.煽风点火 B.点石成金 C.滴水穿石 D.百炼成钢
4.将NaOH固体加热融化,可以使用下列哪种材质的坩埚
A.石英坩埚 B.氧化铝坩埚 C.瓷坩埚 D.铁坩埚
5.下列物质的性质与用途具有对应关系的是
A. 具有强氧化性,可用作漂白剂 B. 能与碱反应,可用作抗酸药
C. 具有两性,可制作耐高温陶瓷 D. 易溶于水,可用于饮用水消
毒
6.生铁的熔点是1100~1200℃,则可推断纯铁的熔点是
A.1085℃ B.1160℃ C.1200℃ D.1535℃
7.中国传统文化对人类文明贡献巨大。下列古代文献及诗句中涉及的化学研究成果,
对其说明合理的是
A.李白诗句“日照香炉生紫烟,遥看瀑布挂前川”,“紫烟”指“香炉”中碘升华
的现象
B.“墨滴无声入水惊,如烟袅袅幻形生”中的“墨滴”的分散质粒子直径在
之间,具有胶体的性质
C.“南朝四百八十寺,多少楼台烟雨中”中的“烟雨”指悬浮在空中的固体颗粒
D.《天工开物·五金》中记载:“若造熟铁,则生铁流出时,相连数尺内,众人柳棍
疾搅,即时炒成熟铁。”炒铁是为了降低铁水中的碳含量,且熟铁比生铁质地更硬,
延展性稍差
8.下列说法不正确的是( )A.电解熔融氯化铝可制取金属铝
B.CO高温条件下还原氧化铁可制铁
C.生产普通玻璃的主要原料为石灰石、纯碱和石英砂
D.用SiO 和C高温条件下制粗硅
2
9.从铝土矿中提取铝的工艺流程如图所示,下列说法正确的是
A.上述流程中涉及的反应均为非氧化还原反应
B.反应②中过量CO 可以用过量HCl代替
2
C.实验室中完成反应③应在蒸发皿中进行
D.反应①中的主要反应为Al O+2OH-=2AlO +H O
2 3 2
10.打磨过的铝箔用酒精灯加热会被氧化,形成一层兜着液体的薄膜,该薄膜的主要
化学成分是
A.Al B.Al O C.AlN D.Al(OH)
2 3 3
11.下列反应,若改变反应物的量或浓度,产物不会有变化的是
A.A1片和硫酸 B.A1 O 和盐酸
2 3
C.AlCl 溶液和氢氧化钠溶液 D.HS在空气中燃烧
3 2
12.甲、乙两烧杯中各盛有100 mL 2 mol·L-1的盐酸和氢氧化钠溶液,向两烧杯中分别
加入一定量的铝粉,反应结束后生成的气体的体积比为2:3时,加入铝粉的质量
A.2.7克 B.1.8克 C.4.5克 D.5.4克
二、填空题
13.阅读材料,回答下列问题。
近年来,科研人员研究得到一种新型材料-泡沫铝。它是把发泡剂加到熔融铝合金中制
成的,其优点是硬度大,密度小(为0.16~0.5 g/cm3),比木材还轻,可浮于水面,又有
很大刚性,且隔音、保温,是一种良好的建筑材料和轻质材料。
(1)中国人民最早使用的合金是_______(填字母序号,下同)。
A.黄铜 B.生铁 C.青铜 D.陨铁
(2)下列关于泡沫铝的说法中错误的是_______ 。
A.泡沫铝是铝单质泡沫 B.泡沫铝是一种合金
试卷第2页,共3页C.泡沫铝是一种优质的建筑材料和轻质材料D.泡沫铝可用于飞机制造
(3)铝制成铝箔用于食品包装,是利用它的_______。
A.金属光泽 B.延展性 C.导电性 D.导热性
(4)甲、乙两烧杯中各盛有100 mL 3 mol·L-1的盐酸和NaOH溶液,向两烧杯中分别加入
等质量的铝粉,反应结束后,测得生成的气体体积比为甲∶乙=1∶2,则加入铝粉质量
为
A.5.4 g B.3.6 g C.2.7 g D.1.8 g
(5)铝在空气中会被氧化生成一层致密的氧化膜而对内部铝起保护作用,但这层氧化膜
遇到强酸或强碱溶液都会溶解,请写出:
①氧化膜与盐酸反应的离子方程式:_______。
②氧化膜与氢氧化钠溶液反应的离子方程式:_______。
14.已知在某温度T℃时,某稀硫酸和盐酸混合液中,c(H+)=10﹣amol•L﹣1,c(OH﹣)=10
﹣bmol•L﹣1,已知a+b=12.向20mL该混合酸溶液中逐滴加入pH=11Ba(OH) 溶液,生
2
成BaSO 的质量与加入的Ba(OH) 溶液体积关系如图所示,当加入60mL Ba(OH) 溶液
4 2 2
时,C点溶液的pH=6(体积变化忽略不计),试计算:
(1)最初混合酸溶液中c(HCl)=_______;
(2)图中______点BaSO 就已被完全沉淀,质量为______克;
4
(3)B点pH=______(第(3)步要求写出计算过程)(已知lg3=0.48)。
三、实验题
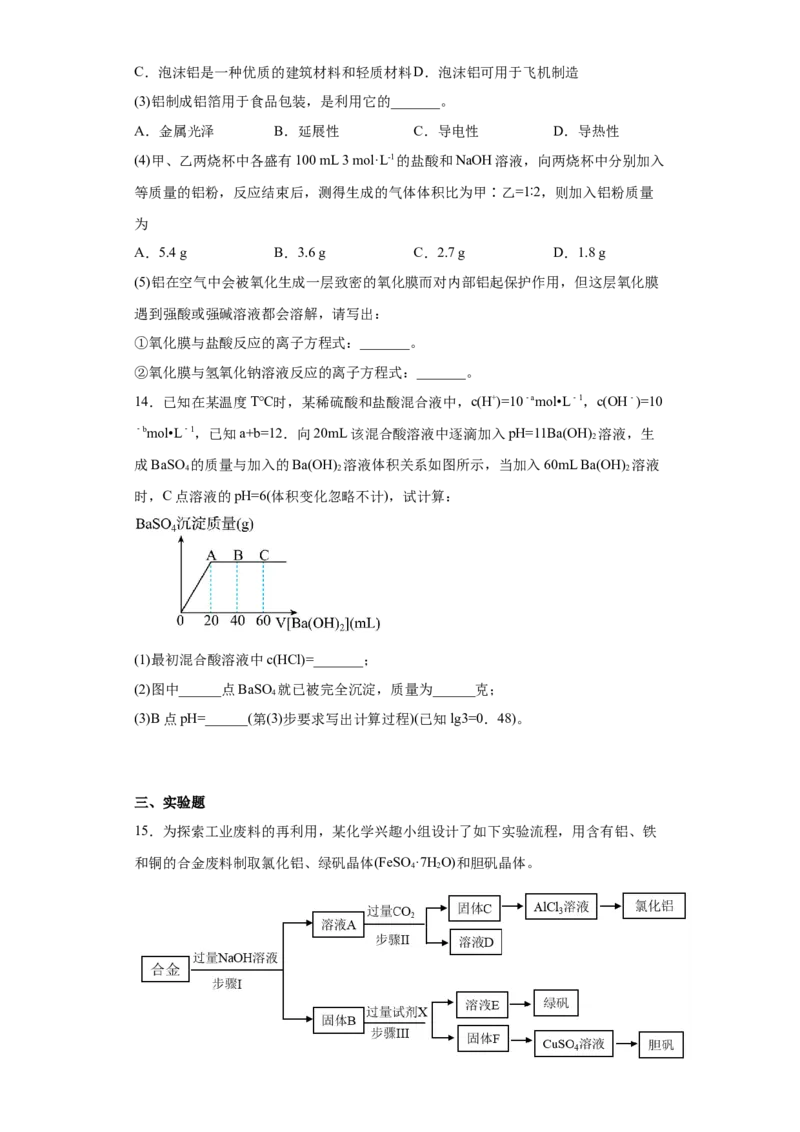
15.为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用含有铝、铁
和铜的合金废料制取氯化铝、绿矾晶体(FeSO ·7H O)和胆矾晶体。
4 2请回答下列问题:
(1)写出步骤Ⅰ反应的离子方程式:___________________________________。
(2)试剂X是________。
(3)步骤Ⅰ、Ⅱ、Ⅲ中均需进行的实验操作是__________; 操作要用到的玻璃仪器主要
有_______、_______、_______。
(4)写出步骤Ⅱ的化学反应方程式:___________________________________。
(5)固体F是________(填化学式);CuSO 溶液经过_________、_________、过滤、洗涤、
4
烘干等一系列操作得到胆矾。
四、有机推断题
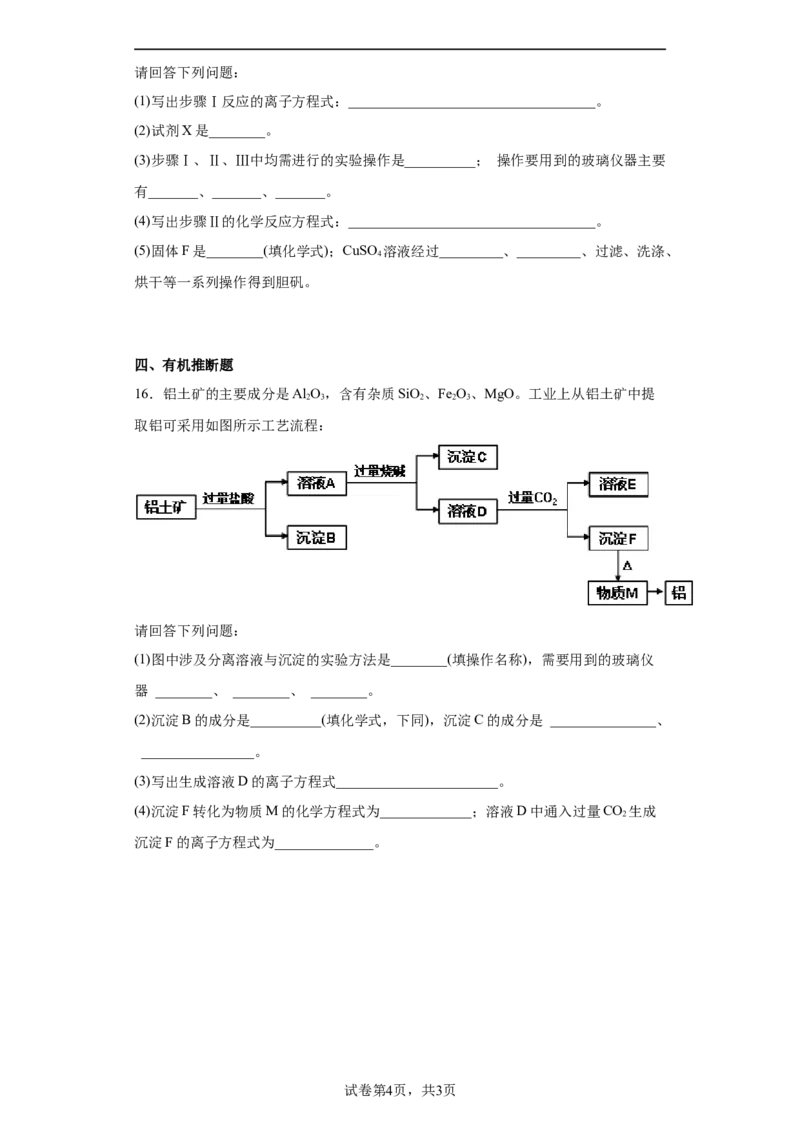
16.铝土矿的主要成分是Al O,含有杂质SiO、Fe O、MgO。工业上从铝土矿中提
2 3 2 2 3
取铝可采用如图所示工艺流程:
请回答下列问题:
(1)图中涉及分离溶液与沉淀的实验方法是________(填操作名称),需要用到的玻璃仪
器 ________、 ________、 ________。
(2)沉淀B的成分是__________(填化学式,下同),沉淀C的成分是 _______________、
________________。
(3)写出生成溶液D的离子方程式_______________________。
(4)沉淀F转化为物质M的化学方程式为_____________;溶液D中通入过量CO 生成
2
沉淀F的离子方程式为______________。
试卷第4页,共3页参考答案:
1.A
【详解】A.氯气溶于水生成的次氯酸具有强氧化性,可用于自来水消毒,A正确;
B.甲醛有毒,不可用作食品防腐剂,B错误;
C.碳酸氢钠可用来治疗胃酸过多,C错误;
D.铝、氧化铝均既能与酸反应,也能与碱反应,因此铝制容器不可长期存放碱性物质,D
错误,
答案选A。
2.C
【详解】A.高碳钢属于钢中的碳素钢,钢的含碳量0.03%~2%,小于2%,故A错误;
B.生铁可铸但不可锻,故B错误;
C.铁合金通常包括生铁和钢两大类,故C正确;
D.钢是用途最广的合金,故D错误;
答案选C。
3.B
【详解】A.煽风点火,促进空气的流通,为燃烧补充氧气,使燃烧更旺,A不合题意;
B.根据元素守恒定律,化学反应前后元素种类不变,所以化学反应不能改变元素种类,
点石成金违背了上述化学理论和观念,B符合题意;
C.“滴水穿石”中包含化学反应原理:CaCO +H O+CO=Ca(HCO ),Ca(HCO ) 易溶于水,
3 2 2 3 2 3 2
石头在水滴的长时间作用下,就会形成小孔,C不合题意;
D.百炼成钢是将铁中过量的碳除去,发生了化学反应,且铁、碳元素的化合价发生变化,
则属于氧化还原反应,D不合题意;
故答案为:B。
4.D
【详解】陶瓷坩埚、石英坩埚以及普通玻璃坩埚中都含有二氧化硅,在高温下都能与氢氧
化钠反应而使坩埚炸裂,不能用于熔融氢氧化钠固体;氧化铝能与氢氧化钠反应而使坩埚
炸裂,只能用铁坩埚,故答案为D。
5.A
【详解】A. 用作漂白剂利用的是强氧化性,A正确;
B. 用作抗酸药利用的是与酸反应的性质,B错误;C. 制作耐高温陶瓷利用的是耐高温的性质,C错误;
D. 用于饮用水消毒利用的是强氧化性,D错误;
故选A。
6.D
【分析】合金的熔点通常比其成分金属低。
【详解】生铁的熔点是1100~1200℃,生铁是铁和碳的合金,合金的熔点比纯铁的熔点
低,所以铁的熔点高于1200℃,选D。
7.B
【详解】A. “日照香炉生紫烟,遥看瀑布挂前川”, “紫烟”是水产生的雾气,不是
碘升华的现象,故A错误;
B.“墨滴”的分散质粒子直径在 之间,形成胶体,具有胶体的性质,故B正
确;
C.“南朝四百八十寺,多少楼台烟雨中”中的“烟雨”指悬浮在空中的小液滴,故C错
误;
D.炒铁是为了降低铁水中的碳含量,熟铁比生铁质地更软,延展性更好,故D错误;
选B。
8.A
【详解】A错误,氯化铝是共价化合物,通电时AlCl 不会电离产生Al3+,故电解AlCl 得
3 3
不到Al,应该电解Al O;故选A。
2 3
【点睛】AlCl 是共价化合物,这是课本上所没有提到的,需要考生在平时的练习中自己积
3
累;也正是因为AlCl 是共价化合物,工业上冶炼铝往往电解熔融的Al O。
3 2 3
9.D
【分析】铝土矿中氧化铝和氢氧化钠溶液反应生成偏铝酸钠溶液,偏铝酸钠和过量二氧化
碳反应生成氢氧化铝沉淀,分解为氧化铝,电解得到铝单质。
【详解】A.①②③中均无元素的化合价变化,为非氧化还原反应, 为氧化还原反应,
故A错误;
B.反应 中过量 不能用过量 代替,因氢氧化铝溶于盐酸,故B错误;
答案第2页,共2页C.反应 应在坩埚中进行,加热固体分解,故C错误;
D.氧化铝与 反应,则反应 中的主要反应为 ,故D
正确;
故选: 。
10.B
【详解】打磨除去表面的氧化铝,剩余单质铝,加热使其熔化,与氧气反应生成氧化铝保
护膜,氧化铝熔点高,使其无法滴落,
故选:B。
11.B
【详解】A.A1片和稀硫酸反应生成硫酸铝和氢气,但和浓硫酸会产生钝化现象浓硫酸显
强氧化性,生成二氧化硫,故A不符;
B. A1 O 和浓、稀盐酸均生成氯化铝和水,故B符合;
2 3
C. AlCl 溶液和少量氢氧化钠溶液生成氢氧化铝沉淀,与浓氢氧化钠溶液生成偏铝酸钠,
3
故C不符;
D. HS在空气中燃烧,氧气不足时生成硫单质,氧气充足时生成二氧化硫,故D不符;
2
故选B。
12.A
【分析】由2Al+6HCl═2AlCl +3H ↑、2Al+2NaOH+2H O═2NaAlO+3H ↑可知,酸碱足量,
3 2 2 2 2
Al不足,生成气体相同;金属足量,酸碱不足,生成气体为1:3,由铝的质量相同,盐酸
和氢氧化钠溶液中溶质的物质的量相同,反应结束后测得生成的气体体积比为甲:乙=2:
3,由化学反应方程式可知,酸与金属反应时酸不过量,Al过量,碱与金属反应时碱过量,
Al不足,来计算解答。
【详解】盐酸和氢氧化钠溶液中溶质的物质的量均为0.1L×2mol/L=0.2mol,又两烧杯中分
别加入等质量的铝粉,反应结束后测得生成的气体体积比为甲:乙=2:3,设铝与酸反应时
酸完全反应,生成的氢气的物质的量为x,则 ,解得
x=0.1mol,一定条件下,气体的物质的量之比等于体积之比,根据气体体积比为甲:乙=2:3,则碱与金属铝反应生成的氢气的物质的量为0.1mol× =0.15mol,碱与金属铝反应
时铝完全反应,设与碱反应的铝的物质的量为y,则
,解得y=0.1mol,则Al的质量为
m(Al)=0.1mol×27g/mol=2.7g;答案为A。
13.(1)C
(2)A
(3)B
(4)A
(5) Al O+6H +=2Al3+ +3 H O Al O +2OH-=2 AlO +H O
2 3 2 2 3 2
【详解】(1)中国人民最早使用的合金是青铜合金,故选C;
(2)A.泡沫铝中含有Al、发泡剂等,所以是一种合金,A错误;
B.泡沫铝中含有Al、发泡剂等,所以是一种合金,B正确;
C.泡沫铝硬度高、密度小、刚性大,且隔音、保温,所以一种良好的建筑材料和轻质材
料,C正确;
D.泡沫铝硬度高、密度小、刚性大,且隔音、保温,所以一种良好的建筑材料和轻质材
料,可用于飞机制造,D正确;
故选A;
(3)铝制成铝箔作食品包装,是利用了铝的延展性,故选B;
(4)其反应原理分别为2Al+6HCl=2AlCl +3H↑,2Al+2NaOH+2HO=2NaAlO +
3 2 2 2
3H↑。可见当参加反应的HCl和NaOH的物质的量一样多时,产生H 的体积比是1:3,
2 2
而题设条件体积比为1:2,说明此题中投入的铝粉对盐酸来说是过量的,而对于NaOH来
说是不足的, ,氢离子完全反应,故生成氢气的物质的量为
答案第4页,共2页,则Al与NaOH反应生成的H 为0.15 mol×2=0.3mol,根据关
2
系式: ,消耗Al的质量为 ,故选A。
(5)①氧化铝和盐酸反应生成盐和水,离子反应方程式为:Al O+6H+=2Al3++3H O;
2 3 2
②氧化铝和强碱反应生成盐和水,离子反应方程式为:Al O+2OH-=2 AlO +H O。
2 3 2
14.(1)0.2mol/L
(2) A 0.233
(3)1.48
【详解】(1)该温度下,K =10﹣a×10﹣b=10﹣(a+b)=10﹣12,pH=11的Ba(OH) 溶液中c(OH
w 2
﹣)=0.1mol/L,c(Ba2+)= c(OH﹣)=0.05mol/L,加入20mLBa(OH) 溶液时,沉淀量达最大,
2
钡离子与硫酸根离子恰好反应,该阶段消耗的n(Ba2+)=0.02L×0.05mol/L=0.001mol,由离子
守恒可知n(H SO )=n(BaSO )=0.001mol,加入60mLBa(OH) 溶液时,溶液的pH=6,呈中性,
2 4 4 2
氢离子与氢氧根离子恰好反应,故混合溶液中n(H+)=n(OH﹣)=0.06L×0.1mol/L=0.006mol,
溶液中n(HCl)=0.006mol﹣2×0.001mol=0.004mol,故原混合溶液中c(HCl)=
=0.2mol/L;
(2)A点沉淀量达最大,硫酸与氢氧化钡恰好反应,由离子守恒可知
n(H SO )=n(BaSO )=0.001mol,质量为0.233g;
2 4 4
(3)B点加入的氢氧化钡溶液中氢氧根离子物质的量为0.04L×0.1mol/L=0.004mol,故参加
反应的氢离子为=0.004mol,溶液中剩余氢离子为0.006mol﹣0.004=0.002,氢离子浓度为
= mol/L,此时溶液pH=﹣lg =1.48。
15. 2Al+2OH-+2HO=2 +3H↑ 稀硫酸 过滤 漏
2 2
斗 烧杯 玻璃棒 NaAlO + CO +2H O=Al(OH) ↓ +
2 2 2 3
NaHCO Cu 蒸发浓缩 冷却结晶
3
【分析】铝、铁和铜的合金中只有金属铝可以和氢氧化钠反应,过滤后,得到溶液A含有NaAlO ,固体B为Cu和Fe。溶液A中通入过量的二氧化碳可以得到氢氧化铝沉淀与碳酸
2
氢钠,过滤分离,得到C为Al(OH) ,D为NaHCO 溶液,氢氧化铝用盐酸溶解得到氯化铝
3 3
溶液,在HCl条件下蒸发、结晶、洗涤、干燥得到氯化铝。固体B用试剂X反应,过滤分
离得到溶液E,溶液E蒸发浓缩、冷却结晶可以获得绿矾晶体,可知试剂X为稀硫酸,E
为FeSO ,F为Cu,Cu转化得到硫酸铜,CuSO 溶液、FeSO 溶液分别经过蒸发浓缩、冷
4 4 4
却结晶、过滤、洗涤、干燥可以获得胆矾、绿矾。据此解答。
【详解】(1)步骤Ⅰ中铝与氢氧化钠溶液反应生成偏铝酸钠与氢气,反应离子方程式为
2Al+2OH-+2HO=2 +3H↑;
2 2
(2)由上述分析可知,试剂X为稀硫酸;
(3)步骤Ⅰ、Ⅱ、Ⅲ均是将固体和液体的分离操作,应该是过滤,过滤操作要用到的玻璃
仪器主要有漏斗、烧杯、玻璃棒;
(4)步骤Ⅱ中通入足量的二氧化碳,因此反应的化学反应方程式为NaAlO + CO +2H O
2 2 2
=Al(OH) ↓ + NaHCO;
3 3
(5)根据以上分析可知固体F是Cu,硫酸铜易溶于水,因此CuSO 溶液经过蒸发浓缩、
4
冷却结晶、过滤、洗涤、烘干等一系列操作得到胆矾。
16. 过滤 烧杯 玻璃棒 漏斗 SiO
2
Mg(OH) Fe(OH) Al3++4OH-=AlO -+2H O 2Al(OH) Al O+3H O AlO-
2 3 2 2 3 2 3 2 2
+CO +2H O=Al(OH) ↓+HCO-
2 2 3 3
【分析】铝土矿主要成分是Al O,其中含有杂质SiO、Fe O、MgO,向加入过量盐酸,
2 3 2 2 3
Al O、MgO、Fe O 与盐酸反应,产生溶液A中含有AlCl 、FeCl 、MgCl 及过量的盐酸,
2 3 2 3 3 3 2
而SiO 与盐酸不反应,所以沉淀B为SiO,向溶液A加入过量烧碱,FeCl 、MgCl 反应产
2 2 3 2
生Fe(OH) 和Mg(OH) 沉淀,所以沉淀C为Fe(OH) 和Mg(OH) ,而AlCl 与过量NaOH溶
3 2 3 2 3
液反应产生NaAlO ,所以溶液D为NaAlO 、NaOH的混合物,向溶液D中通入过量CO
2 2 2
气体,NaAlO 反应产生Al(OH) 沉淀,同时得到NaHCO ,则溶液E为NaHCO ,沉淀F为
2 3 3 3
Al(OH) 。加热Al(OH) ,分解得到M为Al O,经电解可得到Al,据此分析解答。
3 3 2 3
【详解】经上述分析可知A为AlCl 、FeCl 、MgCl 、HCl的混合物;B为SiO,C为
3 3 2 2
Fe(OH) 和Mg(OH) ,D为NaAlO 、NaOH的混合物,E为NaHCO ,沉淀F为Al(OH) ,
3 2 2 3 3
M为Al O。
2 3
答案第6页,共2页(1)图中分离溶液与沉淀的实验方法是过滤;需要用到的玻璃仪器有烧杯、玻璃棒、漏斗;
(2)根据上述分析可知:沉淀B的成分是SiO;沉淀C的成分是Mg(OH) 、Fe(OH) ;
2 2 3
(3)向含有Al3+的溶液中加入过量NaOH溶液,Al3+会反应转化为AlO-,则生成NaAlO 反应
2 2
的离子方程式为:Al3++4OH-=AlO -+2H O;
2 2
(4)沉淀F是Al(OH) ,该物质不稳定,加热分解产生Al O 和 HO,因此沉淀F转化为M
3 2 3 2
的化学方程式为:2Al(OH) Al O+3H O;
3 2 3 2
溶液D为NaAlO 和NaOH的混合物,向其中通入过量CO,NaAlO 与CO2及溶液中的水
2 2 2
反应生成Al(OH) 沉淀,该反应的离子方程式为AlO-+CO +2H O=Al(OH) ↓+HCO-。
3 2 2 2 3 3
【点睛】本题以推断题的形式,考查了元素及化合物的性质,特别是金属铝及其化合物的
相关性质,解题的关键在于熟练掌握“铝三角”的相关反应,题目同时考查了化学方程式
和离子方程式的书写。答案第8页,共2页