文档内容
第三章 第一节 第1课时 铁的单质、氧化物、氢氧化物 测试题
榆次一中 李金虎
一、选择题(每小题只有一个正确选项,每小题4分,共60分)
1. 指南针是我国的四大发明之一,制造指南针的磁性物质是( )
A.FeO B.Fe O
2 3
C.Fe O D.Fe
3 4
2. 下列说法不正确的是( )
A.铁与纯氧气和水蒸气反应都能生成四氧化三铁
B.铁在高温下与水蒸气的反应是置换反应
C.铁与盐酸反应生成氯化铁和氢气
D.铁与盐酸或水蒸气反应,都作还原剂
3. 下列有关铁及其化合物的说法中正确的是( )
A.Fe O 的颜色为红棕色
3 4
B.铁丝可在空气中燃烧生成Fe O
3 4
C.FeCl 可通过置换反应或复分解反应制得
2
D.铁的氧化物均为黑色,不溶于水
4. “秦砖汉瓦”是我国传统建筑文化的一个缩影。同是由黏土烧制的砖瓦,有的是黑色的,有的
却是红色的。你猜测其中的原因可能是( )
A.土壤中含有铁粉、二氧化锰等
B.黑砖瓦是煅烧过程中附着了炭黑,红砖则是添加了红色耐高温染料
C.土壤中含有的铜元素经过不同工艺煅烧,分别生成了黑色CuO和红色Cu
D.土壤中含有的铁元素经过不同工艺煅烧,分别生成了黑色Fe O 或FeO和红色Fe O
3 4 2 3
5. 制印刷电路时常用氯化铁溶液作为“腐蚀液”,发生的反应为:2FeCl +Cu===2FeCl +CuCl 。
3 2 2
向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是烧杯
中( )
A.有铁无铜 B.有铜无铁 C.铁、铜都有 D.铁、铜都无
6. 将NaO 投入到FeCl 溶液中,可观察到的现象是( )
2 2 2
①有气泡产生 ②生成白色沉淀 ③生成红褐色沉淀 ④无变化
A.①③ B.①②
C.①②③ D.④
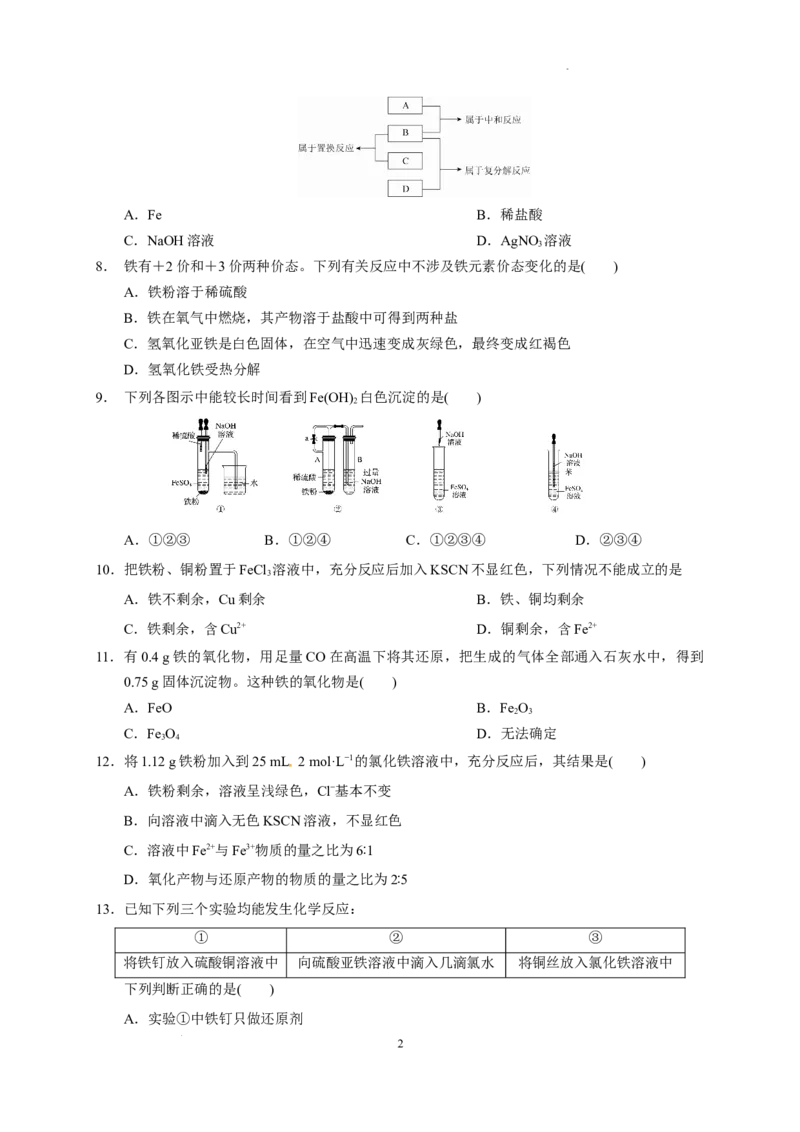
7. 现有A、B、C、D四种物质,它们是Fe、稀盐酸、NaOH溶液、AgNO 溶液四种物质中的一
3
种,它们的反应关系及反应类型如图所示,则物质B为( )
1
学科网(北京)股份有限公司A.Fe B.稀盐酸
C.NaOH溶液 D.AgNO 溶液
3
8. 铁有+2价和+3价两种价态。下列有关反应中不涉及铁元素价态变化的是( )
A.铁粉溶于稀硫酸
B.铁在氧气中燃烧,其产物溶于盐酸中可得到两种盐
C.氢氧化亚铁是白色固体,在空气中迅速变成灰绿色,最终变成红褐色
D.氢氧化铁受热分解
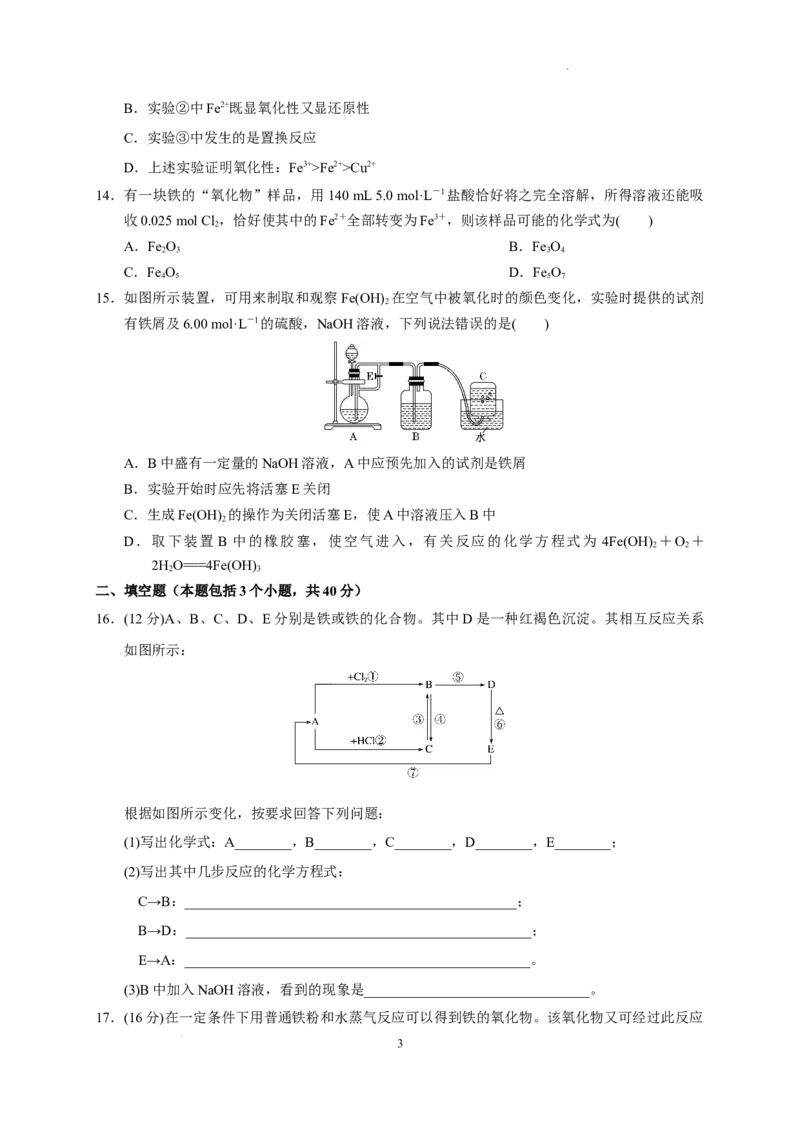
9. 下列各图示中能较长时间看到Fe(OH) 白色沉淀的是( )
2
A.①②③ B.①②④ C.①②③④ D.②③④
10.把铁粉、铜粉置于FeCl 溶液中,充分反应后加入KSCN不显红色,下列情况不能成立的是
3
A.铁不剩余,Cu剩余 B.铁、铜均剩余
C.铁剩余,含Cu2+ D.铜剩余,含Fe2+
11.有0.4 g铁的氧化物,用足量CO在高温下将其还原,把生成的气体全部通入石灰水中,得到
0.75 g固体沉淀物。这种铁的氧化物是( )
A.FeO B.Fe O
2 3
C.Fe O D.无法确定
3 4
12.将1.12 g铁粉加入到25 mL 2 mol·L−1的氯化铁溶液中,充分反应后,其结果是( )
A.铁粉剩余,溶液呈浅绿色,Cl−基本不变
B.向溶液中滴入无色KSCN溶液,不显红色
C.溶液中Fe2+与Fe3+物质的量之比为6∶1
D.氧化产物与还原产物的物质的量之比为2∶5
13.已知下列三个实验均能发生化学反应:
① ② ③
将铁钉放入硫酸铜溶液中 向硫酸亚铁溶液中滴入几滴氯水 将铜丝放入氯化铁溶液中
下列判断正确的是( )
A.实验①中铁钉只做还原剂
2
学科网(北京)股份有限公司B.实验②中Fe2+既显氧化性又显还原性
C.实验③中发生的是置换反应
D.上述实验证明氧化性:Fe3+>Fe2+>Cu2+
14.有一块铁的“氧化物”样品,用140 mL 5.0 mol·L-1盐酸恰好将之完全溶解,所得溶液还能吸
收0.025 mol Cl ,恰好使其中的Fe2+全部转变为Fe3+,则该样品可能的化学式为( )
2
A.Fe O B.Fe O
2 3 3 4
C.Fe O D.Fe O
4 5 5 7
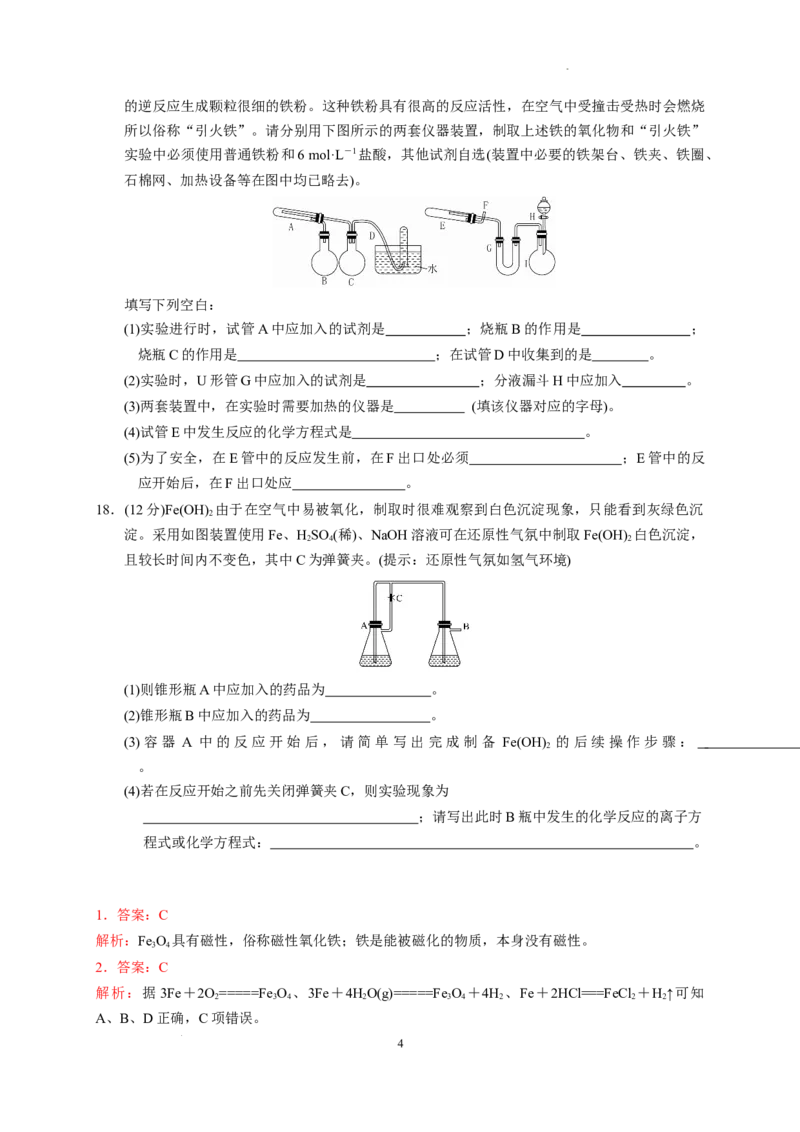
15.如图所示装置,可用来制取和观察Fe(OH) 在空气中被氧化时的颜色变化,实验时提供的试剂
2
有铁屑及6.00 mol·L-1的硫酸,NaOH溶液,下列说法错误的是( )
A.B中盛有一定量的NaOH溶液,A中应预先加入的试剂是铁屑
B.实验开始时应先将活塞E关闭
C.生成Fe(OH) 的操作为关闭活塞E,使A中溶液压入B中
2
D.取下装置 B 中的橡胶塞,使空气进入,有关反应的化学方程式为 4Fe(OH) +O +
2 2
2HO===4Fe(OH)
2 3
二、填空题(本题包括3个小题,共40分)
16.(12分)A、B、C、D、E分别是铁或铁的化合物。其中D是一种红褐色沉淀。其相互反应关系
如图所示:
根据如图所示变化,按要求回答下列问题:
(1)写出化学式:A________,B________,C________,D________,E________;
(2)写出其中几步反应的化学方程式:
C→B:_______________________________________________;
B→D:_________________________________________________;
E→A:_________________________________________________。
(3)B中加入NaOH溶液,看到的现象是________________________________。
17.(16分)在一定条件下用普通铁粉和水蒸气反应可以得到铁的氧化物。该氧化物又可经过此反应
3
学科网(北京)股份有限公司的逆反应生成颗粒很细的铁粉。这种铁粉具有很高的反应活性,在空气中受撞击受热时会燃烧
所以俗称“引火铁”。请分别用下图所示的两套仪器装置,制取上述铁的氧化物和“引火铁”
实验中必须使用普通铁粉和6 mol·L-1盐酸,其他试剂自选(装置中必要的铁架台、铁夹、铁圈、
石棉网、加热设备等在图中均已略去)。
填写下列空白:
(1)实验进行时,试管A中应加入的试剂是 ;烧瓶B的作用是 ;
烧瓶C的作用是 ;在试管D中收集到的是 。
(2)实验时,U形管G中应加入的试剂是 ;分液漏斗H中应加入 。
(3)两套装置中,在实验时需要加热的仪器是 (填该仪器对应的字母)。
(4)试管E中发生反应的化学方程式是 。
(5)为了安全,在E管中的反应发生前,在F出口处必须 ;E管中的反
应开始后,在F出口处应 。
18.(12分)Fe(OH) 由于在空气中易被氧化,制取时很难观察到白色沉淀现象,只能看到灰绿色沉
2
淀。采用如图装置使用Fe、HSO (稀)、NaOH溶液可在还原性气氛中制取Fe(OH) 白色沉淀,
2 4 2
且较长时间内不变色,其中C为弹簧夹。(提示:还原性气氛如氢气环境)
(1)则锥形瓶A中应加入的药品为 。
(2)锥形瓶B中应加入的药品为 。
(3)容器 A 中的反应开始后,请简单写出完成制备 Fe(OH) 的后续操作步骤:
2
。
(4)若在反应开始之前先关闭弹簧夹C,则实验现象为
;请写出此时B瓶中发生的化学反应的离子方
程式或化学方程式: 。
1.答案:C
解析:Fe O 具有磁性,俗称磁性氧化铁;铁是能被磁化的物质,本身没有磁性。
3 4
2.答案:C
解析:据 3Fe+2O=====Fe O 、3Fe+4HO(g)=====Fe O +4H 、Fe+2HCl===FeCl +H↑可知
2 3 4 2 3 4 2 2 2
A、B、D正确,C项错误。
4
学科网(北京)股份有限公司3.答案:C
解析:Fe O 的颜色为黑色;铁丝在空气中不能燃烧;生成 FeCl 的反应有:Fe+2HCl===FeCl +
3 4 2 2
H↑,FeO+2HCl===FeCl +HO等;Fe O 是红棕色粉末。
2 2 2 2 3
4.答案:D
解析:黏土中含有Fe元素,在烧制砖瓦时,与O 反应,生成氧化物,Fe元素的氧化物有3种,
2
FeO与Fe O 为黑色,Fe O 为红棕色,D项正确。
3 4 2 3
5.答案:A
解析:A、向FeCl 溶液中加入Fe和Cu,Fe还原性强于Cu,所以Fe先与FeCl 反应,若Fe反应完
3 3
全,Cu再与FeCl 反应,所以不会出现有铁无铜的情形,故A错误;B、当Fe反应完全,FeCl 少
3 3
量,铜会有剩余,则可能出现有铜无铁的情形,故B正确;C、若FeCl 量少,Fe也有可能有剩余,
3
而此时Cu没有发生反应,则烧杯中铁、铜都有,故C正确;D、若FeCl 量多,加入的铁和铜全部
3
参加反应,都不会有剩余,故D正确。故选A。
6.答案:A
解析:将 NaO 投入 FeCl 溶液中,发生下列反应:2NaO +2HO===4NaOH+O↑,FeCl +
2 2 2 2 2 2 2 2
2NaOH===Fe(OH) ↓+2NaCl,4Fe(OH)+O+2HO===4Fe(OH) ,所以现象为有无色气体产生并有红
2 2 2 2 3
褐色沉淀生成,观察不到白色沉淀,故选A项。
7.答案:B
解析:A和B发生中和反应,则A、B为稀盐酸、NaOH溶液中的一种。B与C发生置换反应,B
与D发生复分解反应,Fe与稀盐酸发生置换反应生成FeCl 和H,则A为NaOH溶液,B为稀盐酸,
2 2
C为Fe,D为AgNO 溶液。
3
8.答案:D
解析:A 项,Fe+HSO ===FeSO +H↑,铁元素化合价由 0 价变为+2 价;B 项,3Fe+
2 4 4 2
2O=====Fe O ,铁元素化合价由 0 价变为+2 价、+3 价;C 项,4Fe(OH) +O +
2 3 4 2 2
2HO===4Fe(OH) ,铁元素化合价由+2价变为+3价;D项,2Fe(OH) =====Fe O +3HO,铁元
2 3 3 2 3 2
素化合价没有变化。
9.答案:B
解析:因为Fe(OH) 在空气中很容易被氧化为红褐色的Fe(OH) ,即发生4Fe(OH) +O+
2 3 2 2
2HO===4Fe(OH) ,因此要较长时间看到Fe(OH) 白色沉淀,就要排除装置中的氧气或空气。①、
2 3 2
②原理一样,都是先用氢气将装置中的空气排尽,并使生成的Fe(OH) 处在氢气的保护中;④中液
2
面加苯阻止了空气进入;③由于空气中的氧气,能迅速将Fe(OH) 氧化,因而不能较长时间看到白
2
色沉淀
10.答案:C
解析:因还原性:Fe>Cu,FeCl 溶液中加入铁粉、铜粉时,依次发生反应:Fe+2FeCl ===3FeCl ,
3 3 2
Cu+2FeCl ===2FeCl +CuCl 。有以下情况:①Fe、Cu均剩余,溶液中只有Fe2+;②只有Cu剩余,
3 2 2
5
学科网(北京)股份有限公司溶液中只有 Fe2+或含 Fe2+、Cu2+;③ Fe、Cu 均不剩余,Fe3+恰好反应,溶液中有 Fe2+、Cu2+;
④Fe、Cu均不剩余,Fe3+剩余,溶液中有Fe3+、Fe2+、Cu2+。C项,Fe剩余,则溶液中不可能含有
Cu2+。
11.答案:B
解析:由反应CO+Ca(OH) ===CaCO ↓+HO和碳酸钙物质的量7.5×10-3 mol,可知反应的CO 的
2 2 3 2 2
物质的量为7.5×10-3 mol,再由CO→CO ,故铁的氧化物中含O的物质的量n(O)=7.5×10-3 mol,
2
m(O)=7.5×10-3 mol×16 g·mol-1=0.12 g,n(Fe)==0.005 mol,所以n(Fe)∶n(O)=0.005∶0.007 5=
2∶3,故为Fe O。
2 3
12.答案:C
解析:n(Fe)=0.02 mol,n(FeCl )=0.05 mol,由Fe+2Fe3+===3Fe2+知,Fe3+过量0.01 mol,铁粉全部溶
3
解,反应生成Fe2+ 0.06 mol;Fe3+过量,滴入无色KSCN溶液,溶液显红色;氧化生成的Fe2+和还
原生成的Fe2+的物质的量之比为1∶2。
13.答案:A
解析:实验①中铁钉做还原剂,氧化性Cu2+ >Fe2+;实验②中Fe2+只表现还原性;实验③中反应为:
Cu+2FeCl ===2FeCl +CuCl 不是置换反应。分析可知:氧化性:Fe3+>Cu2+,综上可知氧化性
3 2 2
Fe3+>Cu2+>Fe2+,故A正确,B、C、D错误。
14.答案:D
解析:根据2Fe2++Cl===2Fe3++2Cl-,可知铁的“氧化物”样品用盐酸溶解后所得溶液中n(Fe2+)
2
=0.025 mol×2=0.05 mol,根据电荷守恒得2n(Fe2+)+3n(Fe3+)=n(Cl-),则n(Fe3+)=0.2 mol,故
n(Fe2+)∶n(Fe3+)=0.05∶0.2=1∶4,故该氧化物可表示为FeO·2Fe O,即Fe O。
2 3 5 7
15.答案:B
解析:制取硫酸亚铁需要铁屑,所以在烧瓶中应该先加入铁屑,所以A中应预先加入的试剂是铁屑,
故A正确;稀硫酸和铁反应生成硫酸亚铁和氢气,实验开始时应打开活塞E,用氢气排出装置中的
空气,B错误;铁和稀硫酸反应有氢气生成,关闭活塞E,导致A中压强逐渐增大,将FeSO 溶液
4
压入B中进行反应生成氢氧化亚铁,C正确;氢氧化亚铁不稳定,容易被空气中的氧气氧化生成红
褐色的氢氧化铁,反应的化学方程式为4Fe(OH) +O+2HO===4Fe(OH) ,故D正确。
2 2 2 3
16.答案: (1) Fe FeCl FeCl Fe(OH) Fe O
3 2 3 2 3
(2) 2FeCl +Cl===2FeCl (合理即可)
2 2 3
FeCl +3NaOH===Fe(OH) ↓+3NaCl(合理即可)
3 3
Fe O+3CO 2Fe+3CO (或Fe O+2Al 2Fe+Al O)
2 3 2 2 3 2 3
(3) 出现白色沉淀,迅速变成灰绿色,最终变成红褐色
解析:(2)解答该题的关键是推断D,因为D为红褐色沉淀,可知D是Fe(OH) ,则E是Fe O ,A
3 2 3
是Fe,B是FeCl ,C是FeCl 。
3 2
6
学科网(北京)股份有限公司17.答案:(1)普通铁粉(或铁粉) 作为水蒸气发生器 防止倒吸(或用作安全瓶);氢气。
(2)碱石灰(或固体NaOH、无水CaCl 等) 6 mol·L-1盐酸
2
(3) ABE
(4) Fe O+4H=====3Fe+4HO。
3 4 2 2
(5)检验氢气的纯度 点燃氢气
解析:(1)根据题干可推断出试管A应是铁和水蒸气反应的装置,在A中装的应是普通铁粉,反应
过程中要生成氢气,所以D是用来收集氢气的,在烧瓶B中产生水蒸气,为了防止向试管中通入水
蒸气使试管骤冷引起水的倒流,在反应装置和收集装置中间加上广口瓶以保证实验安全。(2)装置I
用来制取氢气,故H用于添加盐酸,在产生氢气的同时可能会带出部分水蒸气和氯化氢气体,故应
在U形管中加入固体干燥剂吸收氯化氢和水蒸气。(3)反应在高温条件下进行,所以A和E装置需
要加热,反应需要水蒸气,故B也需要加热。(4)依据装置和实验目的分析,试管E中发生反应是
氢气还原四氧化三铁的反应,反应方程式是:Fe O +4H=====3Fe+4HO。(5)氢气是可燃性气体,
3 4 2 2
做氢气的性质实验时必须保证氢气是纯净的,为了安全,在E管中的反应发生前,在F出口处必须
进行气体验纯;E管中的反应开始后,在F出口处应点燃H,避免排放到空气中遇火爆炸。
2
18.答案:(1)铁和稀硫酸 (2)氢氧化钠溶液
(3)打开弹簧夹C,反应一段时间后关闭弹簧夹C
(4) A中液体被压入B瓶,B瓶内生成白色絮状沉淀,白色沉淀迅速变成灰绿色,最后
变为红褐色 Fe2++2OH-===Fe(OH) 、4Fe(OH) +O+2HO===4Fe(OH)
2 2 2 2 3
解析:(1)根据实验目的,锥形瓶A中用铁和稀硫酸反应制取硫酸亚铁。(2)硫酸亚铁和氢氧化钠溶
液反应生成氢氧化亚铁沉淀,锥形瓶 B中盛放的溶液是氢氧化钠溶液。(3)铁和稀硫酸反应生成氢
气和硫酸亚铁,为防止锥形瓶内空气的干扰,应先利用产生的氢气将空气排尽,所以A中反应开始
后,要打开弹簧夹C,反应一段时间后,要关闭弹簧夹C,利用氢气产生的压强将硫酸亚铁溶液压
入锥形瓶B中,使硫酸亚铁和氢氧化钠溶液反应生成氢氧化亚铁白色沉淀。(4)若在反应开始之前
先关闭弹簧夹C,A中产生氢气的量逐渐增多,导致压强增大,A中液体被压入B中,硫酸亚铁和
氢氧化钠溶液反应生成氢氧化亚铁,锥形瓶B中有空气,生成的氢氧化亚铁被空气中的氧气氧化生
成红褐色氢氧化铁沉淀,所以看到的现象是A中液体被压入B瓶,B瓶内生成白色絮状沉淀,白色
沉淀迅速变成灰绿色,最后变为红褐色,B中发生反应的离子方程式为Fe2++2OH-===Fe(OH) 、
2
4Fe(OH) +O+2HO===4Fe(OH) 。
2 2 2 3
7
学科网(北京)股份有限公司8
学科网(北京)股份有限公司