文档内容
人教版(2019)高一必修第一册 第三章 铁 金属材料 第二
节 金属材料
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列物品所使用的主要材料属于无机非金属材料的是
A B C D
陶瓷工艺品 纸质练习簿 不锈钢脸盆 蚕丝领带
A.A B.B C.C D.D
2.2022年北京冬奥会速滑比赛将在国家速滑馆举行。运动员比赛用速滑冰刀由不锈
钢制成,不锈钢含有的最主要元素是( )
A.铁 B.碳 C.硅 D.铝
3.下列物质的性质与用途不具有对应关系的是
A.单质铝能导电,可用于制作导线
B.NaOH有碱性,可用于治疗胃酸过多
C.镁铝合金密度小,强度高,可用于制造飞机和宇宙飞船
D.Fe O 具有磁性,可用于制造录音磁带和电讯器材
3 4
4.足量下列物质与相同质量的铝反应,放出氢气且消耗溶质物质的量最少的是
A.盐酸 B.稀硫酸 C.氢氧化钠溶液 D.氯化钠溶液
5.下列叙述正确的是
A.金属钠着火时,可用泡沫灭火器灭火
B.将一小块钠投入 溶液中可置换出红色的固体
C. 在空气中加热,生成的主要产物为白色的
D.实验室做钠的实验时,余下的钠屑放回原试剂瓶
6.所谓合金,就是不同金属(也包括一些非金属)在熔化状态下形成的一种熔合物或冷却后的固体,下列组合金属最难形成二元合金的是
Fe Cu Zn Ag Au W
熔点/℃ 1535 1083 419.5 960.8 1063 3380
沸点/℃ 3000 2595 907 2212 2707 5627
A.Fe、Ag B.Ag、Au C.Zn、W D.Fe、Au
7.将一定量由Na和NaO 组成的混合物与足量的水反应,得到一定体积的混合气体,
2 2
将混合气体用电火花引燃,恰好完全反应,无气体剩余。则原混合物中Na和NaO 的
2 2
物质的量之比为
A.4:1 B.2:1 C.1:2 D.1:1
8.两种金属的混合物共15g,跟足量的盐酸反应时,恰好得到11.2L氢气(标况)。
下列各组金属不可能构成上述条件的混合物的是
A.镁和银 B.铜和锌 C.铝和铁 D.镁和铁
9.设阿伏加德罗常数的值为N ,下列说法不正确的是
A
A.0.1molC H 中含有的共用电子对数为1.9N
6 14 A
B.10g质量分数为46%的乙醇溶液中所含氧原子的总数为0.4N
A
C.标准状况下,2.24L己烷中含有的分子数为0.1N
A
D.1mol苯乙烯( )中含有的碳碳双键数为N
A
二、多选题
10.出土的锡青铜(铜锡合金)文物常有 覆盖在其表面。下列说法正确的是
A.锡青铜的熔点比纯铜的高
B.在自然环境中,锡青铜中的锡对铜起保护作用
C.锡青铜文物在潮湿环境中的腐蚀比在干燥环境中的快
D.生成 覆盖物是电化学腐蚀过程,但不是化学反应过程
三、计算题
11.铝、氧化铝的性质与其他常见金属及氧化物相比,有一定的特殊性。
(1)可用NaOH溶液除去铁粉中的铝粉,反应原理是(用离子方程式表示)___________,
试卷第2页,共3页将2.7gAl分别置于足量的NaOH溶液、稀硫酸中,生成H 的体积之比(同温同压)为
2
___________。
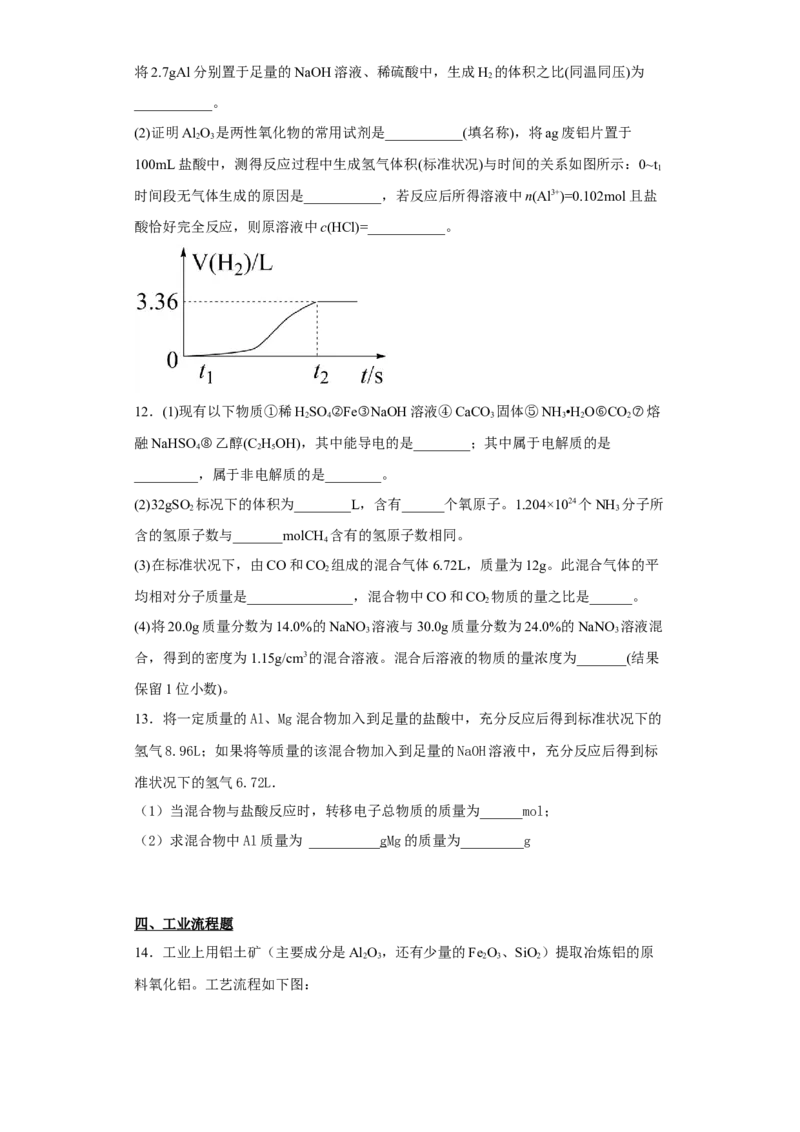
(2)证明Al O 是两性氧化物的常用试剂是___________(填名称),将ag废铝片置于
2 3
100mL盐酸中,测得反应过程中生成氢气体积(标准状况)与时间的关系如图所示:0~t
1
时间段无气体生成的原因是___________,若反应后所得溶液中n(Al3+)=0.102mol且盐
酸恰好完全反应,则原溶液中c(HCl)=___________。
12.(1)现有以下物质①稀HSO ②Fe③NaOH溶液④CaCO 固体⑤NH •H O⑥CO ⑦熔
2 4 3 3 2 2
融NaHSO⑧乙醇(C HOH),其中能导电的是________;其中属于电解质的是
4 2 5
_________,属于非电解质的是________。
(2)32gSO 标况下的体积为________L,含有______个氧原子。1.204×1024个NH 分子所
2 3
含的氢原子数与_______molCH 含有的氢原子数相同。
4
(3)在标准状况下,由CO和CO 组成的混合气体6.72L,质量为12g。此混合气体的平
2
均相对分子质量是_______________,混合物中CO和CO 物质的量之比是______。
2
(4)将20.0g质量分数为14.0%的NaNO 溶液与30.0g质量分数为24.0%的NaNO 溶液混
3 3
合,得到的密度为1.15g/cm3的混合溶液。混合后溶液的物质的量浓度为_______(结果
保留1位小数)。
13.将一定质量的Al、Mg混合物加入到足量的盐酸中,充分反应后得到标准状况下的
氢气8.96L;如果将等质量的该混合物加入到足量的NaOH溶液中,充分反应后得到标
准状况下的氢气6.72L.
(1)当混合物与盐酸反应时,转移电子总物质的质量为______mol;
(2)求混合物中Al质量为 __________gMg的质量为_________g
四、工业流程题
14.工业上用铝土矿(主要成分是Al O,还有少量的Fe O、SiO)提取冶炼铝的原
2 3 2 3 2
料氧化铝。工艺流程如下图:(1) 原料A的名称是______,步骤①反应的离子方程式是_________________。
(2) 滤液1中要加入稍过量原料B,原料B的化学式是_____,步骤②反应的离子方程
式是_____。
(3) 步骤③的化学方程式是:_____________________________。
(4) 如果省去步骤①,即溶解铝土矿是从加入原料B开始,后续操作不变,则会对氧
化铝的提取有什么影响____________________________。
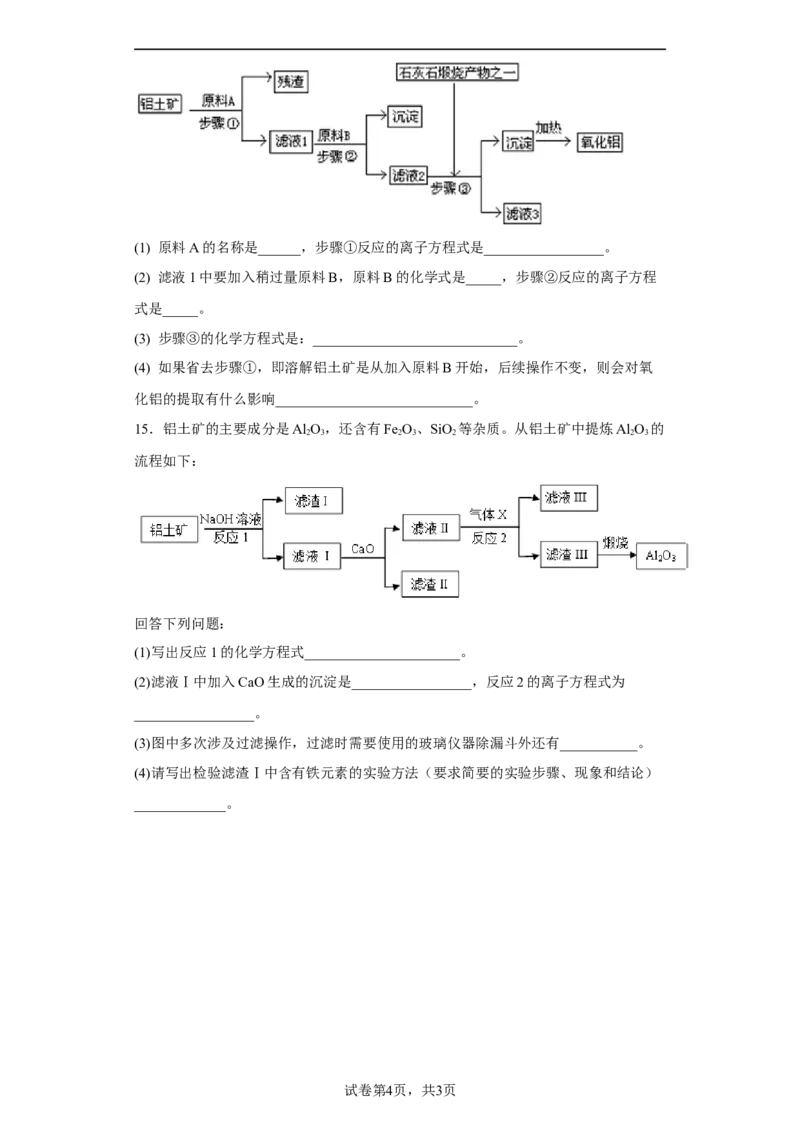
15.铝土矿的主要成分是Al O,还含有Fe O、SiO 等杂质。从铝土矿中提炼Al O 的
2 3 2 3 2 2 3
流程如下:
回答下列问题:
(1)写出反应1的化学方程式______________________。
(2)滤液Ⅰ中加入CaO生成的沉淀是_________________,反应2的离子方程式为
_________________。
(3)图中多次涉及过滤操作,过滤时需要使用的玻璃仪器除漏斗外还有___________。
(4)请写出检验滤渣Ⅰ中含有铁元素的实验方法(要求简要的实验步骤、现象和结论)
_____________。
试卷第4页,共3页参考答案:
1.A
【详解】A.陶瓷工艺品一般主要成分为硅酸盐,属于无机非金属材料,故A选;
B.纸质练习簿的主要成分为纤维素,属于有机非金属材料,故B不选;
C.不锈钢脸盆的主要成分为金属合金材料,属于无机金属材料,故C不选;
D.蚕丝领带的主要成分为蛋白质,属于有机非金属材料,故D不选;
综上所述,答案为A。
2.A
【详解】不锈钢含有Fe、Ni、Ti、Mn、N、Nb、Mo、Si、Cu等元素,最主要元素是铁。
答案选A。
3.B
【详解】A.导线材料需要有良好的导电能力,单质铝的导电性质对应用途,故A不选。
B.氢氧化钠属于强碱,具有强腐蚀性,服用氢氧化钠会造成食管和胃大面积烧灼,因此
不可以用于治疗胃酸过多,故B选。
C.制造飞机和宇宙飞船的材料具有强度高,耐高温,耐腐蚀,密度小等特点,镁铝合金
性质符合,故C不选。
D.录音磁带需要磁性材料作为信息的载体,因此Fe O 具有磁性的性质符合,故D不选。
3 4
故答案为:B。
4.C
【详解】氯化钠溶液与铝不反应,足量盐酸、稀硫酸、氢氧化钠溶液均能与铝反应生成氢
气,1mol铝反应时,消耗盐酸、硫酸和氢氧化钠的物质的量为3mol、1.5mol、1mol,则消
耗氢氧化钠的物质的量最少,故选C。
5.D
【详解】A.活泼金属钠着火用砂土盖灭,故A错误;
B.钠在溶液中无法置换金属,只会产生氢氧化物沉淀,故B错误;
C.加热产生过氧化钠,故C错误;
D.实验室做钠的实验时,余下的钠屑放回原试剂瓶,不能乱放,以防发生安全事故,故
D正确;
故选D。
6.C
【详解】合金是不同种金属在熔化状态下形成的一种熔合物,即两种金属都成为液态时进行混合;
A. 铁的熔点低于银的沸点,两种金属能够形成合金,故不选A;
B. 金的熔点低于银的沸点,两种金属能够形成合金,故不选B;
C. 由于锌的沸点较低,钨的熔点高于锌的沸点,在钨熔化时温度达3380℃,而此时锌已
变成气态,无法完成液态时混合,故不能形成合金,故选C;
D. 铁的熔点低于金的沸点,两种金属能够形成合金,故不选D。
答案选C。
【点睛】由合金的形成可知,两种金属若能够形成合金,则熔点较高的金属的熔点不能大
于熔点较低的金属的沸点。
7.B
【详解】钠与水、过氧化钠与水、氢气与氧气的反应方程式如下:2Na+2HO=2NaOH+H ↑
2 2
钠与氢气的关系式为∶2Na~ H ;2NaO+2H O=4NaOH+O ↑;过氧化钠与氧气的关系式为
2 2 2 2 2
∶2NaO~O ;2H+O 2HO氢气和氧气的关系式为∶2H~O ,将该混合气体通过放
2 2 2 2 2 2 2 2
电,恰好完全反应,说明氢气和氧气反应的物质的量之比恰好等于它们反应的计量数之比,
即氢气和氧气的物质的量之比为2:1,通过钠与氢气、过氧化钠与氧气、氢气与氧气的关系
式可得钠与过氧化钠的关系式为∶4Na-2H -O -2Na O,所以原混合物中Na和NaO 的物质
2 2 2 2 2 2
的量之比为4:2=2:1,故合理选项是B。
8.B
【分析】假设金属都为+2价,金属总物质的量等于氢气物质的量,根据M= 计算金属混
合物的平均相对原子质量,故平均相对原子质量应介于各组分之间,根据电子转移守恒,
若金属不与盐酸反应,其相对原子质量可以视作无穷大,若Al为+2价时,其相对原子质
量为27× =18,由此分析解答。
【详解】标况下11.2L氢气物质的量为=0.5mol,假设金属均为+2价,金属总物质的量等于
氢气物质的量,故混合金属平均相对分子质量为 =30,因为为两种金属的混合物,故平
均相对分子质量应介于各组分之间。
A.Mg的相对原子质量为24,银与盐酸不反应,其相对原子质量视作无穷大,符合题意,
答案第2页,共2页故A正确;
B.铜与盐酸不反应,其相对原子质量视作无穷大,Zn的相对分子质量为65,平均值大于
65,不符合题意,故B错误;
C.若Al为+2价时,其相对原子质量为27× =18,Fe的相对原子质量为56,符合题意,
故C正确;
D.Mg的相对原子质量为24,Fe的相对原子质量为56,平均值可能为30,故D正确;
故选:B。
9.C
【详解】A.根据碳氢的成键原理,1molC H 中含有的共用电子对数为19mol,故
6 14
0.1molC H 中含有的共用电子对数为1.9N ,A正确,不选;
6 14 A
B.在乙醇溶液中,除了乙醇外,水也含氧原子,而10g 46%的乙醇(C HO)水溶液中含乙
2 6
醇的质量为4.6g,物质的量为n=4.6g÷46g/mol=0.1mol,故含氧原子为0.1mol;含水的质量
为5.4g,物质的量为n=5.4g÷18g/mol=0.3mol,故含氧原子为0.3mol,故此溶液中含氧原子
共0.4mol,即氧原子的个数为0.4N ,故B正确,不选;
A
C.己烷是6个碳的烷烃,是液体,故标准状况下,2.24L己烷无法计算物质的量,C错误,
符合题意;
D.苯环不含碳碳双键,故1mol苯乙烯( )中含有的碳碳双键数为N ,D
A
正确,不选;
答案选C。
10.BC
【详解】A. 合金的熔点一般比各组分金属的熔点低,A项错误;
B. 在自然环境中, 与 构成原电池,因 比 的金属活动性强,所以 做负极,
做正极, 对 起保护作用,B项正确;
C. 合金在潮湿环境中发生电化学腐蚀,比在干燥环境中的腐蚀要快,C项正确;
D. 电化学腐蚀属于化学反应过程,D项错误;
故选BC。
11.(1) 2Al+2OH-+2H O=2 +3H ↑ 1:1
2 2
(2) 盐酸和氢氧化钠溶液 开始时铝表面的Al O 与盐酸反应 3.06mol/L
2 3【详解】(1)铁粉中的铝粉中加入NaOH溶液,只有Al与NaOH溶液反应,生成NaAlO
2
和H 等,从而除去Fe中混有的Al,反应原理是:2Al+2OH-+2H O=2 +3H ↑;Al与足
2 2 2
量的NaOH溶液、稀硫酸反应时都表现+3价,所以都存在关系式:2Al——3H,则2.7gAl
2
的物质的量为0.1mol,生成H 的物质的量都为0.15mol,体积之比(同温同压)为1:1。答案
2
为:2Al+2OH-+2H O=2 +3H ↑;1:1;
2 2
(2)依据两性氧化物的定义,两性氧化物既能与强酸反应,又能与强碱反应,且都生成盐
和水,所以证明Al O 是两性氧化物的常用试剂是盐酸和氢氧化钠溶液;将ag废铝片置于
2 3
100mL盐酸中,由于铝表面形成氧化膜,所以0~t 时间段氧化膜与盐酸反应,无气体生成,
1
原因是:开始时铝表面的Al O 与盐酸反应;若反应后所得溶液中n(Al3+)=0.102mol且盐酸
2 3
恰好完全反应,则依据守恒法,n(HCl)=n(Cl-)=3n(Al3+)=0.306mol,原溶液中c(HCl)=
=3.06mol/L。答案为:盐酸和氢氧化钠溶液;开始时铝表面的Al O 与盐酸反应;
2 3
3.06mol/L。
【点睛】废铝片中除去含Al O 和Al外,还含有其它杂质,所以我们不能利用ag进行计算。
2 3
12. ①②③⑦ ④⑤⑦ ⑥⑧ 11.2 N 1.5
A
40 1:3 2.7mol/L
【详解】(1)能导电的物质是指含有能够自由移动的离子或电子的物质,电解质是指在水溶
液或熔融状态下能够导电的化合物,非电解质是指在水溶液和熔融状态下都不能导电的化
合物,故①稀HSO ②Fe③NaOH溶液④CaCO 固体⑤NH •H O⑥CO ⑦熔融NaHSO⑧乙
2 4 3 3 2 2 4
醇(C HOH),其中能导电的是①②③⑦,其中属于电解质的是④⑤⑦,属于非电解质的是
2 5
⑥⑧,故答案为:①②③⑦;④⑤⑦;⑥⑧;
(2)32gSO 标况下的体积为 ,含有
2
个氧原子,根据
,则 , 解得:n(CH)=1.5mol,故
4
答案第4页,共2页答案为:11.2L;N ;1.5;
A
(3)设混合气体中CO物质的量为n,CO 物质的量为n,则有:22.4L/mol n+22.4
1 2 2 1
L/moln =6.72L和28g/moln +44g/moln =12g,解得:n=0.075mol,n=0.225mol,故此混合
2 1 2 1 2
气体的平均摩尔质量为: ,故气体的平均相对分
子质量是40,混合物中CO和CO 物质的量之比是0.075mol:0.225mol=1:3,故答案为:
2
40;1:3;
(4)将20.0g质量分数为14.0%的NaNO 溶液与30.0g质量分数为24.0%的NaNO 溶液混合,
3 3
得到的密度为1.15g/cm3的混合溶液,混合后溶液的物质的量浓度为
,故答案为:2.7mol/L。
13. 0.8 mol 2.4g 5.4g
【详解】(1)反应中生成的气体都是氢气,当混合物与盐酸反应时生成氢气的物质的量为:
=0.4mol,根据电子守恒可知反应转移电子的物质的量为:0.4mol×2=0.8mol;
(2)Al、Mg都与盐酸反应产生氢气,但只有Al与氢氧化钠溶液反应产生氢气,又由于等质
量铝与盐酸、氢氧化钠反应产生的氢气体积相同,都为6.72 L,则镁产生的氢气为:8.96 L
-6.72 L=2.24 L,
设Mg的质量为x,Al的质量为y,
Mg+2HCl=MgCl +H ↑
2 2
24g 22.4L
x 2.24 L
则:x=2.4 g,
2Al+6HCl═2AlCl +3H ↑ 或2Al+2NaOH+2H O═2NaAlO+3H
3 2 2 2 2
54g 67.2 L 54g 67.2 L
y 6.72 L y 6.72 L
则y=5.4g,
答:混合物中Mg的质量为2.4g,铝的质量为5.4g。
点睛:混合物成分分析的综合计算,本题解题关键是熟悉Mg与Al的性质相似与差异,Al、Mg均能与盐酸反应,而Al与NaOH溶液反应,而Mg不能与NaOH溶液反应,由此
结合反应原理,根据化学方程式逐一计算,还可以根据两次生成的气体差就是Mg与稀盐
酸反应生成的氢气进行计算。
14. 盐酸(硫酸、硝酸) Al O+6H+=2Al3++3H O、Fe O+6H+=2Fe3+
2 3 2 2 3
+3H O NaOH H++OH-=H O、Fe3++3OH-=Fe(OH) ↓、 Al3++4OH-=AlO -+2H O
2 2 3 2 2
NaAlO +CO +2H O=Al(OH) ↓+NaHCO 若用NaOH溶液溶解铝土矿,则有部分SiO 溶解
2 2 2 3 3 2
在NaOH溶液中生成硅酸钠,最后使加热制得的Al O 混有SiO 杂质
2 3 2
【详解】由工艺流程可知步骤③通入的为二氧化碳,生成的沉淀为氢氧化铝,所以滤液②
含有AlO-.步骤②应加入氢氧化钠,所以滤液①中含有Al3+,步骤①应为加入盐酸,除去
2
SiO。(1)由上述分析可知,步骤①加入盐酸,除去SiO,所以原料A为盐酸,氧化铝与
2 2
酸反应离子方程式为Al O+6H+=2Al3++3H O,氧化铁与盐酸反应离子方程式为
2 3 2
Fe O+6H+=2Fe3++3H O;
2 3 2
(2)步骤①加入过量盐酸,滤液①中含有Al3+、Fe3+、H+等,应加入NaOH,除去铁离子,
将铝离子转化为AlO-,反应为 H++OH-=H O,Fe3++3OH-=Fe(OH) ↓,Al3++4OH-=AlO -
2 2 3 2
+2H O;
2
(3)滤液②含有AlO-,步骤③通入二氧化碳,与AlO-反应生成的沉淀为氢氧化铝,反应
2 2
化学方程式为NaAlO +CO +2H O=Al(OH) ↓+NaHCO;
2 2 2 3 3
(4)若用NaOH溶液溶解铝土矿,则有部分SiO 溶解在NaOH溶液中生成硅酸钠,通入
2
二氧化碳会生成硅酸沉淀,最后使加热制得的Al O 混有SiO 杂质。
2 3 2
15. Al O+2NaOH=2NaAlO +H O;2NaOH+SiO =Na SiO+H O CaSiO
2 3 2 2 2 2 3 2 3
AlO-+CO +2H O=Al(OH) ↓+HCO-(或2AlO-+CO +3H O=2Al(OH) ↓+CO 2-) 烧
2 2 2 3 3 2 2 2 3 3
杯、玻璃棒 取少量滤渣I溶于足量的盐酸中,向澄清液中滴加KSCN溶液,若变
红色则说明滤渣I中含有铁元素。
【分析】铝土矿主要成分是Al O,还含有Fe O、SiO 等杂质。向铝土矿中加入NaOH溶
2 3 2 3 2
液,Al O、SiO 发生反应产生可溶性的NaAlO 、NaSiO 进入溶液I中,Fe O 不能反应进
2 3 2 2 2 3 2 3
入滤渣I,向滤液I中加入CaO,CaO与溶液中的HO反应产生Ca(OH) ,Ca(OH) 与
2 2 2
NaSiO 反应形成CaSiO 沉淀,NaAlO 不反应,留在滤液II中,向滤液II中通入足量CO
2 3 3 2 2
气体,NaAlO 溶液与CO 及HO反应产生Al(OH) 沉淀和NaHCO ,则滤渣III为
2 2 2 3 3
Al(OH) ,滤液II中含有NaHCO ,将Al(OH) 沉淀经过滤、洗涤,然后灼烧,发生分解产
3 3 3
生Al O。
2 3
答案第6页,共2页【详解】经上述分析可知滤渣I为Fe O,滤液I为NaAlO 、NaSiO 和过量的NaOH的混
2 3 2 2 3
合物,滤渣II为CaSiO ,滤液II为NaAlO 、NaOH的混合物,气体X为CO,滤液III为
3 2 2
NaHCO ,滤渣III为Al(OH) 。
3 3
(1) AlO 与NaOH溶液反应生成NaAlO 和H,SiO 与NaOH溶液反应生成NaSiO 和H,
2 3 2 2 2 2 3 2
所以反应1的方程式为Al O+2NaOH=2NaAlO +H O;2NaOH+SiO =Na SiO+H O;
2 3 2 2 2 2 3 2
(2)滤液I中含有NaAlO 、NaSiO 及过量的NaOH,向滤液I中加入CaO,CaO溶于水生成
2 2 3
氢氧化钙,氢氧化钙与硅酸钠反应生成硅酸钙沉淀,反应的化学方程式为
NaSiO+Ca(OH) =CaSiO ↓+2NaOH;反应2是向偏铝酸钠溶液中通入足量CO 生成Al(OH)
2 3 2 3 2 3
沉淀,反应的化学方程式为:AlO-+CO +2H O=Al(OH) ↓+HCO-(或写为2AlO-
2 2 2 3 3 2
+CO +3H O=2Al(OH) ↓+CO 2-);
2 2 3 3
(3)图中多次涉及过滤操作,过滤时需要使用的玻璃仪器除漏斗外还有玻璃棒、烧杯;
(4)滤渣Ⅰ含有Fe O,检验其中含有铁元素的方法是:取少量滤渣I,溶于足量的盐酸中,
2 3
然后向溶液中滴加硫氰化钾溶液,若变为血红色,说明滤渣I中含有铁元素。
【点睛】本题考查了无机物推断、混合物的分离、离子的检验等。理解工艺流程是解题的
关键,需要学生基本扎实的据此与运用知识分析解决问题的能力。答案第8页,共2页