文档内容
第四单元 物质结构和元素周期律
第3课 化学键(一)
一、基础巩固
1.元素性质呈周期性变化的原因是( )
A.原子量逐渐增大
B.核电荷数逐渐增大
C.核外电子排布呈周期性变化
D.元素化合价呈周期性变化
2.元素性质呈现周期性变化的根本原因是( )
A.元素原子的核外电子排布呈周期性变化
B.元素的相对原子质量递增,量变引起质变
C.元素的原子半径呈周期性变化
D.元素的化合价呈周期性变化
3.Mg、Ca、Sr、Ba是按原子序数由小到大的顺序排列的第ⅡA族元素。已知: Mg(OH) 难溶于水,
2
而Ca(OH) 微溶于水; MgSO 溶于水,而CaSO 微溶于水。下列推测中,①不正确的是( )
2 4 4
A.Sr(OH) 2 溶解于水 ②
B.SrSO 易溶于水
4
C.BaSO 不溶于水
4
D.Ba(OH) 比Ca(OH) 更易溶于水
2 2
4.硒( Se)元素是人体必需的微量元素之一,与溴同周期。下列说法不正确的是( )
34
A.原子半径由大到小顺序:Se>Br>Cl
B.氢化物的稳定性:硒化氢<水<氟化氢
C.SeO 和NaOH溶液反应生成Na SeO 和水
2 2 4
D.SeO 既可发生氧化反应,又可发生还原反应
2
5.锂是第2周期ⅠA族元素,下列有关锂元素性质推测正确的是( )
A.最高化合价为+2B.原子半径比钠的大
C.单质与水的反应比钠更剧烈
D.最高价氧化物对应的水化物碱性比钠的弱
6.关于As及同主族元素,下列说法中正确的是( )
A.As是第三周期ⅤA族元素
B.元素的主要正化合价为+3、+5
C.气态氢化物的还原性:NH >PH >AsH
3 3 3
D.同主族元素的单质从上到下,氧化性逐渐减弱,熔点逐渐降低
7.补充完成表:(请把序号 ~ 的答案填在相应的位置上)
元素 甲 ① ⑦ 乙 丙
元素符号 O
原子结构示意图 ① ②
③ ④
周期 三 三
族 ⅦA ⑤
⑥ ⑦
① ② ③ ④ ⑤ ⑥
二、⑦拓展提升
8.已知X、Y、Z、W四种元素是元素周期表中连续三个不同短周期的元素,且原子序数依次增大.X、
W同主族,Y、Z为同周期的相邻元素.W原子的质子数等于Y、Z原子最外层电子数之和.Y的氢化
物分子中有3个共价键.Z原子最外层电子数是次外层电子数的3倍.试推断:
(1)X、Y、Z、W四种元素的符号:
X 、Y 、Z 、W
(2)由以上元素中的两种元素组成的能溶于水且水溶液显碱性的化合物的电子式分别为
, .
(3)由X、Y、Z所形成的离子化合物是 ,它与W的最高氧化物的水化物的浓溶液加
热时反应的离子方程式是 .
9. X、Y和W为原子序数依次递增的1﹣18号元素,X和Y有相同的最外层电子数,X元素原子最外层电
子数是次外层电子数的3倍。
(1)写出实验室制取W 的离子方程式 。
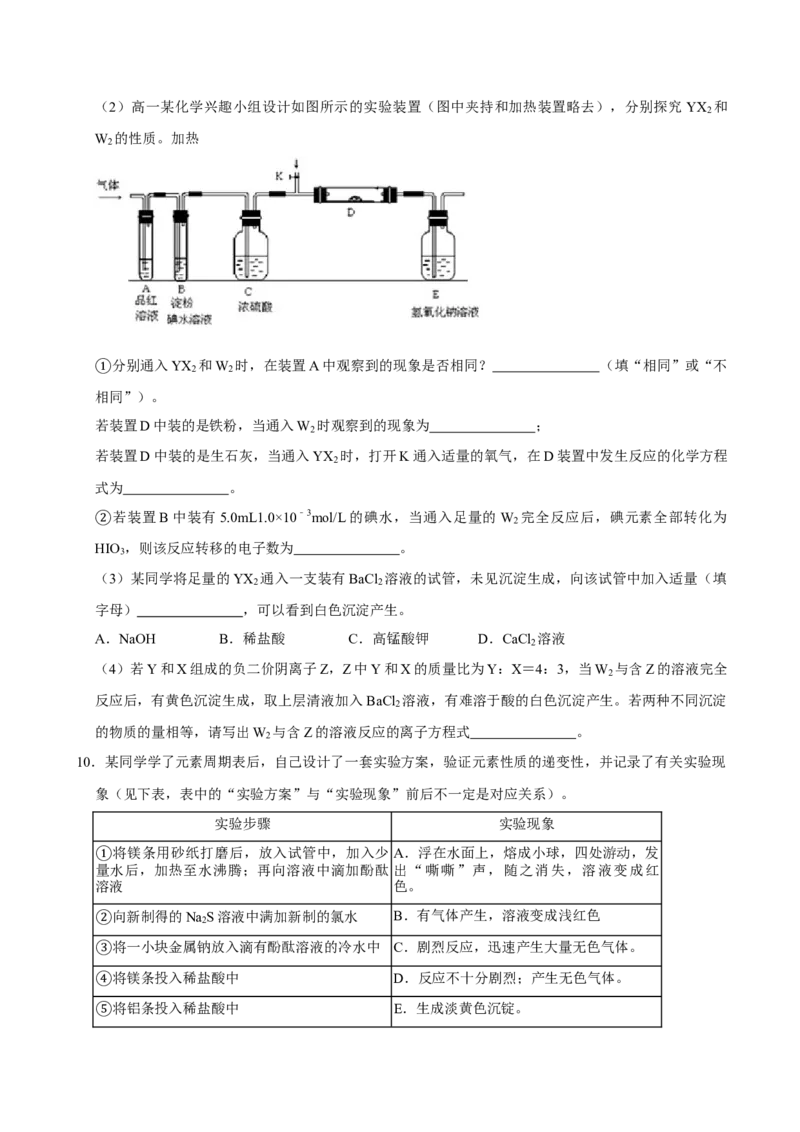
2(2)高一某化学兴趣小组设计如图所示的实验装置(图中夹持和加热装置略去),分别探究 YX 和
2
W 的性质。加热
2
分别通入YX 和W 时,在装置A中观察到的现象是否相同? (填“相同”或“不
2 2
①相同”)。
若装置D中装的是铁粉,当通入W 时观察到的现象为 ;
2
若装置D中装的是生石灰,当通入YX 时,打开K通入适量的氧气,在D装置中发生反应的化学方程
2
式为 。
若装置B中装有5.0mL1.0×10﹣3mol/L的碘水,当通入足量的W 完全反应后,碘元素全部转化为
2
②HIO ,则该反应转移的电子数为 。
3
(3)某同学将足量的YX 通入一支装有BaCl 溶液的试管,未见沉淀生成,向该试管中加入适量(填
2 2
字母) ,可以看到白色沉淀产生。
A.NaOH B.稀盐酸 C.高锰酸钾 D.CaCl 溶液
2
(4)若Y和X组成的负二价阴离子Z,Z中Y和X的质量比为Y:X=4:3,当W 与含Z的溶液完全
2
反应后,有黄色沉淀生成,取上层清液加入BaCl 溶液,有难溶于酸的白色沉淀产生。若两种不同沉淀
2
的物质的量相等,请写出W 与含Z的溶液反应的离子方程式 。
2
10.某同学学了元素周期表后,自己设计了一套实验方案,验证元素性质的递变性,并记录了有关实验现
象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系)。
实验步骤 实验现象
将镁条用砂纸打磨后,放入试管中,加入少 A.浮在水面上,熔成小球,四处游动,发
量水后,加热至水沸腾;再向溶液中滴加酚酞 出“嘶嘶”声,随之消失,溶液变成红
①溶液 色。
向新制得的Na S溶液中满加新制的氯水 B.有气体产生,溶液变成浅红色
2
②将一小块金属钠放入滴有酚酞溶液的冷水中 C.剧烈反应,迅速产生大量无色气体。
③将镁条投入稀盐酸中 D.反应不十分剧烈;产生无色气体。
④将铝条投入稀盐酸中 E.生成淡黄色沉锭。
⑤请你帮助该同学整理并完成实验报告。
实验目的:研究同周期元素性质的递变性
(1)实验用品:
试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na S溶液,AlC1 溶液,NaOH溶液,酚酞溶
2 3
液等。
仪器: (写两种以上的玻璃仪器),试管夹,胶头滴管,镊子,小刀,玻璃片,砂纸,
火柴等。
(2)实验记录:(填写与实验步骤对应的实验现象的编号和步骤 、步骤 反应的离子方程式)
实验内容 ② ⑤
实验现象(填A~E) ① ② ③ ④ ⑤
步骤 ,
步骤② ,
(3)⑤实验结论: 。
(4)总结反思:
从原子结构角度分析,同周期元素产生性质递变性的原因是 。