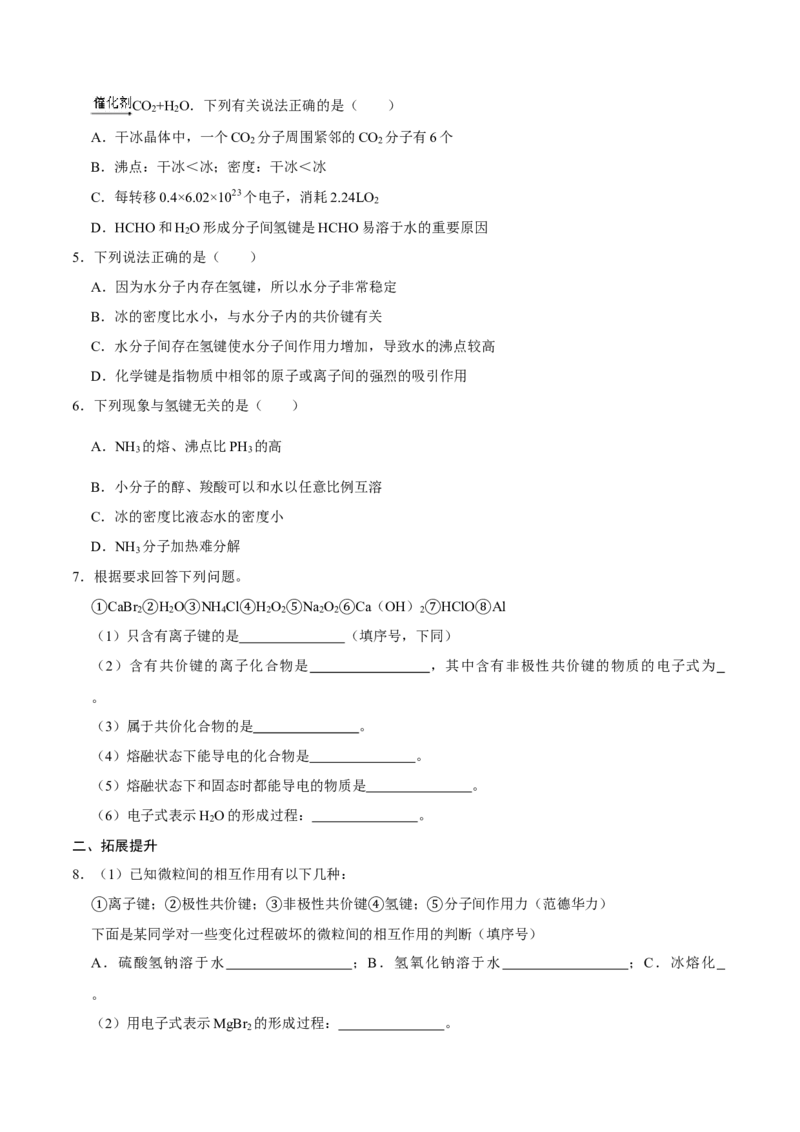文档内容
第四单元 物质结构和元素周期律
第3课 化学键(二)
一、基础巩固
1.意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的气态N 分子,其分子结构如图所示。
4
N 转变为N 并释放出大量能量。判断下列说法正确的是( )
4 2
A.N 属于一种新型的化合物
4
B.N 分子中存在非极性键
4
C.N 和N 互为同位素
4 2
D.N 比N 更稳定
4 2
2.利用固体表面催化工艺进行NO分解的过程如图所示(●N〇O)。下列说法不正确的是( )
A.NO属于极性分子
B.O 含有非极性共价键
2
C.过程 释放能量,过程 吸收能量
D.标准②状况下,NO分解生③成5.6LN
2
转移电子数为6.02×1023
3.清洁的水对人类的生存非常重要,关于H O的描述正确的是( )
2
A.含有非极性键和极性键
B.纯水几乎不导电,属于非电解质
C.带静电的玻璃棒接近,水流会发生偏转
D.水分子间作用力大,所以加热很难分解
4.我国科学家研制出一种催化剂,能在室温下高效催化空气中甲醛的氧化,其反应如下:HCHO+O
2CO +H O.下列有关说法正确的是( )
2 2
A.干冰晶体中,一个CO 分子周围紧邻的CO 分子有6个
2 2
B.沸点:干冰<冰;密度:干冰<冰
C.每转移0.4×6.02×1023个电子,消耗2.24LO
2
D.HCHO和H O形成分子间氢键是HCHO易溶于水的重要原因
2
5.下列说法正确的是( )
A.因为水分子内存在氢键,所以水分子非常稳定
B.冰的密度比水小,与水分子内的共价键有关
C.水分子间存在氢键使水分子间作用力增加,导致水的沸点较高
D.化学键是指物质中相邻的原子或离子间的强烈的吸引作用
6.下列现象与氢键无关的是( )
A.NH 的熔、沸点比PH 的高
3 3
B.小分子的醇、羧酸可以和水以任意比例互溶
C.冰的密度比液态水的密度小
D.NH 分子加热难分解
3
7.根据要求回答下列问题。
CaBr H O NH Cl H O Na O Ca(OH) HClO Al
2 2 4 2 2 2 2 2
①(1)只含②有离子③键的是 ④ ⑤ ⑥(填序号,下⑦同) ⑧
(2)含有共价键的离子化合物是 ,其中含有非极性共价键的物质的电子式为
。
(3)属于共价化合物的是 。
(4)熔融状态下能导电的化合物是 。
(5)熔融状态下和固态时都能导电的物质是 。
(6)电子式表示H O的形成过程: 。
2
二、拓展提升
8.(1)已知微粒间的相互作用有以下几种:
离子键; 极性共价键; 非极性共价键 氢键; 分子间作用力(范德华力)
①下面是某同学②对一些变化过程③破坏的微粒间的④相互作用⑤的判断(填序号)
A.硫酸氢钠溶于水 ;B.氢氧化钠溶于水 ;C.冰熔化
。
(2)用电子式表示MgBr 的形成过程: 。
2(3)下列物质各原子都达8e﹣稳定结构的是 (填序号)
A.CH B.CS C.PCl D.PH E.N F.HCl
4 2 5 3 2
(4)向含Cr O 2﹣的酸性废水中加入FeSO 溶液,使Cr O 2﹣全部转化为Cr3+.写出该反应的离子方程
2 7 4 2 7
式: 。
9.(1)比较给出H+的能力的相对强弱:H CO H O (填“>”、“<”或“=”);
2 3 2
用一个离子方程式说明CO 2﹣和C H O﹣结合H+能力的相对强弱 。
3 6 5
(2)Ca(CN) 是离子化合物,各原子均满足 8 电子稳定结构。写出 Ca(CN) 的电子式
2 2
。
(3)常压下,水晶的硬度比晶体硅的硬度大,其主要原因是 。
10.按要求回答下面问题。
(1)N 电子式 、结构式 。
2
(2)CO 电子式 、结构式 。
2
(3)Cl 电子式 、结构式 。
2
(4)CH 电子式 。
4
(5)H O+电子式 。
3
(6)F﹣电子式 。
(7)CaCl 电子式 。
2