文档内容
第二章 第三节 化学反应的方向 测试题
榆次一中 李金虎
一、选择题(本题共有15小题,每小题4分,共60分,每小题只有一个正确选项)
1. 下列关于自发反应的说法中错误的是( )
A.非自发反应在一定条件下可以实现
B.能够设计成原电池的反应是自发进行的氧化还原反应
C.电解质在水溶液中的电离是一个自发过程,该过程为熵增过程
D.2NO (g)+4CO(g)===N (g)+4CO(g) ΔH<0,则该反应高温下利于自发进行
2 2 2
2. 下列过程均为自发过程的是( )
①铵盐的溶解 ②烧碱与盐酸反应 ③Zn与稀硫酸反应 ④氢气在氧气中燃烧
⑤Mg在空气中燃烧 ⑥铝热反应 ⑦墨水在水中扩散 ⑧电解熔融的氯化钠
A.①②③④ B.⑤⑥⑦⑧
C.②④⑥⑧ D.①②③④⑤⑥⑦
3. 下列反应中,熵显著增加的反应是( )
A.CO(g)+2H(g)===CH OH(g)
2 3
B.CaCO +2HCl===CaCl +H O+CO↑
3 2 2 2
C.C(s)+O(g) ===CO (g)
2 2
D.2Na(s)+O (g) ===Na O(s)
2 2
4. 下列对熵变的判断中不正确的是( )
A.少量的食盐溶于水中:ΔS>0
B.碳和氧气反应生成CO(g);ΔS>0
C.气态水变成液态水;ΔS>0
D.CaCO (s)受热分解为CaO(s)和CO(g);ΔS>0
3 2
5. 某反应A===B+C 在室温下不能自发进行,在高温下能自发进行,对该反应过程的焓变(ΔH)、
熵变(ΔS)的判断正确的是( )
A.ΔH<0、ΔS>0 B.ΔH>0、ΔS<0
C.ΔH>0、ΔS>0 D.ΔH<0、ΔS<0
6. 自由能变化(ΔG)是反应方向判断的复合判据:ΔG=ΔH-TΔS,ΔG<0时反应自发进行。已知某化
学反应其ΔH=-122 kJ·mol-1,ΔS=+231 J·mol-1·K-1,则此反应在下列哪种情况下可自发进行(
)
A.在任何温度下都能自发进行
1
学科网(北京)股份有限公司B.在任何温度下都不能自发进行
C.仅在高温下自发进行
D.仅在低温下自发进行
7. 下列自发反应可以用熵判据来解释的是( )
A.2NO (g) NO(g) ΔH=-56.9 kJ·mol-1
2 2 4
B.2NO(g) ===4NO(g)+O(g) ΔH=+56.7 kJ·mol-1
2 5 2 2
C.N(g)+3H(g) 2NH (g) ΔH=-92.3 kJ·mol-1
2 2 3
1
D.H(g)+ O(g) ===H O(l) ΔH=-285.8 kJ·mol-1
2 2 2
2
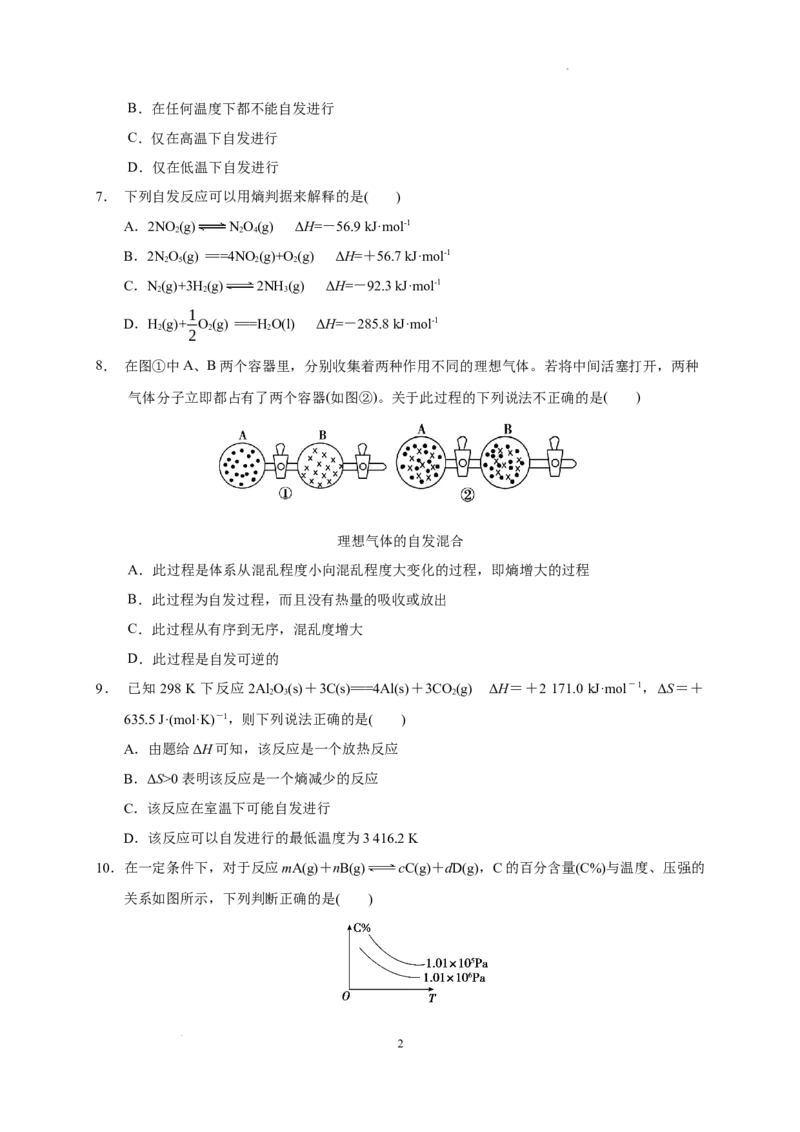
8. 在图①中A、B两个容器里,分别收集着两种作用不同的理想气体。若将中间活塞打开,两种
气体分子立即都占有了两个容器(如图②)。关于此过程的下列说法不正确的是( )
理想气体的自发混合
A.此过程是体系从混乱程度小向混乱程度大变化的过程,即熵增大的过程
B.此过程为自发过程,而且没有热量的吸收或放出
C.此过程从有序到无序,混乱度增大
D.此过程是自发可逆的
9. 已知298 K下反应 2Al O(s)+3C(s)===4Al(s)+3CO(g) ΔH=+2 171.0 kJ·mol-1,ΔS=+
2 3 2
635.5 J·(mol·K)-1,则下列说法正确的是( )
A.由题给ΔH可知,该反应是一个放热反应
B.ΔS>0表明该反应是一个熵减少的反应
C.该反应在室温下可能自发进行
D.该反应可以自发进行的最低温度为3 416.2 K
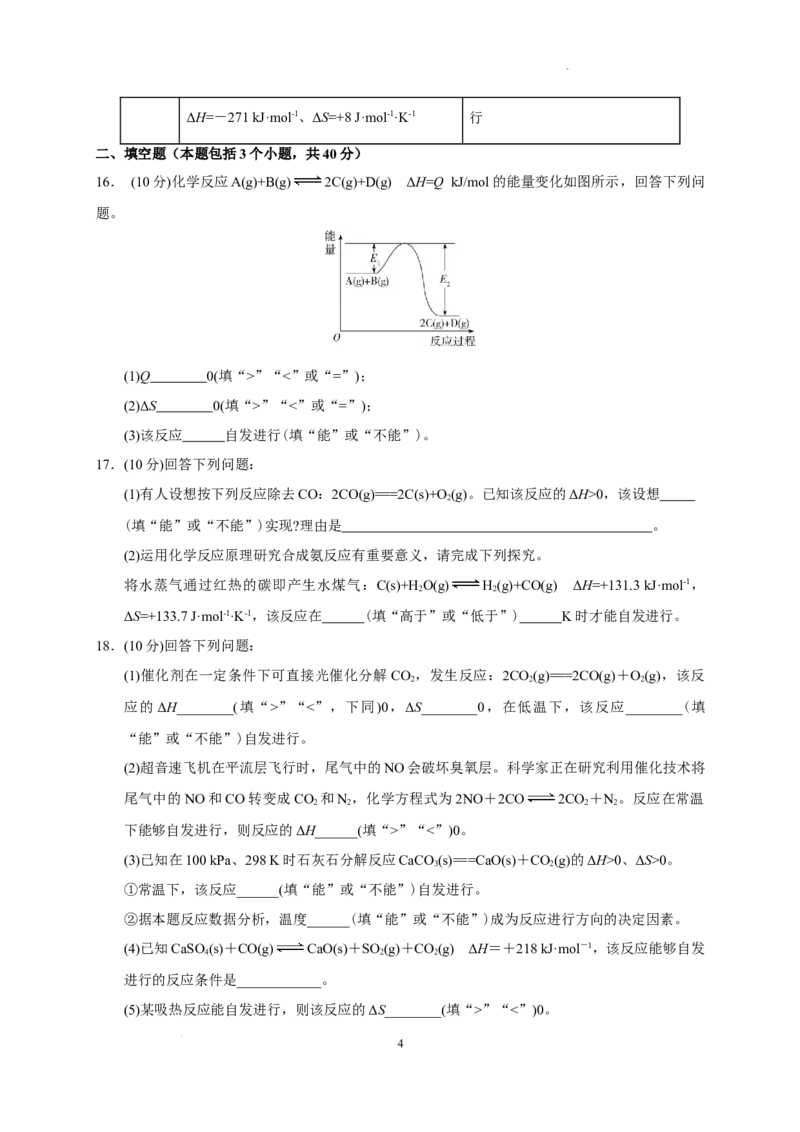
10.在一定条件下,对于反应mA(g)+nB(g) cC(g)+dD(g),C的百分含量(C%)与温度、压强的
关系如图所示,下列判断正确的是( )
2
学科网(北京)股份有限公司A.ΔH<0、ΔS>0 B.ΔH>0、ΔS<0
C.ΔH>0、ΔS>0 D.ΔH<0、ΔS<0
11.某反应过程中的能量变化如图所示。下列叙述正确的是( )
A.该反应的ΔH= E -E
2 1
B.该反应的能量变化与合成氨反应的能量变化相同
C.加入催化剂既能减小反应的ΔH,又能加快反应速率
D.若该反应在常温下能自发进行,则反应的ΔS>0
12.下列反应常温时能自发进行,并既能用焓判据又能用熵判据解释的是( )
A.HCl(g)+NH (g) NH Cl(s)
3 4
B.2KClO(s) 2KCl(s)+3O(g)
3 2
C.2NaO+2H O 4NaOH+O ↑
2 2 2 2
D.Ba(OH) ·8H O+2NH Cl BaCl + 2NH ↑+10H O
2 2 4 2 3 2
13.下列关于化学反应的自发性和进行方向的说法正确的是( )
A.非自发反应在任何条件下都不能发生
B.一定温度下,反应Mg(l)+Cl (g) ===MgCl (l)的ΔH<0,ΔS<0
2 2
C.由ΔG=ΔH-TΔS可知,所有放热反应都能自发进行
D.只有不需要任何条件就能够自动进行的过程才是自发过程
14.一定温度下,HF分子容易双聚或多聚:nHF(g) (HF) (g) ΔH<0。欲测定HF的相对分子
n
质量,最适合的条件是( )
A.低温高压 B.高温低压
C.低温低压 D.高温高压
15.下列内容与原因或结论不对应的是( )
选项 内容 原因或结论
A HO(g)变成HO(l) 该过程ΔS>0
2 2
B 硝酸铵溶于水可自发进行 因为ΔS>0
C 一个反应的ΔH>0、ΔS<0 该反应不能自发进行
D H(g)+F (g) 2HF(g)的 该反应在任何温度下均可自发进
2 2
3
学科网(北京)股份有限公司ΔH=-271 kJ·mol-1、ΔS=+8 J·mol-1·K-1 行
二、填空题(本题包括3个小题,共40分)
16. (10分)化学反应A(g)+B(g) 2C(g)+D(g) ΔH=Q kJ/mol的能量变化如图所示,回答下列问
题。
(1)Q 0(填“>”“<”或“=”);
(2)ΔS 0(填“>”“<”或“=”);
(3)该反应 自发进行(填“能”或“不能”)。
17.(10分)回答下列问题:
(1)有人设想按下列反应除去CO:2CO(g)===2C(s)+O (g)。已知该反应的ΔH>0,该设想
2
(填“能”或“不能”)实现?理由是 。
(2)运用化学反应原理研究合成氨反应有重要意义,请完成下列探究。
将水蒸气通过红热的碳即产生水煤气:C(s)+HO(g) H(g)+CO(g) ΔH=+131.3 kJ·mol-1,
2 2
ΔS=+133.7 J·mol-1·K-1,该反应在 (填“高于”或“低于”) K时才能自发进行。
18.(10分)回答下列问题:
(1)催化剂在一定条件下可直接光催化分解 CO ,发生反应:2CO(g)===2CO(g)+O(g),该反
2 2 2
应的 ΔH________(填“>”“<”,下同)0,ΔS________0,在低温下,该反应________(填
“能”或“不能”)自发进行。
(2)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将
尾气中的NO和CO转变成CO 和N ,化学方程式为2NO+2CO 2CO +N 。反应在常温
2 2 2 2
下能够自发进行,则反应的ΔH______(填“>”“<”)0。
(3)已知在100 kPa、298 K时石灰石分解反应CaCO (s)===CaO(s)+CO(g)的ΔH>0、ΔS>0。
3 2
①常温下,该反应______(填“能”或“不能”)自发进行。
②据本题反应数据分析,温度______(填“能”或“不能”)成为反应进行方向的决定因素。
(4)已知CaSO(s)+CO(g) CaO(s)+SO (g)+CO(g) ΔH=+218 kJ·mol-1,该反应能够自发
4 2 2
进行的反应条件是____________。
(5)某吸热反应能自发进行,则该反应的ΔS________(填“>”“<”)0。
4
学科网(北京)股份有限公司19.(10分)(1)汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)===2C(s)+
O(g)。已知该反应的ΔH>0,简述该设想能否实现的依据:
2
______________________________________________。
(2)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将
尾气中的NO和CO转变成CO 和N,化学方程式如下:2NO+2CO===2CO +N。反应能够
2 2 2 2
自发进行,则反应的ΔH________0(填“>”“<”或“=”)。理由是
_____________________________。
1.答案:D
解析:非自发反应在一定条件下能实现自发进行,如ΔH>0、ΔS>0的反应高温下可以自发进行,低
温下不能自发进行,A正确;理论上,能够设计成原电池的反应是常温下能自发进行的氧化还原反
应,B正确;电解质在水溶液中的电离是一个自发过程,该过程中电解质电离产生自由移动的离子,
微粒数目增大,故该过程为熵增过程,C 正确;反应 2NO (g)+4CO(g)===N (g)+4CO(g)的
2 2 2
ΔH<0、ΔS<0,若自发进行,应满足ΔH-TΔS<0,故该反应低温下有利于自发进行,D错误。
2.答案:D
解析:自发过程是不借助外力就能自动发生的过程,而电解熔融的氯化钠要在直流电作用下进行。
3.答案:B
解析:根据固态的熵值最小,液态的的熵值次之,气态的熵值最大,可以判断B对
4.答案:C
解析:食盐溶于水是典型的熵增过程;2C(s)+O(g) 2CO(g),反应后气体的物质的量增大,为
2
熵增加的反应;气态水变成液态水,体系混乱度减小,为熵减小的过程;CaCO (s)分解产生了气体,
3
为熵增加的反应。
5.答案:C
解析:根据室温下ΔG=ΔH-TΔS>0,在高温下ΔG<0,可推出ΔH>0、ΔS>0,故C项正确。
6.答案:A
解析:由公式ΔG=ΔH-TΔS可得,当ΔH<0,ΔS>0时,不管T取什么数值,ΔG总是小于0,所以
在任何温度下反应都能自发进行。
7.答案:B
解析:A、C、D三个选项的反应均是熵减小的反应,ΔS<0,只有B项中ΔS>0,是熵增大的自发反
应,可用熵判据来解释。
5
学科网(北京)股份有限公司8.答案:D
解析:由题意可知,此过程为不伴随能量变化的自发过程,是体系混乱度增大的过程。而自发过
程是不可逆的。
9.答案:D
解析:该反应的ΔH>0,为吸热反应,A项错误;ΔS>0,表明该反应是熵增的反应,B项错误;由
常温下,该反应的ΔH-TΔS>0可知,该反应在常温下不能自发进行,C项错误;该反应可以自发
进行的最低温度为T== K=3 416.2 K,D项正确。
10.答案:A
解析:由图可知,当压强一定时,升高温度,C的百分含量减小,说明升高温度,平衡逆向移动,
则有ΔH<0;当温度一定时,增大压强,C的百分含量减小,说明增大压强,平衡逆向移动,则有
m+n0,A正确。
11.答案:D
解析:ΔH=正反应的活化能-逆反应的活化能=E -E ,A错误;合成氨反应为放热反应,图示反应
1 2
为吸热反应,图示反应的能量变化与合成氨反应的能量变化不同,B错误;加催化剂能够降低反应
的活化能,但不影响反应的始态和终态,因此不能改变反应的ΔH,但可以加快反应速率,C错误;
图示反应为吸热反应,ΔH>0,若该反应在常温下能自发进行,即 ΔG=ΔH-TΔS<0,则反应的
ΔS>0,D正确。
12.答案:C
解析:A项中两种气体生成一种固体,熵减小,不能用熵判据解释,A不符合题意;B项是吸热反
应,不能用焓判据解释,B不符合题意;C项中的反应是放热反应,生成物能量降低,能用焓判据
解释,同时,固体与液体反应生成了气体,熵增加,也能用熵判据解释,C符合题意;D 项NH Cl
4
与Ba(OH) ·8H O反应产生NH ,熵增加,能用熵判据解释,同时产生结冰现象,温度降低,是一
2 2 3
个吸热反应,不能用焓判据解释,D不符合题意。
13.答案:B
解析:非自发反应在一定条件下也可发生,A错误;该反应为放热反应,且反应过程中气体分子数
减小,因此ΔH<0,ΔS<0,B正确;所有放热且熵增加的反应都能自发进行,放热且熵减小的反应
在高温下不能自发进行,C错误;自发过程并不是不需要条件,D错误。
14.答案:B
解析:由于存在平衡nHF(g) (HF) (g),(HF) 的存在会影响HF的相对分子质量的测定,故应采
n n
取措施使平衡逆向移动,以减少(HF) 的含量;该反应的正反应为气体体积减小的放热反应,高温
n
6
学科网(北京)股份有限公司低压有利于平衡逆向移动。
15.答案:A
解析:HO(g)变成HO(l),体系混乱度减小,则ΔS<0,A错误;常温下硝酸铵溶于水是一个能自发
2 2
进行的吸热过程,硝酸铵溶解生成自由移动的离子,是熵增大的过程,ΔS>0,B正确;一个反应的
ΔH>0、ΔS<0,则 ΔH-TΔS>0,所以该反应不能自发进行,C 正确;ΔH=-271 kJ·mol-1,ΔS=+8
J·mol-1·K-1,由ΔH-TΔS<0的反应可自发进行可知,该反应在任何温度下都能自发进行,D正确。
16.答案:(1) < (2) > (3)能
17.答案:(1)不能 该反应的ΔH>0、ΔS<0,任何温度下均不能自发进行 (2)高于 982.0
解析:(1)该反应的 ΔH>0、ΔS<0,根据 ΔG=ΔH-TΔS可知 ΔG>0,故该设想不能实现。(2)根据
ΔG=ΔH-TΔS<0时反应能自发进行,ΔH=+131.3 kJ·mol-1,ΔS=+133.7 J·mol-1·K-1=+0.133 7 kJ·mol-1·K-1,解
得T> 131.3 kJ·mol-1 ≈982.0 K,即温度高于982.0 K时该反应能自发进行。
0.133 7 kJ·mol-1·K-1
18.答案:(1) > > 不能 (2) < (3)① 不能 能 (4)高温 (5) >
解析:(1)由于CO在O 中燃烧生成CO 为放热反应,则二氧化碳分解生成CO和氧气的反应为吸热
2 2
反应,ΔH>0,根据化学方程式可知,反应后气体的化学计量数之和增加,ΔS>0,故低温下ΔG=
ΔH-TΔS>0,反应不能自发进行。(2)ΔG=ΔH-TΔS<0时反应能自发进行,通过化学方程式可知
ΔS<0,常温下反应能够自发进行,则 ΔH<0。(3)①ΔG=ΔH-TΔS<0时反应能自发进行,已知
ΔH>0,ΔS>0,则常温下不能自发进行;②该反应的ΔH>0、ΔS>0,高温条件下能使ΔG=ΔH-
TΔS<0,而低温条件下ΔG=ΔH-TΔS>0,则该反应中温度是决定反应进行方向的因素。(4)该反应
的ΔS>0、ΔH>0,则高温时ΔG=ΔH-TΔS<0,反应能自发进行。 (5)已知某吸热反应能自发进行,
即ΔG=ΔH-TΔS<0,ΔH>0,则ΔS>0。
19.答案:(1)不能实现,因为该反应的ΔH>0,ΔS<0,反应不可能自发进行 (2)< 该反应的ΔS
<0,因该反应能自发进行,根据ΔG=ΔH-TΔS<0,可知ΔH<0
7
学科网(北京)股份有限公司8
学科网(北京)股份有限公司