文档内容
第 10 讲 物质的量 摩尔质量
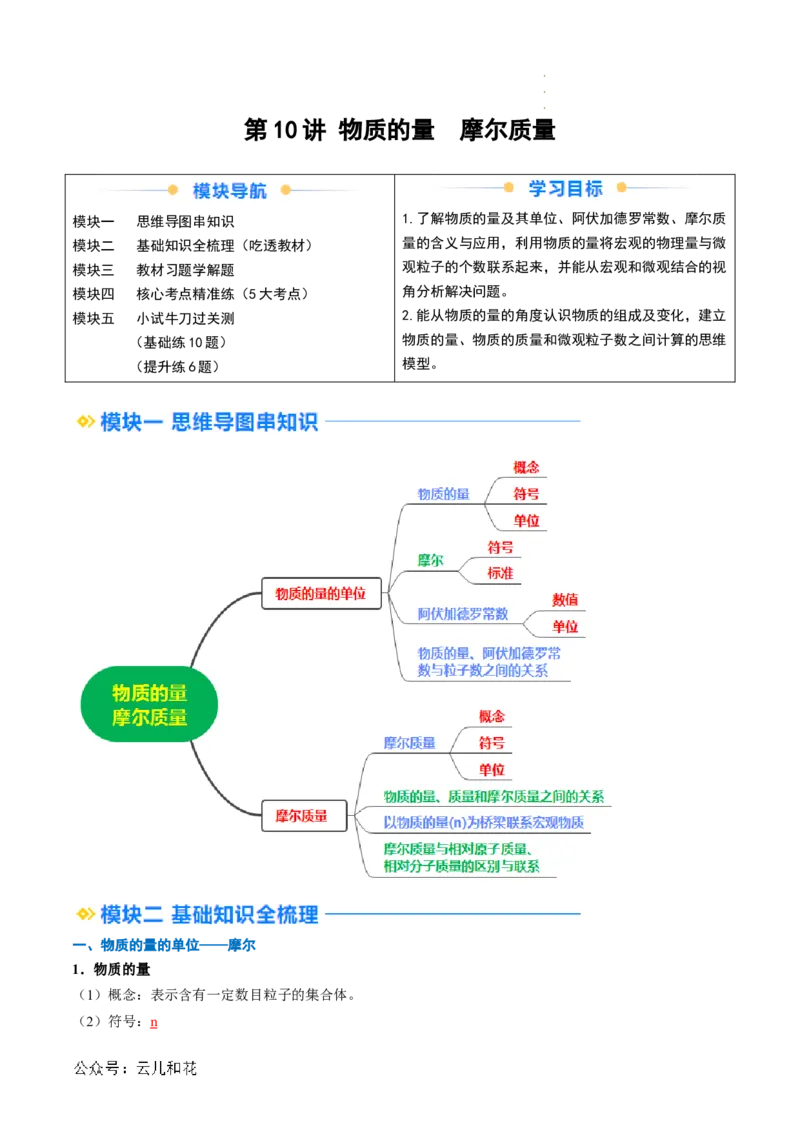
模块一 思维导图串知识 1.了解物质的量及其单位、阿伏加德罗常数、摩尔质
模块二 基础知识全梳理(吃透教材) 量的含义与应用,利用物质的量将宏观的物理量与微
模块三 教材习题学解题 观粒子的个数联系起来,并能从宏观和微观结合的视
模块四 核心考点精准练(5大考点) 角分析解决问题。
模块五 小试牛刀过关测 2.能从物质的量的角度认识物质的组成及变化,建立
(基础练10题) 物质的量、物质的质量和微观粒子数之间计算的思维
(提升练6题) 模型。
一、物质的量的单位——摩尔
1.物质的量
(1)概念:表示含有一定数目粒子的集合体。
(2)符号:n
学科网(北京)股份有限公司(3)单位:mol
(4)描述对象:微观粒子
2.摩尔
(1)符号:mol
(2)标准:1 mol粒子集体所含的粒子数与0.012 kg 12C中所含的C原子个数相同,即含有6.02×1023个粒
子的任何粒子集合体称为1 mol。
(3)注意事项:①摩尔使用于微观粒子;②使用时指明微粒种类或组合。
【特别提醒】表述微观粒子的物质的量时,必须指明微观粒子的符号、化学式或具体名称,而不能直接用
元素名称表示,一般用“数量+单位+粒子”来表示,如1 mol H指 1 mol 氢原子 ,1 mol H 指 1 mol 氢分
2
子,而不能指1 mol氢。
3.阿伏加德罗常数
(1)数值: 6.02×10 23
(2)阿伏加德罗常数的单位: mol - 1 。
【易错警示】阿伏加德罗常数是一个物理量,单位是mol-1,而不是纯数。不能误认为N 就是6.02×1023。
A
4.物质的量、阿伏加德罗常数与粒子数之间的关系
(1)关系式:n=。
(2)结论:微粒之间的物质的量之比等于微粒的粒子数之比。
【归纳提升】物质的量的理解——“四化”
二、摩尔质量
1.摩尔质量
(1)概念:单位物质的量的物质所具有的质量
(2)符号: M 单位: g·mol - 1 或 kg·mol - 1
(3)数值:任何粒子的摩尔质量,当以 g·mol - 1 为单位时,数值上等于其化学式的式量。
2.物质的量、质量和摩尔质量之间的关系
学科网(北京)股份有限公司n=
3. 以物质的量(n)为桥梁联系宏观物质
质量(m)与微观微粒数(N)之间的关系: = n = 。
4.摩尔质量与相对原子质量、相对分子质量的区别与联系
摩尔质量(M) 相对原子质量 相对分子质量
①单位物质的量的物质所具有 ①一个原子的质量与 12C的1/12 ①化学式中各元素相对
概念
的质量; 作比较,所得的比值; 原子质量之和;
单位 ②单位是g/mol或kg/mol ②单位:无 ②单位:无
摩尔质量以g/mol为单位时,在数值上等于其相对分子质量或相对原子质量;
联系 混合物组成一定时,1 mol 混合物的质量在数值上就是该混合物的摩尔质量,在数值上等于
该混合物的平均相对分子质量
【归纳总结】
(1)摩尔质量概念的理解
①等值性:摩尔质量以g·mol-1为单位时,在数值上与其相对分子质量或相对原子质量相等。
②确定性:对于指定的物质来说,其摩尔质量的值是一个定值,不随物质的物质的量的多少而改变。
(2)摩尔质量的计算方法
①已知任意状态物质的质量时:M=(定义式)。
②已知一个分子的质量时:M=m(分子)×N 。
A
教材习题01 解题思路
下列说法错误的是( ) 【解析】物质的量是含有一定数目粒子的集合体的
A.物质的量是表示含有一定数目粒子的集合体的 物理量,其单位是摩尔,使用摩尔所指的对象是微
粒,而微粒种类繁多,需要指明其名称;构成物质的
物理量
B.使用摩尔作单位时必须指明微粒的名称
粒子除原子外,还有分子、离子等。选项C正确。
C.1 mol 任何物质都含有阿伏加德罗常数个原子
D.物质的量适用于计量分子、原子、离子等粒子
【答案】C
教材习题02 解题思路
下列有关摩尔质量的描述或应用正确的是( ) 【解析】质量的单位为“g”,A错误;摩尔质量的
A.1 mol OH-的质量为17 g·mol-1 单位应为“g·mol-1”,B错误;摩尔质量等于它的以
B.二氧化碳的摩尔质量为44 g “g·
C.铁原子的摩尔质量等于它的相对原子质量 mol-1”为单位相对原子质量,二者在数值上相等,C
D.一个钠原子的质量等于 g 错误。选项D正确。
学科网(北京)股份有限公司【答案】D
核心考点一:物质的量及单位
【例1】下列叙述正确的是( )
A.1 mol任何物质都含有6.02×1023个分子
B.摩尔只能用来计量纯净物中微观粒子数目
C.摩尔是物质的量的单位,简称摩,符号mol
D.我们把含有6.02×1023个粒子的任何粒子的集合体计量为1摩尔
【答案】C
【解析】物质不一定都是由分子组成的,可能是由原子或离子组成的,摩尔是物质的量的单位,1 mol任
何粒子的粒子数约为6.02×1023,A错误;摩尔既能用来计量纯净物中微观粒子数目,也能用来计量混合物
中微观粒子数目,B错误;含有6.02×1023个粒子的集合体计量不一定为1 mol,如含有6.02×1023个O的O
2
的物质的量为0.5 mol,D错误。
核心考点二:摩尔质量
【例2】下列关于摩尔质量的说法正确的是( )
A.摩尔质量表示单位物质的量的物质所具有的质量
B.1 mol H SO 的质量与HSO 的摩尔质量相同
2 4 2 4
C.摩尔质量与该物质的相对分子质量或相对原子质量相等
D.某物质的物质的量越多,对应的摩尔质量越大
【答案】A
【解析】B项,二者的数值相同,但单位分别为 g和g·mol-1,错误;C项,以g·mol-1为单位时,摩尔质
量的数值与该物质的相对分子质量或相对原子质量相等,错误;D项,摩尔质量不随物质的量发生变化,
错误。
核心考点三:与=n=有关的综合计算
【例3】已知1.505×1023个X气体分子的质量为8 g,则X气体的摩尔质量是( )
A.16 g B.32 g
C.64 g·mol-1 D.32 g·mol-1
【答案】D
【解析】气体的物质的量n==0.25 mol,气体的摩尔质量M===32 g·mol-1。
核心考点四:阿伏加德罗常数
【例4】设N 代表阿伏加德罗常数的值,下列说法正确的是( )
A
A.2.4 g金属镁变成镁离子时失去的电子数目为0.1N
A
学科网(北京)股份有限公司B.在1 mol Na SO 溶液中Na+的数目约为6.02×1023
2 4
C.1 mol氮气所含的电子数目为N
A
D.17 g氨气所含电子数目为10N
A
【答案】D
【解析】2.4 g Mg的物质的量是=0.1 mol,变成镁离子时失去的电子数目为0.2N ,A错误;在1 mol
A
NaSO 溶液中Na+的数目约为1.204×1024,B错误;1个N 分子中含有14个电子,故1 mol N 含有14N 个
2 4 2 2 A
电子,C错误;17 g氨气的物质的量为=1 mol,1个NH 分子中含有10个电子,故1 mol NH 所含电子数目
3 3
为10N ,D正确。
A
核心考点五 综合考查
【例5】科学家发现了某种元素的一个原子,其质量是a g,一个12C 原子的质量是b g,N 是阿伏加德罗
A
常数的值。下列说法正确的是( )
A.该原子的摩尔质量是aN
A
B.W g该原子的物质的量是 mol
C.W g该原子中含有N 个该原子
A
D.由已知信息可得N =
A
【答案】B
【解析】摩尔质量是单位物质的量的物质所具有的质量,单位是 g·mol-1,一个原子的质量是a g,则1
mol即N 个原子的质量为aN g,所以该原子的摩尔质量应为aN g·mol-1,A错误;W g该原子的物质的
A A A
量为= mol,B正确;由题意可知,W g该原子的数目为=,C错误;12C原子的摩尔质量为12 g·mol-1,
一个12C原子的质量为b g,故N b=12,所以N =,D错误。
A A
【基础练】
1.下列单位中哪一个是物质的量n的单位是
A.mol B.L C.mol/L D.mL
【答案】A
【解析】物质的量的单位是摩尔,为mol,故选A。
2.下列各物质中所含氢原子最多的是
A.0.1molNH Cl B.0.1molNH HCO
4 4 3
C.0.2molH D.0.2molHPO
2 3 4
【答案】D
【解析】A.0.1 mol NH Cl中含有0.4 mol氢原子;
4
B.0.1 mol NH HCO 含0.5 mol氢原子;
4 3
C.0.2 mol H 中含有0.4mol氢原子;
2
D.0.2 mol HPO 含0.6 mol氢原子;
3 4
则所含氢原子最多的是0.2molHPO ,故选D。
3 4
学科网(北京)股份有限公司3.下列关于物质的量及其单位摩尔使用正确的是
A.1mol钠原子 B.1mol香蕉 C.1mol铅笔 D.1mol大米
【答案】A
【解析】物质的量是描述微观粒子的数目多少的物理量;香蕉、铅笔、大米均为宏观物质,不能使用物质
的量描述;1mol钠原子化学用语使用正确;故选A。
4.水是生命之源。18g水中含有
A.1molH B.1mol氧 C.1molH D.1molO
2
【答案】D
【解析】18g水的物质的量为1mol,含有1molH O,2molH,1molO,故选D。
2
5.下列叙述正确的是
A.摩尔是基本物理量之一 B.1 mol CO 的质量为44g/mol
2
C.HSO 的摩尔质量为98g/mol D.2 mol Al的摩尔质量为54 g
2 4
【答案】C
【解析】A.物质的量是基本物理量之一,摩尔是物质的量的单位,故A错误;
B.1 mol二氧化碳的质量为1 mol×44g/mol=44g,故B错误;
C.硫酸的相对分子质量为98,数值上与摩尔质量相等,则硫酸的摩尔质量为98g/mol,故C正确;
D.铝的摩尔质量为27g/mol,2mol铝的质量为2mol×27g/mol=54g,故D错误;
故选C。
6.下列关于物质的量的说法错误的是
A.单位是摩尔 B.研究对象是微观粒子
C.就是物质的质量 D.符号n
【答案】C
【解析】A.物质的量的单位是摩尔,故A正确;
B.物质的量是描述微观粒子集合体的一个基本物理量,其单位为摩尔,故B正确;
C.物质的量和物质的质量是两个不同的基本物理量,故C错误;
D.物质的量的单位为摩尔,符号为n,故D正确;
故选C。
7.下列关于阿伏加德罗常数的叙述不正确的是
A.阿伏加德罗常数是指1mol物质中所含有的原子数
B.0.5molHO中含有的原子数目为1.5N
2 A
C.国际上规定0.012kg12C中所含碳原子数为阿伏加德罗常数
D.1molO 中的分子数为N ,而原子数为2N
2 A A
【答案】A
【解析】A.阿伏加德罗常数是指1 mol物质中含有的粒子数,A错误;
B.1个HO中含有3个原子,所以0.5 mol HO中含有1.5 mol原子,含有的原子个数为1.5N ,B正确;
2 2 A
C.国际上规定0.012 kg 12C中所含碳原子数为阿伏加德罗常数,C正确;
学科网(北京)股份有限公司D.每个O 分子由2个氧原子构成,1 mol O 中含2 mol氧原子,D正确;
2 2
故选A。
8.下列对于“摩尔”的理解正确的是
A.摩尔是国际单位制的七个物理量之一
B.摩尔是表示物质质量的单位
C.国际上规定含有阿伏加德罗常数个粒子的任何粒子集体为1 mol
D.1 mol氧约含6.02×1022个O
【答案】C
【解析】A.物质的量是国际单位制的七个物理量之一,摩尔是物质的量的单位,A错误;
B.摩尔是表示物质的量的单位,B错误;
C.国际上规定0.012 kg12C所含有的C原子数是阿伏加德罗常数,任何物质所含有基本微粒数若与0.012
kg12C所含有的C原子数相同,我们就说其含有的粒子集体的物质的量为1 mol,C正确;
D.未指明是氧元素的哪种微粒,因此不能确定其含有的微粒就是O原子,D错误;
故选C。
9.下列说法中,不正确的是
A.“物质的量”表示含有一定数目粒子的集体,是七个基本物理量之一
B.“摩尔”是物质的量的单位
C.1 mol任何物质都约含6.02×1023个原子
D.一个水分子的质量约为 g
【答案】C
【解析】A.在国际单位制中规定了七个基本物理量的单位,“物质的量”是七个基本物理量之一,它表
示的意义是含有一定数目粒子的集体,A正确;
B.“物质的量”是一个基本物理量,“摩尔”是物质的量的单位,B正确;
C.物质构成的基本微粒有原子、分子、离子,物质的基本构成微粒若是原子,则1 mol任何物质都约含
6.02×1023个原子,若原子不是构成物质的基本微粒,则1 mol该物质中含有的原子数目就不可能约是含
6.02×1023个原子,C错误;
D.1 mol H O中含有约6.02×1023个HO分子,1 mol H O的质量是18 g,则一个水分子的质量约为
2 2 2
g,D正确;
故选C。
10.下列叙述错误的是
①摩尔是国际单位制中七个基本物理量之一
② 任何粒子含有的粒子数都约为 个
③ 就是阿伏加德罗常数
④氢原子的摩尔质量是1g
学科网(北京)股份有限公司⑤物质的量浓度的单位都是
⑥硫酸的摩尔质量就是硫酸的相对分子质量
A.②⑤ B.①②③⑥ C.①③④⑥ D.①③④⑤⑥
【答案】D
【解析】①摩尔是国际单位制中七个基本物理量之一的单位,错误;
② 任何粒子含有的粒子数都为阿伏加德罗常数个,约为 ,正确;
③阿伏加德罗常数约为 ,错误;
④氢原子的摩尔质量是1g/mol,错误;
⑤物质的量浓度的单位是 、 、 等,错误;
⑥硫酸的摩尔质量和硫酸的相对分子质量数值相等,错误;
综上所诉,错误的为①③④⑤⑥;
故选D;
【提升练】
11.2018年11月13日至16日,第26届国际计量大会在巴黎召开,会上,对物质的量的单位——摩尔的
定义进行了修改。摩尔来源于拉丁文moles,原意为大量、堆积,是在1971年10月,有41个国家参加的
第14届国际计量大会决定增加的国际单位制(SI)的第七个基本单位。下列对于“摩尔”的理解正确的是
A.1mol任何物质所含有的原子数都相同
B.摩尔是物质的量的单位,简称摩,符号为mol
C.摩尔可以把物质的宏观数量与微观粒子的数量联系起来
D.国际上规定,0.012kg12C中所含有的碳原子数目为1摩
【答案】B
【解析】A.因不同物质分子中所含有的原子个数不尽相同,A错误;
B.摩尔是物质的量的单位,简称摩,符号为mol,B正确;
C.物质的量是一个物理量,摩尔是物质的量的单位,不是物理量,物质的量把宏观物质与微观粒子联系
起来,C错误;
D.0.012kg12C中所含有的碳原子数目是阿伏加德罗常数,D错误;
故选B。
12.青蒿素的分子式为 ,相对分子质量是282。下面关于青蒿素的说法正确的是
A. 的摩尔质量为
B. 分子中氢原子与氧原子质量比为
C.1个 分子的质量约为
D.含有 个碳原子的 的物质的量为
【答案】C
学科网(北京)股份有限公司【解析】A. 的摩尔质量为 ,故A错误;
B. 分子中氢原子与氧原子质量比为 ,故B错误;
C.1mol 的质量为282g,1mol 中含有 个分子,所以1个 分子的质量约
为 ,故C正确;
D.含有 个碳原子的 的物质的量为 ,故D错误;
选C。
13.下列与“物质的量”相关的计算正确的是
A.a g Cl 中有b个氯原子,则阿伏加德罗常数N 的数值可表示为
2 A
B.28 g CO和22.4 L CO 中含有的碳原子数相等
2
C.标准状况下,11.2 L X气体分子的质量为16 g,则X气体的摩尔质量是32
D.10 g HO含有的中子数为10 mol
2
【答案】A
【解析】A.agCl 中有b个氯原子,则阿伏加德罗常数N 的数值可表示为
2 A
,A正确;
B.28gCO中含有的碳原子数为1mol,但CO 气体所处状态未知,无法计算22.4LCO 中含有的碳原子数,
2 2
B错误;
C.标准状况下,11.2LX气体分子的质量为16g,则X气体的摩尔质量是
,摩尔质量有单位,C错误;
D.10gHO含有的中子数为 ,不是10mol,D错误;
2
故选A。
14.下列叙述正确的是
A.Fe的摩尔质量是56g
B.常温常压下,14g 含有的分子数约为
C.2mol 的质量为88g
D.64g 含有的氧原子数约为
【答案】C
学科网(北京)股份有限公司【解析】A.铁的摩尔质量为56g/mol,故A错误;
B.常温常压下,14g氮气含有的分子数约为 ×6.02×1023mol—1=3.01×1023,故B错误;
C.2mol二氧化碳的质量为2mol×44 g/mol =88g,故C正确;
D.64g二氧化硫含有的氧原子数约为 ×2×6.02×1023mol—1=1.204×1024,故D错误;
故选C。
15.下列有关摩尔质量的描述或应用中,正确的是
A.1molNH 的质量为17
3
B.二氧化碳的摩尔质量为44g
C.铁原子的摩尔质量等于它的相对原子质量
D.一个钠原子的质量等于 g
【答案】D
【解析】A.1 mol NH 的质量是17g,A错误;
3
B.二氧化碳的摩尔质量为44g/mol,B错误;
C.铁原子的摩尔质量如果用g/mol作单位,在数值上等于它的相对原子质量,C错误;
D.1mol钠的质量是23,因此一个钠原子的质量约等于 ,D正确;
故选D。
16.填空。
(1)3.01×1023个SO 分子中含有氧原子的个数为 ;SO 气体的质量为 。
2 2
(2)常温常压下,160g的SO 气体含有的原子数为 (用N 表示阿伏加德罗常数的值)。
3 A
(3)NO和O 可发生反应:2NO+O=2NO,现有amolNO和bmolO 充分反应后,氮原子与氧原子的个数比
2 2 2 2
为 。
(4)1molOH-中含有 mol质子, mol电子。
(5)1.5molNa SO ·10H O中所含的Na+的物质的量是 ,所含的SO 的物质的量是
2 4 2
,所含HO的数目是 。
2
【答案】(1) 6.02×1023 32g
(2)8N
A
(3)a∶(a+2b)
(4) 9 10
(5) 3 mol 1.5 mol 9.03×1024或15N
A
【解析】(1)1个SO 分子含有2个氧原子,则3.01×1023个SO 分子含有氧原子个数为3.01×1023×2=
2 2
6.02×1023;该SO 气体的物质的量 ,其质量 ;
2
学科网(北京)股份有限公司(2)160 g的SO 气体的物质的量为2 mol,故所含原子个数为8N ;
3 A
(3)化学反应中原子进行了重新组合,但是原子的个数和种类没有改变。反应后氮原子与氧原子的个数
比等于反应前氮原子与氧原子的个数比,即a∶(a+2b);
(4)1 mol OH-中含有9 mol质子,10 mol电子;
(5)每个NaSO ·10H O中含有Na+、硫酸根离子、HO数目分别为:2、1、10,故1.5 mol Na SO ·10H O
2 4 2 2 2 4 2
中所含Na+、硫酸根离子物质的量分别是:1.5 mol×2=3 mol、1.5 mol,含HO的数目为:1.5
2
mol×10×6.02×1023 mol-1=9.03×1024。
学科网(北京)股份有限公司