文档内容
化学(三) 参考答案
1~5 ADACD 6~10BDDBB 11~14 ACDC
1. A【解析】略。
2. D
【解析】
A. Al³+与 S²⁻发生双水解反应;
B. 酸性溶液中 SiO2-3-与H⁺反应生成 H₂SiO₃沉淀;
的溶液可能是碱性溶液,Mg²⁺会与OH⁻反应生成Mg(OH)₂沉淀;
D. 常温饱和 NaHCO₃的 pH大于8, 故在pH=8的溶液中, Na⁺、K⁺、Cl⁻、HCO-3一定能大量共存。
3. A
【解析】
A. 盐酸与 Cu(OH)₂发生酸碱中和反应, 氨水与Cu(OH)₂发生络合反应;
B. Fe 与水蒸气反应生成 Fe₃O₄, 不是碱;
C. SO₂能使紫色石蕊试纸变红,不能使红色石蕊试纸变色;
D. SiO₂在高温下与C反应生成CO。
4. C
【解析】
A. 铜元素位于周期表的 ds区;
B. 该催化剂中铜的配位数为4;
C. 结构中 C、N原子的杂化类型都是 sp²;
D. 基态 N 原子核外有5 种不同空间运动状态的电子。
5. D
【解析】用图④装置蒸干 FeCl₃溶液制得的是 Fe₂O₃固体。
6. B
【解析】
A. 未说明状态,无法计算;
B. 58.5gNaCl的物质的量为1mol, 反应生成 1mol NaClO, ClO⁻数目为 NA;
C. 转移的电子数目为 2NA;
D. 1个 CO₂分子中有2个π键, 该反应消耗的 CO₂为1mol, 含有π键数目为2NA。
7. D
【解析】
A. X分子中最多应有11个原子共平面。
B. 甲苯和Y 都能使酸性高锰酸钾溶液褪色,无法检验。
学科网(北京)股份有限公司C. Z 熔沸点较高,难溶于水。
D. X有3种官能团,分别是碳氟键、碳碳双键、酯基,碳碳双键能与溴水反应、酯基能与NaOH溶液反应。
8. D
【解析】
A. 该方程式电荷不守恒;
B. b过程反应为 消耗 1molNO, 转移3mole⁻,
C. 高温下酶会失去活性,不利于H⁺和e⁻的转移;
D. 总反应式为:
9. B
【解析】 a、 b、 c、 d分别是H、 B、 N、 Na。
A. NaH是离子化合物,熔点较高;
B. N的氧化物中NO 不溶于水;
C. [BH₄]⁻中的H元素为-1价, 有较强的还原性;
D. b的最高价氧化物对应的水化物是 H₃BO₃, H₃BO₃是弱酸。
10. B
【解析】
A. 相同浓度的 Na₂CO₃和 NaHCO₃, Na₂CO₃溶液碱性强, 曲线①表示盐酸滴入 Na₂CO₃溶液的过程;
B. e点的pH 小,酸性强,对水的抑制强,水的电离程度小;
C. 温度相同, Kw相同;
D. 电荷不守恒,阴离子中还有 Cl-未写进去。
11. A
【解析】A. 该晶胞中 Mg有8个,Si 有4个,该晶胞所表示的物质的化学式为Mg₂Si。
12. C
【解析】
A. 加入淀粉 KI 溶液变蓝, 不能说明有 Cl₂, 因为HClO也会把I⁻氧化成I₂;
B. 加入KNO₃后, H⁺和NO-3 将Cu氧化, KNO₃没有起催化作用;
D. NaCl中的Cl⁻不是氯元素对应的最高价含氧酸根离子,无法比较。
13. D
【解析】公众号:高中试卷君
A. 由装置中稀 NaCl溶液变成了浓的 NaCl溶液,说明最右侧的 Na⁺往左边移动了,故b为阳极;
B. c为阳离子交换膜,d 为阴离子交换膜;
学科网(北京)股份有限公司C. a为阴极,电极上发生的反应为:
D. b电极产生3.36L(标况)O₂, 即0.15mol, 转移的电子为 0.15mol×4=0.6mol, 理论上有 透过e
膜。
14. C
【解析】由横坐标, V₁至V₄逐渐增大, V₄与V₂转化率相同, 而 V₄大于 V₂, V₄的浓度更小速率更小, 说
明 V₂速率更快已经达到平衡,V₁体积最小应该速率更快,也已达到平衡,V₃转化率虽然在四组中最大,
但不确定为最大转化率,因此无法判断是否平衡。
A. V₃转化率虽然在四组中最大, 但不确定为最大转化率,因此无法判断是否平衡,a、b已达平衡;
B. b、 d两点NOCl的转化率相等,则 t min时气体总物质的量相等,由于 则b点的压强大于d
点;
C. a点已达到平衡,且体积更小压强更大,速率更大,所以a点 v逆大于 c 点 v正;
D. 相同温度下平衡常数相同。
15. (14分)
(1) +3 (1分) 3d¹⁰4s² (1分)
(2)铜失去 1 个电子后的价电子排布式为 3d¹⁰,3d轨道处于全满状态,再失去1个电子需要的能量较高;
锌失去1个电子后的价电子排布式为3d¹⁰4s¹,再失去1个电子需要能量比铜失去第2个电子需要能量
低。 (2分)
(3) 延长酸浸时间、酸浸过程中不断搅拌等(2分)
(2分)
(5) 根据反应 pH过低, 平衡逆向移动; pH 过高,12Ge⁴+;水解程度增大,均
不利于 GeR₂生成 (2分)
(6) 蒸发浓缩(1分) 冷却结晶(1分)
(7) ZnSO₄(2分)
【解析】(7) 设 为100g, 其中 结合图形可知,688℃时
所得固体的化学式为 ZnSO₄。
16. (15分)
(1) 三颈烧瓶 (1分)
(2) 除去 HNO₃和水蒸气(2分); 防止水蒸气进入C装置(2分)。
学科网(北京)股份有限公司(3)用止水夹夹住 A、 B间的橡皮管,往分液漏斗中加入足量水,再打开分液漏斗的活塞,过一会分液漏
斗中的水不再流下,则气密性良好(2分)。
(2分)
(5) 停止加热,需继续通入N₂O 至三颈瓶冷却后,再关闭分液漏斗活塞,以免引起倒吸(2分)
(2分)
② (2分)
【 解 析 】 (6) 反 应
产 品 中 的 质 量 分 数
17. (14分)
(1) ①-41 (2分) ②C(1分)
(2) HD(2分)
(3)30(2分)
(4) 1:3 (1分) 0.01 (2分)
(2分) 67.2 (2分)
【解析】
(1) △H₂=1075+2×463-2×803-436=-41kJ·mol-1。
(3) 由 经 验 公 式 读 图 有 和 解 得
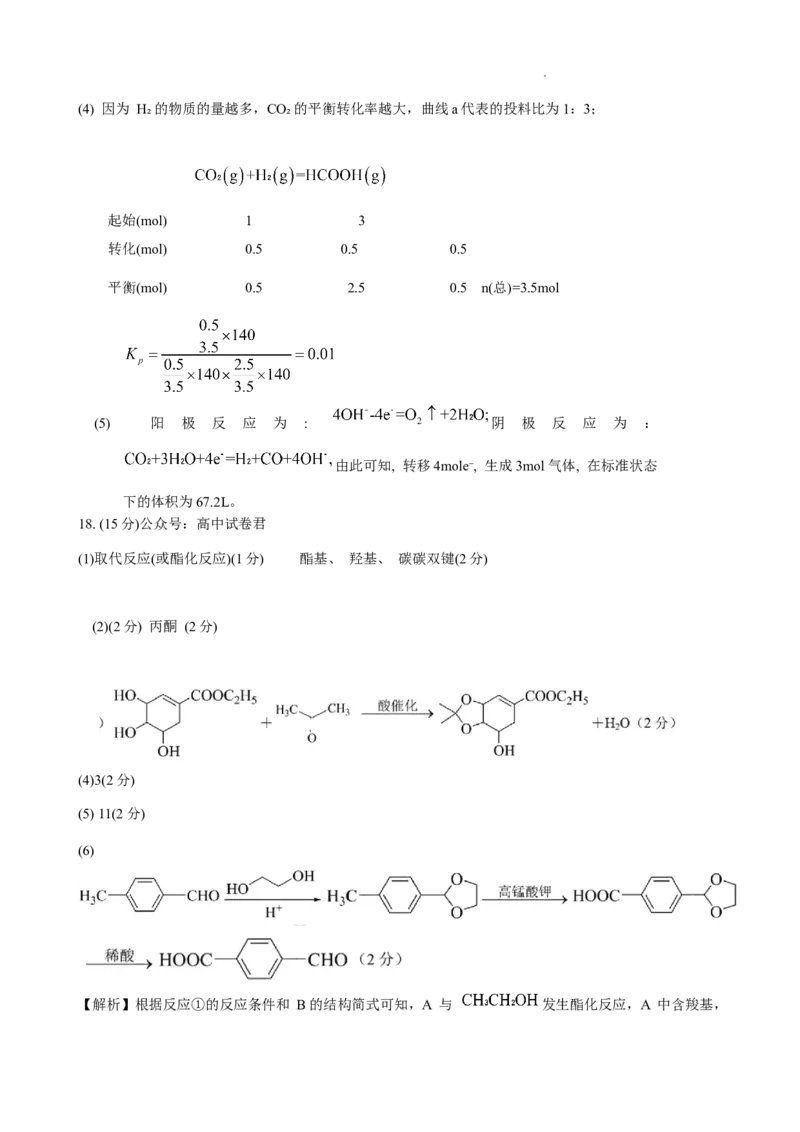
学科网(北京)股份有限公司(4) 因为 H₂的物质的量越多,CO₂的平衡转化率越大,曲线a代表的投料比为1:3;
起始(mol) 1 3
转化(mol) 0.5 0.5 0.5
平衡(mol) 0.5 2.5 0.5 n(总)=3.5mol
(5) 阳 极 反 应 为 : 阴 极 反 应 为 :
由此可知, 转移4mole⁻, 生成3mol气体, 在标准状态
下的体积为67.2L。
18. (15分)公众号:高中试卷君
(1)取代反应(或酯化反应)(1分) 酯基、 羟基、 碳碳双键(2分)
(2)(2分) 丙酮 (2分)
(4)3(2分)
(5) 11(2分)
(6)
【解析】根据反应①的反应条件和 B的结构简式可知,A 与 发生酯化反应,A 中含羧基,
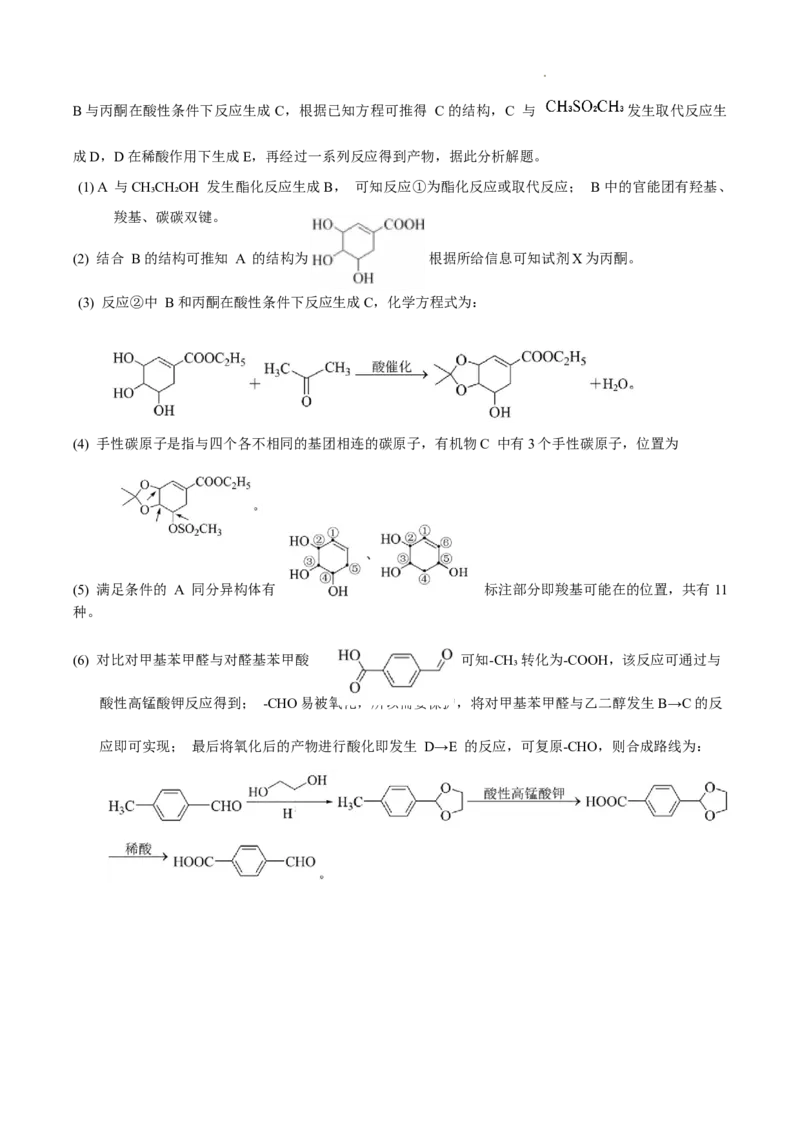
学科网(北京)股份有限公司B与丙酮在酸性条件下反应生成C,根据已知方程可推得 C的结构,C 与 发生取代反应生
成D,D在稀酸作用下生成E,再经过一系列反应得到产物,据此分析解题。
(1) A 与CH₃CH₂OH 发生酯化反应生成B, 可知反应①为酯化反应或取代反应; B中的官能团有羟基、
羧基、碳碳双键。
(2) 结合 B的结构可推知 A 的结构为 根据所给信息可知试剂X为丙酮。
(3) 反应②中 B和丙酮在酸性条件下反应生成C,化学方程式为:
(4) 手性碳原子是指与四个各不相同的基团相连的碳原子,有机物C 中有3个手性碳原子,位置为
(5) 满足条件的 A 同分异构体有 标注部分即羧基可能在的位置,共有11
种。
(6) 对比对甲基苯甲醛与对醛基苯甲酸 可知-CH₃转化为-COOH,该反应可通过与
酸性高锰酸钾反应得到; -CHO易被氧化,所以需要保护,将对甲基苯甲醛与乙二醇发生B→C的反
应即可实现; 最后将氧化后的产物进行酸化即发生 D→E 的反应,可复原-CHO,则合成路线为:
学科网(北京)股份有限公司