文档内容
杭州学军中学第一学期期中考试
高一化学试卷
相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 S-32 Cl-35.5 Fe-56 Cu-64
Ba-137
一、选择题
1. NaCO 俗名纯碱,下面是对纯碱采用不同分类法的分类,不正确的是
2 3
A. NaCO 是碱 B. NaCO 是盐 C. NaCO 是钠盐 D. NaCO 是碳酸盐
2 3 2 3 2 3 2 3
【答案】A
【解析】
【详解】A.NaCO 电离产生的阴离子是 ,并不是OH-,因此不属于碱,A错误;
2 3
B.NaCO 是由金属阳离子和酸根离子组成的化合物,因此属于盐,B正确;
2 3
C.NaCO 属于盐,由于其电离产生的阳离子的Na+,所以根据阳离子进行分类,NaCO 是钠盐,C正确;
2 3 2 3
D.NaCO 是由金属阳离子和酸根离子组成的化合物,因此属于盐;由于电离产生的阴离子是 ,因
2 3
此碳酸钠属于碳酸盐,D正确;
故合理选项是A。
2. 仪器名称为“容量瓶”的是( )
A. B. C. D.
【答案】C
【解析】
【详解】A.此仪器为圆底烧瓶,A与题意不符;
B.此仪器为分液漏斗,B与题意不符;
C.此仪器为容量瓶,C符合题意;
D.此仪器为锥形瓶,D与题意不符;
答案为C。
3. 下列分散系能产生“丁达尔效应”的是( )
A. 葡萄糖溶液 B. 氢氧化铁胶体 C. 盐酸 D. 油水【答案】B
【解析】
【详解】胶体分散系能产生“丁达尔效应”,不属于胶体的分散系不能产生“丁达尔效应”, 葡萄糖溶液、盐
酸、油水均不属于胶体分散系,氢氧化铁胶体属于胶体分散系,故答案为:B。
4. 下列说法中错误的是( )
A. 0.3 mol HSO B. 1 mol H O C. 0.5 mol氧 D. 3 mol氢原子
2 4 2
【答案】C
【解析】
【详解】A.HSO 可表示微观粒子,可用物质的量描述,0.3 mol H SO 描述正确,A说法正确;
2 4 2 4
B.HO可表示微观粒子,可用物质的量描述,1 mol H O描述正确,B说法正确;
2 2
C.物质的量用来描述微观粒子,如分子、原子、离子等等;0.5mol氧,没有指明具体的微观粒子的种类,
描述错误,C说法错误;
D.氢原子为微观粒子,可用物质的量描述,3 mol氢原子描述正确,D说法正确;
答案为C。
【点睛】物质的量是一个物理量,它表示含有一定数目粒子的集合体,符号为n,物质的量的单位为摩尔
(mol),它可以计量所有微观粒子(包括原子、分子、离子、原子团、电子、质子、中子等)。
5. 0.5L 1mol/L FeCl 溶液与0.2L 1mol/L KCl溶液中的c(Cl- )之比是( )
3
A. 5:2 B. 15:2 C. 3:1 D. 1:3
【答案】C
【解析】
【详解】给定浓度的溶液中氯离子的浓度与溶液的体积无关,则 1mol/L FeCl 溶液中c(Cl- )=3mol/L,
3
1mol/L KCl溶液中的c(Cl- )=1mol/L,则c(Cl- )之比为3:1,答案为C。
6. 下列反应不属于四种基本反应类型,但属于氧化还原反应的是( )
A. Fe+CuSO=FeSO+Cu
4 4
B. AgNO+NaCl=AgCl↓+NaNO
3 3
C. Fe O+3CO=2Fe+3CO
2 3 2
D. 2KMnO KMnO +МnO+O ↑
4 2 4 2 2
【答案】C
【解析】
【详解】A.该反应为置换反应,属于四种基本反应类型,同时 Fe和Cu元素的化合价发生了变化,属于
氧化还原反应,A不符合题意;B.该反应为复分解反应,属于四种基本反应类型,但没有元素的化合价发生变化,不属于氧化还原反应,
B不符合题意;
C.该反应不属于四种基本反应类型,同时Fe和C元素的化合价发生了变化,属于氧化还原反应,C符合
题意;
D.该反应为分解反应,属于四种基本反应类型,同时Mn和O元素的化合价发生了变化,属于氧化还原
反应,D不符合题意;
故选C。
7. 食盐中的碘以碘酸钾(KIO )形式存在,可根据反应: +5I-+6H+=3I +3H O 验证食盐中存在 ,
3 2 2
根据上述反应,下列说法错误的是( )
A. 作氧化剂,发生还原反应
B. I 既是氧化产物又是还原产物
2
C. 该反应下氧化性: > I
2
D. 每生成 3 个 I 转移 6 个电子
2
【答案】D
【解析】
【详解】A.由 +5I-+6H+═3I +3H O可知, 中碘元素化合价由+5价得电子变为0价,被还原,作氧
2 2
化剂,发生还原反应,故A正确;
B.由 +5I-+6H+═3I +3H O可知, 中碘元素化合价由+5价得电子变为0价,I-化合价由-1价失电子
2 2
变化为0价,I 既是氧化产物又是还原产物,故B正确;
2
C.氧化还原反应中氧化剂的氧化性强于氧化产物的氧化性,所以该条件下 是氧化剂,I 是氧化产物,
2
氧化性 >I,故C正确;
2
D.由 +5I-+6H+═3I +3H O可知,每生成3mol I ,转移电子的物质的量为5mol,即每生成 3个I 转移5
2 2 2 2
个电子,故D错误;
答案为D。
8. 下列各组离子在溶液中能大量共存的是( )A. NH 、K+、H+、Ba2+、Cl-、NO B. Mg2+、Na+、OH-、K+、CO
C. Ag+、Fe3+、Cl-、H+、Ca2+ D. K+、CO 、H+、Na+、NH
【答案】A
【解析】
【详解】A. NH 、K+、H+、Ba2+、Cl-、NO 在溶液中不反应,可以大量共存,A选;
B. 镁离子与氢氧根离子、碳酸根离子分别生成氢氧化镁沉淀和碳酸镁沉淀,均不能大量共存,B不选;
C. 银离子和氯离子反应生成氯化银沉淀,不能大量共存,C不选;
D. 氢离子与碳酸根离子反应生成水和二氧化碳,不能大量共存,D不选;
答案选A。
9. 下列反应的离子方程式书写正确的是( )
A. 碳酸镁和盐酸反应的离子方程式:CO +2H+=CO↑+HO
2 2
B. 制备氢氧化铁胶体的离子方程式:Fe3++3HO=Fe(OH)(胶体)+3H+
2 3
C. 氢氧化钡溶液与稀硫酸反应:Ba2++SO +H++OH-=BaSO↓+HO
4 2
D. 铁粉与稀硫酸反应:2Fe+6H+=2Fe3++3H↑
2
【答案】B
【解析】
【详解】A. 碳酸镁难溶,碳酸镁不能拆,正确应为MgCO +2H+=CO↑+HO+Mg2+,A错误;
3 2 2
B. 制备氢氧化铁胶体的离子方程式:Fe3++3HO=Fe(OH)(胶体)+3H+,B正确;
2 3
C. 氢氧化钡溶液与稀硫酸反应阴阳离子个数比不对,正确应为:Ba2++SO +2H++2OH-=BaSO↓+2HO,C
4 2
错误;
D. 铁粉与稀硫酸反应不能生成铁离子而应为亚铁离子:Fe+2H+=Fe2++H↑,D错误;答案选B。
2
10. 下列关于化学发展几个重要的里程碑说法不正确的是( )
A. 英国化学家波义尔提出元素的概念,标志着近代化学的诞生
B. 法国化学家拉瓦锡建立燃烧现象的氧化学说,使近代化学取得了革命性进展
C. 英国科学家道尔顿提出分子学说,为近代化学的发展奠定了坚实的基础
D. 俄国化学家门捷列夫发现了元素周期律,使化学的研究变得有规律可循
【答案】C
【解析】【详解】A.1661年,英国化学家波义尔提出元素的概念,认为元素是用一般化学方法不能再分解为更简
单的某些实物,标志着近代化学的诞生,A正确;
B.1774年,法国化学家拉瓦锡正式提出了氧化学说,认为燃烧的本质是物体与氧的化合,使近代化学取
得了革命性进展,B正确;
C.1803年,英国科学家道尔顿提出原子论,为近代化学的发展奠定了坚实的基础,C错误;
D.1869年,俄国化学家门捷列夫发现了元素周期律,并预言了未知元素的性质,使化学的研究变得有规
律可循,D正确;
故选C。
11. 下列关于决定物质体积的因素的说法不正确的是( )
A. 物质的体积取决于粒子数目、粒子大小和粒子间距
B. 相同条件下,分子数相同的任何气体的体积基本相同
C. 同温同压下,1mol任何物质所占有的体积均相同
D. 等质量的 ,压强越小、温度越高,气体所占体积越大
【答案】C
【解析】
【详解】A.从微观角度来说,物质的体积由粒子数目、粒子大小和粒子间距决定,故A正确;
B.分子数相同的气体的物质的量相同,则相同条件下体积基本相同,故B正确;
C.该结论只适用于气态物质,故C错误;
D.压强和气体体积成反比,温度和气体体积成正比,等质量的 ,压强越小,温度越高,气体体积越大,
故D正确;
故选C。
12. 中国药学家屠呦呦因发现青蒿素开创了治疗疟疾的新方法,荣获了诺贝尔奖。第十三届全国人民代表
大会常务委员会第十三次会议决定授予屠呦呦“共和国勋章”,表彰他及其团队为新中国建设和发展作出
的杰出贡献。已知青蒿素的分子式为C H O,下列有关说法正确的是( )
15 22 5
A. 青蒿素的摩尔质量为282g/mol
B. 青蒿素中C、H、O的质量之比为15:22:5
C. 标准状况下,1mol青蒿素的体积约为22.4L
D. 1mol青蒿素中含11molH
2
【答案】A
【解析】
【详解】A、青蒿素的分子式为C H O,摩尔质量为282g/mol,选项A正确;
15 22 5B、青蒿素中C、H、O三种元素的质量比为(12×15):(1×22):(16×5)=90:11:40≠15:22:
5,选项B错误;
C、标准状况下,青蒿素不是气体,1mol青蒿素的体积不是22.4L,选项C错误;
D、青蒿素中不含H,选项D错误。
2
答案选A。
【点睛】本题主要考查化学式的意义、有机物、气体摩尔体积及相对分子质量计算方法的掌握,学习中注
意相关基础知识的积累,易错点为选项C:标准状况下,青蒿素不是气体,1mol青蒿素的体积不是
22.4L。
13. 相等物质的量的CO和CO 相比较,下列有关叙述中正确的是( )。
2
①它们所含的分子数目之比为1∶1; ②它们所含的O原子数目之比为1∶2; ③它们所含的原子总数
目之比为2∶3; ④它们所含的C原子数目之比为1∶1;⑤它们所含的电子数目之比为7∶11
A. ①②③④ B. ②和③ C. ④和⑤ D. ①②③④⑤
【答案】D
【解析】
【详解】根据化学式可知,如果CO和CO 的物质的量相等,则二者的分子数相等,所含的氧原子数是 1
2
︰2的。而原子总数是2︰3的,碳原子数是1︰1的,含有的电子数是14︰22,所以正确的答案选D。
14. 下列关于钠的反应现象的叙述中,不正确的是( )
选项 反应内容 反应现象
A 切开钠,其颜色的变化 钠切面颜色变暗,最后呈淡黄色
B 把小块钠投入硫酸铜溶液中 钠浮在水面上、四处游动、产生蓝色沉淀
钠熔化成闪亮的小球,在水面上四处游
把小块钠投入到滴有紫色石蕊试液的
C 动,有“嘶嘶”的响声发出,反应后溶液变
盛冷水中
蓝
把一小块钠迅速投入到热坩埚中,继 钠受热后先融化,然后与氧气剧烈反应,
D
续加热坩埚片刻 发出黄色火焰
A. A B. B C. C D. D
【答案】A
【解析】
【详解】A.切开钠,钠与空气中 的氧气接触,反应生成氧化钠,切面颜色变暗,但最后不会呈淡黄色,故
A错误;
B.把小块钠投入硫酸铜溶液中,钠与水反应生成氢氧化钠与氢气,氢氧化钠与硫酸铜反应生成蓝色沉淀,
故B正确;C.钠投入到紫色石蕊试液的冷水中,钠与水反应生成氢氧化钠与氢气,钠熔化成闪亮的小球,在水面上四
处游动,有“嘶嘶”的响声发出,反应后溶液变蓝,故C正确;
D.钠的熔点低,加热熔化后燃烧,发出黄色火焰,故D正确。
故答案选:A。
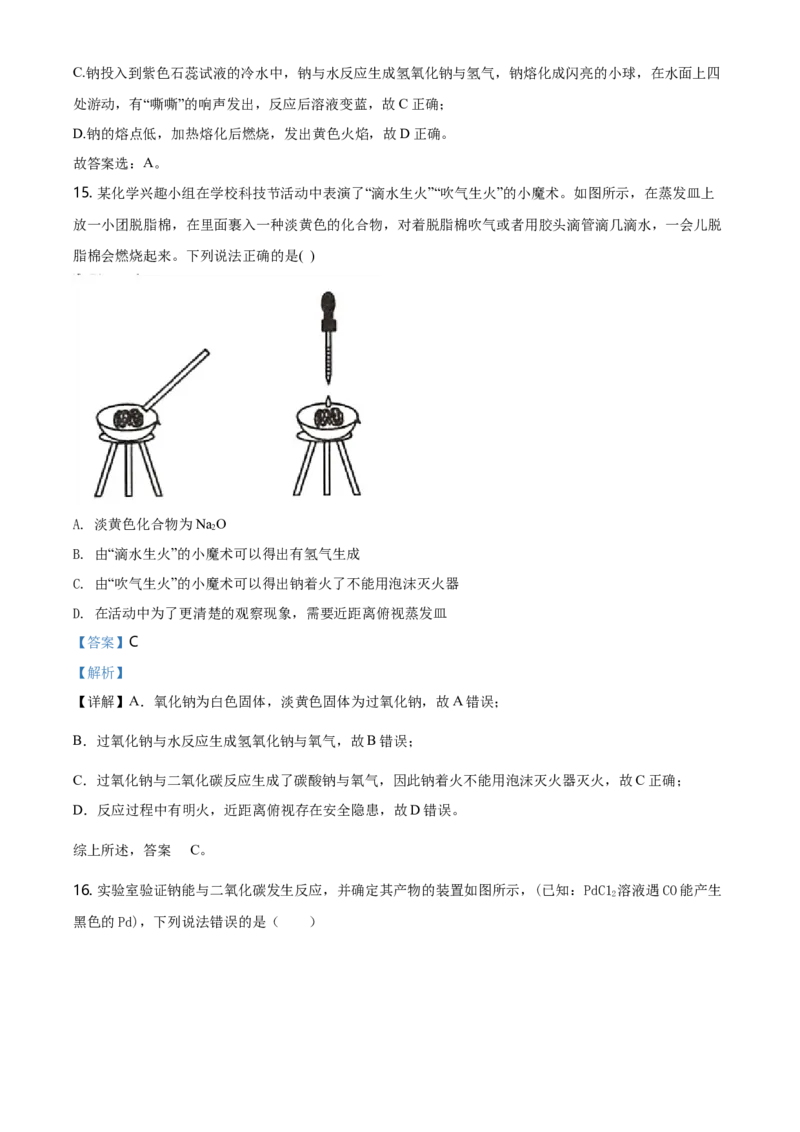
15. 某化学兴趣小组在学校科技节活动中表演了“滴水生火”“吹气生火”的小魔术。如图所示,在蒸发皿上
放一小团脱脂棉,在里面裹入一种淡黄色的化合物,对着脱脂棉吹气或者用胶头滴管滴几滴水,一会儿脱
脂棉会燃烧起来。下列说法正确的是( )
A. 淡黄色化合物为NaO
2
B. 由“滴水生火”的小魔术可以得出有氢气生成
C. 由“吹气生火”的小魔术可以得出钠着火了不能用泡沫灭火器
D. 在活动中为了更清楚的观察现象,需要近距离俯视蒸发皿
【答案】C
【解析】
【详解】A.氧化钠为白色固体,淡黄色固体为过氧化钠,故A错误;
B.过氧化钠与水反应生成氢氧化钠与氧气,故B错误;
C.过氧化钠与二氧化碳反应生成了碳酸钠与氧气,因此钠着火不能用泡沫灭火器灭火,故C正确;
D.反应过程中有明火,近距离俯视存在安全隐患,故D错误。
综上所述,答案 为C。
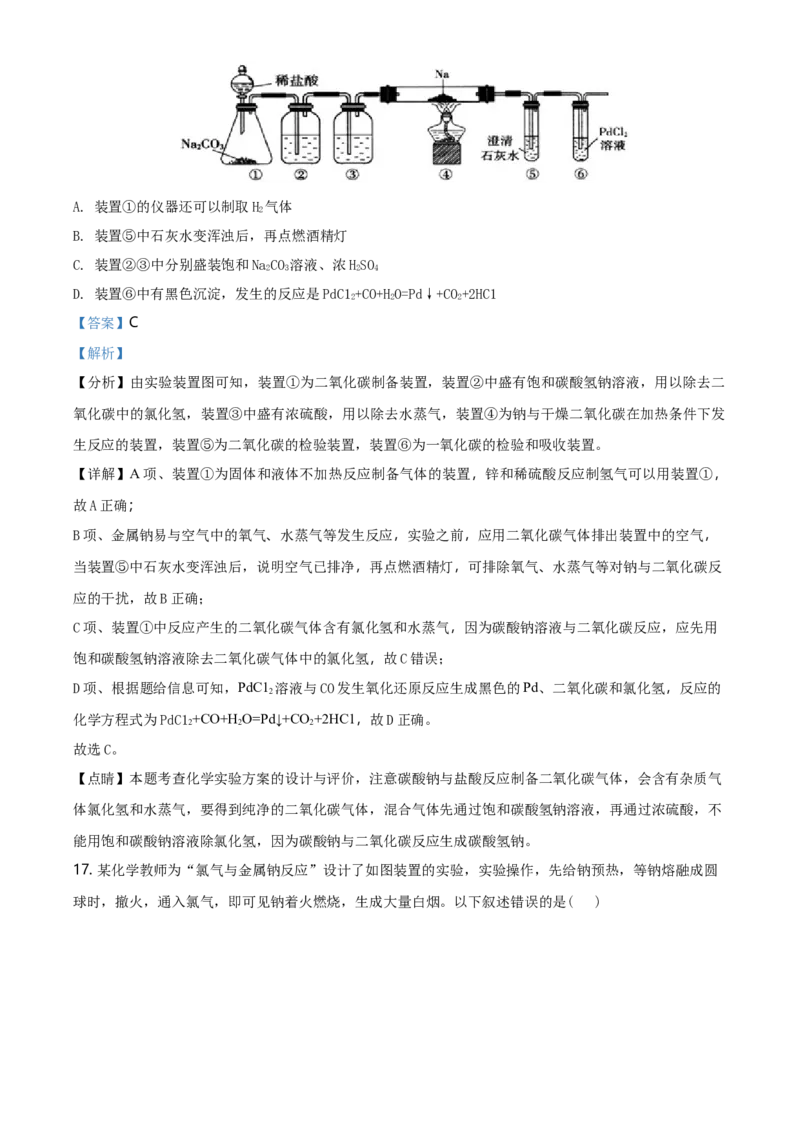
16. 实验室验证钠能与二氧化碳发生反应,并确定其产物的装置如图所示,(已知:PdC1 溶液遇CO能产生
2
黑色的Pd),下列说法错误的是( )A. 装置①的仪器还可以制取H 气体
2
B. 装置⑤中石灰水变浑浊后,再点燃酒精灯
C. 装置②③中分别盛装饱和NaCO 溶液、浓HSO
2 3 2 4
D. 装置⑥中有黑色沉淀,发生的反应是PdC1+CO+HO=Pd↓+CO+2HC1
2 2 2
【答案】C
【解析】
【分析】由实验装置图可知,装置①为二氧化碳制备装置,装置②中盛有饱和碳酸氢钠溶液,用以除去二
氧化碳中的氯化氢,装置③中盛有浓硫酸,用以除去水蒸气,装置④为钠与干燥二氧化碳在加热条件下发
生反应的装置,装置⑤为二氧化碳的检验装置,装置⑥为一氧化碳的检验和吸收装置。
【详解】A项、装置①为固体和液体不加热反应制备气体的装置,锌和稀硫酸反应制氢气可以用装置①,
故A正确;
B项、金属钠易与空气中的氧气、水蒸气等发生反应,实验之前,应用二氧化碳气体排出装置中的空气,
当装置⑤中石灰水变浑浊后,说明空气已排净,再点燃酒精灯,可排除氧气、水蒸气等对钠与二氧化碳反
应的干扰,故B正确;
C项、装置①中反应产生的二氧化碳气体含有氯化氢和水蒸气,因为碳酸钠溶液与二氧化碳反应,应先用
饱和碳酸氢钠溶液除去二氧化碳气体中的氯化氢,故C错误;
D项、根据题给信息可知,PdC1 溶液与CO发生氧化还原反应生成黑色的Pd、二氧化碳和氯化氢,反应的
2
化学方程式为PdC1+CO+H O=Pd↓+CO +2HC1,故D正确。
2 2 2
故选C。
【点睛】本题考查化学实验方案的设计与评价,注意碳酸钠与盐酸反应制备二氧化碳气体,会含有杂质气
体氯化氢和水蒸气,要得到纯净的二氧化碳气体,混合气体先通过饱和碳酸氢钠溶液,再通过浓硫酸,不
能用饱和碳酸钠溶液除氯化氢,因为碳酸钠与二氧化碳反应生成碳酸氢钠。
17. 某化学教师为“氯气与金属钠反应”设计了如图装置的实验,实验操作,先给钠预热,等钠熔融成圆
球时,撤火,通入氯气,即可见钠着火燃烧,生成大量白烟。以下叙述错误的是( )A. 反应生成的大量白烟是氯化钠晶体
B. 玻璃管尾部塞一团浸有NaOH溶液的棉球是用于吸收过量的氯气,以免其污染空气
C. 钠熔点高,所以先预热再反应
D. 若在棉球外沿滴一滴石蕊溶液,可据其颜色变化判断氯气是否被碱液完全吸收
【答案】C
【解析】
【详解】A. 钠在氯气中燃烧能生成氯化钠固体小颗粒,所以能看到白烟,A叙述正确;
B. 氯气排放到空气中是有害的,因其能和氢氧化钠溶液反应,故可用浸有NaOH溶液的棉球用于吸收过
量的氯气,B叙述正确;
C. 钠熔点低,先预热是为了先升高温度使氯气反应较完全,C叙述错误;
D. 氯气与水反应生成氯化氢和次氯酸,紫色石蕊遇酸变红,如果氢氧化钠溶液不能完全吸收掉氯气,则
过量的氯气会和水反应,而紫色石蕊变红,石蕊变红则说明氢氧化钠溶液没有完全吸收掉氯气,D叙述正
确。故答案选C。
18. 下列说法不正确 的是( )
A. 热的纯碱溶液可以去除物品表面的油污
B. 在医疗上,苏打是治疗胃酸过多的一种药剂
C. 漂白粉可用于游泳池的消毒杀菌
D. 氯气是一种重要的化工原料,大量用于制造盐酸、有机溶剂、农药等
【答案】B
【解析】
【详解】A.纯碱溶液水解显碱性,碱性溶液促进油污水解,A正确;
B.碳酸钠溶液的碱性较强,碳酸氢钠在医疗上是治疗胃酸过多的一种药剂,B错误;
C.漂白粉具有强氧化性能杀菌消毒,漂白粉可用于游泳池的消毒杀菌,C正确;
D.氯气有毒,可用于制农药,盐酸,与烷烃反应制备卤代烃等有机溶剂,D正确;答案选B。
19. 下列关于氯水的说法正确的( )
A. 新制氯水呈浅黄绿色,是因为氯水中含有HClO
B. 新制氯水在光照的条件下,可以产生气体,该气体是氯气
C. 新制氯水中滴加硝酸银溶液,没有任何现象D. 新制氯水可以和金属镁反应
【答案】D
【解析】
【分析】氯气溶于水,部分与氯气与水反应生成氯化氢和次氯酸,溶液中存在氯气、次氯酸、水三种分子,
H+、ClO−、Cl−、OH−四种离子。
【详解】A. 氯水成分中,只有氯气为黄绿色,氯水的颜色呈浅黄绿色,说明氯水中含有Cl,故A错误;
2
B. 新制氯水中存在次氯酸,不稳定,见光分解为盐酸和氧气,不会出现氯气放出,故B错误;
C. 新制氯水中含氯离子,滴加硝酸银溶液,会出现白色沉淀,故C错误;
D. 氯水中含有盐酸和次氯酸,溶液呈酸性,与镁反应生成氯化镁和氢气,故D 正确;
故选D。
20. 下列关于物质的量浓度表述正确的是( )
A. 在标准状况下,VL氨气溶于1L水配成密度为ρg/cm3的氨水,该氨水的物质的量浓度为
mol/L
B. 实验室使用的浓盐酸的溶质质量分数为36.5%,密度为1.19g/cm3,则该浓盐酸物质的量浓度是
11.9mol/L
C. 将40g氢氧化钠固体溶于1L水中,物质的量浓度为1mol/L
D. 0.3mol/L硫酸钠溶液中含有钠离子和硫酸根离子总物质的量为0.9mol
【答案】B
【解析】
【 详 解 】 A. 标 况 下 VL 氨 气 的 物 质 的 量 为 n= mol , 溶 液 的 体 积 V =
液
,c= mol/L,故A错误;
.
B 根据公式 ,故B正确;
C. 氢氧化钠固体溶于1L水中,溶液的体积会发生改变,体积不再是1L,物质的量浓度不是1mol/L,故
C错误;D. 硫酸钠溶液物质的量浓度已知,但溶液体积未知,不能计算离子物质的量,故D错误;
答案选B。
21. 下列叙述正确的是( )
①标准状况下,0.2mol任何物质的体积均为4.48L
②若1mol气体的体积为22.4L,则它一定处于标准状况下
③标准状况下,1LHCl和1LHO的物质的量相同
2
④标准状况下,1gH 和14gN 的体积相同
2 2
⑤28gCO的体积为22.4L
⑥两种物质的物质的量相同,则它们在标准状况下的体积也相同
⑦在同温同体积时,气体物质的物质的量越大,则压强越大
⑧同温同压下,气体的密度与气体的相对分子质量成正比
A. ①④⑧ B. ⑥⑦⑧ C. ②③⑤ D. ④⑦⑧
【答案】D
【解析】
【详解】①标准状况下,0.2mol任何气体物质的体积均为4.48L,但所有物质并不都是气体,故①错误,
①不选;
②若1mol气体的体积为22.4L,由于温度、压强影响气体摩尔体积,则它可能处于标准状况下,也可能不
是标况下,故②错误,②不选;
③标准状况下,HCl为气体,而HO不是气体,二者体积相等,它们物质的量不相等,故错误,③不选;
2
④1gH 物质的量为 ,14gN 的物质的量为 ,二者物质的量相等,标况
2 2
下,二者体积相等,故正确,④选;
⑤28gCO为1mol,但不一定处于标况下,CO的体积不一定为22.4L,故错误,⑤不选;;
⑥标况下,两种物质不一定都是气体,它们物质的量相等,占有的体积不一定相等,故错误,⑥不选;
⑦在同温同体积时,气体压强与物质的量成正比,则气体物质的物质的量越大,压强越大,故正确,⑦选;
⑧同温同压下,气体的密度之比等于摩尔质量之比,也等于相对分子质量之比,即气体的密度与气体的相
对分子质量成正比,故正确,⑧选;
综上所诉,④⑦⑧正确,答案选D。
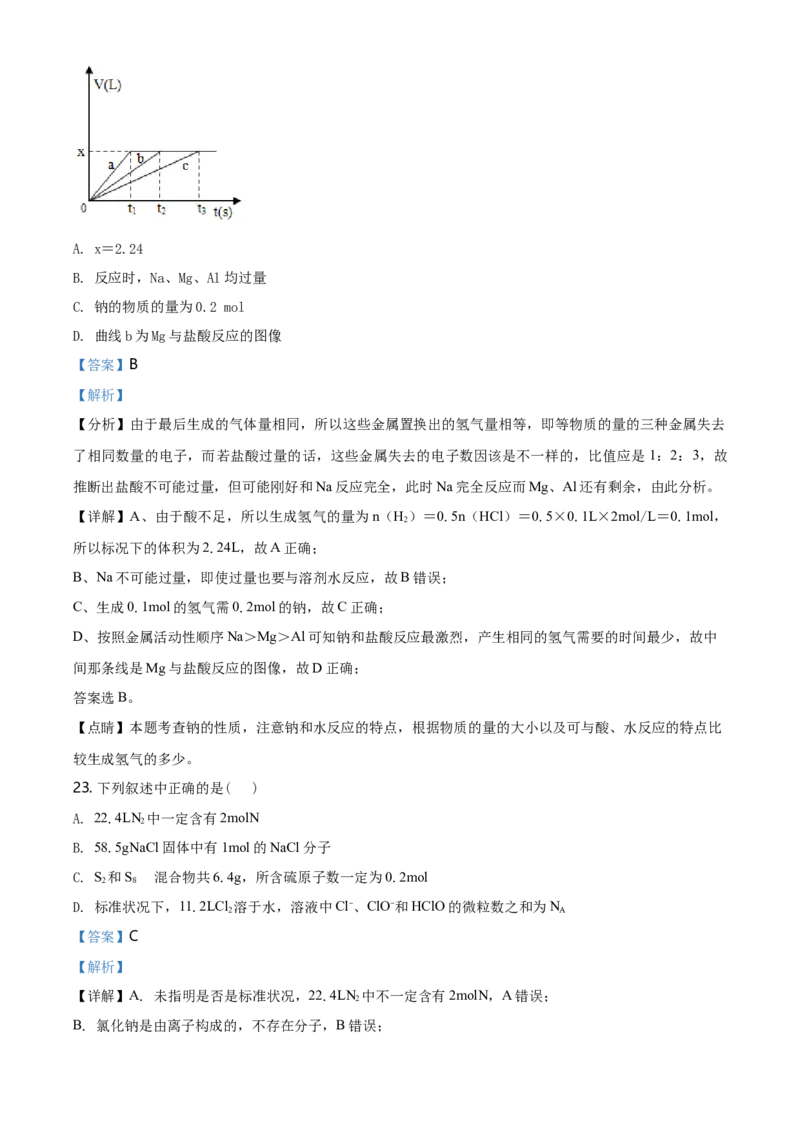
22. 将等物质的量的金属Na、Mg、Al分别与100mL2mol/L盐酸反应,实验测得生成气体的体积V(已折合为
标准状况)与时间t的关系如图所示,则下列说法不正确的是( )A. x=2.24
B. 反应时,Na、Mg、Al均过量
C. 钠的物质的量为0.2 mol
D. 曲线b为Mg与盐酸反应的图像
【答案】B
【解析】
【分析】由于最后生成的气体量相同,所以这些金属置换出的氢气量相等,即等物质的量的三种金属失去
了相同数量的电子,而若盐酸过量的话,这些金属失去的电子数因该是不一样的,比值应是1:2:3,故
推断出盐酸不可能过量,但可能刚好和Na反应完全,此时Na完全反应而Mg、Al还有剩余,由此分析。
【详解】A、由于酸不足,所以生成氢气的量为n(H )=0.5n(HCl)=0.5×0.1L×2mol/L=0.1mol,
2
所以标况下的体积为2.24L,故A正确;
B、Na不可能过量,即使过量也要与溶剂水反应,故B错误;
C、生成0.1mol的氢气需0.2mol的钠,故C正确;
D、按照金属活动性顺序Na>Mg>Al可知钠和盐酸反应最激烈,产生相同的氢气需要的时间最少,故中
间那条线是Mg与盐酸反应的图像,故D正确;
答案选B。
【点睛】本题考查钠的性质,注意钠和水反应的特点,根据物质的量的大小以及可与酸、水反应的特点比
较生成氢气的多少。
23. 下列叙述中正确的是( )
A. 22.4LN 中一定含有2molN
2
B. 58.5gNaCl固体中有1mol的NaCl分子
C. S 和S 的混合物共6.4g,所含硫原子数一定为0.2mol
2 8
D. 标准状况下,11.2LCl 溶于水,溶液中Cl-、ClO-和HClO的微粒数之和为N
2 A
【答案】C
【解析】
【详解】A. 未指明是否是标准状况,22.4LN 中不一定含有2molN,A错误;
2
B. 氯化钠是由离子构成的,不存在分子,B错误;C. S 和S 均是硫原子组成的单质,硫原子的物质的量n=m/M=6.4g÷32g/mol=0.2mol,C正确;
2 8
D. 氯气与水是可逆反应,溶液中还存在氯气,溶液中Cl-、ClO-和HClO的微粒数之和小于N ,D错误;
A
答案选C。
24. 中国科学技术大学的钱逸泰教授等以CCl 和金属钠为原料,在700℃时反应制造出纳米级金刚石粉末和
4
另一种化合物。该成果发表在世界权威的《科学》杂志上,立即被科学家们高度评价为“稻草变黄金”。
同学们对此有下列一些“理解”,你认为其中错误的是( )
A. 这个反应是氧化还原反应 B. 制造过程中元素种类没有改变
C. 另一种化合物为NaCl D. 纳米级金刚石粉末为胶体
【答案】D
【解析】
【详解】A. CCl 和金属钠反应生成金刚石(碳单质),碳元素的化合价降低,钠元素化合价升高,有元素
4
的化合价变化属于氧化还原反应,故A正确;
B. 根据元素守恒定律可知制造过程中元素种类没有改变,故B正确;
C. 根据原子守恒可知CCl 和金属钠反应生成金刚石(碳单质)和NaCl,故C正确;
4
D. 金刚石为单质,分散系中的胶体为混合物,故D错误;
答案选D。
25. NaClO 是一种重要的杀菌消毒剂,其一种生产工艺如图,下列说法不正确的是( )
2
A. “反应”步骤中生成ClO 的化学方程式:HSO +SO +2NaClO=2ClO +2NaHSO
2 2 4 2 3 2 4
B. “电解”所用食盐水由粗盐水精制而成,精制时,为除去杂质SO 和Ca2+,需要加入适当过量的除杂
试剂,添加顺序为为BaCl 、NaCO
2 2 3
C. 吸收反应NaOH+HO+ClO NaClO+O+HO中,氧化产物是O,氧化剂与还原剂的物质的量之比为
2 2 2 2 2 2 2
1:2
D. 270gClO 与过量的NaOH、HO 完全反应,计算生成的NaClO 的物质的量为4mol
2 2 2 2
【答案】C
【解析】【分析】由制备流程可知,NaClO 和SO 在HSO 酸化条件下生成ClO ,其中NaClO 是氧化剂,回收产
3 2 2 4 2 3
物为NaHSO ,说明生成硫酸氢钠,且产生ClO ,根据得失电子守恒可知此反应的化学方程式;然后电解
4 2
装置中阴极ClO 得电子生成ClO ,阳极Cl-失电子生成Cl ,含过氧化氢的氢氧化钠溶液吸收ClO ,最后
2 2 2
NaClO 溶液结晶、干燥得到产品,以此解答该题。
2
【详解】A.NaClO 和SO 在HSO 酸化条件下生成ClO ,其中NaClO 是氧化剂,还原产物为NaCl,回
3 2 2 4 2 3
收产物为NaHSO ,说明生成硫酸氢钠,且产生ClO ,根据得失电子守恒可知,此反应的化学方程式为:
4 2
HSO +SO +2NaClO=2ClO +2NaHSO,故A正确;
2 4 2 3 2 4
B.食盐中混有SO 和Ca2+,一般用氯化钡除去硫酸根,用碳酸钠除去钙离子和过量的钡离子,因此除去
时需要加入的试剂分别为BaCl 、NaCO,故B正确;
2 2 3
C.根据流程图可知,利用含过氧化氢的氢氧化钠溶液吸收ClO ,产物为ClO ,则此反应中ClO 为氧化
2 2
剂,还原产物为ClO ,Cl的化合价从+4价降为+3价,1molClO 参加反应得到1mol电子,HO 为还原剂,
2 2 2
氧化产物为O,1molH O 参加反应失去2mol电子,依据得失电子守恒可知氧化剂和还原剂的物质的量之
2 2 2
比为2:1,故C错误
D.270gClO 的物质的量是270g÷67.5g/mol=4mol,与过量的NaOH、HO 完全反应,根据氯原子守恒
2 2 2
可知生成的NaClO 的物质的量为4mol,故D正确。
2
故答案选C。
二、填空题
26. 现有下列物质:①稀硫酸②小苏打③氨水④二氧化碳⑤FeCl 固体⑥稀NaOH溶液⑦硝酸亚铁溶液。
3
(1)上述物质中属于电解质的物质序号为__________
(2)物质①可以导电,其电离方程式为____________
(3)向⑥中通入过量④的离子方程式为____________
【答案】 (1). ②⑤ (2). HSO =2H++SO2- (3). OH-+CO =HCO-
2 4 4 2 3
【解析】
【分析】电解质须为化合物,在水溶液或熔融状态下能够导电;非电解质须为化合物,自身不能电离出离
子,不能导电。
【详解】(1)根据定义可知,①③⑥⑦虽能导电,但属于混合物,不属于电解质;④虽为化合物,但在水溶
液中不是本身电离出自由移动的阴阳离子,所以不属于电解质;②和⑤属于盐,在水溶液中或熔融状态下
能够导电,属于电解质,故答案为:②⑤;
(2)硫酸为二元强酸,其电离方程式为:HSO =2H++SO2-,故答案为:HSO =2H++SO2-;
2 4 4 2 4 4(3)向氢氧化钠溶液中通入过量的二氧化碳,氢氧化钠先与二氧化碳生成碳酸钠,生成的碳酸钠再与二氧化
碳反应生成碳酸氢钠,故离子方程式为:OH-+CO =HCO-,故答案为:OH-+CO =HCO-。
2 3 2 3
27. (1)写出下列物质的化学式:漂白粉的主要成分_________
(2)①氯气与铁反应的化学方程式________________
②氯气与水反应的化学方程式 ________________
【答案】 (1). CaCl 、Ca(ClO) (2). 2Fe+3Cl 2FeCl (3). HO+Cl =HCl+HClO
2 2 2 3 2 2
【解析】
【详解】(1)写出下列物质的化学式:漂白粉的主要成分CaCl 、Ca(ClO) ,有效成分是Ca(ClO) ;故答案为:
2 2 2
CaCl 、Ca(ClO) 。
2 2
(2)①氯气与铁反应生成氯化铁,其化学方程式2Fe+3Cl 2FeCl ;故答案为:2Fe+3Cl 2FeCl 。
2 3 2 3
②氯气与水反应生成盐酸和次氯酸,其化学方程式HO+Cl =HCl+HClO;故答案为:
2 2
HO+Cl =HCl+HClO。
2 2
28. 现有X、Y、Z三种元素(1-18号)。
①Z的单质可以在Y的单质中燃烧,生成ZY。②X的单质可与Y的单质化合,生成两种液态化合物
2 2
XY,XY
2 2 2
(1)X、Y、Z的元素符号分别为_____、____、_____。
(2)将Z的单质溶于XY中的离子方程式为____________。
2
【答案】 (1). H (2). O (3). Na (4). 2Na+2HO=2Na++2OH-+H↑
2 2
【解析】
【分析】因Z的单质可在Y的单质中燃烧,生成ZY,X的单质可与Y的单质化合,生成两种液态化合物
2 2
XY,XY,可推出X为H、Y为O、Z为Na,据此解答。
2 2 2
【详解】(1)根据以上分析可知X、Y、Z的元素符号分别为H、O、Na。
(2)将钠的单质溶于HO中生成氢氧化钠和氢气,反应的离子方程式为2Na+2HO=2Na++2OH-+H↑。
2 2 2
三、实验题
29. 纯碱是生活中常用的去油污洗涤剂,某同学欲用碳酸钠晶体(NaCO·10HO)配制220mL1mol/L的
2 3 2
NaCO 溶液,请回答下列问题:
2 3
(1)与实验有关的图标和名称正确是是_____________。
A B C D护目镜 洗手 用电 加热
(2)配制过程中需要NaCO·10HO的质量为__________。
2 3 2
(3)实验过程中除需要托盘天平(带砝码)、药匙、烧杯、量筒、玻璃棒、试剂外,还需要的玻璃仪器有
__________。
(4)配制溶液时正确的操作顺序是 __________。
a.称量NaCO·10HO固体
2 3 2
b.将烧杯中的溶液沿玻璃注入容量瓶
c.轻轻摇动容量瓶,使溶液合均匀
d.反复上下颠倒,摇匀
e.将称好的NaCO·10HO固体放入烧杯中,加入适量蒸馏水,搅拌,使固体全部溶解
2 3 2
f.计算需要NaCO·10HO固体的质量
2 3 2
g.将蒸馏水注入容量瓶,后定容
h.将配制好的溶液倒入试剂瓶中,并贴好标签
i.用少量蒸馏水洗涤烧杯内壁和玻璃棒2-3次,将洗涤液也都注入容量瓶
(5)定容的具体操作:将蒸馏水注入容量瓶______________。
(6)配制溶液时,下列实验操作会使配制溶液浓度偏高的是__________。
A.容量瓶清洗后,未经过干燥处理
B.定容操作时,俯视刻度线
C.溶液未经冷却直接倒入容量瓶中
D.定容后倒转容量瓶几次,发现液面最低点低于刻度线,再补加几滴水到刻度
【答案】 (1). B (2). 71.5g (3). 250mL容量瓶、胶头滴管 (4). faebicgdh (5). 至刻度线以下1~
2cm,改用胶头滴管滴加,直至凹液面最低处与刻度线相切 (6). BC
【解析】
【详解】(1)A. 护目镜表示对眼睛有损伤的强光或药品,需对眼睛进行保护,碳酸钠碱性较弱,不需要佩
戴护目镜,故不选A;
B. 洗手是表示药品对皮肤有伤害,碳酸钠溶液显碱性,使用药品后要洗手,故选择B;
C. 用电是提醒用电安全,本实验不需要用到电能,故不选C;
D. 本实验不需要加热,故不选D;答案选B。
(2)配制220mL溶液,需要用250mL容量瓶,则配制过程中需要NaCO·10HO的质量为
2 3 2
m=nM=cVM=1mol/L×0.25L×286g/mol=71.5g;
(3)配制一定物质的量浓度溶液的基本步骤是计算、称量、溶解、冷却、转移、洗涤、摇匀、定容、振荡、
装瓶等,则配制220mL1mol/L的NaCO 溶液使用的仪器为:托盘天平(带砝码)、药匙、玻璃棒、烧杯、
2 3
胶头滴管、250mL容量瓶,所以还缺少胶头滴管、250mL容量瓶,故答案为:胶头滴管、250mL容量瓶;
(4)根据以上分析可知配制溶液时的操作顺序是计算、称量、溶解、冷却、转移、洗涤、摇匀、定容、振
荡、装瓶等,即faebicgdh;
(5)定容的具体操作为:将蒸馏水注入容量瓶至刻度线以下1~2cm,改用胶头滴管滴加,直至凹液面最低
处与刻度线相切;
(6)A.容量瓶内有水,未经过干燥处理,对溶质的物质的量和溶液体积都不会产生影响,溶液浓度不变,
故A不选;
B.定容时,俯视刻度线,导致溶液体积偏小,溶液浓度偏高,故B选;
C.溶液未冷却转移至容量瓶,冷却后导致溶液体积偏小,浓度偏大,故C选;
D.定容后倒转容量瓶几次,发现液面最低点低于刻度线,再补加几滴水到刻度线,导致溶液体积偏大,溶
液浓度偏低,故D不选;
答案选BC。
30. Ⅰ“侯氏制碱法”是我国化工专家侯德榜为世界制破工业作出的突出贡献。某实验小组模拟“侯氏
法”的工艺流程及实验装置(部分夹持装置省略)如下:
气体A的饱和溶液 A与食盐的饱和溶液 悬浊液 晶体
纯碱
(1)气体A为______(填化学式)。
(2)工业上粗盐(含Ca2+、Mg2+、SO 等杂质)经除杂得到氯化钠,判断氯化钠中的钠元素的具体操作为
___________。
(3)第Ⅲ步操作用到的主要玻璃仪器是________。
Ⅱ、某小组利用传感器探究NaCO 和NaHCO 的性质。已知:氢氧根离子的浓度越小,溶液碱性越弱,(具
2 3 3
体过程如图)
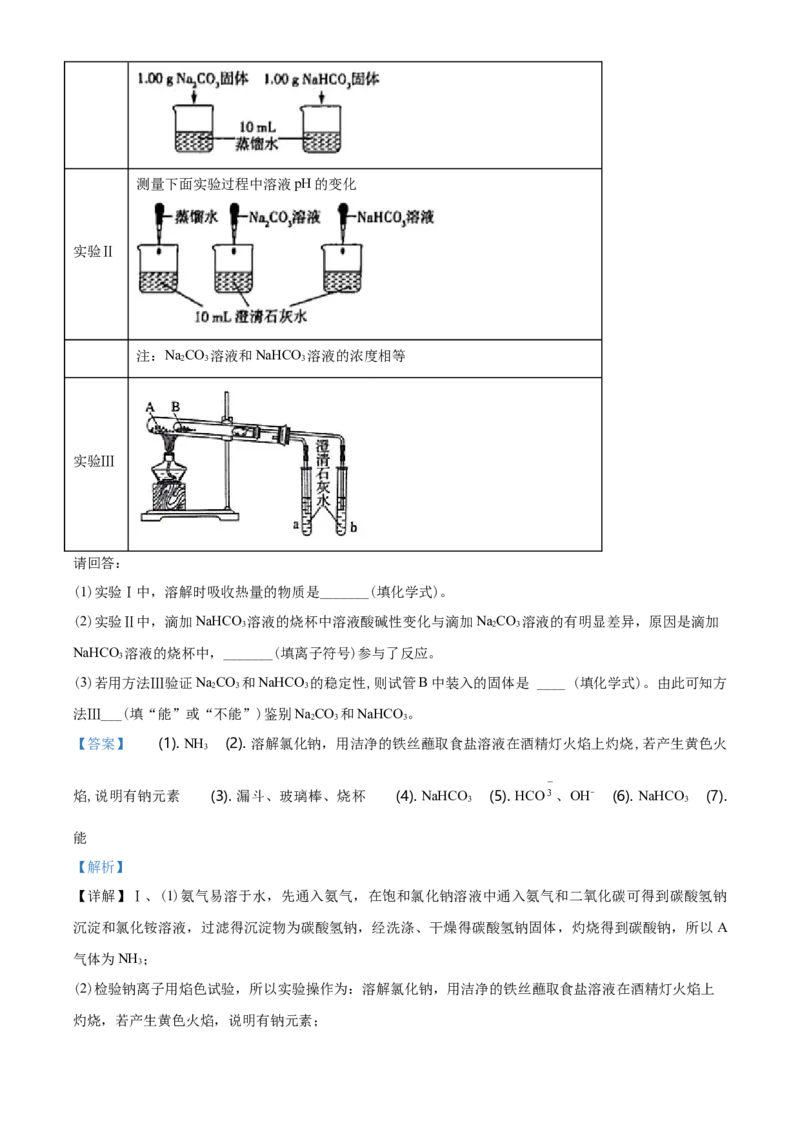
编号 实验操作
实验Ⅰ 测量下面实验过程中温度的变化测量下面实验过程中溶液pH的变化
实验Ⅱ
注:NaCO 溶液和NaHCO 溶液的浓度相等
2 3 3
实验Ⅲ
请回答:
(1)实验Ⅰ中,溶解时吸收热量的物质是_______(填化学式)。
(2)实验Ⅱ中,滴加NaHCO 溶液的烧杯中溶液酸碱性变化与滴加NaCO 溶液的有明显差异,原因是滴加
3 2 3
NaHCO 溶液的烧杯中,_______(填离子符号)参与了反应。
3
(3)若用方法Ⅲ验证NaCO 和NaHCO 的稳定性,则试管B中装入的固体是 ____ (填化学式)。由此可知方
2 3 3
法Ⅲ___(填“能”或“不能”)鉴别NaCO 和NaHCO 。
2 3 3
【答案】 (1). NH (2). 溶解氯化钠,用洁净的铁丝蘸取食盐溶液在酒精灯火焰上灼烧,若产生黄色火
3
焰,说明有钠元素 (3). 漏斗、玻璃棒、烧杯 (4). NaHCO (5). HCO 、OH- (6). NaHCO (7).
3 3
能
【解析】
【详解】Ⅰ、(1)氨气易溶于水,先通入氨气,在饱和氯化钠溶液中通入氨气和二氧化碳可得到碳酸氢钠
沉淀和氯化铵溶液,过滤得沉淀物为碳酸氢钠,经洗涤、干燥得碳酸氢钠固体,灼烧得到碳酸钠,所以A
气体为NH ;
3
(2)检验钠离子用焰色试验,所以实验操作为:溶解氯化钠,用洁净的铁丝蘸取食盐溶液在酒精灯火焰上
灼烧,若产生黄色火焰,说明有钠元素;(3)第Ⅲ步操作是过滤,过滤过程中需要用到的玻璃仪器有玻璃棒、漏斗、烧杯;
Ⅱ、(1)碳酸钠溶于水有明显的放热,而碳酸氢钠是吸热的;
(2)碳酸氢钠与氢氧化钙发生反应生成碳酸钙沉淀,所以滴加NaHCO 溶液的烧杯中,HCO 、OH-参与了
3
反应;
(3)酒精灯直接加热试管A,可知A中温度比B中高,因此试管B中盛放NaHCO ,且与B连接的澄清石
3
灰水变浑浊,而与A相连的澄清石灰水未变浑浊,更能说明碳酸钠比碳酸氢钠稳定,所以也能鉴别碳酸钠
与碳酸氢钠。
四、计算题
31. 某固体粉末由NaO与NaO 组成,将其分成等量的二份,一份与足量的CO 气体作用,发现该固体质
2 2 2 2
量增加了11.6g,同时生成了新的气体A;另一份溶于水后,所得溶液恰好被含硫酸29.4g的酸溶液中和,
试计算:
(1)A气体在标况下的体积是___;
(2)固体中NaO与NaO 的物质的量之比是___(写出计算过程)
2 2 2
【答案】 (1). 1.12L (2). 2:1
【解析】
【分析】NaO、NaO 与水反应都会生成NaOH,NaOH与硫酸反应后生成NaSO ,根据根据 和钠离
2 2 2 2 4
子守恒可知每一份中NaO、NaO 的总物质的量,设二者各自物质的量分别为xmol、ymol,根据NaO、
2 2 2 2
NaO 与CO 反应的方程式可以表示出各自反应使固体增重,结合固体总质量增重列方程计算解答。
2 2 2
【详解】NaOH 与硫酸反应后生成 NaSO ,根据 Na+守恒可知,n(Na SO )=n(Na O、NaO)=n(H SO )=
2 4 2 4 2 2 2 2 4
=0.3mol,
设每一份中NaO为xmol、NaO 为ymol,则:
2 2 2所以: ,解得x=0.2,y=0.1,
(1)由2NaO+2CO =2Na CO+O 可知,0.1mol Na O 反应生成O 为0.05mol,0.05mol O 在标况下的体积是
2 2 2 2 3 2 2 2 2 2
0.05mol×22.4L/mol=1.12L;
(2)由以上计算可知,氧化钠与过氧化钠的物质的量之比为2:1。