文档内容
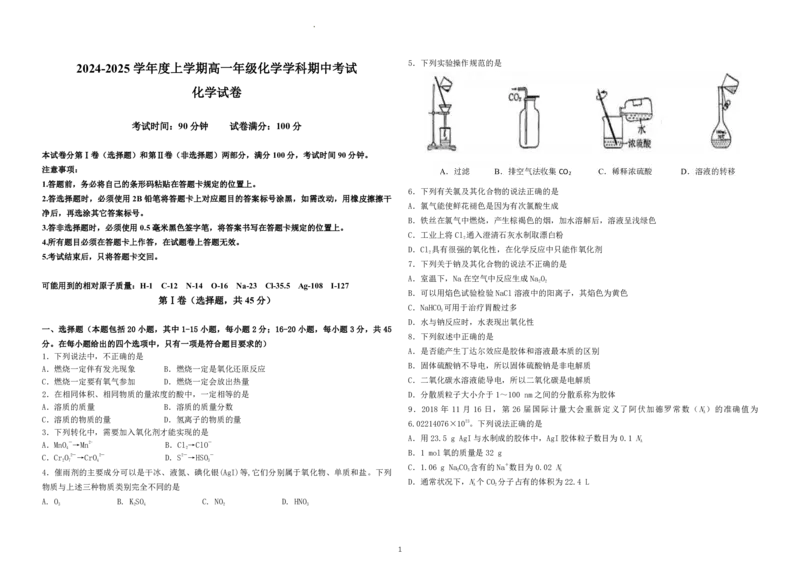
5.下列实验操作规范的是
2024-2025 学年度上学期高一年级化学学科期中考试
化学试卷
考试时间:90分钟 试卷满分:100分
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,满分100分,考试时间90分钟。
注意事项: A.过滤 B.排空气法收集CO C.稀释浓硫酸 D.溶液的转移
2
1.答题前,务必将自己的条形码粘贴在答题卡规定的位置上。
6.下列有关氯及其化合物的说法正确的是
2.答选择题时,必须使用2B铅笔将答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦擦干
A.氯气能使鲜花褪色是因为有次氯酸生成
净后,再选涂其它答案标号。
B.铁丝在氯气中燃烧,产生棕褐色的烟,加水溶解后,溶液呈浅绿色
3.答非选择题时,必须使用0.5毫米黑色签字笔,将答案书写在答题卡规定的位置上。
C.工业上将Cl 通入澄清石灰水制取漂白粉
2
4.所有题目必须在答题卡上作答,在试题卷上答题无效。
D.Cl 具有很强的氧化性,在化学反应中只能作氧化剂
2
5.考试结束后,只将答题卡交回。
7.下列关于钠及其化合物的说法不正确的是
A.室温下,Na在空气中反应生成NaO
2 2
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Cl-35.5 Ag-108 I-127
B.可以用焰色试验检验NaCl溶液中的阳离子,其焰色为黄色
第Ⅰ卷(选择题,共 45分)
C.NaHCO 可用于治疗胃酸过多
3
D.水与钠反应时,水表现出氧化性
一、选择题(本题包括20小题,其中1-15小题,每小题2分;16-20小题,每小题 3分,共45
8.下列叙述中正确的是
分。在每小题给出的四个选项中,只有一项是符合题目要求的)
A.是否能产生丁达尔效应是胶体和溶液最本质的区别
1.下列说法中,不正确的是
B.固体硫酸钠不导电,所以固体硫酸钠是非电解质
A.燃烧一定伴有发光现象 B.燃烧一定是氧化还原反应
C.燃烧一定要有氧气参加 D.燃烧一定会放出热量 C.二氧化碳水溶液能导电,所以二氧化碳是电解质
2.在相同体积、相同物质的量浓度的酸中,一定相等的是 D.分散质粒子大小介于1~100 nm之间的分散系称为胶体
A.溶质的质量 B.溶质的质量分数 9.2018 年 11 月 16 日,第 26 届国际计量大会重新定义了阿伏加德罗常数(N)的准确值为
A
C.溶质的物质的量 D.氢离子的物质的量
6.02214076×1023。下列说法正确的是
3.下列转化中,需要加入氧化剂才能实现的是
A.用23.5 g AgI与水制成的胶体中,AgI胶体粒子数目为0.1 N
A.MnO―→Mn2+ B.Cl→ClO― A
4 2
B.1 mol氧的质量是32 g
C.CrO2―→CrO2― D.S2―→HSO―
2 7 4 3
C.1.06 g NaCO 含有的Na+数目为0.02 N
4.催雨剂的主要成分可以是干冰、液氮、碘化银(AgI)等,它们分别属于氧化物、单质和盐。下列 2 3 A
D.通常状况下,N个CO 分子占有的体积为22.4 L
物质与上述三种物质类别完全不同的是 A 2
A. O B. KSO C. NO D. HNO
3 2 4 2 3
学科网(北京)股份有限公司 110.下列化学方程式或离子方程式中,正确的是 16.从铁钛矿(主要成分FeTiO)制取金属钛(Ti),其在一定条件下的主要反应有:
3
A.氨水与醋酸溶液反应:H++ NH·HO=== NH++ HO ①FeTiO+H=Fe+TiO+HO;②TiO+2C+2Cl=X+2CO;③TiCl+2Mg=2MgCl+Ti
3 2 4 2 3 2 2 2 2 2 4 2
B.工业上制备漂白液:Cl + 2OH-=== Cl-+ ClO-+ HO 下列叙述不正确的是
2 2
C.Na与FeSO 溶液反应:2Na + Fe2+ === Fe + 2Na+ A.反应①中的H 被氧化 B.反应②中钛元素失电子
4 2
D.氯化铁溶液与铜反应: 2Fe3+ + 3Cu ===3Cu2+ + 2Fe C.反应②中X为TiCl D.反应③是置换反应
4
11.在无色透明溶液中,能够大量共存的离子组是 17.某溶液仅由Na+、Cu2+、Ba2+、Fe3+、CO2-、SO2-、Cl-中的若干种离子组成,取适量溶液进行
3 4
A.MnO―、K+、S2―、Na+ B.Mg2+、NO―、OH―、Cl― 如下实验:
4 3
C.CO2―、K+、H+、Cl― D.Na+、NO―、SO2―、Cl―
3 3 4
12.配制一定体积、一定物质的量浓度的溶液,下列操作会使配得的溶液浓度偏小的是
A.容量瓶中有少量蒸馏水 B.溶液从烧杯转移到容量瓶后没有洗涤烧杯
C.未冷却即将溶液转移到容量瓶 D.定容时俯视容量瓶刻度线
13.同温同压下,等质量的二氧化碳和一氧化碳气体的下列有关比较正确的是 根据以上实验,下列推断错误的是
A.氧原子数比为1:1 B.体积比为11:7
A.气体1通入澄清石灰水中,溶液变浑浊 B.白色沉淀2中加稀硝酸,沉淀不溶解
C.物质的量比为11:7 D.密度比为11:7
C.原溶液中一定存在Na+,一定不存在Ba2+ D.白色沉淀3说明原溶液中一定存在Cl−
14.中医典籍记载了许多化学知识,下列有关记载体现出被记载的物质具有氧化性的是
18.下列“假说”在化学发展过程中曾经起到一定作用,至今仍得到公认的是
A.金(Au):“虽被火亦未熟"
A.18世纪末化学家提出的“与氧化合的反应为氧化反应,失去氧的反应为还原反应”
B.石灰(CaO):“以水沃之,即热蒸而解”
C.石硫黄(S):“能化……银、铜、铁,奇物” B.1808年盖·吕萨克提出的“同温同压下,相同体积的不同气体含有相同数目的原子”
C.1861年Graham提出的“胶体是一种粘性液体”
D.石钟乳(CaCO):“色黄,以苦酒(醋)洗刷则白”
3
15.某实验小组通过下图所示实验,探究NaO 与水的反应: D.1887年阿伦尼乌斯提出的“电解质在溶液中会自发离解成带电的粒子”
2 2
19.标准状况下a L氨溶于水(水的密度近似为1.0 g/mL)中,得V mL氨水,其密度为ρg/ mL,溶
质的质量分数为ω,物质的量浓度为c mol/L,则下列说法正确的是
① ω=35a/Vρ;② ρ<1.0 g/ mL;③ 用等体积水稀释上述溶液,所得溶液质量分数大于ω/2;
④ c = 1000a/22.4V
A.①② B.③④ C.②④ D.①③
20.对于白磷引起的中毒,硫酸铜溶液是一种解毒剂,有关反应如下:
11P + 60CuSO + 96HO = 20 X +24 HPO + 60HSO,
下列说法正确的是 4 4 2 3 4 2 4
关于该反应下列说法不正确的是
A.②中的大量气泡主要成分是氢气
A.X中铜的化合价为+1价,CuSO 仅作氧化剂
4
B.③中溶液变红,说明有酸性物质生成
B.48molHO参加反应时,被CuSO 氧化的P 为3mol
2 4 4
C.④中现象可能是由于溶液中含有强氧化性物质造成的
C.每消耗1.1molP 时,有12mol电子转移
4
D.⑤中MnO 的主要作用是降低了水中氧气的溶解度 D.氧化产物和还原产物的物质的量之比为6∶5
2
学科网(北京)股份有限公司 2第Ⅱ卷(选择题,共 55 分) 23.(14分) A、B、C、D为四种可溶性的盐,它们包含的阳离子和阴离子分别为Ba2+、Fe2+、Na+、
Cu2+和NO-、SO2-、Cl-、CO2- (离子在物质中不能重复出现)。
3 4 3
21. (14分)已知下列物质: ①若把四种盐分别溶于盛有蒸馏水的四支试管中,观察到C盐的溶液呈蓝色,且C盐固体中阴阳离
①金刚石 ②石墨 ③冰水混合物 ④纯净无污染的空气 ⑤红磷 ⑥白磷 ⑦食盐水 ⑧氧化 子个数之比为1:1;
钠 ⑨胆矾 ⑩CuSO 溶液 氧化钙 ②若向①的四支试管中分别加入足量稀盐酸,只有D的盐溶液有无色无味的气体逸出;
4
(1)属于混合物的是___________(填序号,下同),属于单质的是___________,属于化合物的是 ③向B盐溶液中加入硝酸酸化的AgNO 溶液,有白色沉淀产生;
⑪ 3
___________,属于电解质的是___________。 ④A盐溶液与C盐溶液混合后有白色沉淀产生。
(2)上述物质中能导电的是___________。 (1)根据以上实验事实可推断它们的化学式为:C___________;D___________。
(3)属于由同种元素组成的不同单质的是___________。 (2)写出足量稀盐酸与D盐溶液反应放出气体的离子方程式: 。
(4)下列变化不属于化学变化的是___________(填字母)。 (3)写出④中发生反应的离子方程式: 。
A.石墨转化成金刚石 B.冰融化成冰水混合物 (4)向B盐与C盐的混合溶液中加入一定量的Zn粉,可能发生的反应有 (按
C.氧化钙溶于水 D.无水硫酸铜遇水变蓝 照反应的先后顺序写出相应的离子方程式)。若加入Zn粉后,有金属析出,过滤、洗涤后向滤渣中
E.泥水中加入Fe(OH) 胶体 加入稀盐酸,无气体产生,则滤液中一定含有的金属阳离子为 。
3
22. (12分)海洋是一个巨大的化学资源宝库,其中钠元素和氯元素是海洋中含量较高的元素。生 24.(15分)某小组探究酸化条件对0.1mol/L KI溶液氧化反应的影响。
活中也有很多含钠、含氯的化合物。请结合所学化学知识,回答下列问题。 序号 操作及现象
(1)过氧化钠可以在潜水艇和消防员的呼吸面具中作为氧气来源。若只考虑过氧化钠与二氧化碳
取放置一段时间的0.1mol/LKI溶液,加入淀粉溶液,溶液不变蓝;向溶液中继
实验1
反应,每消耗1mol过氧化钠固体、反应转移电子数为 。
续加入2滴6 mol/L的稀硫酸,溶液立即变蓝
(2)漂白粉广泛用于环境的消毒、杀菌。漂白粉溶于水后,与空气中的二氧化碳反应,能生成具
取新制的0.1mol/L KI溶液,加入淀粉溶液,溶液不变蓝;向溶液中继续加入2
实验2
有强漂白性的物质。请用离子方程式表示该过程: 。
滴6 mol/L的稀硫酸,溶液10s后微弱变蓝
(3)“84消毒液”能有效杀灭病毒,某同学购买了瓶“84消毒液”,其说明中有如下信息:NaClO
(1)溶液变蓝,说明溶液中含有 。结合实验1和实验2,该小组
质量分数为25%、密度为1.19g·cm-3、1000mL、请稀释后使用。
同学认为酸化能够加快I-氧化反应的速率。
①该“84消毒液”中NaClO的物质的量浓度为 mol·L-1。(保留至小数点后一位)
(2)同学甲对滴加稀硫酸后溶液变蓝速率不同的原因提出猜想:放置一段时间后的0.1mol/L KI
②现实验室需要480mL0.2mol·L-1的NaClO溶液,某同学用NaClO固体配制该物质的量浓度的溶液。
溶液成分与新制0.1mol/L KI溶液可能存在差异,并继续进行实验3。取新制的0.1mol/L KI溶液
应用托盘天平称取NaCl0固体 g。配制NaClO溶液时需用的主要仪器有托盘天平、
在空气中放置,测得pH如下:
药匙、烧杯、量筒、玻璃棒、 、 。
时间 5分钟 1天 3天 10天
③实验时遇到下列情况,会导致溶液物质的量浓度偏高的是 (填标号)。 实验3
pH 7.2 7.4 7.8 8.7
A.容量瓶内壁附有水珠而未干燥处理 B.称量使用的砝码已生锈
资料:
C.溶解时使用的烧杯及玻璃棒未洗涤 D.溶解后没有冷却便进行定容
ⅰ. pH是描述溶液酸碱性的常用方法。常温下,pH=7的溶液呈中性,pH>7的溶液呈碱性,且
E.定容时俯视刻度线 F.摇匀后发现液面低于刻度线后未做处理
c(OH-)越大、pH越大、溶液的碱性越强。
ⅱ. pH<11.7时,I-能被O 氧化为I。
2 2
学科网(北京)股份有限公司 3ⅲ.一定碱性条件下,I 容易发生歧化反应,产物中氧化产物与还原产物的物质的量之比为1∶5。
2
①用离子方程式表达资料ⅲ中I 所发生反应的方程式: 。
2
②依据实验3,用离子方程式解释0.1mol/L KI溶液放置初期pH升高的原因: 。
③对比实验1和实验2,用离子方程式解释实验1中加稀硫酸后“溶液立即变蓝”的主要原因可能
....
是______。
④同学甲进一步设计实验验证分析的合理性。
序号 操作 现象
实验4 重复实验2操作后,继续向溶液中加入 。 溶液立即变蓝
(3)该组同学想进一步探究pH对I 发生歧化反应的影响,进行了如下实验。
2
实验5:用20mL4种不同浓度的KOH溶液与2mL淀粉溶液进行混合,测量混合液的pH后,向其中加
入2滴饱和碘水,观察现象。记录如下:
实验5 A B C D
pH 11.4 10.6 9.5 8.4
现象 无颜色变化 产生蓝色后瞬间消失 产生蓝色,30s后蓝色消失
①从实验5可以看出pH越大,歧化反应速率越_________(填“快”或“慢”)。
②从反应速率的角度解释pH=8.4时,“产生蓝色,30s后蓝色消失”的原因: 。
学科网(北京)股份有限公司 4参考答案
1-5CCDDB 6-10AADCB 11-15DBDCC 16-20BDDCB
21(14分)(1)④⑦⑩ ①②⑤⑥ ③⑧⑨ ③⑧⑨
(2)②③⑦⑩ (3)①和②,⑤和⑥ ⑪ ⑪
(4)BE(每空2分)
22(12分)(1)N (2分)
A
(2)Ca2 2ClO CO H OCaCO 2HClO(2分)
2 2 3
(3) ① 4.0(2分) ②7.5(2分) ③胶头滴管(1分) 500mL容量瓶(1分) ③ BDE(2分)
23(14分)(1) CuSO Na CO
4 2 3
(2)CO2- +2H+=CO ↑+H O
3 2 2
(3)Ba2++SO2- =BaSO ↓ (4) Cu2++Zn=Cu+Zn2+、Fe2++Zn=Zn2++Fe Fe2+、Zn2+(每空2)
4 4
24.(15分)
(1)I 或碘单质(2分)
2
(2)①3I 6OH IO 5I 3H O(2分)
2 3 2
②2H O4I O 2I 4OH(2分)
2 2 2
③IO 5I 6H 3H O3I (该反应的速度快)(2分)
3 2 2
④少量KIO 固体(2分)
3
(3)①快(2分)
②pH8.4时,同时发生反应:碘与淀粉变蓝和碘单质与氢氧化钾的歧化反应。
由于碘与淀粉变蓝反应快,所以先产生蓝色,随着歧化反应的进行,碘单质浓度降低,蓝色消失。(3分)
学科网(北京)股份有限公司 1