文档内容
2025 年秋季学期⾼⼆ 1 ⽉⽉考化学答
案 ⼀ 、单选题(每⼩题 3 分, 共 42 分)
1 . “ 嫦娥” 揽⽉ ,“ 天和” 驻空 ,“ 天问” 探⽕ ,“ 奋⽃者” 号探秘深海,我国科技事业
取 得巨⼤成就 。下列说法不正确的是
A. “ 嫦娥” 六号运载⽕箭的助推器采⽤液氧-煤油发动机 ,燃料燃烧时存在化学能到热能
的 转化
B. “ 天和” 核⼼舱 太阳能电池板主要成分是⼆氧化硅
C. “ 天问” ⼀号⽕星车使⽤的保温材料为纳⽶⽓凝胶, 具有丁达尔效应
D. “ 奋⽃者” 号潜⽔器含钛合⾦, 其强度⾼于纯钛⾦属
2. 下列图示或化学⽤语正确的是
A. HC10 的电⼦式:
B. 基态镁原⼦最外层电⼦的电⼦云轮廓图:
C. Ga 的价层电⼦排布:3d1
04s'4p' D. 中⼦数为 20 的钾原
⼦: K
3. 下列事实能证明MOH 是弱碱的有
① 0. Imo1.L'MOH 溶液可以使酚酞试液变红
0.In ol-L'o c(OH)<0.I mol-L'
②常温下 溶液中
,
③相同温度下 0. Imo1.L-'MOH 溶液的导电能⼒⽐0.I molL'NaoH 溶液的弱
,
④等体积的0. Imo1.L'MOH 溶液与0.1mo1. L" 盐酸恰好完全反应
A. ①② B. ②③ C. ②④ D. ③④
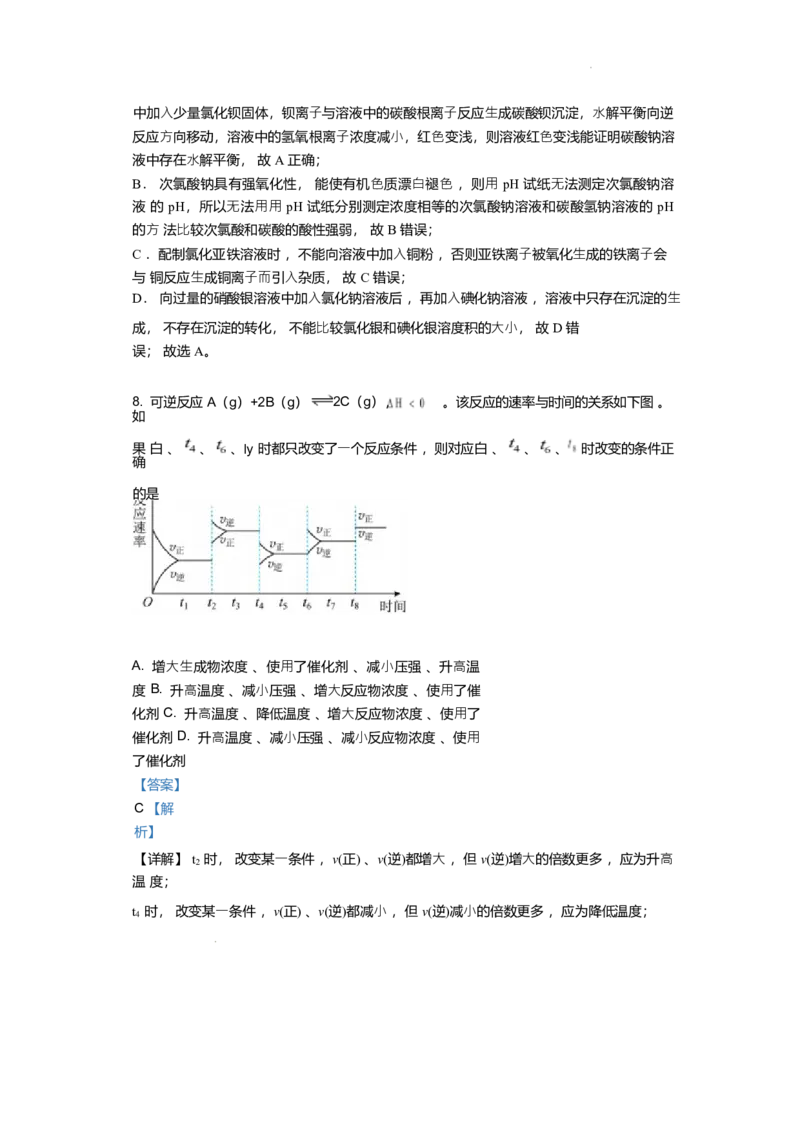
4. 在⼀定温度下,某反应达到了化学平衡,其反应过程对应的能量变化如图。下列说法正确
的是A. 为逆反应活化能, 为正反应活化能
AH=E'-E
B. 该反应为放热反应
,
C. 活化分⼦之间发⽣的碰撞⼀定是有效碰撞
D. 温度升⾼, 逆反应速率加快幅度⼤于正反应速率加快幅度 ,使平衡逆向移动
5. 10mL 浓度为l mo1/L 的盐酸和过量的锌反应 ,为减缓反应速率 ,⼜不影响⽣成氢⽓的
总 量, 可采⽤的⽅法是
A. 加⼊少量NaoH 溶液 B. 加⼊⼏滴CUC2溶液
C. 加⼊⼏滴NaNO; 溶液 D. 加⼊少量CH ;COON a 溶液
6.⽔凝结冰的过程中, 其烩变和熵变正确的是 ( )
A.ΔH>0,ΔS<0 B.ΔH<0,ΔS>0 C.ΔH>0,ΔS>0 D.ΔH<0, ΔS<0
7.下列实验能达到预期⽬的的是
选
实验内容 实验⽬的
项
向含有酚酞的Na, C0; 溶液中加⼊少 固体, 证明Na, CO; 溶液中存在
A
量 溶液红⾊变浅 ⽔ 解平衡
室温下 ,⽤ pH 试纸分别测定浓度相等的NacI O 溶 ⽐较HC10 与 H2CO3的酸
B
液 和 NaHCO;溶液的 pH 性 强弱
配制 溶液时, 先将 溶于适量浓盐酸中
抑制Fe* ⽔解, 并防⽌
C , 再⽤蒸馏⽔稀释到所需浓度, 最后在试剂瓶中加
Fe2* 被氧化
⼊少 量铜粉向盛有2mL0.0l mol/LAg NO;溶液的试管中滴加 2
证明在相同温度下
滴0.0Imo lIL NacI 溶液,有⽩⾊沉淀⽣成,再向其
D
K,(A gc1)>K,(A gl
中 滴加 2 滴0.0Imo lIL Nal 溶液 ,产⽣黄⾊沉淀
A. A B. B C. C D. D
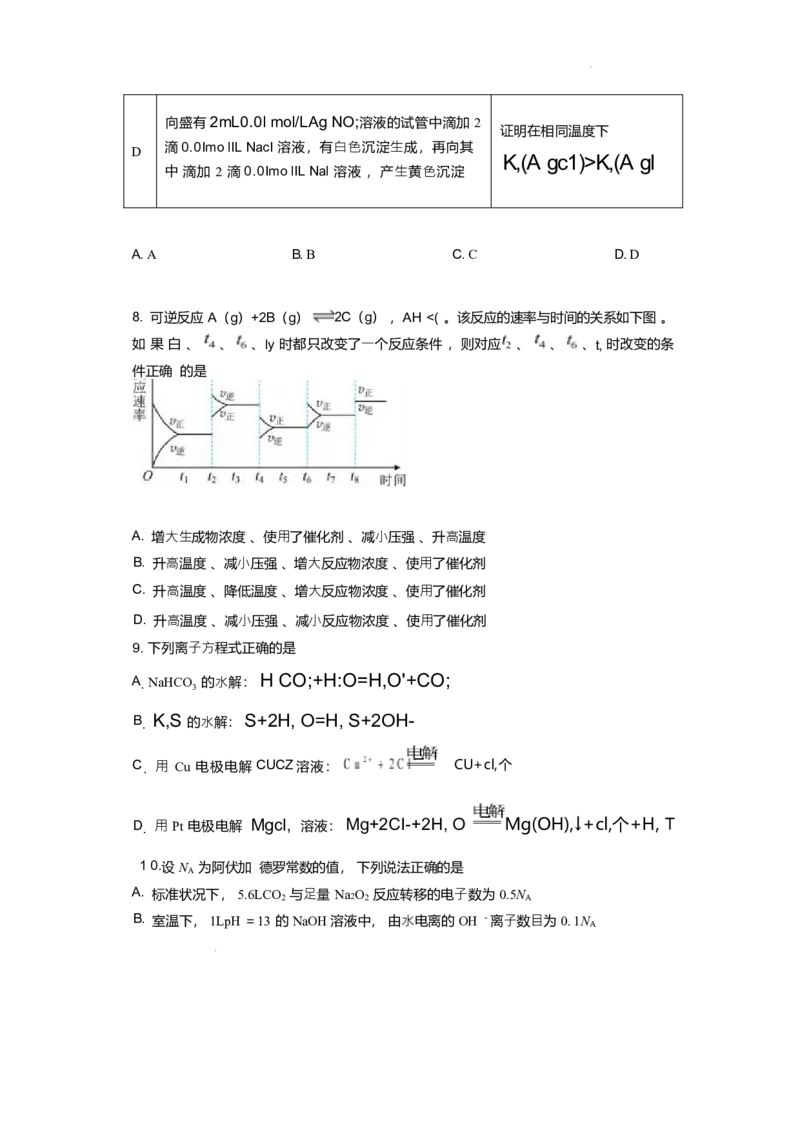
8. 可逆反应 A(g)+2B(g) 2C(g) ,AH <( 。该反应的速率与时间的关系如下图 。
如 果 白 、 、 、ly 时都只改变了⼀个反应条件 ,则对应 、 、 、t, 时改变的条
件正确 的是
A. 增⼤⽣成物浓度 、使⽤了催化剂 、减⼩压强 、升⾼温度
B. 升⾼温度 、减⼩压强 、增⼤反应物浓度 、使⽤了催化剂
C. 升⾼温度 、降低温度 、增⼤反应物浓度 、使⽤了催化剂
D. 升⾼温度 、减⼩压强 、减⼩反应物浓度 、使⽤了催化剂
9. 下列离⼦⽅程式正确的是
A. NaHCO 的⽔解: H CO;+H:O=H,O'+CO;
3
B. K,S 的⽔解: S+2H, O=H, S+2OH-
C. ⽤ Cu 电极电解CUCZ溶液: CU+cl,个
D. ⽤ Pt 电极电解 Mgcl, 溶液: Mg+2CI-+2H, O Mg(OH),↓+cl,个+H, T
1 0.设 N 为阿伏加 德罗常数的值, 下列说法正确的是
A
A. 标准状况下, 5.6LCO
2
与⾜量 Na2O
2
反应转移的电⼦数为 0.5N
A
B. 室温下, 1LpH =13 的 NaOH 溶液中, 由⽔电离的 OH -离⼦数⽬为 0. 1N
AC. 氢氧燃料电池正极消耗 22.4L(标准状况) ⽓体时, 电路中通过的电⼦数⽬为 2N
A
D. 2.0gH 18O 与 D O 的混合物中所含中⼦数为 N
2 2 A
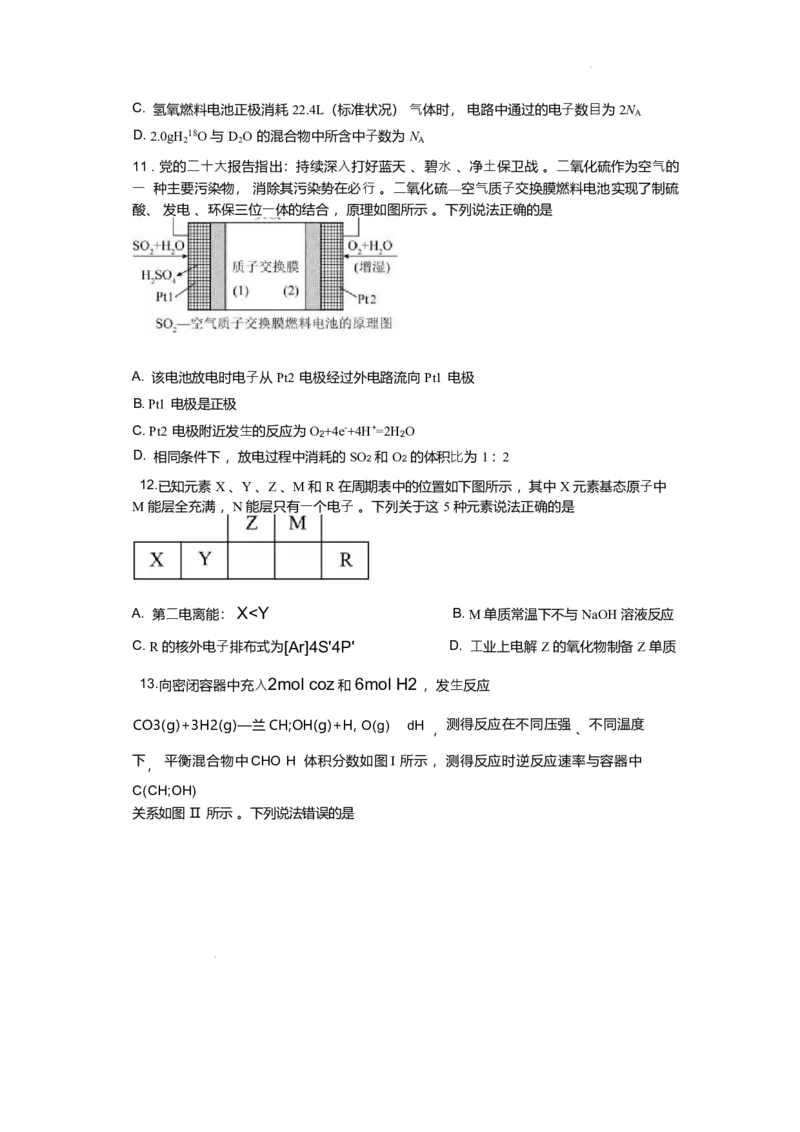
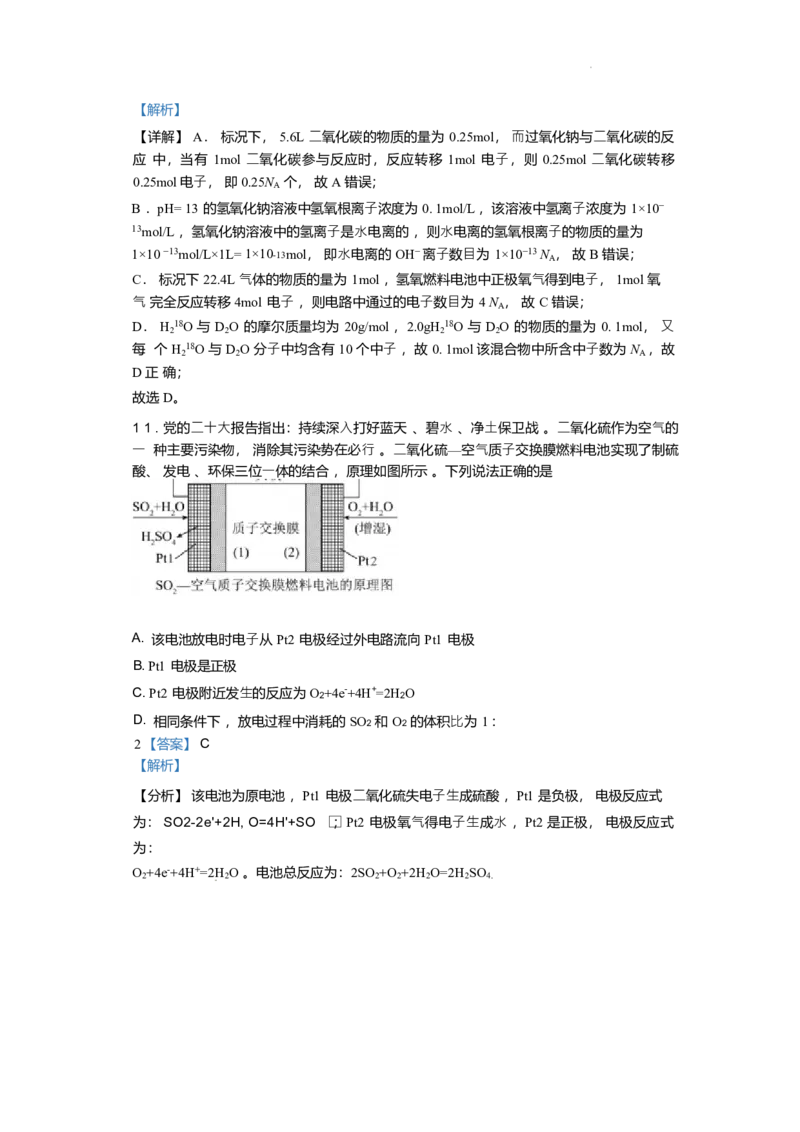
11 . 党的⼆⼗⼤报告指出:持续深⼊打好蓝天 、碧⽔ 、净⼟保卫战 。⼆氧化硫作为空⽓的
⼀ 种主要污染物, 消除其污染势在必⾏ 。⼆氧化硫—空⽓质⼦交换膜燃料电池实现了制硫
酸、 发电 、环保三位⼀体的结合 ,原理如图所示 。下列说法正确的是
A. 该电池放电时电⼦从 Pt2 电极经过外电路流向 Pt1 电极
B. Pt1 电极是正极
C. Pt2 电极附近发⽣的反应为 O 2 +4e-+4H+=2H 2 O
D. 相同条件下 ,放电过程中消耗的 SO2 和 O2 的体积⽐为 1 : 2
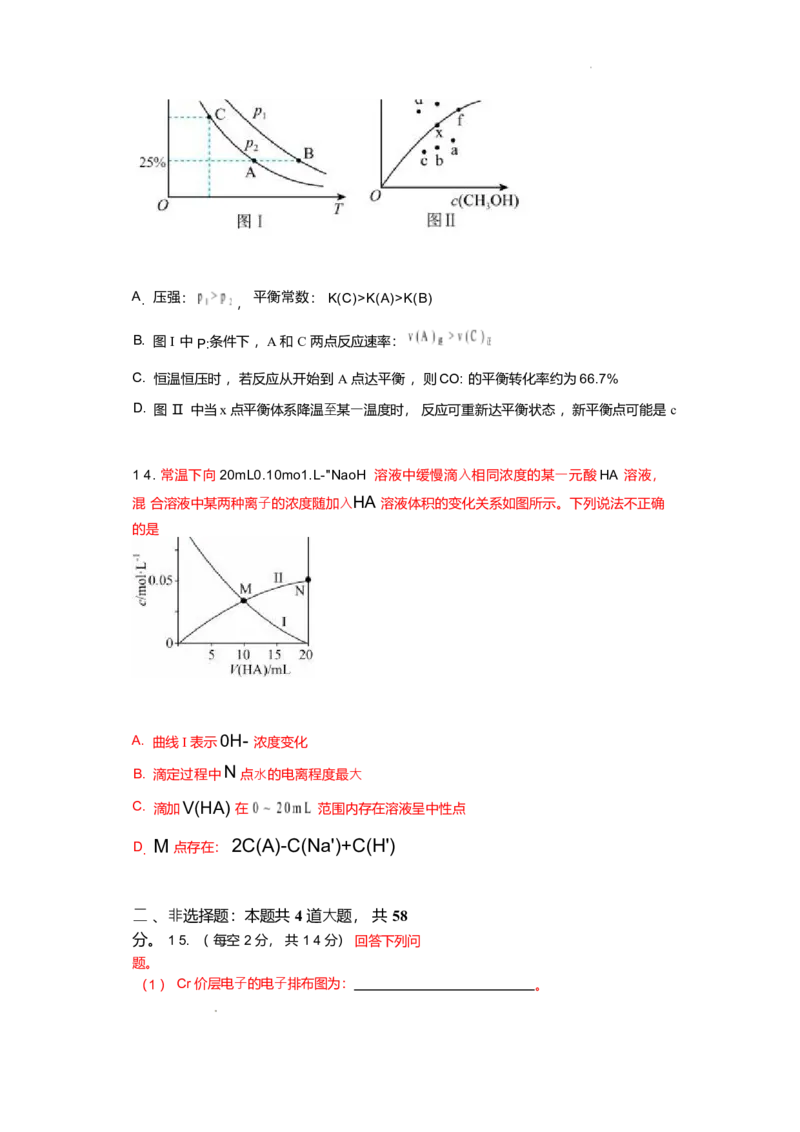
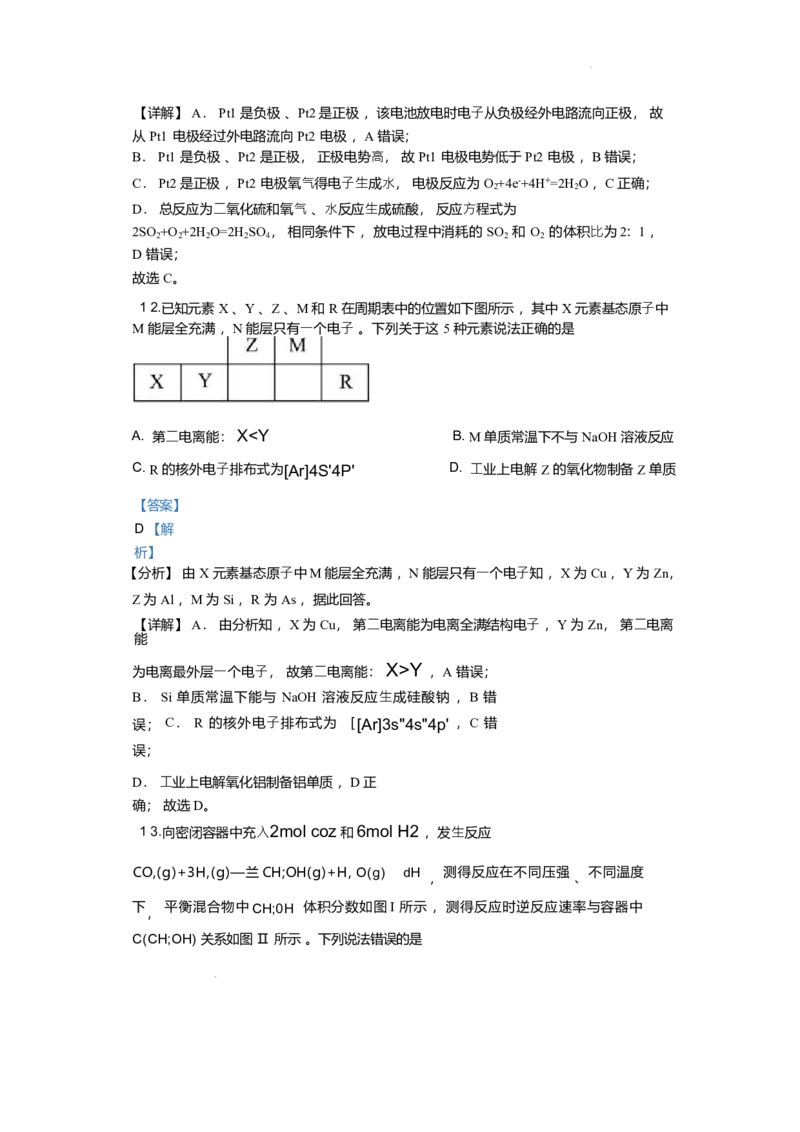
12.已知元素 X 、Y 、Z 、M 和 R 在周期表中的位置如下图所示 ,其中 X 元素基态原⼦中
M 能层全充满 ,N 能层只有⼀个电⼦ 。下列关于这 5 种元素说法正确的是
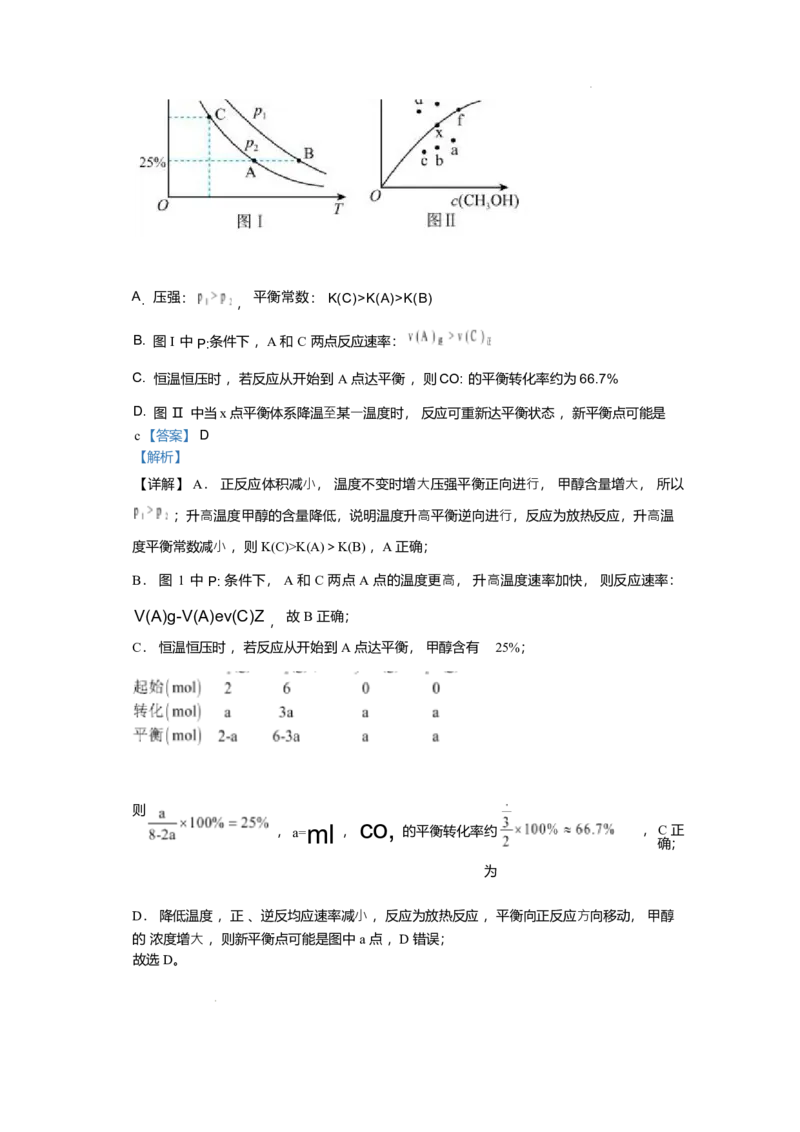
A. 第⼆电离能: XK(A)>K(B)
B. 图 I 中 P:条件下 ,A 和 C 两点反应速率:
C. 恒温恒压时 ,若反应从开始到 A 点达平衡 ,则CO: 的平衡转化率约为66.7%
D. 图 Ⅱ 中当x 点平衡体系降温⾄某⼀温度时, 反应可重新达平衡状态 ,新平衡点可能是 c
1 4. 常温下向20mL0.10mo1.L-"NaoH 溶液中缓慢滴⼊相同浓度的某⼀元酸HA 溶液,
混 合溶液中某两种离⼦的浓度随加⼊HA 溶液体积的变化关系如图所示。下列说法不正确
的是
A. 曲线 I 表示0H- 浓度变化
N
B. 滴定过程中 点⽔的电离程度最⼤
C. 滴加V(HA) 在 范围内存在溶液呈中性点
D. M 点存在: 2C(A)-C(Na')+C(H')
⼆ 、⾮选择题:本题共 4 道⼤题, 共 58
分。 1 5. ( 每空 2 分, 共 1 4 分) 回答下列问
题。
(1 ) Cr 价层电⼦的电⼦排布图为: 。(2)写出明矾溶液中溶质的电离⽅程式: ,⽤离⼦⽅程式表
示其溶液呈酸性的原因: 。
(3)SOCl (亚硫酰氯)是⼀种液态化合物, 沸点为 77℃ 。向盛有 10mL⽔的锥形瓶中⼩⼼
2
滴 加 8~10 滴 SOCl 2,可观察到剧烈反应, 液⾯上有⽩雾形成, 并有带刺激性⽓味的⽓体逸
出,
该⽓体中含有能使品红溶液褪⾊的 S0 2。轻轻振荡锥形瓶 ,待⽩雾消失后, 向溶液中滴加
AgNO 3 溶液 ,有不溶于稀硝酸的⽩⾊沉淀析出 。根据实验现象, 写出SOCl 2 与⽔反应的化
学
⽅程式 。
(4) ⾦属防护的⽅法有很多 ,右图是为了减缓海
⽔ 对钢闸⻔的腐蚀 。该电化学保护⽅法的名称是
_________________________。
(5) 已知:在 25℃ , 有关弱电解质的电离平衡常数如下表:
弱电解质 HC10
电离平衡常数 K,=4.7x10"
①将 通⼊氨⽔中, 当c(OH) 降⾄ 时, 溶液中的
__________。
②下列微粒在溶液中不能⼤量共存的是 。
A HC10 B c10- HCO; C HC10 HCO; D HS0;
. 、 . 、 . 、 . 、
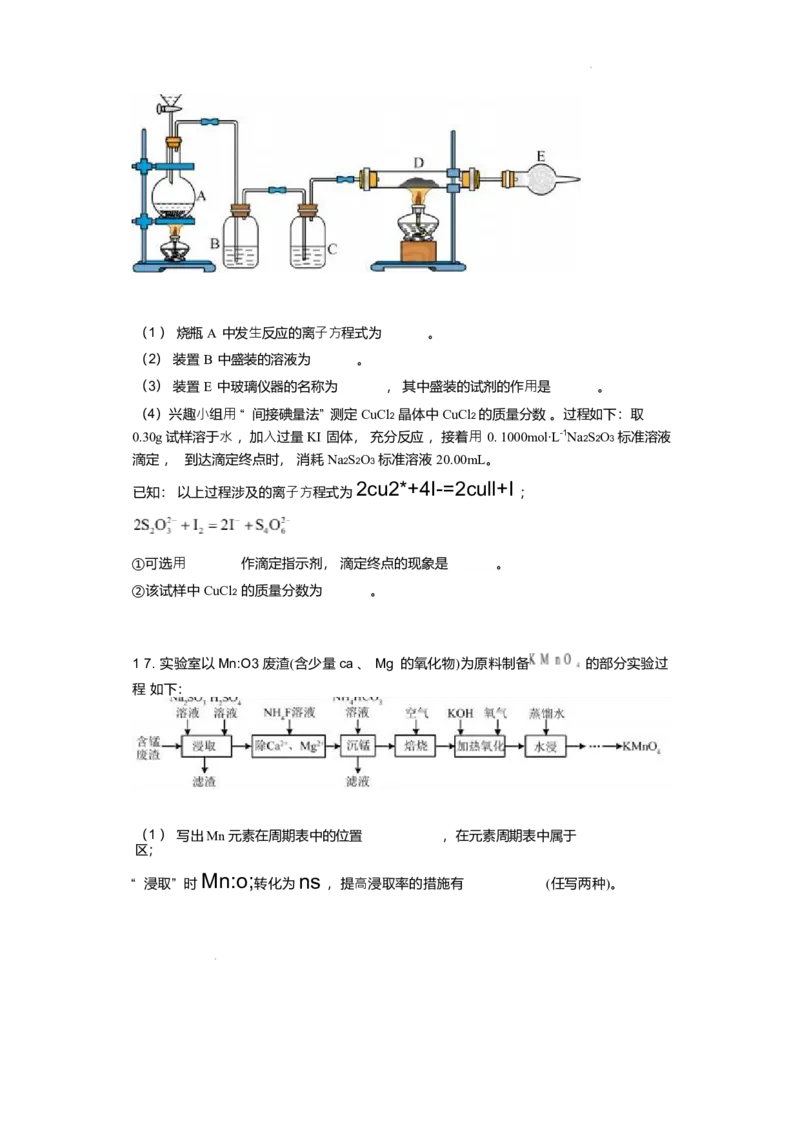
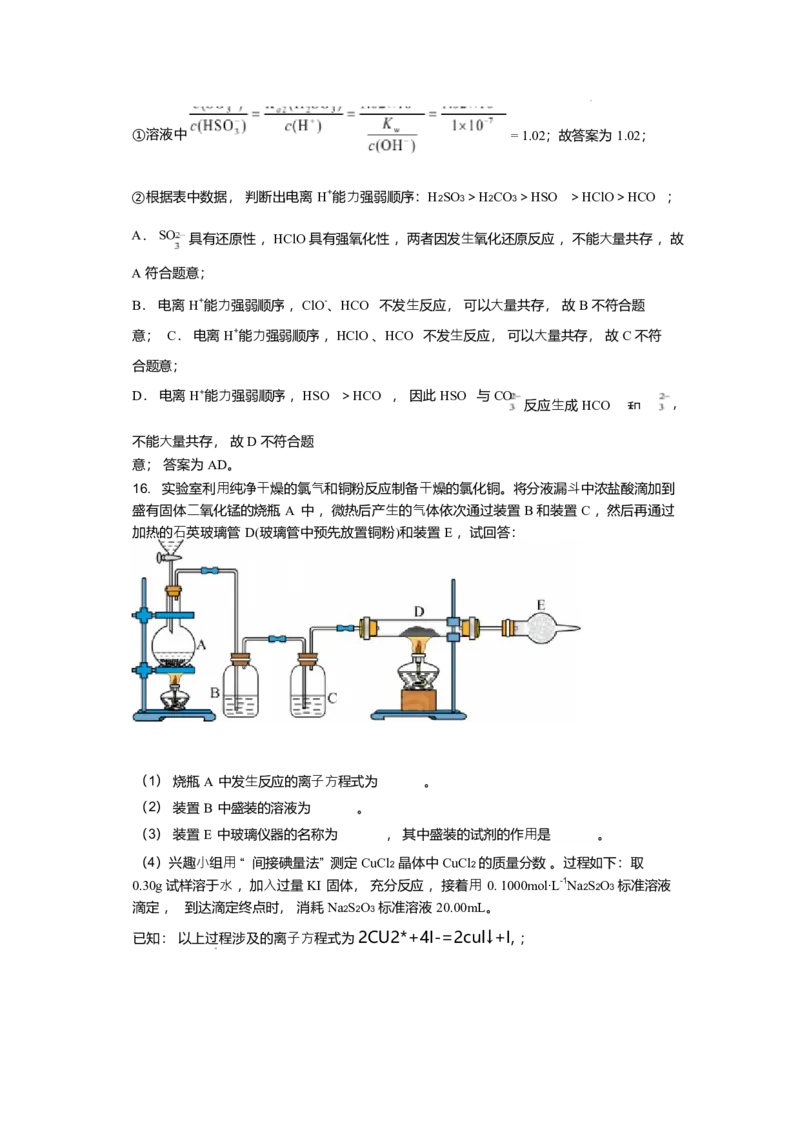
cO; 16. 实验室利⽤纯净⼲燥的氯⽓和铜粉反应制备⼲燥的氯化铜。将分液漏⽃中浓盐酸
滴加到 盛有固体⼆氧化锰的烧瓶 A 中 ,微热后产⽣的⽓体依次通过装置 B 和装置 C ,然
后再通过 加热的⽯英玻璃管 D(玻璃管中预先放置铜粉)和装置 E ,试回答:(1 ) 烧瓶 A 中发⽣反应的离⼦⽅程式为 。
(2) 装置 B 中盛装的溶液为 。
(3) 装置 E 中玻璃仪器的名称为 , 其中盛装的试剂的作⽤是 。
(4)兴趣⼩组⽤ “ 间接碘量法” 测定 CuCl2 晶体中 CuCl2 的质量分数 。过程如下:取
0.30g 试样溶于⽔ ,加⼊过量 KI 固体, 充分反应 ,接着⽤ 0. 1000mol∙L-1Na2S2O3 标准溶液
滴定 , 到达滴定终点时, 消耗 Na2S2O3 标准溶液 20.00mL。
2cu2*+4I-=2cull+I
已知: 以上过程涉及的离⼦⽅程式为 ;
①可选⽤ 作滴定指示剂, 滴定终点的现象是 。
②该试样中 CuCl2 的质量分数为 。
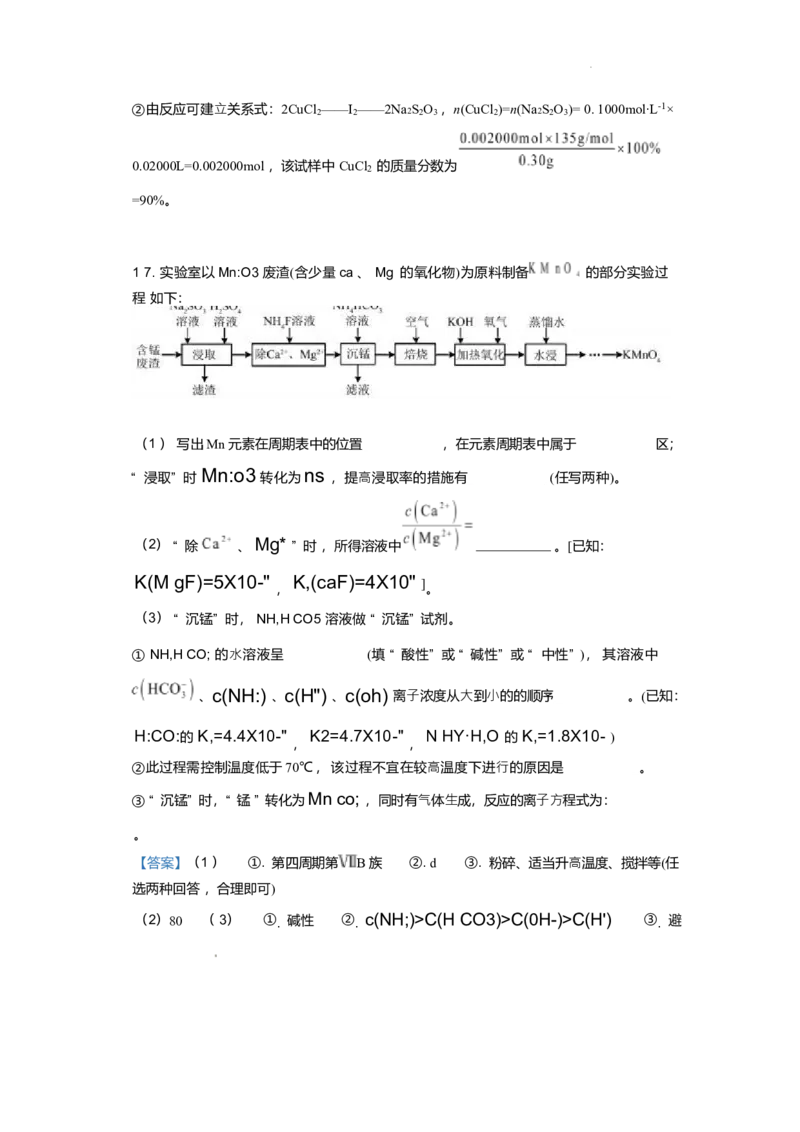
1 7. 实验室以Mn:O3废渣(含少量ca 、 Mg 的氧化物)为原料制备 的部分实验过
程 如下:
(1 ) 写出Mn 元素在周期表中的位置 ,在元素周期表中属于
区;
Mn:o; ns
“ 浸取” 时 转化为 ,提⾼浸取率的措施有 (任写两种)。(2) “ 除 、 Mg* ” 时 ,所得溶液中 __________ 。[已知:
K(M gF)=5X10-" K,,(caF)=4X10" ]
, 。
(3) “ 沉锰” 时, NH,H CO3 溶液做 “ 沉锰” 试剂。
① NH,H CO; 的⽔溶液呈 (填 “ 酸性” 或 “ 碱性” 或 “ 中性” ), 其溶液中
、c(NH:) 、c(H") 、c(oh) 离⼦浓度从⼤到⼩的的顺序 。(已知:
H:CO3的 K,=4.4X10-" K2=4.7X10-" N HY·H,O 的 K,=1.8X10- )
, ,
②此过程需控制温度低于70℃ , 该过程不宜在较⾼温度下进⾏的原因是 。
③ “ 沉锰” 时,“ 锰 ” 转化为Mn co; ,同时有⽓体⽣成,反应的离⼦⽅程式为:
。
18. 我国的能源以煤炭为主,燃煤烟⽓中s0: 、co 等有害⽓体的排放会污染环境,⽤ co
还 原脱除S0: 将其转化为单质硫 ,对⼯业⽣产具有重要的意义。
(1) cO 与 NO 的反应为2col g)+2NO(g)=2CO3(g)+N, lg)
AH 已知: 2co(g)+03(g)=2co2lg) AH,=-558KJ/mol
N lg)+o2lg)=2NO(g) AH=+180KJIm ol
则 AH =
(2)在某温度时 进⾏CO 还原脱除S0: : 2CO(g)+SO2lg)=2CO3(g)+S(g)
, 。
①若在刚性容器中进⾏, 下列说法⼀定能确定反应达到平衡状态的是 。
A v z(co)=2vg(s) B co 与 s0: 的浓度之⽐不再改变
. .
C. 容器内的压强不再改变 D. 的值不再改变
②若控制 进料⽐(物质的量)为 4:1 ,反应达平衡时,混合⽓体中so. 的体积分数为ss
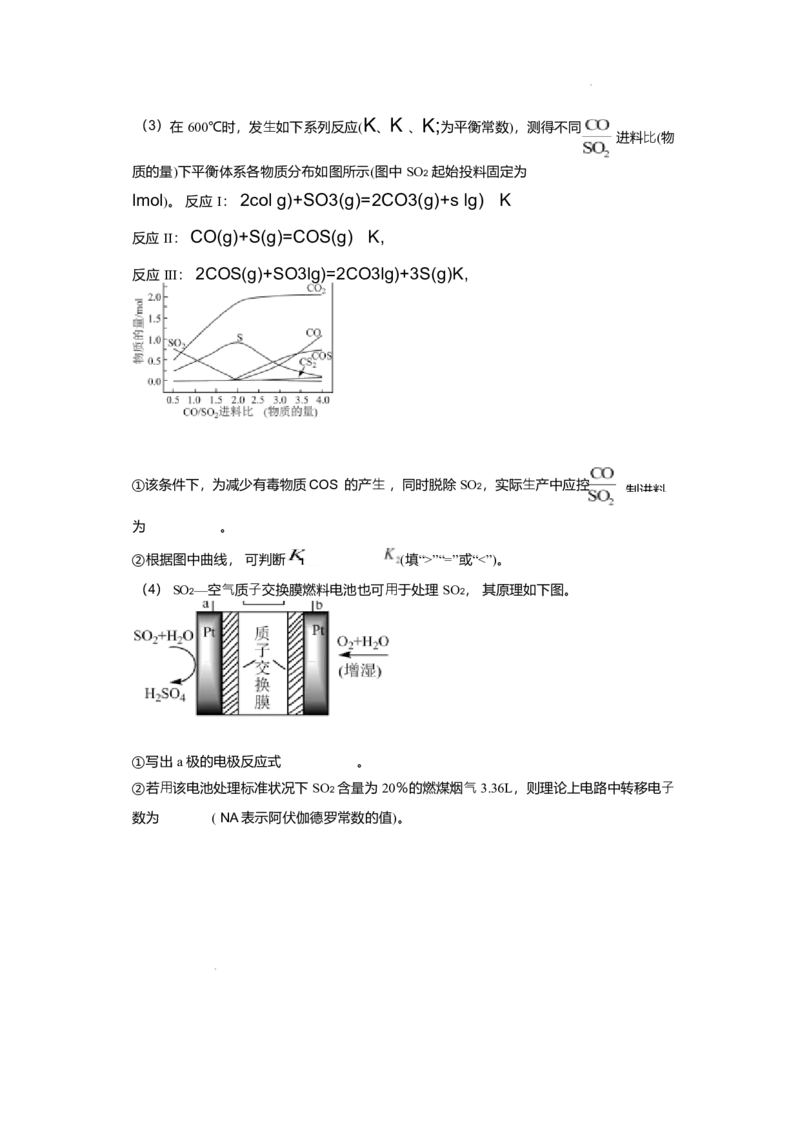
, 则该反应在此温度下的平衡常数为 。(3)在 600℃时,发⽣如下系列反应( K 、 K 、 K; 为平衡常数),测得不同
进料⽐(物
质的量)下平衡体系各物质分布如图所示(图中 SO2 起始投料固定为
lmol)。 反应 I: 2col g)+SO3(g)=2CO3(g)+s lg) K
反应 II: CO(g)+S(g)=COS(g) K,
反应 III: 2COS(g)+SO3lg)=2CO3lg)+3S(g)K,
①该条件下,为减少有毒物质COS 的产⽣ ,同时脱除 SO2,实际⽣产中应控
制进料
为 。
②根据图中曲线, 可判断 (填“>”“=”或“<”)。
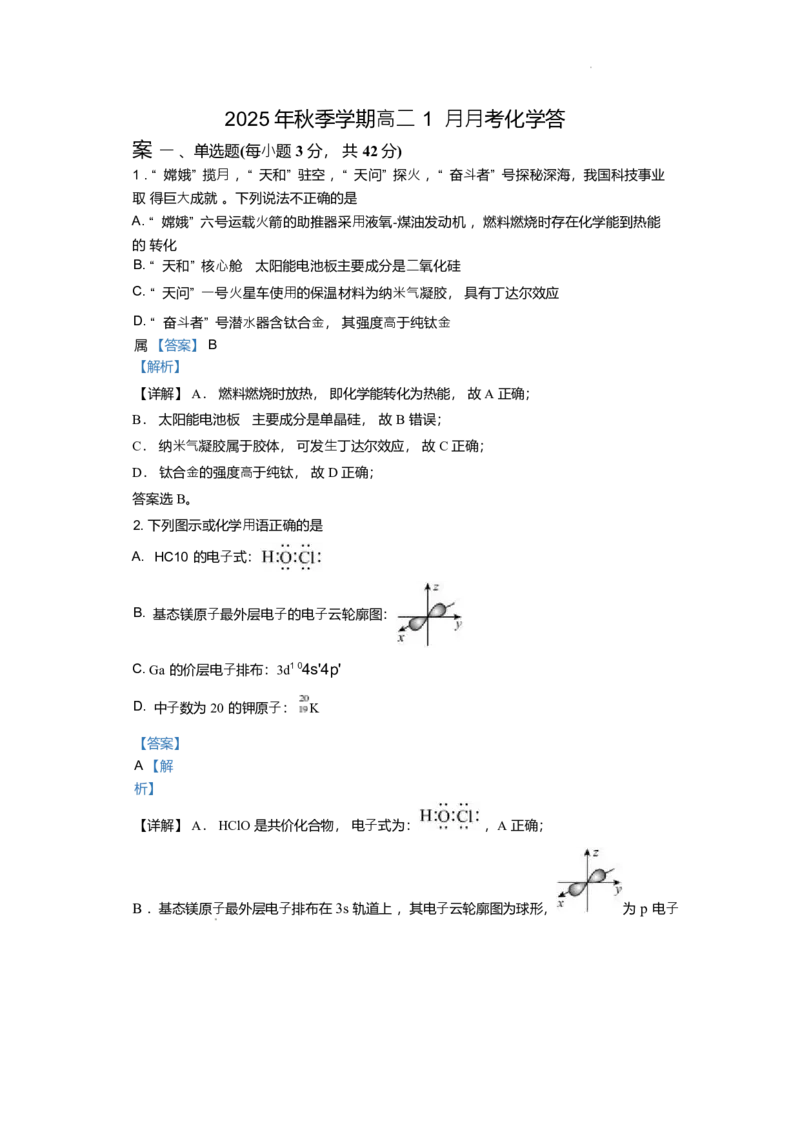
(4) SO2—空⽓质⼦交换膜燃料电池也可⽤于处理 SO2, 其原理如下图。
①写出 a 极的电极反应式 。
②若⽤该电池处理标准状况下 SO2 含量为 20%的燃煤烟⽓ 3.36L,则理论上电路中转移电⼦
数为 ( NA表示阿伏伽德罗常数的值)。2025 年秋季学期⾼⼆ 1 ⽉⽉考化学答
案 ⼀ 、单选题(每⼩题 3 分, 共 42 分)
1 . “ 嫦娥” 揽⽉ ,“ 天和” 驻空 ,“ 天问” 探⽕ ,“ 奋⽃者” 号探秘深海,我国科技事业
取 得巨⼤成就 。下列说法不正确的是
A. “ 嫦娥” 六号运载⽕箭的助推器采⽤液氧-煤油发动机 ,燃料燃烧时存在化学能到热能
的 转化
B. “ 天和” 核⼼舱 太阳能电池板主要成分是⼆氧化硅
C. “ 天问” ⼀号⽕星车使⽤的保温材料为纳⽶⽓凝胶, 具有丁达尔效应
D. “ 奋⽃者” 号潜⽔器含钛合⾦, 其强度⾼于纯钛⾦
属 【答案】 B
【解析】
【详解】 A. 燃料燃烧时放热, 即化学能转化为热能, 故 A 正确;
B. 太阳能电池板 主要成分是单晶硅, 故 B 错误;
C. 纳⽶⽓凝胶属于胶体, 可发⽣丁达尔效应, 故 C 正确;
D. 钛合⾦的强度⾼于纯钛, 故 D 正确;
答案选 B。
2. 下列图示或化学⽤语正确的是
A. HC10 的电⼦式:
B. 基态镁原⼦最外层电⼦的电⼦云轮廓图:
C. Ga 的价层电⼦排布:3d1 04s'4p'
D. 中⼦数为 20 的钾原⼦: K
【答案】
A 【解
析】
【详解】 A. HClO 是共价化合物, 电⼦式为: ,A 正确;
B .基态镁原⼦最外层电⼦排布在 3s 轨道上 ,其电⼦云轮廓图为球形, 为 p 电⼦云轮廓图 ,B 错误;
C. Ga 是 33 号元素 ,Ga 的价层电⼦排布式为: 4s24p' ,C 错误;
"K
D. 中⼦数为 20 的钾原⼦质量数为 20+19=39 ,表示为: ,D 错
误; 故选 A。
3. 下列事实能证明MOH 是弱碱的有
① 0. Imo1.L'MOH 溶液可以使酚酞试液变红
0.In ol-L'o c(0H)<0.I mol-L'
②常温下, 溶液中
③相同温度下 0.1mo1.L-'MOH 溶液的导电能⼒⽐0.I molL'NaoH 溶液的弱
,
④等体积的0.1mo1.L'MOH 溶液与0.I mal.L-' 盐酸恰好完全反应
A. ①② B. ②③ C. ②④ D. ③④
【答案】
B 【解
析】
【分析】
【详解】 ① 0. Imo1.L'MOH 溶液可以使酚酞试液变红 ,说明MOH 是碱, 不能说明
MOH
部分电离 ,则不能证明MOH 是弱碱;
②常温下 , 溶液中C(0H)<0.I mol-L' ,说明 MOH 部分电离,能证
明 MOH 为弱碱;
③相同温度下 0.1mo1.L-'MOH 溶液的导电能⼒⽐0.I molL'NaoH 溶液的弱
, ,
NaOH 是强碱 ,则 MOH 部分电离, 能证明MOH 为弱碱;
④等体积的0. Imo1.L-'MOH 溶液与0.1mo1.L-" 盐酸恰好完全反应 ,说明MOH 是⼀元碱,
不能说明MOH 部分电离 ,则不能证明MOH 是弱
碱; 综上所述 ,②③符合题意, 答案选 B。
4. 在⼀定温度下,某反应达到了化学平衡,其反应过程对应的能量变化如图。下列说法正确
的是A. 为逆反应活化能, 为正反应活化能
AH=E'-E
B. 该反应为放热反应
,
C. 活化分⼦之间发⽣的碰撞⼀定是有效碰撞
D. 温度升⾼, 逆反应速率加快幅度⼤于正反应速率加快幅度 ,使平衡逆向移
动 【答案】 D
【解析】
【详解】 A. 从图中可以看出, 为正反应活化能, 为逆反应活化能 ,A 不正确;
AH=E-E'
B .因为⽣成物的总能量⼩于反应物的总能量,所以该反应为放热反应 , ,
B 不正确;
C .活化分⼦是指能量⾜够可以发⽣有效碰撞的分⼦ ,但活化分⼦之间发⽣化学反应的碰撞
才是有效碰撞 ,C 不正确;
D .温度升⾼ ,对活化能⼤的反应更有利 ,则逆反应速率加快幅度⼤于正反应速率加快幅度,
平衡逆移 ,D 正
确; 故选:D。
5. 10mL 浓度为 l mol/L 的盐酸和过量的锌反应 ,为减缓反应速率 ,⼜不影响⽣成氢⽓的
总 量, 可采⽤的⽅法是
A. 加⼊少量NaoH 溶液 B. 加⼊⼏滴CU C1,溶液
C. 加⼊⼏滴NaNO; 溶液 D. 加⼊少量CH ;COON a 溶液
【答案】
D 【解
析】
【详解】 A .NaOH 与盐酸反应⽣成消耗氢离⼦, 降低氢离⼦浓度 ,反应速率减慢 ,⽣成
氢 ⽓的量减少 ,A 错误;B. CuCl 溶液与锌反应⽣成铜 ,锌 、铜 、盐酸构成原电池, 反应速率加快 ,B 错误;
2
C .NO 、H+与锌反应不产⽣氢⽓ ,C 错误;
D .CH COONa 溶液与盐酸相遇⽣成 CH COOH ,强酸变为弱酸 ,氢离⼦浓度减⼩ ,反应
3 3
速 率减慢 ,但是⽣成氢⽓的量不变 ,D 正确;
故选:D。
6.⽔凝结冰的过程中, 其烩变和熵变正确的是 ( )
A.ΔH>0,ΔS<0 B.ΔH<0,ΔS>0 C.ΔH>0,ΔS>0 D.ΔH<0, ΔS<0
【答案】 D
7.下列实验能达到预期⽬的的是
选
实验内容 实验⽬的
项
向含有酚酞的Na, C0; 溶液中加⼊少量BacI; 固 证明Na, C0; 溶液中存在
A
体, 溶液红⾊变浅 ⽔ 解平衡
室温下 ,⽤ pH 试纸分别测定浓度相等的NacI O 溶 ⽐较HC10 与 H2CO3的酸
B
液 和 NaHCO;溶液的 pH 性 强弱
配制Fec I; 溶液时, 先 溶于适量浓盐酸中,
将 抑制Fe* ⽔解, 并防⽌
C
再⽤蒸馏⽔稀释到所需浓度, 最后在试剂瓶中加⼊ Fe2* 被氧化
少 量铜粉
向盛有2mL0.0l mol/LAg NO3溶液的试管中滴加 2
证明在相同温度下
滴0.0Imo lIL NacI 溶液,有⽩⾊沉淀⽣成,再向其
D
K,(A gc1)>K,(A gl
中 滴加 2 滴0.0Imo lIL Nal 溶液 ,产⽣黄⾊沉淀
A. A B. B C. C D. D
【答案】
A 【解
析】
【详解】A .碳酸钠是强碱弱酸盐 ,在溶液中⽔解使溶液呈碱性, 向滴有酚酞的碳酸钠溶液中加⼊少量氯化钡固体,钡离⼦与溶液中的碳酸根离⼦反应⽣成碳酸钡沉淀,⽔解平衡向逆
反应⽅向移动,溶液中的氢氧根离⼦浓度减⼩,红⾊变浅,则溶液红⾊变浅能证明碳酸钠溶
液中存在⽔解平衡, 故 A 正确;
B. 次氯酸钠具有强氧化性, 能使有机⾊质漂⽩褪⾊ ,则⽤ pH 试纸⽆法测定次氯酸钠溶
液 的 pH,所以⽆法⽤⽤ pH 试纸分别测定浓度相等的次氯酸钠溶液和碳酸氢钠溶液的 pH
的⽅ 法⽐较次氯酸和碳酸的酸性强弱, 故 B 错误;
C .配制氯化亚铁溶液时 ,不能向溶液中加⼊铜粉 ,否则亚铁离⼦被氧化⽣成的铁离⼦会
与 铜反应⽣成铜离⼦⽽引⼊杂质, 故 C 错误;
D. 向过量的硝酸银溶液中加⼊氯化钠溶液后 ,再加⼊碘化钠溶液 ,溶液中只存在沉淀的⽣
成, 不存在沉淀的转化, 不能⽐较氯化银和碘化银溶度积的⼤⼩, 故 D 错
误; 故选 A。
8. 可逆反应 A(g)+2B(g) 2C(g), 。该反应的速率与时间的关系如下图 。
如
果 白 、 、 、ly 时都只改变了⼀个反应条件 ,则对应白 、 、 、 时改变的条件正
确
的是
A. 增⼤⽣成物浓度 、使⽤了催化剂 、减⼩压强 、升⾼温
度 B. 升⾼温度 、减⼩压强 、增⼤反应物浓度 、使⽤了催
化剂 C. 升⾼温度 、降低温度 、增⼤反应物浓度 、使⽤了
催化剂 D. 升⾼温度 、减⼩压强 、减⼩反应物浓度 、使⽤
了催化剂
【答案】
C 【解
析】
【详解】 t 时, 改变某⼀条件 ,v(正) 、v(逆)都增⼤ ,但 v(逆)增⼤的倍数更多 ,应为升⾼
2
温 度;
t 时, 改变某⼀条件 ,v(正) 、v(逆)都减⼩ ,但 v(逆)减⼩的倍数更多 ,应为降低温度;
4t 时, 改变某⼀条件 ,v(正)增⼤ 、v(逆)不变, 平衡正向移动 ,应为增⼤反应物的浓
6
度; t 时, 改变某⼀条件 ,v(正) 、v(逆)同等程度增⼤ ,但平衡不移动 ,应为使⽤了
8
催化剂;
综合以上分析 ,C 符合题意, 故选 C。
9. 下列离⼦⽅程式正确的是
A. NaHCO 的⽔解:
3
B. K;S 的⽔解: S+2H, O=H, S+2OH-
C. ⽤ Cu 电极电解 溶液: CU2t+2C I CU+cl,个
D. ⽤ Pt 电极电解 溶液: Mg+2CI-+2H, O Mg(OH),↓+cl,个+H,个
【答案】
D 【解
析】
【详解】 A NaHCO ⽔解的离⼦⽅程式为: H CO;+H, O=OH +(cid:1)H, CO; A 错
. 3 ,
误; B. K;S 中硫离⼦的⽔解是分步的, 其⽔解的⽅程式为: S"+H,0=HS'+OH-
,B 错 误;
C. 铜是活泼电极, 阳极铜失去电⼦, 阴极铜离⼦得到电⼦ ,C 错误;
D. ⽤ Pt 电极电解 MgcI Y 溶液, 阳极氯离⼦失去电⼦形成氯⽓, 阴极⽔电离的氢离⼦
得
Mg+2CI-+2H, O Mg(OH),↓+cl,个+H,个
到电⼦⽣成氢⽓ 总⽅程式为:
,
,
D 正
确; 故
选 D
10.设 N 为阿伏加 德罗常数的值, 下列说法正确的是
A
A. 标准状况下, 5.6LCO
2
与⾜量 Na2O
2
反应转移的电⼦数为 0.5N
A
B. 室温下, 1LpH =13 的 NaOH 溶液中, 由⽔电离的 OH -离⼦数⽬为 0. 1N
A
C. 氢氧燃料电池正极消耗 22.4L(标准状况) ⽓体时, 电路中通过的电⼦数⽬为 2N
A
D. 2.0gH 18O 与 D O 的混合物中所含中⼦数为 N
2 2 A
【答案】 D【解析】
【详解】 A. 标况下, 5.6L ⼆氧化碳的物质的量为 0.25mol, ⽽过氧化钠与⼆氧化碳的反
应 中,当有 1mol ⼆氧化碳参与反应时,反应转移 1mol 电⼦,则 0.25mol ⼆氧化碳转移
0.25mol 电⼦, 即 0.25N 个, 故 A 错误;
A
B .pH= 13 的氢氧化钠溶液中氢氧根离⼦浓度为 0. 1mol/L ,该溶液中氢离⼦浓度为 1×10−
13mol/L ,氢氧化钠溶液中的氢离⼦是⽔电离的 ,则⽔电离的氢氧根离⼦的物质的量为
1×10 −13mol/L×1L= 1×10-13mol, 即⽔电离的 OH− 离⼦数⽬为 1×10−13 N
A
, 故 B 错误;
C. 标况下 22.4L ⽓体的物质的量为 1mol ,氢氧燃料电池中正极氧⽓得到电⼦, 1mol 氧
⽓ 完全反应转移4mol 电⼦ ,则电路中通过的电⼦数⽬为 4 N , 故 C 错误;
A
D. H 18O 与 D O 的摩尔质量均为 20g/mol ,2.0gH 18O 与 D O 的物质的量为 0. 1mol, ⼜
2 2 2 2
每 个 H 18O 与 D O 分⼦中均含有 10 个中⼦ ,故 0. 1mol 该混合物中所含中⼦数为 N ,故
2 2 A
D 正 确;
故选 D。
1 1 . 党的⼆⼗⼤报告指出:持续深⼊打好蓝天 、碧⽔ 、净⼟保卫战 。⼆氧化硫作为空⽓的
⼀ 种主要污染物, 消除其污染势在必⾏ 。⼆氧化硫—空⽓质⼦交换膜燃料电池实现了制硫
酸、 发电 、环保三位⼀体的结合 ,原理如图所示 。下列说法正确的是
A. 该电池放电时电⼦从 Pt2 电极经过外电路流向 Pt1 电极
B. Pt1 电极是正极
C. Pt2 电极附近发⽣的反应为 O 2 +4e-+4H+=2H 2 O
D. 相同条件下 ,放电过程中消耗的 SO2 和 O2 的体积⽐为 1 :
2 【答案】 C
【解析】
【分析】 该电池为原电池 ,Pt1 电极⼆氧化硫失电⼦⽣成硫酸 ,Pt1 是负极, 电极反应式
为: SO2-2e'+2H, O=4H'+SO (cid:1) ; Pt2 电极氧⽓得电⼦⽣成⽔ ,Pt2 是正极, 电极反应式
为:
O +4e-+4H+=2H O 。电池总反应为:2SO +O +2H O=2H SO
2 2 2 2 2 2 4.【详解】 A. Pt1 是负极 、Pt2 是正极 ,该电池放电时电⼦从负极经外电路流向正极, 故
从 Pt1 电极经过外电路流向 Pt2 电极 ,A 错误;
B. Pt1 是负极 、Pt2 是正极, 正极电势⾼, 故 Pt1 电极电势低于 Pt2 电极 ,B 错误;
C. Pt2 是正极 ,Pt2 电极氧⽓得电⼦⽣成⽔, 电极反应为 O +4e-+4H+=2H O ,C 正确;
2 2
D. 总反应为⼆氧化硫和氧⽓ 、⽔反应⽣成硫酸, 反应⽅程式为
2SO +O +2H O=2H SO , 相同条件下 ,放电过程中消耗的 SO 和 O 的体积⽐为2: 1 ,
2 2 2 2 4 2 2
D 错误;
故选 C。
1 2.已知元素 X 、Y 、Z 、M 和 R 在周期表中的位置如下图所示 ,其中 X 元素基态原⼦中
M 能层全充满 ,N 能层只有⼀个电⼦ 。下列关于这 5 种元素说法正确的是
A. 第⼆电离能: XY
为电离最外层⼀个电⼦, 故第⼆电离能: ,A 错误;
B. Si 单质常温下能与 NaOH 溶液反应⽣成硅酸钠 ,B 错
误; C. R 的核外电⼦排布式为 [[Ar]3s"4s"4p' ,C 错
误;
D. ⼯业上电解氧化铝制备铝单质 ,D 正
确; 故选 D。
1 3.向密闭容器中充⼊2mol coz和6mol H2 ,发⽣反应
CO,(g)+3H,(g)—兰CH;OH(g)+H, O(g) dH 测得反应在不同压强 不同温度
, 、
下 平衡混合物中CH;0H 体积分数如图I 所示 ,测得反应时逆反应速率与容器中
,
C(CH;OH) 关系如图 Ⅱ 所示 。下列说法错误的是A. 压强:
,
平衡常数: K(C)>K(A)>K(B)
B. 图 I 中 P:条件下 ,A 和 C 两点反应速率:
C. 恒温恒压时 ,若反应从开始到 A 点达平衡 ,则CO: 的平衡转化率约为66.7%
D. 图 Ⅱ 中当x 点平衡体系降温⾄某⼀温度时, 反应可重新达平衡状态 ,新平衡点可能是
c 【答案】 D
【解析】
【详解】 A. 正反应体积减⼩, 温度不变时增⼤压强平衡正向进⾏, 甲醇含量增⼤, 所以
; 升⾼温度甲醇的含量降低,说明温度升⾼平衡逆向进⾏,反应为放热反应,升⾼温
度平衡常数减⼩ ,则 K(C)>K(A)>K(B) ,A 正确;
B. 图 1 中 P: 条件下, A 和 C 两点 A 点的温度更⾼, 升⾼温度速率加快, 则反应速率:
V(A)g-V(A)ev(C)Z 故 B 正确;
,
C. 恒温恒压时 ,若反应从开始到 A 点达平衡, 甲醇含有 25%;
则
co,
, a= ml , 的平衡转化率约 , C 正
确;
为
D. 降低温度 ,正 、逆反均应速率减⼩ ,反应为放热反应 ,平衡向正反应⽅向移动, 甲醇
的 浓度增⼤ ,则新平衡点可能是图中 a 点 ,D 错误;
故选 D。1 4. 常温下向20mL0.10mo1.L'NaoH 溶液中缓慢滴⼊相同浓度的某⼀元酸HA 溶液,
混 合溶液中某两种离⼦的浓度随加⼊HA 溶液体积的变化关系如图所示。下列说法不正确
的是
A. 曲线 I 表示0H- 浓度变化
B. 滴定过程中 N 点⽔的电离程度最⼤
C. 滴加V(HA) 在 ]~ 2)mL 范围内存在溶液呈中性点
D. M 点存在: 2e(A)-C(Na')
+C(H')
【答案】 C
【解析】
【详解】 A. 初始溶液为 NaOH,c(OH- )=0.1 0 mol/L, 随 HA 加⼊ ,OH-被中和, 浓度逐
渐降 低, 曲线 I 起点为 0.1 0 mol/L 且持续下降, 故曲线 I 表示 OH-浓度变化 ,A 正确;
B. N 点为 HA 体积 20 mL,此时 NaOH 与 HA 恰好完全反应⽣成 NaA,⽔的电离不受抑
制;
滴定过程中, NaOH 过量时 OH- 抑制⽔的电离, HA 过量时 H+ 抑制⽔的电离, 故 N 点⽔
的电 离程度最⼤, B 正确;
C. 0~20 mL 范围内, HA 不⾜, 溶液中始终有剩余 NaOH, 溶质为 NaOH 和 NaA, 溶液
呈碱 性, ⽆中性点, 故 0~20 mL 范围内不存在中性点 ,C错误;
D. M 点为曲线 I( OH-) 与曲线 II(A-) 交点, 即 c(OH-)=c(A-) 。根据电荷守
恒:c (Na+)+c(H+)=c(OH⁻)+c(A-) ,代⼊ c(OH- )=c(A- )得 2c(A-)=c(Na+)+c(H+), D
正确;
故答案选 C。
⼆ 、⾮选择题:本题共 4 道⼤题, 共 58
分。 1 5. ( 每空 2 分, 共 1 4 分) 回答下列问
题。
(1 ) Cr 价层电⼦的电⼦排布图为: 。(2)写出明矾溶液中溶质的电离⽅程式: ,⽤离⼦⽅程式表
示其溶液呈酸性的原因: 。
(3)SOCl (亚硫酰氯)是⼀种液态化合物, 沸点为 77℃ 。向盛有 10mL⽔的锥形瓶中⼩⼼
2
滴 加 8~10 滴 SOCl 2,可观察到剧烈反应, 液⾯上有⽩雾形成, 并有带刺激性⽓味的⽓体逸
出,
该⽓体中含有能使品红溶液褪⾊的 S0 2。轻轻振荡锥形瓶 ,待⽩雾消失后, 向溶液中滴加
AgNO 3 溶液 ,有不溶于稀硝酸的⽩⾊沉淀析出 。根据实验现象, 写出SOCl 2 与⽔反应的化
学
⽅程式 。
(4) ⾦属防护的⽅法有很多 ,右图是为了减缓海
⽔ 对钢闸⻔的腐蚀 。该电化学保护⽅法的名称是
_________________________。
(5) 已知:在 25℃ , 有关弱电解质的电离平衡常数如下表:
弱电解质 HC10
电离平衡常数 K,=4.7x10"
①将 通⼊氨⽔中, 当c(OH) 降⾄ 时, 溶液中的
__________。
②下列微粒在溶液中不能⼤量共存的是 。
A HC10 B c10- HCO; C HC10 HCO; D HS0; cO;
. 、 . 、 . 、 . 、
【答案】 ( 1)
(2) KAl ( SO ) =K+ +Al 3++2SO 2- Al3+ + 3H O = Al(OH)₃ +
4 2 4 2
3H+ (3)SOCl +H O=SO ↑ +2HCl
2 2 2
(4) 外加电流法
(5) ①. 10.2 ②. AD
【解析】
【⼩问 5 详解】①溶液中 = 1.02;故答案为 1.02;
②根据表中数据, 判断出电离 H+能⼒强弱顺序:H2SO3>H2CO3>HSO >HClO>HCO ;
A. SO 具有还原性 ,HClO 具有强氧化性 ,两者因发⽣氧化还原反应 ,不能⼤量共存 ,故
A 符合题意;
B. 电离 H+能⼒强弱顺序 ,ClO-、HCO 不发⽣反应, 可以⼤量共存, 故 B 不符合题
意; C. 电离 H+能⼒强弱顺序 ,HClO 、HCO 不发⽣反应, 可以⼤量共存, 故 C 不符
合题意;
D. 电离 H+能⼒强弱顺序 ,HSO >HCO , 因此 HSO 与 CO
反应⽣成 HCO 和 ,
不能⼤量共存, 故 D 不符合题
意; 答案为 AD。
16. 实验室利⽤纯净⼲燥的氯⽓和铜粉反应制备⼲燥的氯化铜。将分液漏⽃中浓盐酸滴加到
盛有固体⼆氧化锰的烧瓶 A 中 ,微热后产⽣的⽓体依次通过装置 B 和装置 C ,然后再通过
加热的⽯英玻璃管 D(玻璃管中预先放置铜粉)和装置 E ,试回答:
(1) 烧瓶 A 中发⽣反应的离⼦⽅程式为 。
(2) 装置 B 中盛装的溶液为 。
(3) 装置 E 中玻璃仪器的名称为 , 其中盛装的试剂的作⽤是 。
(4)兴趣⼩组⽤ “ 间接碘量法” 测定 CuCl2 晶体中 CuCl2 的质量分数 。过程如下:取
0.30g 试样溶于⽔ ,加⼊过量 KI 固体, 充分反应 ,接着⽤ 0. 1000mol∙L-1Na2S2O3 标准溶液
滴定 , 到达滴定终点时, 消耗 Na2S2O3 标准溶液 20.00mL。
已知: 以上过程涉及的离⼦⽅程式为2CU2*+4I-=2cul↓+I, ;①可选⽤ 作滴定指示剂, 滴定终点的现象是 。
②该试样中 CuCl2 的质量分数为 。
【答案】 ( 1 )
(2)饱和⻝盐⽔ ( 3) 球形⼲燥管 吸收未反应的氯⽓, 防⽌污染空⽓; 防⽌
空⽓中⽔蒸⽓等进⼊装置 D
(4) ①. 淀粉溶液 ②. 当滴⼊最后半滴 Na2S
2
O
3
标准溶液时,溶液由蓝⾊变为⽆⾊,
且在半分钟内不变⾊ ③. 90%
【解析】
【分析】将分液漏⽃中浓盐酸滴加到盛有固体⼆氧化锰的烧瓶 A 中 ,微热后产⽣ Cl ;由于
2
浓盐酸易挥发 ,制得的 Cl
2
中混有 HCl 和⽔蒸⽓;B 装置中盛有饱和⻝盐⽔ ,⽤于除去 Cl
2
中混有的 HCl;装置 C 中盛有浓硫酸 ,⽤于⼲燥 Cl ;装置 D 中铜粉与 Cl 反应制取
2 2
CuCl ; 装置 E 中的碱⽯灰⽤于吸收 Cl 尾⽓, 并防⽌空⽓中的⽔蒸⽓进⼊ D 装置。
2 2
【⼩问 1 详解】
烧瓶 A 中 ,MnO 与浓盐酸在加热条件下反应制取 Cl , 同时⽣成 MnCl 等 ,依据得失电
2 2 2
⼦ 恒 、电荷守恒和质量守恒, 可得出发⽣反应的离⼦⽅程式为
。
【⼩问 2 详解】
由分析可知 ,B 装置⽤于除去 Cl 中混有的 HCl ,则装置 B 中盛装的溶液为:饱和⻝盐
2
⽔。 【⼩问 3 详解】
Cl 是⼤⽓污染物, 需进⾏尾⽓处理 ,CuCl 易吸收⽔⽽⽣成⽔合物 。装置 E 中 ,玻璃仪
2 2
器 的名称为:球形⼲燥管 ,其中盛装的试剂的作⽤是:吸收未反应的氯⽓ ,防⽌污染空
⽓;防 ⽌空⽓中⽔蒸⽓等进⼊装置 D。
【⼩问4 详解】
①⽤ 0. 1000mol∙L-1Na2S
2
O
3
标准溶液滴定溶液中的 I
2
,起初溶液呈蓝⾊ ,I
2
全部被还原后
, 溶液呈⽆⾊ ,则选⽤淀粉溶液作滴定指示剂 ,滴定终点的现象是: 当滴⼊最后半滴
Na2S
2
O
3
标准溶液时, 溶液由蓝⾊变为⽆⾊, 且在半分钟内不变⾊ 。②由反应可建⽴关系式:2CuCl
2
——I
2
——2Na2S
2
O
3
,n(CuCl
2
)=n(Na2S
2
O
3
)= 0. 1000mol∙L-1×
0.02000L=0.002000mol ,该试样中 CuCl 的质量分数为
2
=90%。
1 7. 实验室以Mn:O3废渣(含少量ca 、 Mg 的氧化物)为原料制备 的部分实验过
程 如下:
(1 ) 写出Mn 元素在周期表中的位置 ,在元素周期表中属于 区;
Mn:o3 ns
“ 浸取” 时 转化为 ,提⾼浸取率的措施有 (任写两种)。
(2) “ 除 、 Mg* ” 时 ,所得溶液中 __________ 。[已知:
K(M gF)=5X10-" K,(caF)=4X10" ]
, 。
(3) “ 沉锰” 时, NH,H CO5 溶液做 “ 沉锰” 试剂。
① NH,H CO; 的⽔溶液呈 (填 “ 酸性” 或 “ 碱性” 或 “ 中性” ), 其溶液中
、c(NH:) 、c(H") 、c(oh) 离⼦浓度从⼤到⼩的的顺序 。(已知:
H:CO:的 K,=4.4X10-" K2=4.7X10-" N HY·H,O 的 K,=1.8X10- )
, ,
②此过程需控制温度低于70℃ , 该过程不宜在较⾼温度下进⾏的原因是 。
③ “ 沉锰” 时,“ 锰 ” 转化为Mn co; ,同时有⽓体⽣成,反应的离⼦⽅程式为:
。
【答案】(1 ) ①. 第四周期第 B 族 ②. d ③. 粉碎、适当升⾼温度、搅拌等(任
选两种回答 ,合理即可)
(2)80 ( 3) ①. 碱性 ②. c(NH;)>C(H CO3)>C(0H-)>C(H') ③. 避免碳酸氢铵温度过⾼分解 ④. Mn2"+2H CO;=Mn co;↓+CO, T+H,0
【解析】
【分析】 废渣( 含少量 Ca 、Mg 的氧化物) 加⼊ H2SO4 溶液和 Na2SO3 溶液浸取,
溶液中存在 Mn2+、Ca2+和 Mg2+, 加⼊ NH 4 F, 将 CaF 2 沉淀和 MgF 2 沉淀过滤除去, 加⼊
NH4HCO3 溶液将 Mn2+转化为 MnCO3,“焙烧” 时 ,MnCO3 ⽣成活性Mn303 ,“加热氧化”
时,
Mno3发⽣反应⽣成 KMnO4,⽔浸后经过⼀系列操作得到 KMnO4 固体, 以此解
答。 【⼩问 1 详解】
vl
Mn 元素原⼦序数是 25 ,在周期表中的位置第四周期第 B 族;在元素周期表中属于d 区;
“浸取” 时 转化为 ,提⾼浸取率的措施有粉碎 、适当升⾼温度 、搅拌等(任选两
种回答 ,合理即
可); 【⼩问 2 详
解】
“ 除 、 Mg* ”时,所得溶液中 =
=80;
【⼩问 3 详解】
① NH,H CO5 的⽔溶液存在铵根 、碳酸氢根的⽔解平衡, NH的⽔解常数为
, HCO; 的⽔解常数为 , 可知
HCO;⽔解程度更⼤ 溶液呈碱性;其溶液中 c(NH:) c(H") c(OH) 离
, 、 、 、
⼦浓度从⼤到⼩的的顺序: c(NH;)>C(H CO3)>C(0H-)>C(H') ;
②此过程需控制温度低于70℃ , 该过程不宜在较⾼温度下进⾏的原因是:碳酸氢铵温度
过 ⾼会分解;
③“沉锰” 时 ,“锰”转化为Mn co5 ,⽣成⼆氧化碳, 离⼦⽅程式为:
。
18. 我国的能源以煤炭为主,燃煤烟⽓中s0: 、co 等有害⽓体的排放会污染环境,⽤ co 还
原脱除S0: 将其转化为单质硫 ,对⼯业⽣产具有重要的意义。(1 ) cO 与 NO 的反应为 2CO(g)+2NO(g)=2col g)+N,(g)
AH 已知: 2CO(g)+O3(g)=2CO2lg) AH,=-558KJIm ol
N2lg)+o2lg)=2NO(g) AH,=+180KJIm ol
则 AH =
(2)在某温度时 进⾏CO 还原脱除S0: : 2CO(g)+SO03(g)=2cog)+s lg)
, 。
①若在刚性容器中进⾏, 下列说法⼀定能确定反应达到平衡状态的是 。
A v z(co)=2vg(s) B co 与 s0: 的浓度之⽐不再改变
. .
C. 容器内的压强不再改变 D. 的值不再改变
②若控制 进料⽐(物质的量)为4:1 ,反应达平衡时,混合⽓体中so. 的体积分数为5%
, 则该反应在此温度下的平衡常数为 。
(3)在 600℃时,发⽣如下系列反应( 、 、 为平衡常数),测得不同 进料⽐(物
质的量)下平衡体系各物质分布如图所示(图中 SO2 起始投料固定为
lmol)。 反应 I:
反应 II: CO(g)+S(g)=COS(g) K⃞K⃞(cid:1)
反应 III: 2COS(g)+SO3g)=2CO]g)+3S(g)K;
①该条件下,为减少有毒物质COS 的产⽣ ,同时脱除 SO2,实际⽣产中应控
制进料
为 。②根据图中曲线, 可判断 (填“>”“=”或“<”)。
(4) SO2—空⽓质⼦交换膜燃料电池也可⽤于处理 SO2, 其原理如下图。
①写出 a 极的电极反应式____________。
②若⽤该电池处理标准状况下 SO2 含量为 20%的燃煤烟⽓ 3.36L,则理论上电路中转移电⼦
数为______ ( NA表示阿伏伽德罗常数的值)。
【答案】 ( 1 ) -738KJ, moI'
(2) ①. AD ②. 1.08 或 27/25
(3) ①. 2.0 ②. >
(4) ①. SO2-2e'+2H2O=SO +(cid:1)4H' ②.
【解析】
【⼩问 1 详解】
将已知反应依次编号为①② , 由盖斯定律可知,反应①—②得到⼀氧化碳与⼀氧化氮的反
应, 则反应△H=(—558kJ/mol)—(+180kJ/mol)=—738 kJ/mol, 故答案为:—738 kJ/mol;
【⼩问 2 详解】
①A. v z(co)=2vg(s) 说明正逆反应速率相等, 反应已达到平衡, 故正确;
B.若⼀氧化碳与⼆氧化硫起始浓度之⽐为 2 :1 ,反应中浓度之⽐始终不变,则⼀氧化碳
与 ⼆氧化硫浓度之⽐不再改变不能说明正逆反应速率相等,⽆法判断反应是否达到平衡,
故错 误;
C .该反应是⽓体体积不变的反应 ,反应中容器内的压强始终不变 ,则容器内的压强不再
改 变不能说明正逆反应速率相等, ⽆法判断反应是否达到平衡, 故错误;
D. 反应中浓度熵 的值增⼤ ,则 的值不再改变说明正逆
反应速率相等, 反应已达到平衡, 故正确;故选AD;
②设容器的体积为 VL ,起始⼀氧化碳和⼆氧化硫的物质的量分别为4mol 和 1mol, 平衡
时 硫蒸⽓的物质的量为 amol, 由题意可建⽴如下三段式:
由⼆氧化硫的体积分数为 5%可得: × 100%=5% ,解得 a=0.75 ,则反应的平衡常数为
= 1.08, 故答案为:
1.08; 【⼩问 3 详解】
①由图可知, ⼀氧化碳与⼆氧化硫的进料⽐为 2 时, ⼆氧化碳和硫蒸⽓的物质的量⽐较⼤
, ⽽⼆氧化硫和 COS 的物质的量很⼩,所以为减少有毒物质 COS 的产⽣ ,同时脱除⼆氧化
硫, 实际⽣产中应控制⼀氧化碳与⼆氧化硫的进料⽐为 2.0, 故答案为:2.0;
②由图可知, ⼀氧化碳与⼆氧化硫的进料⽐为 2 时, ⼆氧化碳和硫蒸⽓的物质的量⽐较
⼤, ⽽⼀氧化碳和⼆氧化硫的物质的量很⼩ ,说明反应 I 的反应程度很⼤ ,平衡常数很⼤
,反应 II 的⽣成物 COS 的物质的量很⼩ ,说明反应的程度很⼩, 平衡常数很⼩ ,所以 K1
⼤于 K2,
故答案为:>;
【⼩问4 详解】
①由图可知 ,a 电极为燃料电池的负极 ,⽔分⼦作⽤下⼆氧化硫在负极失去电⼦发⽣氧化
反 应⽣成硫酸根离⼦和氢离⼦, 电极反应式为SO2-2e'+2H, O=SO +(cid:1)4H' , 故答案
为:
SO⃞O2-2e'+2H2O=SO⃞(cid:1)+4H' ;
②由化合价的变化控制 ,⽤该电池处理标准状况下⼆氧化硫含量为20%的燃煤烟⽓ 3.36L
时, 电路中转移电⼦数
× 2× NAmol—1=0.06NA, 故答案为:0.06NA。
为 18.