文档内容
高二化学试题(附中版) 第页(共8页)(这是边文,请据需要手工删加)
题 答 要 不 内 线 封 密
号位座____________ 号场考____________ 号 学____________ 名 姓
____________ 级 班____________ 级 年
(这是边文,请据需要手工删加)
湖南师大附中2024—2025学年度高二第一学期期末考试
化 学
时量:75分钟 满分:100分
得分:________
可能用到的相对原子质量:H~1 C~12 O~16 Na~23 Si~28 S~32 Cl~35.5 K~39 Ca
~40 Ti~48
Cu~64
一、选择题(本题包括14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合
题目要求的)
1.化学与科学技术、生产、生活密切相关。下列说法不正确的是
A.可用红外光谱仪测得未知物质的化学键或官能团
B. 明矾净水与自来水用漂白粉杀菌消毒的原理相同
C.医学上常采用硫酸钡作为“钡餐”,因为硫酸钡不会被盐酸溶解
D.TiO 广泛用于涂料、橡胶和造纸等工业,可通过TiCl 与水反应制备
2 4
2.下列有关化学用语表示正确的是
A.基态钠原子电子占据的最高能级的电子云轮廓图:
B.基态Fe2+的价层电子排布式为3d44s2
C.基态Ge原子的价层电子轨道表示式:
D.基态氟原子核外电子的运动状态有9种
3.用N 表示阿伏加德罗常数的值,下列叙述正确的是
A
A.6 g SiO 中含有0.1N 个SiO 分子
2 A 2
B.在0.1 mol/L Na S溶液中,c(H S)+c(HS-)+c(S2-)=0.1 mol/L
2 2
C.电解法精炼铜时,阳极质量减少32 g时,转移电子数一定为N
A
D.46 g乙醇中发生sp3杂化的原子数为2N
A
4.下列指定反应的离子方程式正确的是
A.用高锰酸钾标准溶液滴定草酸:2MnO +5C O +16H+===2Mn2++10CO↑+8HO
2 2 2
B.KI有助于I 溶于水:I+I- I
2 2
C.铅酸蓄电池充电时阴极的电极反应式:Pb2++2HO+2e-=== PbO +4H+
2 2
D.向Ca(ClO) 溶液通入少量SO :Ca2++2ClO-+SO +HO===CaSO ↓+2HClO
2 2 2 2 3
5.下列关于物质结构的说法正确的是
A.前四周期元素中基态原子的4s能级中只有1个电子的元素共有3种
B.PCl 分子的空间结构与它的VSEPR模型一致
3
C.O 分子中的共价键是极性键,中心氧原子呈负电性
3
D.HO的稳定性高,是因为水分子间存在氢键
2
6.类比是一种重要的学习方法,下列类比正确的是
A.电解熔融NaCl可制Na,则电解熔融AlCl 可制Al
3
B.Al3+与HCO 在溶液中可发生相互促进的水解反应生成沉淀和气体,则Fe3+与HCO 也
可以
C.Na在氧气中燃烧生成NaO,则Li在氧气中燃烧生成LiO
2 2 2 2
D.过量NaOH溶液与CuSO 溶液反应生成Cu(OH) 沉淀和NaSO ,则过量氨水与CuSO 溶液反应生
4 2 2 4 4
成Cu(OH) 沉淀和(NH )SO
2 4 2 4
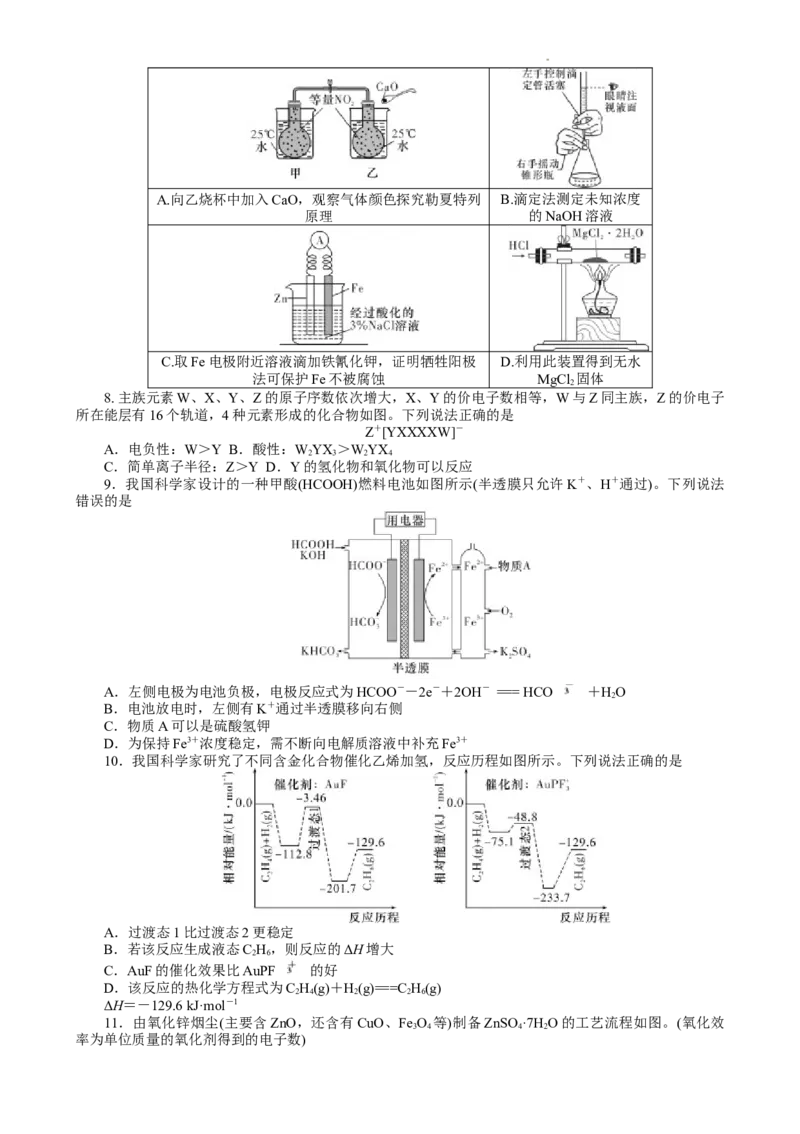
7.下列实验不能达到预期目的的是A.向乙烧杯中加入CaO,观察气体颜色探究勒夏特列 B.滴定法测定未知浓度
原理 的NaOH溶液
C.取Fe电极附近溶液滴加铁氰化钾,证明牺牲阳极 D.利用此装置得到无水
法可保护Fe不被腐蚀 MgCl 固体
2
8. 主族元素W、X、Y、Z的原子序数依次增大,X、Y的价电子数相等,W与Z同主族,Z的价电子
所在能层有16个轨道,4种元素形成的化合物如图。下列说法正确的是
Z+[YXXXXW]-
A.电负性:W>Y B.酸性:WYX >WYX
2 3 2 4
C.简单离子半径:Z>Y D.Y的氢化物和氧化物可以反应
9.我国科学家设计的一种甲酸(HCOOH)燃料电池如图所示(半透膜只允许K+、H+通过)。下列说法
错误的是
A.左侧电极为电池负极,电极反应式为HCOO--2e-+2OH- === HCO +HO
2
B.电池放电时,左侧有K+通过半透膜移向右侧
C.物质A可以是硫酸氢钾
D.为保持Fe3+浓度稳定,需不断向电解质溶液中补充Fe3+
10.我国科学家研究了不同含金化合物催化乙烯加氢,反应历程如图所示。下列说法正确的是
A.过渡态1比过渡态2更稳定
B.若该反应生成液态C H,则反应的ΔH增大
2 6
C.AuF的催化效果比AuPF 的好
D.该反应的热化学方程式为C H(g)+H(g)===C H(g)
2 4 2 2 6
ΔH=-129.6 kJ·mol-1
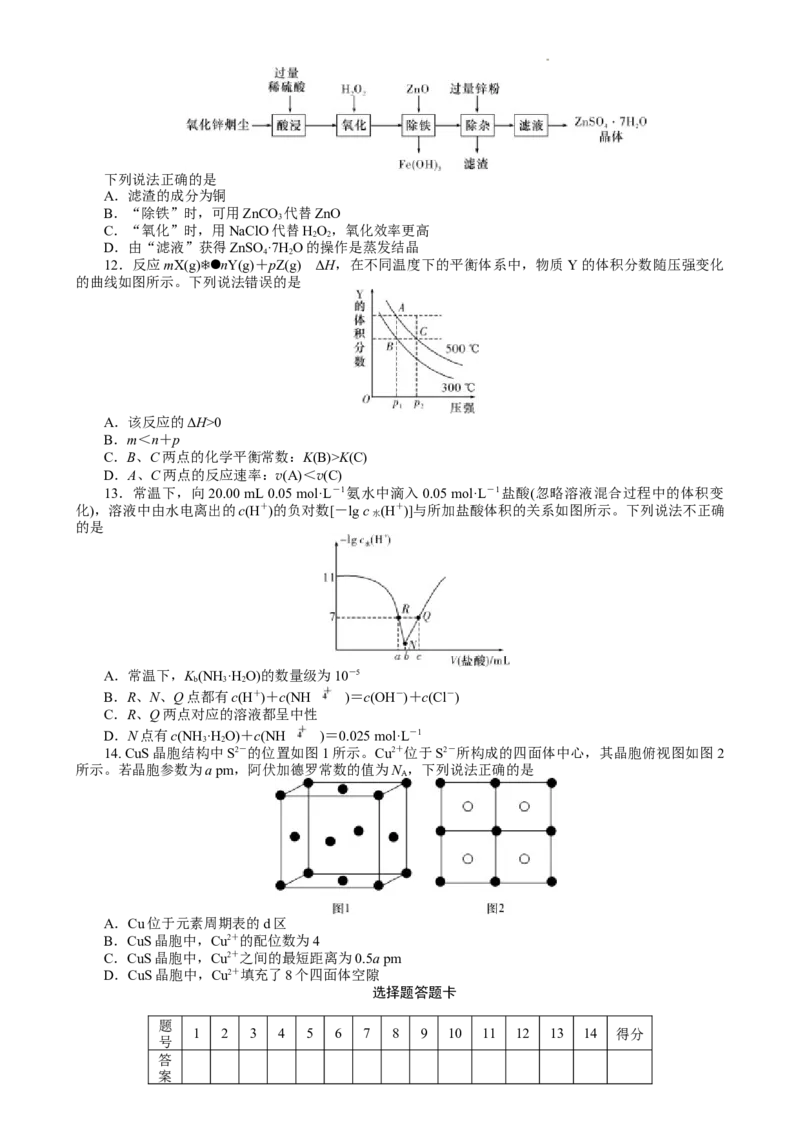
11.由氧化锌烟尘(主要含ZnO,还含有CuO、Fe O 等)制备ZnSO·7H O的工艺流程如图。(氧化效
3 4 4 2
率为单位质量的氧化剂得到的电子数)下列说法正确的是
A.滤渣的成分为铜
B.“除铁”时,可用ZnCO 代替ZnO
3
C.“氧化”时,用NaClO代替HO,氧化效率更高
2 2
D.由“滤液”获得ZnSO·7H O的操作是蒸发结晶
4 2
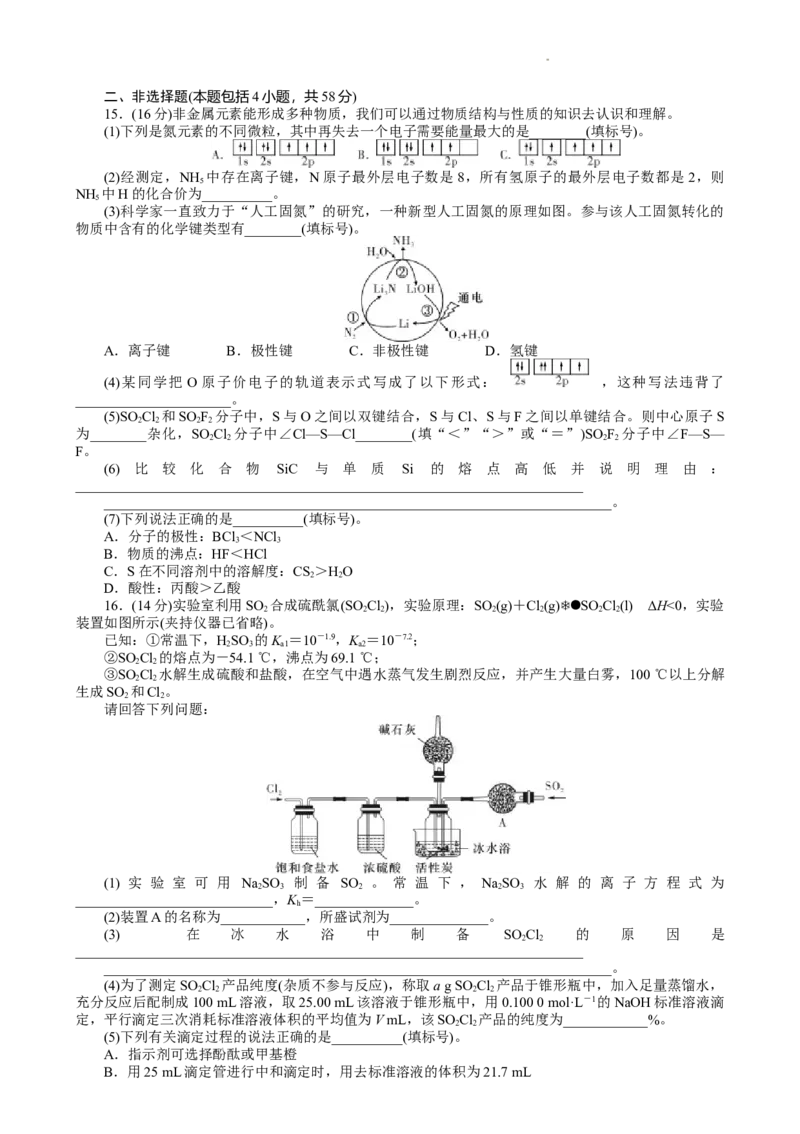
12.反应mX(g)nY(g)+pZ(g) ΔH,在不同温度下的平衡体系中,物质Y的体积分数随压强变化
的曲线如图所示。下列说法错误的是
A.该反应的ΔH>0
B.m<n+p
C.B、C两点的化学平衡常数:K(B)>K(C)
D.A、C两点的反应速率:v(A)<v(C)
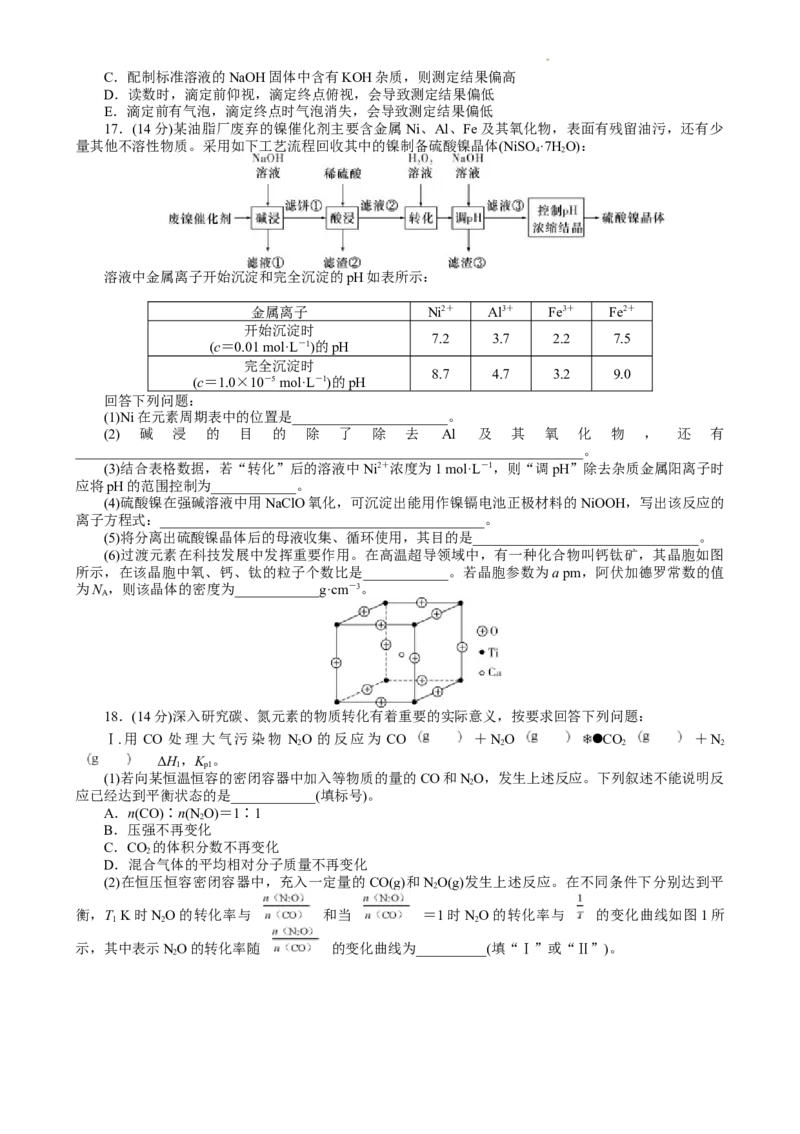
13.常温下,向20.00 mL 0.05 mol·L-1氨水中滴入0.05 mol·L-1盐酸(忽略溶液混合过程中的体积变
化),溶液中由水电离出的c(H+)的负对数[-lg c (H+)]与所加盐酸体积的关系如图所示。下列说法不正确
水
的是
A.常温下,K (NH ·H O)的数量级为10-5
b 3 2
B.R、N、Q点都有c(H+)+c(NH )=c(OH-)+c(Cl-)
C.R、Q两点对应的溶液都呈中性
D.N点有c(NH ·H O)+c(NH )=0.025 mol·L-1
3 2
14. CuS晶胞结构中S2-的位置如图1所示。Cu2+位于S2-所构成的四面体中心,其晶胞俯视图如图2
所示。若晶胞参数为a pm,阿伏加德罗常数的值为N ,下列说法正确的是
A
A.Cu位于元素周期表的d区
B.CuS晶胞中,Cu2+的配位数为4
C.CuS晶胞中,Cu2+之间的最短距离为0.5a pm
D.CuS晶胞中,Cu2+填充了8个四面体空隙
选择题答题卡
题
1 2 3 4 5 6 7 8 9 10 11 12 13 14 得分
号
答
案二、非选择题(本题包括4小题,共58分)
15.(16分)非金属元素能形成多种物质,我们可以通过物质结构与性质的知识去认识和理解。
(1)下列是氮元素的不同微粒,其中再失去一个电子需要能量最大的是________(填标号)。
(2)经测定,NH 中存在离子键,N原子最外层电子数是8,所有氢原子的最外层电子数都是 2,则
5
NH 中H的化合价为__________。
5
(3)科学家一直致力于“人工固氮”的研究,一种新型人工固氮的原理如图。参与该人工固氮转化的
物质中含有的化学键类型有________(填标号)。
A.离子键 B.极性键 C.非极性键 D.氢键
(4)某同学把 O 原子价电子的轨道表示式写成了以下形式: ,这种写法违背了
______________________。
(5)SO Cl 和SO F 分子中,S与O之间以双键结合,S与Cl、S与F之间以单键结合。则中心原子S
2 2 2 2
为________杂化,SO Cl 分子中∠Cl—S—Cl________(填“<”“>”或“=”)SO F 分子中∠F—S—
2 2 2 2
F。
(6) 比 较 化 合 物 SiC 与 单 质 Si 的 熔 点 高 低 并 说 明 理 由 :
________________________________________________________________________
________________________________________________________________________。
(7)下列说法正确的是__________(填标号)。
A.分子的极性:BCl <NCl
3 3
B.物质的沸点:HF<HCl
C.S在不同溶剂中的溶解度:CS>HO
2 2
D.酸性:丙酸>乙酸
16.(14分)实验室利用SO 合成硫酰氯(SO Cl),实验原理:SO (g)+Cl(g)SO Cl(l) ΔH<0,实验
2 2 2 2 2 2 2
装置如图所示(夹持仪器已省略)。
已知:①常温下,HSO 的K =10-1.9,K =10-7.2;
2 3 a1 a2
②SO Cl 的熔点为-54.1 ℃,沸点为69.1 ℃;
2 2
③SO Cl 水解生成硫酸和盐酸,在空气中遇水蒸气发生剧烈反应,并产生大量白雾,100 ℃以上分解
2 2
生成SO 和Cl。
2 2
请回答下列问题:
(1) 实 验 室 可 用 NaSO 制 备 SO 。 常 温 下 , NaSO 水 解 的 离 子 方 程 式 为
2 3 2 2 3
____________________________,K =______________。
h
(2)装置A的名称为____________,所盛试剂为______________。
(3) 在 冰 水 浴 中 制 备 SO Cl 的 原 因 是
2 2
________________________________________________________________________
________________________________________________________________________。
(4)为了测定SO Cl 产品纯度(杂质不参与反应),称取a g SO Cl 产品于锥形瓶中,加入足量蒸馏水,
2 2 2 2
充分反应后配制成100 mL溶液,取25.00 mL该溶液于锥形瓶中,用0.100 0 mol·L-1的NaOH标准溶液滴
定,平行滴定三次消耗标准溶液体积的平均值为V mL,该SO Cl 产品的纯度为____________%。
2 2
(5)下列有关滴定过程的说法正确的是__________(填标号)。
A.指示剂可选择酚酞或甲基橙
B.用25 mL滴定管进行中和滴定时,用去标准溶液的体积为21.7 mLC.配制标准溶液的NaOH固体中含有KOH杂质,则测定结果偏高
D.读数时,滴定前仰视,滴定终点俯视,会导致测定结果偏低
E.滴定前有气泡,滴定终点时气泡消失,会导致测定结果偏低
17.(14分)某油脂厂废弃的镍催化剂主要含金属Ni、Al、Fe及其氧化物,表面有残留油污,还有少
量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO ·7H O):
4 2
溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
金属离子 Ni2+ Al3+ Fe3+ Fe2+
开始沉淀时
7.2 3.7 2.2 7.5
(c=0.01 mol·L-1)的pH
完全沉淀时
8.7 4.7 3.2 9.0
(c=1.0×10-5 mol·L-1)的pH
回答下列问题:
(1)Ni在元素周期表中的位置是______________________。
(2) 碱 浸 的 目 的 除 了 除 去 Al 及 其 氧 化 物 , 还 有
________________________________________________________________________。
(3)结合表格数据,若“转化”后的溶液中Ni2+浓度为1 mol·L-1,则“调pH”除去杂质金属阳离子时
应将pH的范围控制为____________。
(4)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH,写出该反应的
离子方程式:______________________________________________。
(5)将分离出硫酸镍晶体后的母液收集、循环使用,其目的是________________________________。
(6)过渡元素在科技发展中发挥重要作用。在高温超导领域中,有一种化合物叫钙钛矿,其晶胞如图
所示,在该晶胞中氧、钙、钛的粒子个数比是____________。若晶胞参数为a pm,阿伏加德罗常数的值
为N ,则该晶体的密度为____________g·cm-3。
A
18.(14分)深入研究碳、氮元素的物质转化有着重要的实际意义,按要求回答下列问题:
Ⅰ.用 CO 处理大气污染物 NO 的反应为 CO +NO CO +N
2 2 2 2
ΔH,K 。
1 p1
(1)若向某恒温恒容的密闭容器中加入等物质的量的CO和NO,发生上述反应。下列叙述不能说明反
2
应已经达到平衡状态的是____________(填标号)。
A.n(CO)∶n(N O)=1∶1
2
B.压强不再变化
C.CO 的体积分数不再变化
2
D.混合气体的平均相对分子质量不再变化
(2)在恒压恒容密闭容器中,充入一定量的CO(g)和NO(g)发生上述反应。在不同条件下分别达到平
2
衡,T K时NO的转化率与 和当 =1时NO的转化率与 的变化曲线如图1所
1 2 2
示,其中表示NO的转化率随 的变化曲线为__________(填“Ⅰ”或“Ⅱ”)。
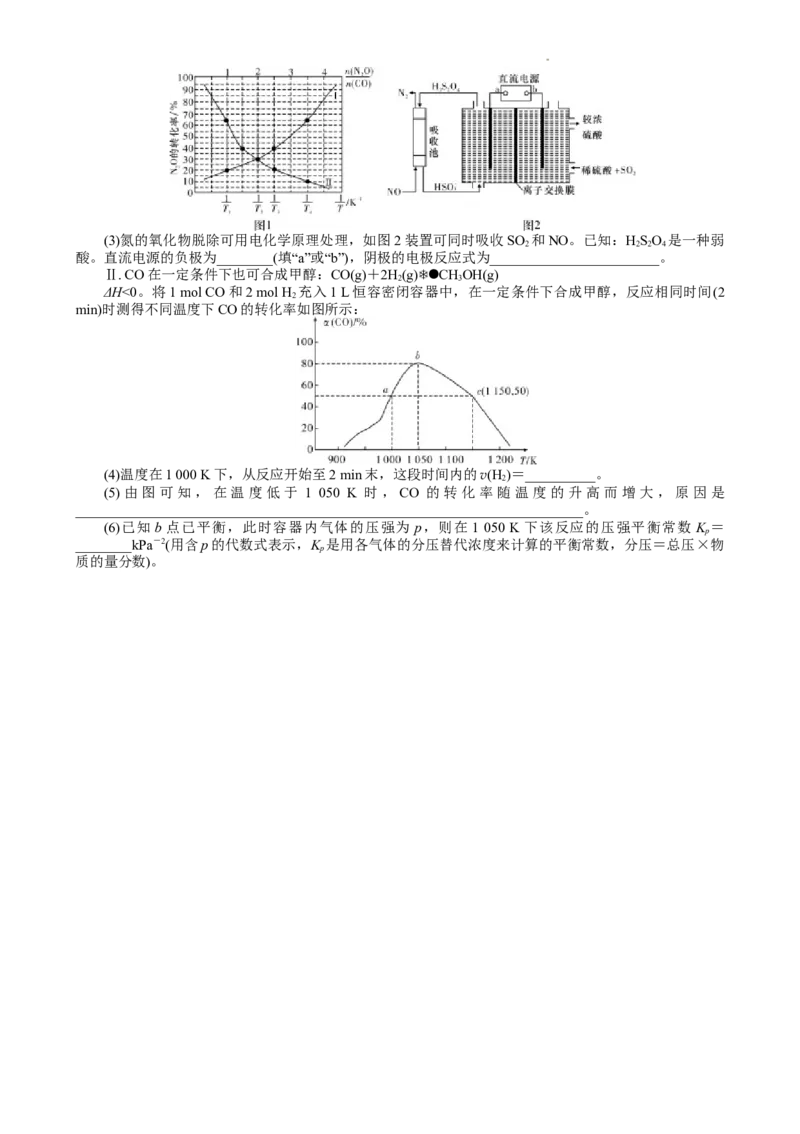
2(3)氮的氧化物脱除可用电化学原理处理,如图2装置可同时吸收SO 和NO。已知:HSO 是一种弱
2 2 2 4
酸。直流电源的负极为________(填“a”或“b”),阴极的电极反应式为________________________。
Ⅱ. CO在一定条件下也可合成甲醇:CO(g)+2H(g)CHOH(g)
2 3
ΔH<0。将1 mol CO和2 mol H 充入1 L恒容密闭容器中,在一定条件下合成甲醇,反应相同时间(2
2
min)时测得不同温度下CO的转化率如图所示:
(4)温度在1 000 K下,从反应开始至2 min末,这段时间内的v(H )=__________。
2
(5)由图可知,在温度低于 1 050 K 时,CO 的转化率随温度的升高而增大,原因是
________________________________________________________________________。
(6)已知 b点已平衡,此时容器内气体的压强为 p,则在 1 050 K 下该反应的压强平衡常数 K =
p
________kPa-2(用含p的代数式表示,K 是用各气体的分压替代浓度来计算的平衡常数,分压=总压×物
p
质的量分数)。