文档内容
2024-2025 学年下学期高二第一次月考卷
化 学
可能用到的相对原子质量:H∶1 C∶12 N∶14 O∶16 Na∶23 S∶32 Cl∶35.5
K∶39
一、单选题(每题3分,共42分)
1.下列有关化学用语表示错误的是( )
A.氯气的共价键电子云轮廓图:
B.二氧化硅的分子式为SiO
2
C.N H 的电子式:
2 4
D.基态氧原子电子轨道表示式为:
2.CH COOH与CH COONa等物质的量混合配制成的稀溶液,pH=4.7,下列说
3 3
法或离子浓度关系正确的是( )
A.CH COONa的水解程度大于CH COOH的电离程度
3 3
B.CH COONa的存在抑制了CH COOH的电离
3 3
C.c(CH COO-)>c(Na+)>c(OH-)>c(H+)
3
D.c(CH COO-)+c(OH-)CCl COOH CF COOH的羧基中O—H的极性更大
3 3 3
B 熔点:SiO >CO 相对分子质量:SiO 大于CO
2 2 2 2
C O 与O 分子极性相同 二者都是由非极性键构成的分子
2 3
D 沸点:对羟基苯甲醛>邻羟 对羟基苯甲醛分子间范德华力更强基苯甲醛
7.下列关于化学键和分子间作用力的说法中正确的个数是( )
①含有金属元素的化合物一定是离子化合物
②第IA族和第ⅦA族原子化合时,一定形成离子键
③由非金属元素形成的化合物一定是共价化合物
④物质中一定存在化学键
⑤含有离子键的化合物一定是离子化合物
⑥冰的密度比水小,是因为水分子之间存在氢键
⑦CO 溶于水和干冰升华都只有分子间作用力的改变
2
⑧纯碱和烧碱熔化时克服的化学键类型相同
A.2个 B.3个 C.4个 D.5个
8.由徐光宪院士发起院士学子同创的《分子共和国》科普读物生动形象地戏说
了 、 、 、 、 等众多“分子共和国”中的明星。下
列说法错误的是( )
A.第一电离能大小:C<O<N
B.分子的极性:
C.键能N—N>P—P、N—H>P—H,因此 的沸点大于 的沸点
D.酸性:
9.下列说法中,正确的是( )
A. 空间结构为正四面体形,与VSEPR模型一致
B.离子晶体中不可能存在共价键
C.共价键和氢键都是化学键,且都具有饱和性和方向性
D.通过X射线衍射实验难以区分玻璃和水晶
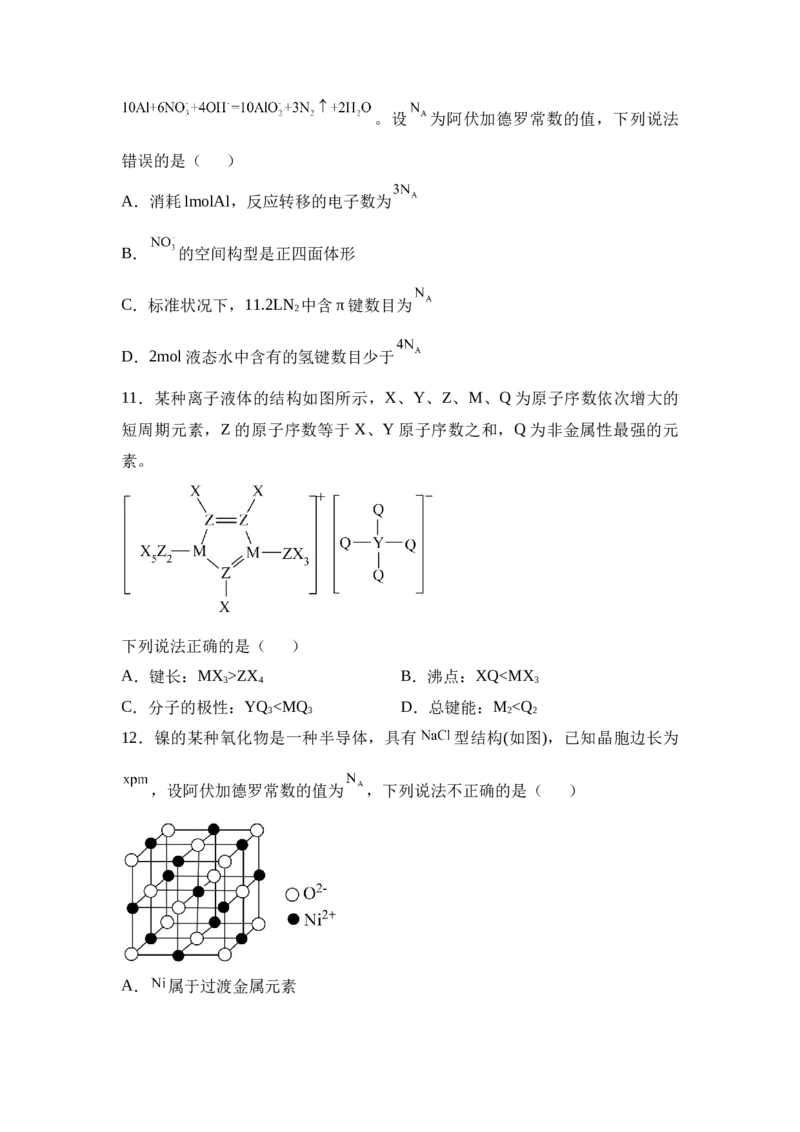
10.饮用水中的 对人类健康会产生危害,为了降低饮用水中 的浓度,
可 以 在 碱 性 条 件 下 用 铝 粉 将 还 原 为 N , 反 应 的 离 子 方 程 式 为
2。设 为阿伏加德罗常数的值,下列说法
错误的是( )
A.消耗lmolAl,反应转移的电子数为
B. 的空间构型是正四面体形
C.标准状况下,11.2LN 中含π键数目为
2
D.2mol液态水中含有的氢键数目少于
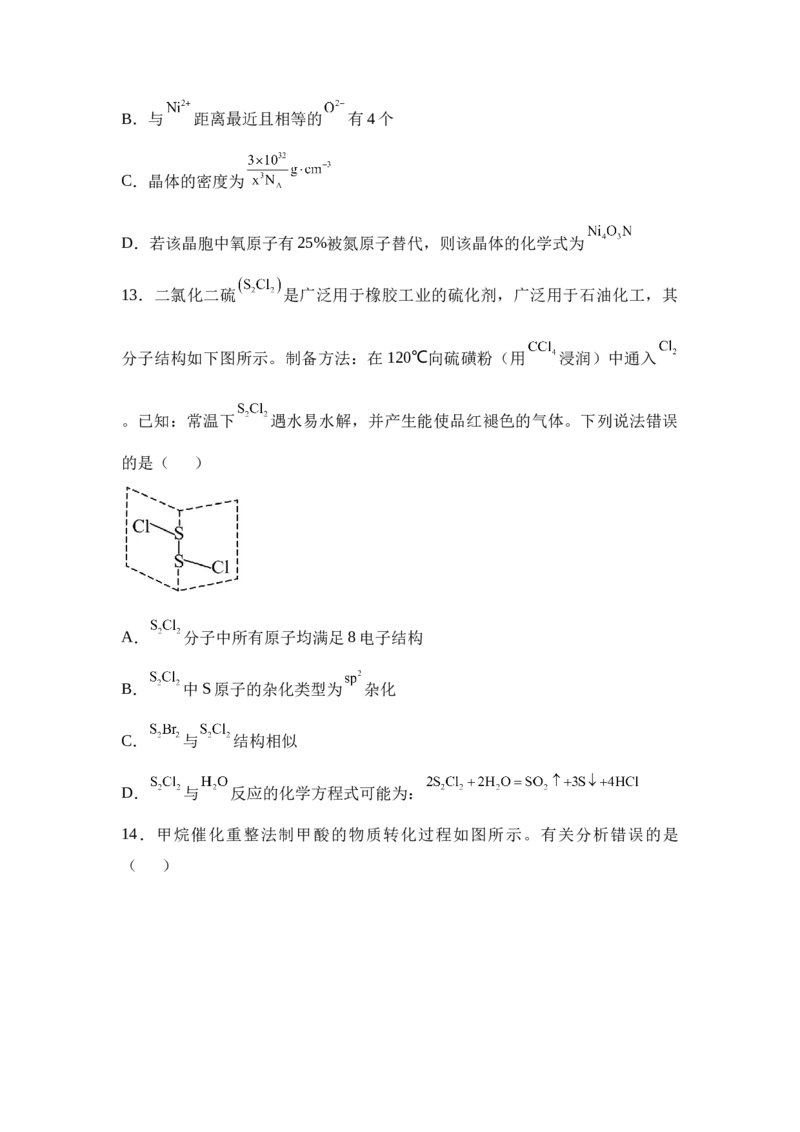
11.某种离子液体的结构如图所示,X、Y、Z、M、Q为原子序数依次增大的
短周期元素,Z的原子序数等于X、Y原子序数之和,Q为非金属性最强的元
素。
下列说法正确的是( )
A.键长:MX >ZX B.沸点:XQ、<或=),其原因是
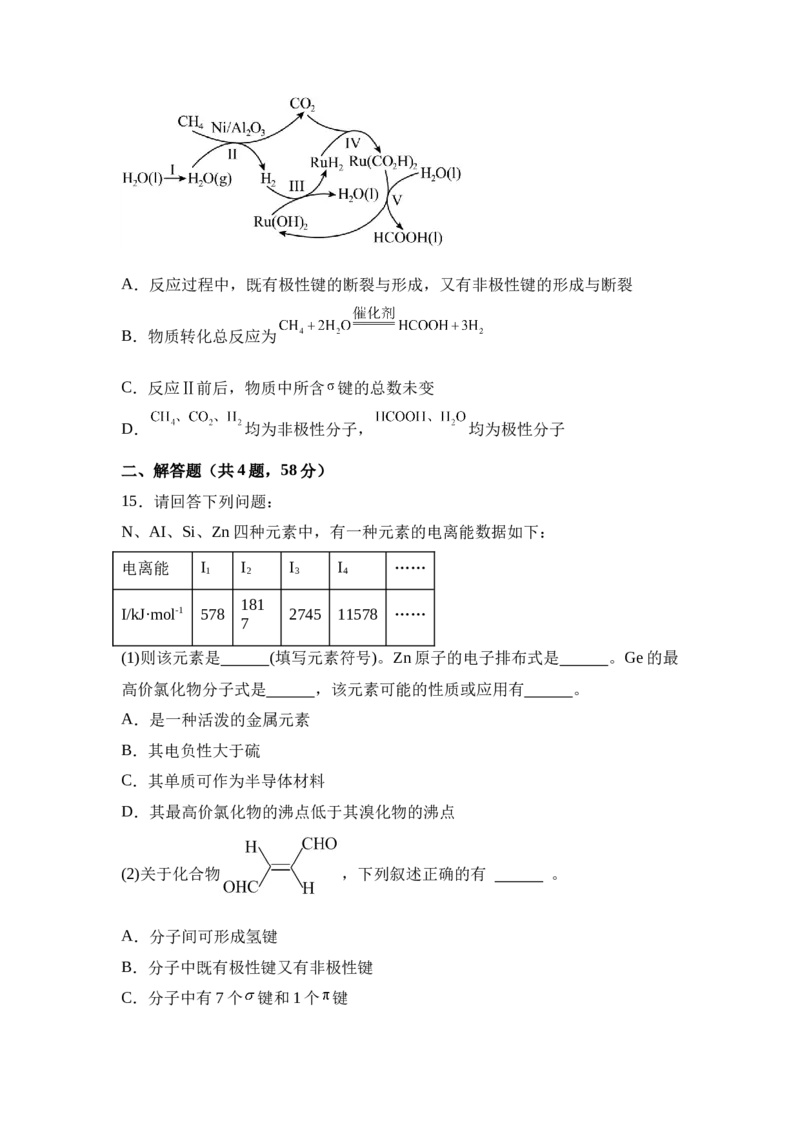
16.铁、铜及其化合物在日常生产、生活中有着广泛的应用。回答下列问题:
(1)基态Cu原子的价层电子的电子排布图为 。
(2)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华。易
溶于水,也易溶于乙醚、丙酮等有机溶剂。在蒸气中也容易双聚,据此判断三
氯化铁晶体为
(填“分子晶体”或“离子晶体”)。
(3)(NH ) Fe(SO ) ·6H O俗称摩尔盐,其阴离子 的空间构型为 。
4 2 4 2 2
(4)Fe(CO) 可用作催化剂、汽油抗爆剂等,其分子中σ键和π键的数目之比为
5
。CO的沸点高于N 的原因是 。
2
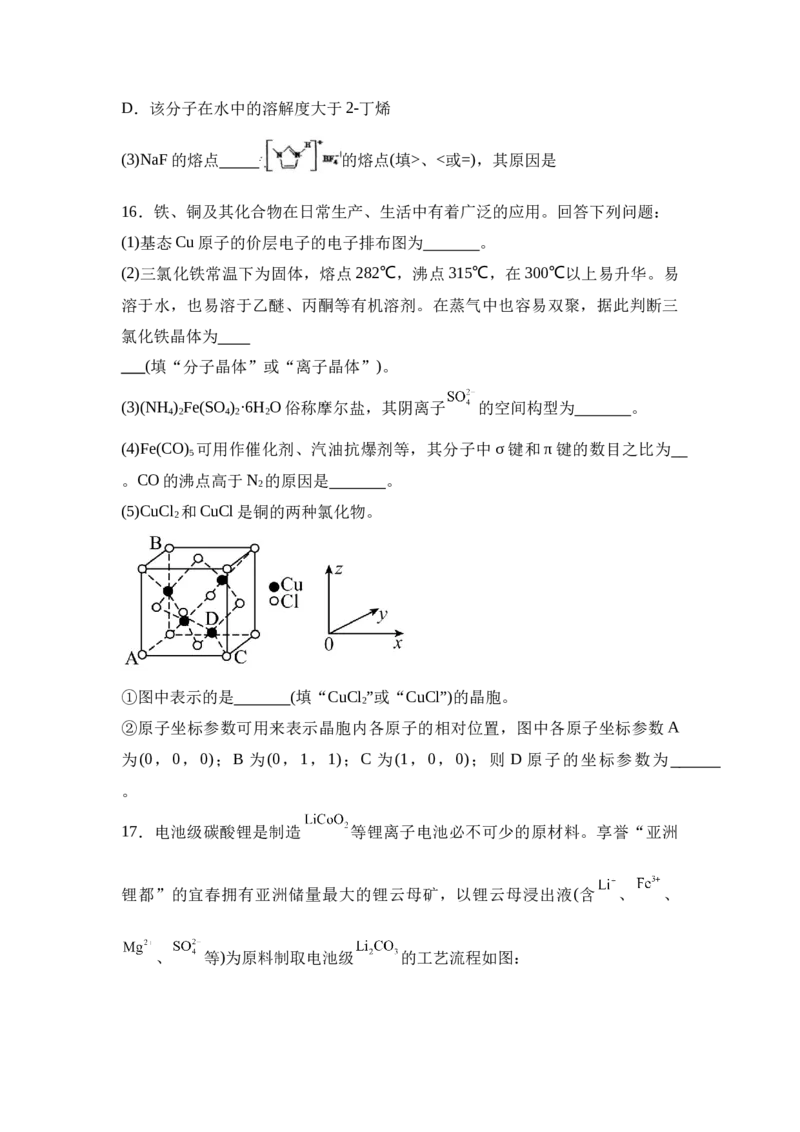
(5)CuCl 和CuCl是铜的两种氯化物。
2
①图中表示的是 (填“CuCl ”或“CuCl”)的晶胞。
2
②原子坐标参数可用来表示晶胞内各原子的相对位置,图中各原子坐标参数A
为(0,0,0);B 为(0,1,1);C 为(1,0,0);则 D 原子的坐标参数为
。
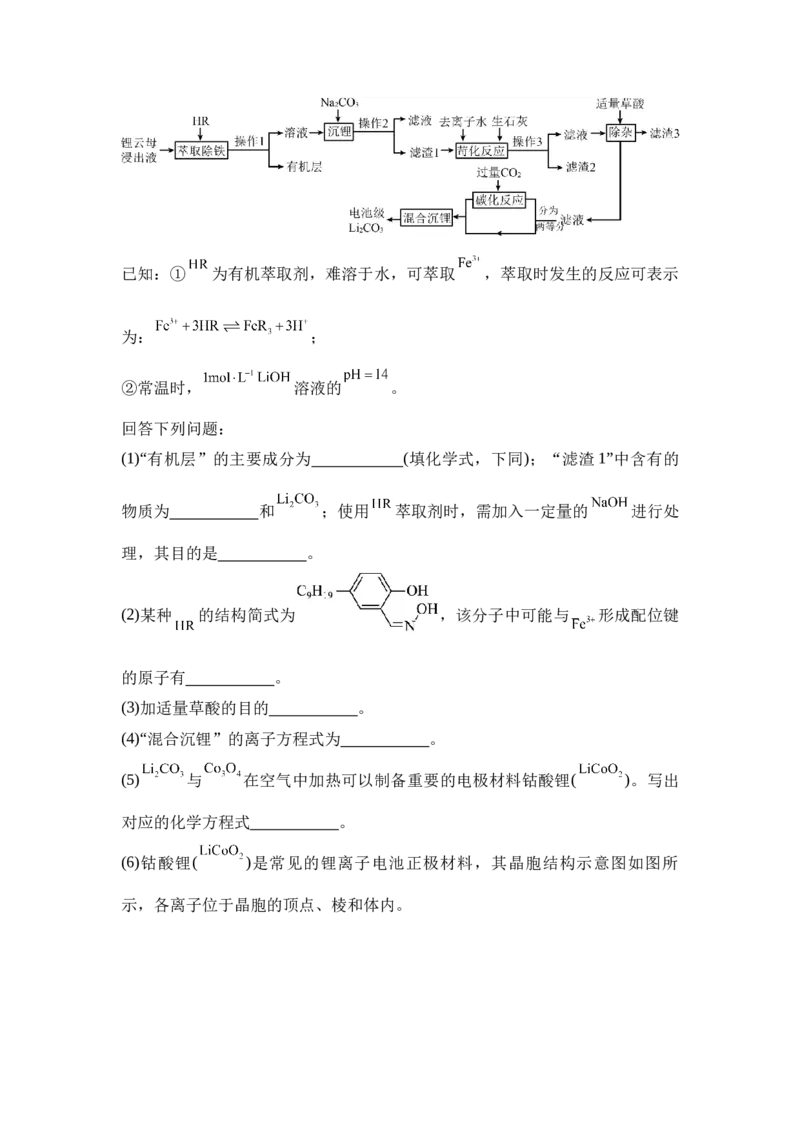
17.电池级碳酸锂是制造 等锂离子电池必不可少的原材料。享誉“亚洲
锂都”的宜春拥有亚洲储量最大的锂云母矿,以锂云母浸出液(含 、 、
、 等)为原料制取电池级 的工艺流程如图:已知:① 为有机萃取剂,难溶于水,可萃取 ,萃取时发生的反应可表示
为: ;
②常温时, 溶液的 。
回答下列问题:
(1)“有机层”的主要成分为 (填化学式,下同);“滤渣1”中含有的
物质为 和 ;使用 萃取剂时,需加入一定量的 进行处
理,其目的是 。
(2)某种 的结构简式为 ,该分子中可能与 形成配位键
的原子有 。
(3)加适量草酸的目的 。
(4)“混合沉锂”的离子方程式为 。
(5) 与 在空气中加热可以制备重要的电极材料钴酸锂( )。写出
对应的化学方程式 。
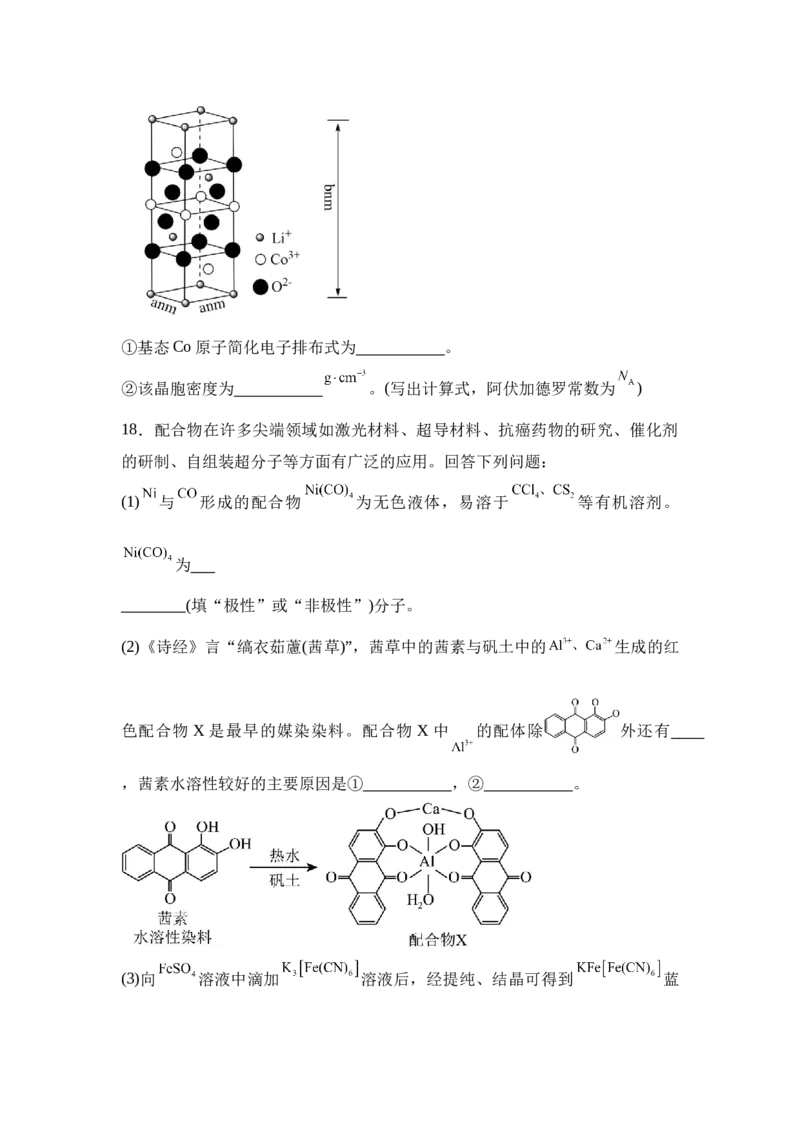
(6)钴酸锂( )是常见的锂离子电池正极材料,其晶胞结构示意图如图所
示,各离子位于晶胞的顶点、棱和体内。①基态Co原子简化电子排布式为 。
②该晶胞密度为 。(写出计算式,阿伏加德罗常数为 )
18.配合物在许多尖端领域如激光材料、超导材料、抗癌药物的研究、催化剂
的研制、自组装超分子等方面有广泛的应用。回答下列问题:
(1) 与 形成的配合物 为无色液体,易溶于 等有机溶剂。
为
(填“极性”或“非极性”)分子。
(2)《诗经》言“缟衣茹藘(茜草)”,茜草中的茜素与矾土中的 生成的红
色配合物 X 是最早的媒染染料。配合物 X 中 的配体除 外还有
,茜素水溶性较好的主要原因是① ,② 。
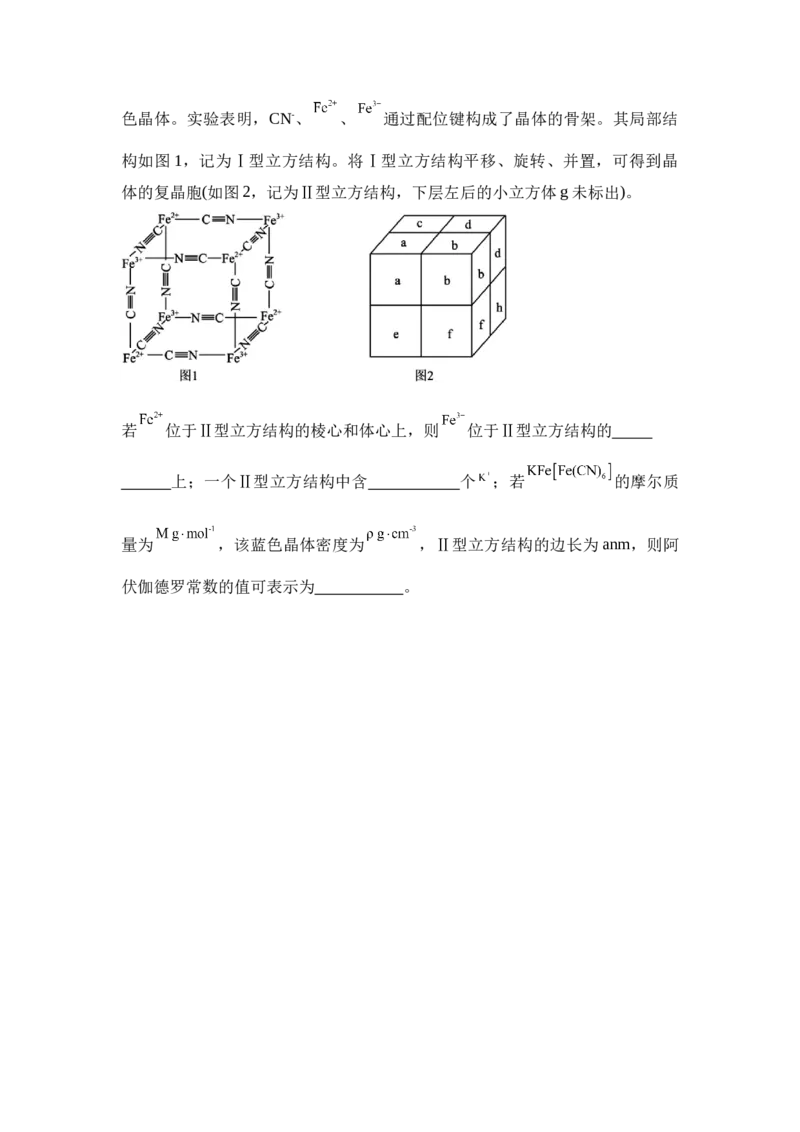
(3)向 溶液中滴加 溶液后,经提纯、结晶可得到 蓝色晶体。实验表明,CN-、 、 通过配位键构成了晶体的骨架。其局部结
构如图1,记为Ⅰ型立方结构。将Ⅰ型立方结构平移、旋转、并置,可得到晶
体的复晶胞(如图2,记为Ⅱ型立方结构,下层左后的小立方体g未标出)。
若 位于Ⅱ型立方结构的棱心和体心上,则 位于Ⅱ型立方结构的
上;一个Ⅱ型立方结构中含 个 ;若 的摩尔质
量为 ,该蓝色晶体密度为 ,Ⅱ型立方结构的边长为anm,则阿
伏伽德罗常数的值可表示为 。化学参考答案
1.【答案】B
2.【答案】B
3.【答案】A
4.【答案】A
5.【答案】B
6.【答案】A
7.【答案】B
8.【答案】C
9.【答案】A
10.【答案】B
11.【答案】C
12.【答案】B
13.【答案】B
14.【答案】C15.【答案】(1)Al(2分) (2分) (2
分) CD(2分)
(2)BD(2分)
(3)>(2分) 两者均为离子化合物,阴阳离子电荷数均为 1,但前者的离
子半径较小,离子键较强,熔点较高(2分)
16.【答案】(1) (2分)
(2)分子晶体(2分)
(3)正四面体(2分)
(4)1:1(2分) CO是极性分子,极性越强,沸点越高(2分)
(5)CuCl(2分) (2分)
17.【答案】(1)FeR (1分) (1分) 加入氢氧化钠后氢离
3
子会被消耗,从而使平衡正向移动,提高萃取率(2分)
(2)N、O(2分)
(3)使钙离子生成草酸钙,便于除掉(2分)
(4) (2分)
(5) (2分)
(6) (2分) (2分)
18.【答案】(1)非极性(2分)
(2)H O、OH-(2分) 分子中含有亲水性的羟基、羰基(2分) 能和水
2
分子形成氢键(2分)
(3)顶点和面心(2分) 4(2分) (2分)