文档内容
2024 年兰州市高二级第一学期期中学业质量检测卷(2)
化 学
时长:75分钟 总分:100分
一、单选题(每题3分,共48分)
1. 如图是家用消毒液发生器,下列分析错误的是
A. 碳棒a是阴极
B. 反应中碳棒b附近溶液显酸性
C. 电子由碳棒a经溶液流向碳棒b
D. 发生器中 总的反应:NaCl+HO NaClO+H↑
2 2
2. 对于可逆反应M+N Q达到平衡时,下列说法正确的是
A. M、N、Q三种物质的⇌浓度一定相等 B. M、N全部变成了Q
C. 反应混合物中各组分的浓度不再变化 D. 反应已经停止
3. 在一个不传热的固定容积的容器中,对于反应 A(g)+2B(g) 3C(g)(正反应为吸热反应),下列叙述为
平衡状态标志的是
①体系的温度不再变化 ②外界条件不变时,A、B、C浓度保持不变 ③气体平均分子量不再变化 ④体
系的压强不再变化 ⑤气体密度不再变化 ⑥3 v (B)=2 v (C) ⑦单位时间内消耗1 mol A(g)的同时生成
正 逆
3 mol C(g)
A. ①②⑥ B. ①②③⑤ C. ②③④⑤ D. ①②④⑤⑦
4. 溶液与 溶液发生反应:
,达到平衡。下列说法不正确的是
A. 加入苯,振荡,平衡正向移动B. 经苯2次萃取分离后,在水溶液中加入 ,溶液呈血红色,表明该化学反应存在限度
C. 加入 固体,平衡逆向移动
D. 该反应的平衡常数
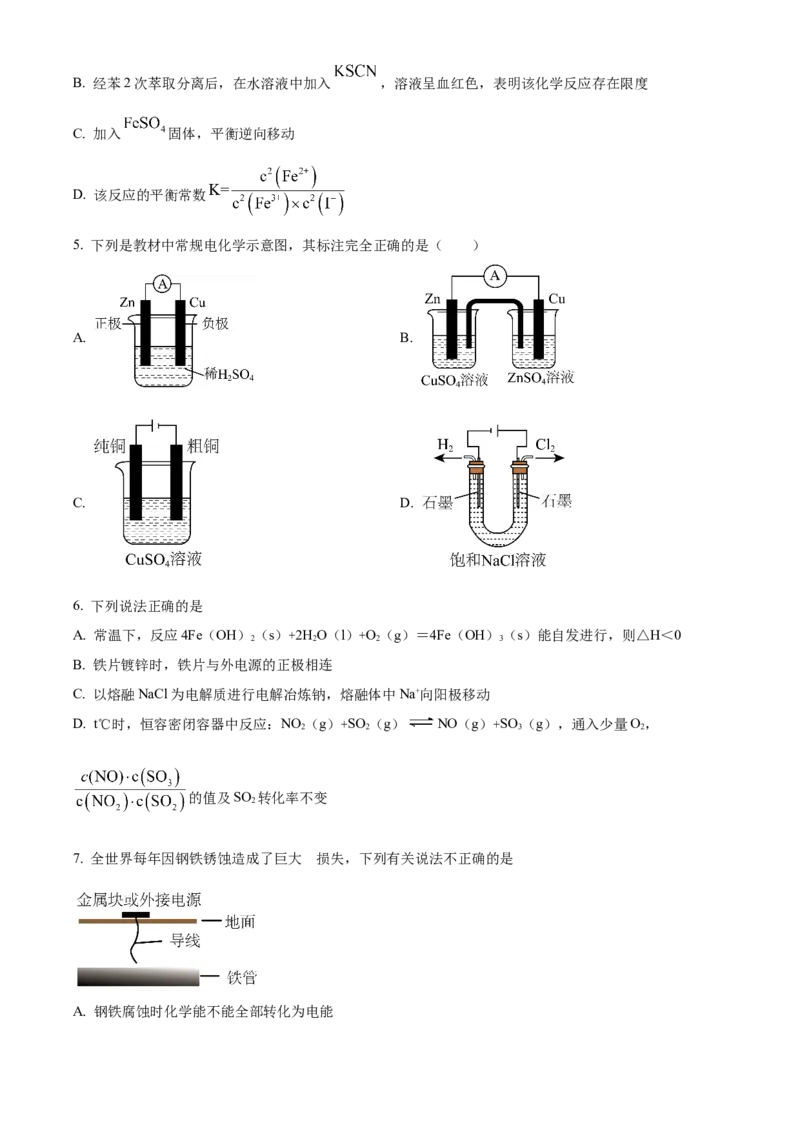
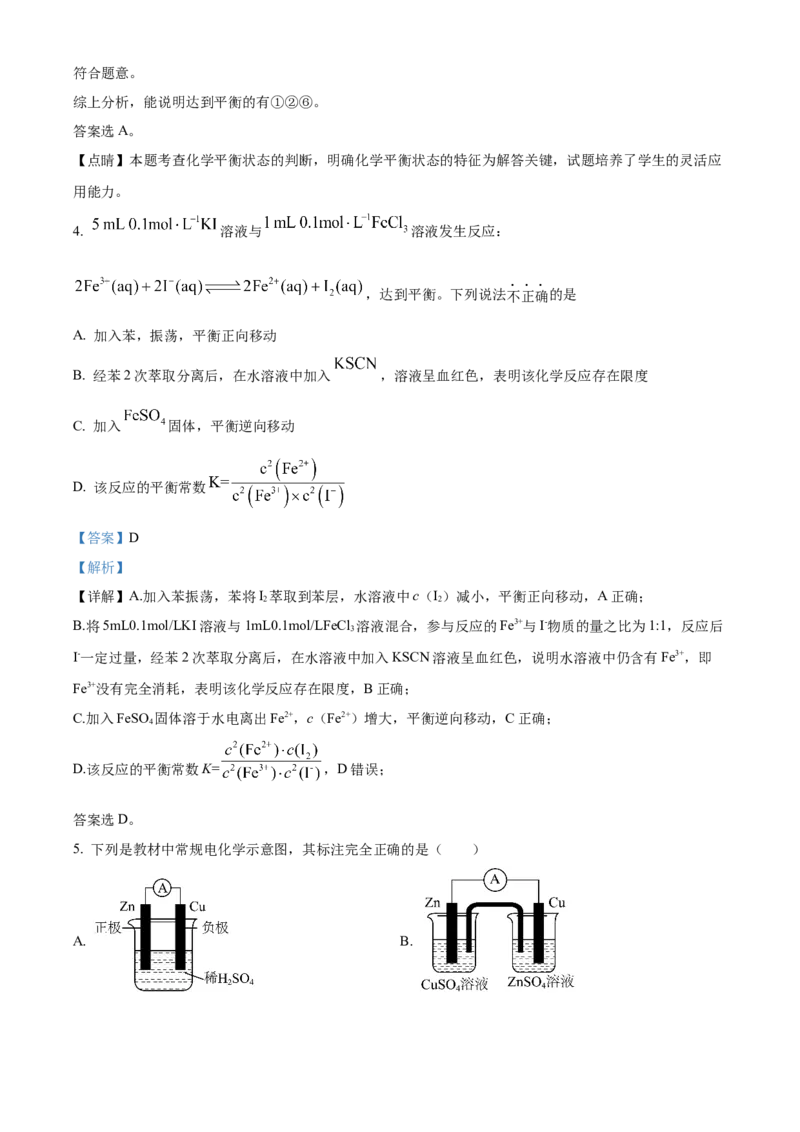
5. 下列是教材中常规电化学示意图,其标注完全正确的是( )
A. B.
C. D.
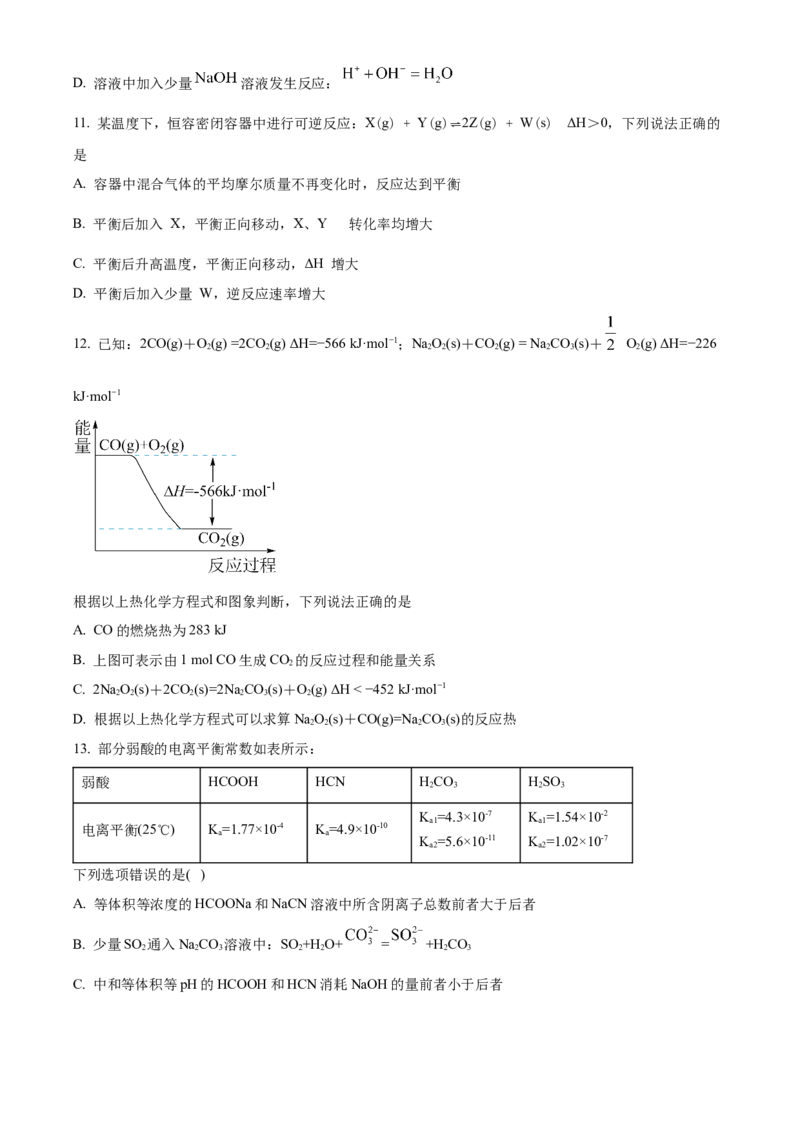
6. 下列说法正确的是
A. 常温下,反应4Fe(OH)(s)+2HO(l)+O(g)=4Fe(OH)(s)能自发进行,则△H<0
2 2 2 3
B. 铁片镀锌时,铁片与外电源的正极相连
C. 以熔融NaCl为电解质进行电解冶炼钠,熔融体中Na+向阳极移动
D. t℃时,恒容密闭容器中反应:NO (g)+SO (g) NO(g)+SO (g),通入少量O,
2 2 3 2
的值及SO 转化率不变
2
的
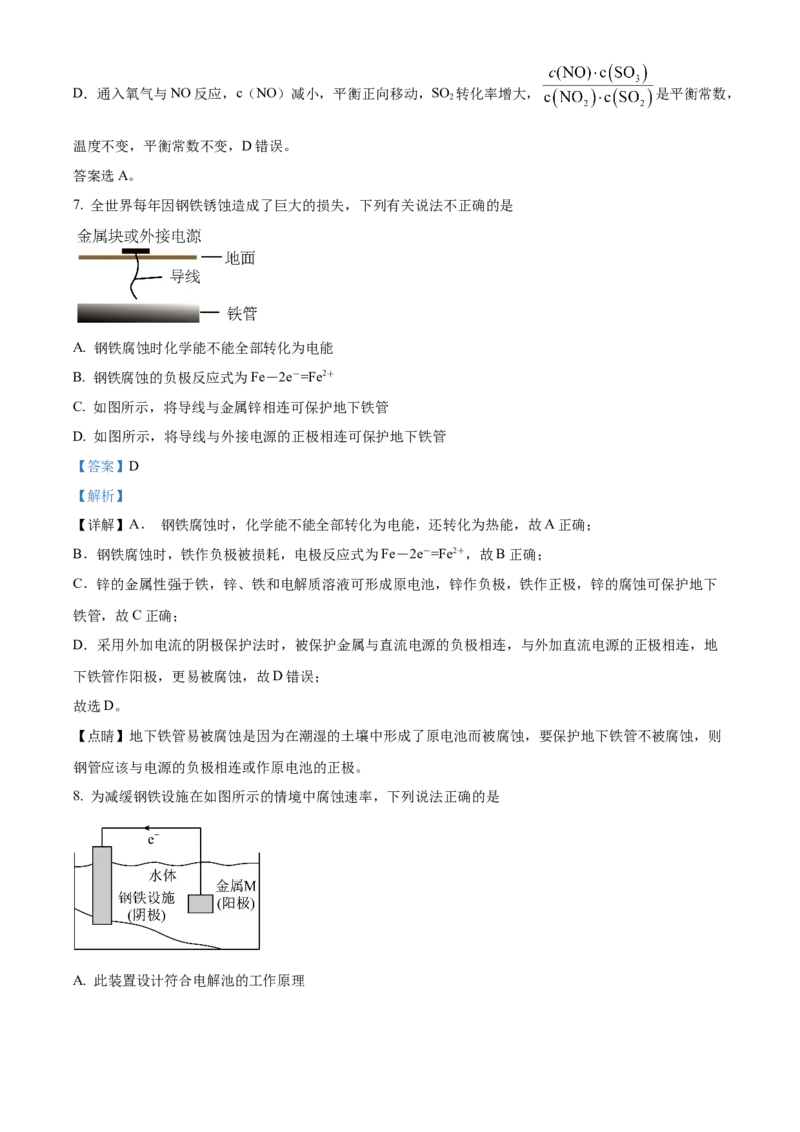
7. 全世界每年因钢铁锈蚀造成了巨大 损失,下列有关说法不正确的是
A. 钢铁腐蚀时化学能不能全部转化为电能B. 钢铁腐蚀的负极反应式为Fe-2e-=Fe2+
C. 如图所示,将导线与金属锌相连可保护地下铁管
D. 如图所示,将导线与外接电源的正极相连可保护地下铁管
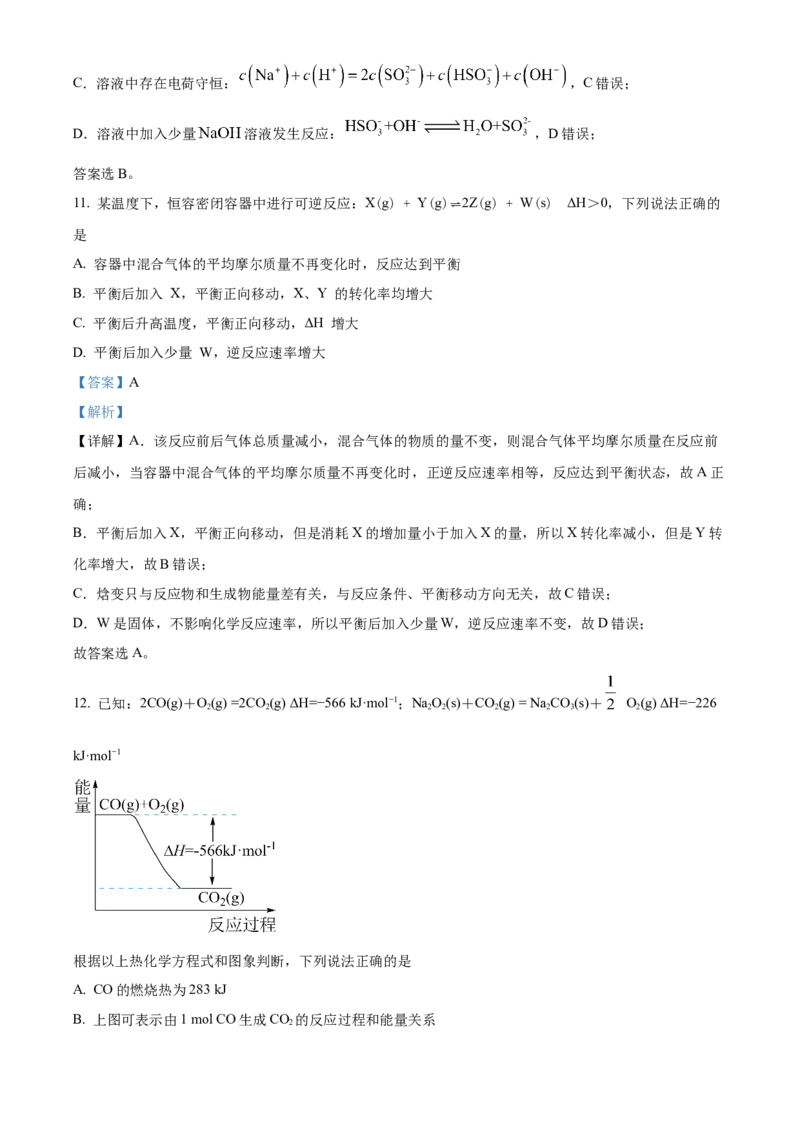
8. 为减缓钢铁设施在如图所示的情境中腐蚀速率,下列说法正确的是
A. 此装置设计符合电解池的工作原理
B. 金属 的还原性应该比 的还原性弱
C. 当水体环境呈较强酸性时,钢铁设施表面会有气泡冒出
D. 当水体环境呈中性时,发生的反应有
9. 设N 为阿伏加德罗常数的值。已知反应:
A
(1)CH (g)+2O(g)=CO(g)+2HO(l) △H=akJ/mol
4 2 2 2
(2)CH (g)+2O(g)=CO(g)+2HO(g) △H=bkJ/mol。其他数据如表:
4 2 2 2
化学键 C‒O O‒O C‒H O‒H
键能/(kJ•mol‒1) 798 x 413 463
下列说法正确的是( )
A. 上表中x=
B. HO(g)=HO(l)的△S<0,△H=(a-b)kJ/mol
2 2
C. 当有4N 个C‒H键断裂时,反应放出的热量一定为akJ
A
D. a>b且甲烷燃烧热为bkJ/mol
10. 已知常温下 溶液 ,说法正确的是
A. 溶液中:
B. 溶液中:
C. 溶液中:D. 溶液中加入少量 溶液发生反应:
11. 某温度下,恒容密闭容器中进行可逆反应:X(g) + Y(g) 2Z(g) + W(s) ΔH>0,下列说法正确的
⇌
是
A. 容器中混合气体的平均摩尔质量不再变化时,反应达到平衡
的
B. 平衡后加入 X,平衡正向移动,X、Y 转化率均增大
C. 平衡后升高温度,平衡正向移动,ΔH 增大
D. 平衡后加入少量 W,逆反应速率增大
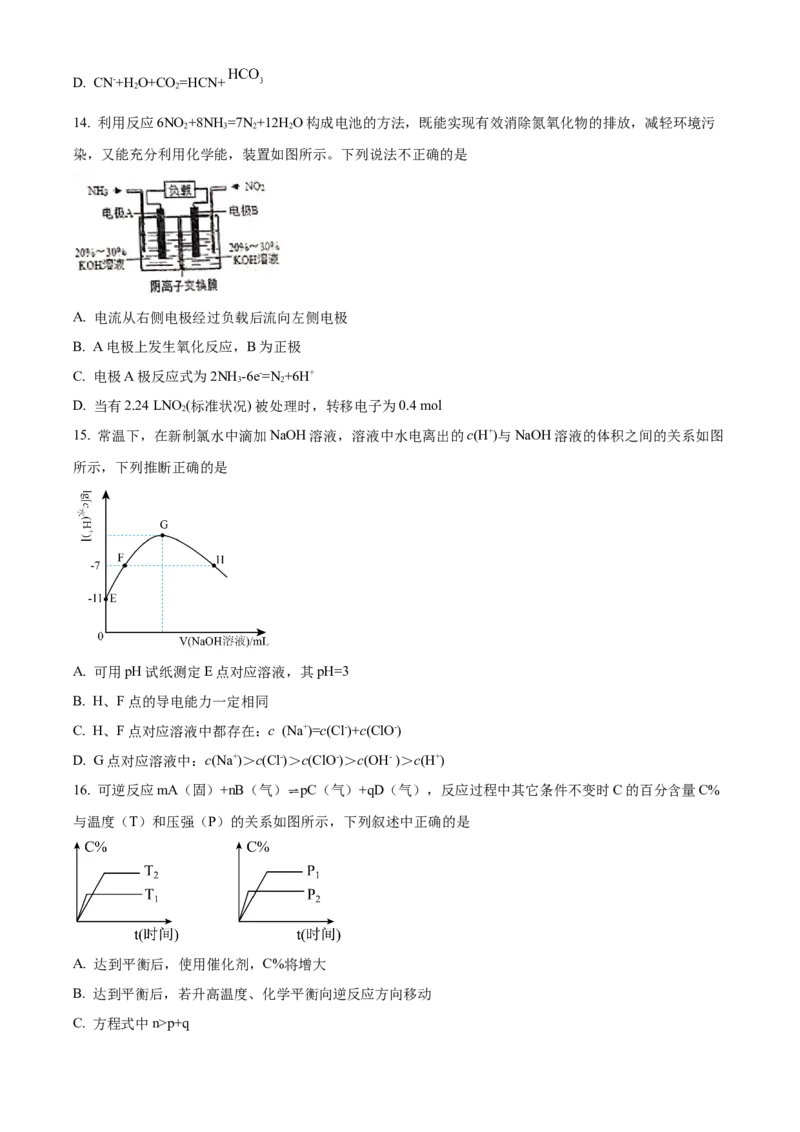
12. 已知:2CO(g)+O(g) =2CO (g) ΔH=−566 kJ·mol−1;NaO(s)+CO(g) = Na CO(s)+ O(g) ΔH=−226
2 2 2 2 2 2 3 2
kJ·mol−1
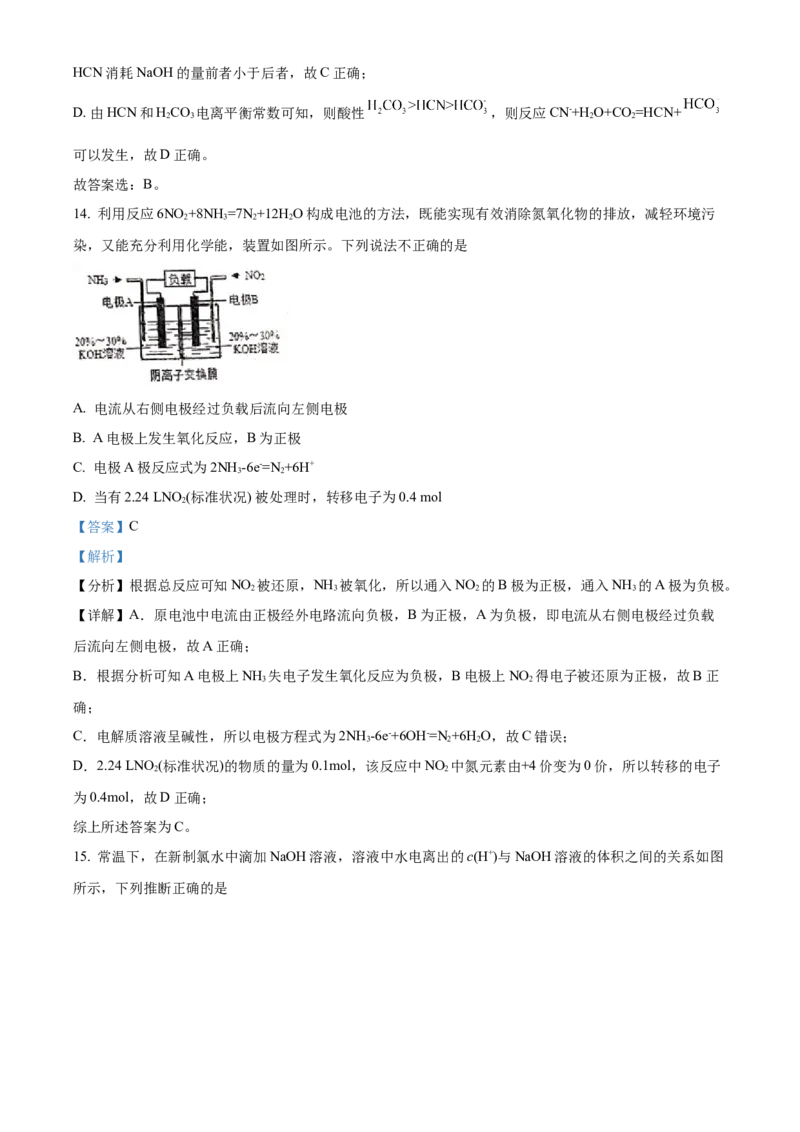
根据以上热化学方程式和图象判断,下列说法正确的是
A. CO的燃烧热为283 kJ
B. 上图可表示由1 mol CO生成CO 的反应过程和能量关系
2
C. 2NaO(s)+2CO(s)=2Na CO(s)+O(g) ΔH < −452 kJ·mol−1
2 2 2 2 3 2
D. 根据以上热化学方程式可以求算NaO(s)+CO(g)=Na CO(s)的反应热
2 2 2 3
13. 部分弱酸的电离平衡常数如表所示:
弱酸 HCOOH HCN HCO HSO
2 3 2 3
K =4.3×10-7 K =1.54×10-2
a1 a1
电离平衡(25℃) K=1.77×10-4 K=4.9×10-10
a a
K =5.6×10-11 K =1.02×10-7
a2 a2
下列选项错误的是( )
A. 等体积等浓度的HCOONa和NaCN溶液中所含阴离子总数前者大于后者
B. 少量SO 通入NaCO 溶液中:SO +H O+ = +H CO
2 2 3 2 2 2 3
C. 中和等体积等pH的HCOOH和HCN消耗NaOH的量前者小于后者D. CN-+H O+CO=HCN+
2 2
14. 利用反应6NO +8NH=7N +12H O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污
2 3 2 2
染,又能充分利用化学能,装置如图所示。下列说法不正确的是
A. 电流从右侧电极经过负载后流向左侧电极
B. A电极上发生氧化反应,B为正极
C. 电极A极反应式为2NH -6e-=N +6H+
3 2
D. 当有2.24 LNO (标准状况) 被处理时,转移电子为0.4 mol
2
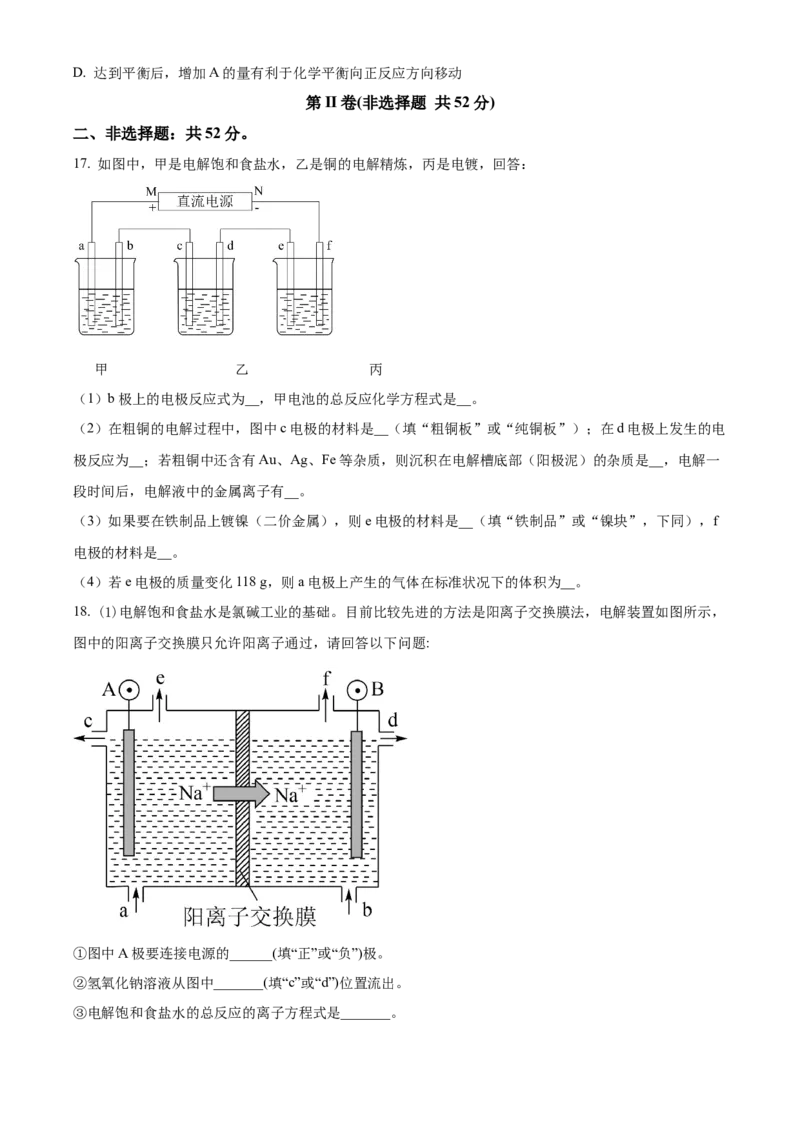
15. 常温下,在新制氯水中滴加NaOH溶液,溶液中水电离出的c(H+)与NaOH溶液的体积之间的关系如图
所示,下列推断正确的是
A. 可用pH试纸测定E点对应溶液,其pH=3
B. H、F点的导电能力一定相同
C. H、F点对应溶液中都存在:c (Na+)=c(Cl-)+c(ClO-)
D. G点对应溶液中:c(Na+)>c(Cl-)>c(ClO-)>c(OH- )>c(H+)
16. 可逆反应mA(固)+nB(气) pC(气)+qD(气),反应过程中其它条件不变时C的百分含量C%
⇌
与温度(T)和压强(P)的关系如图所示,下列叙述中正确的是
A. 达到平衡后,使用催化剂,C%将增大
B. 达到平衡后,若升高温度、化学平衡向逆反应方向移动
C. 方程式中n>p+qD. 达到平衡后,增加A的量有利于化学平衡向正反应方向移动
第II卷(非选择题 共52分)
二、非选择题:共52分。
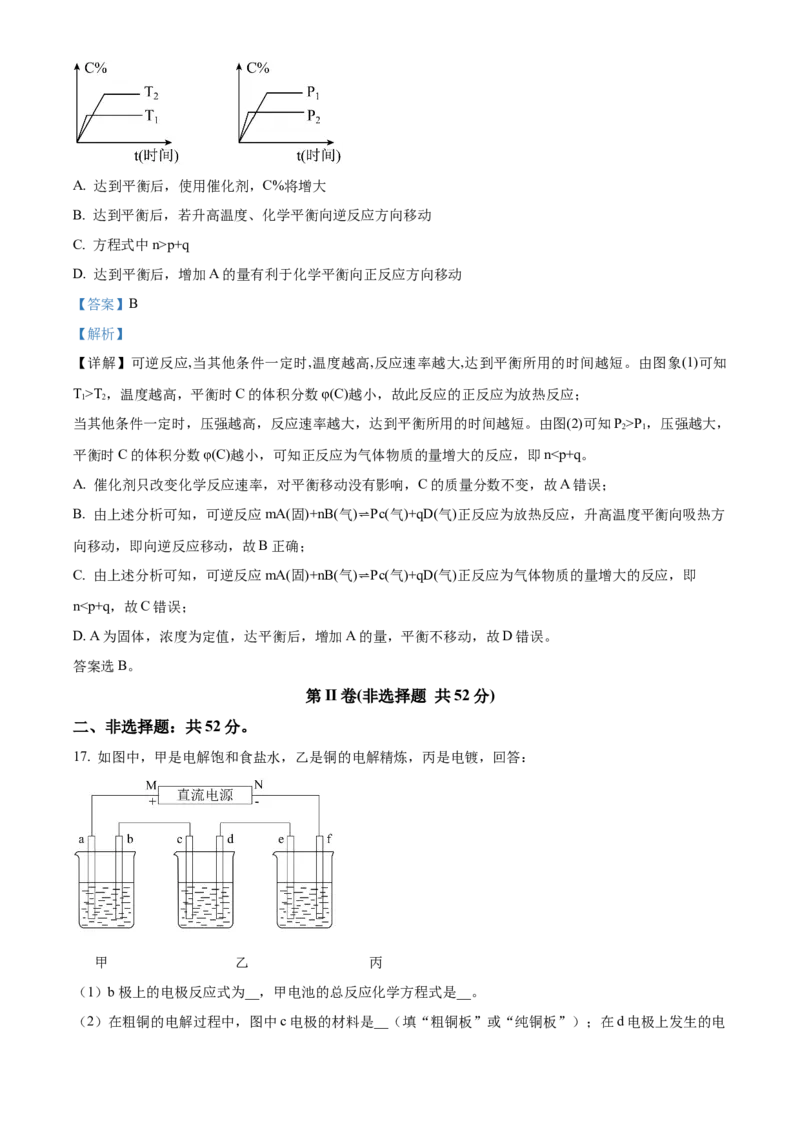
17. 如图中,甲是电解饱和食盐水,乙是铜的电解精炼,丙是电镀,回答:
甲 乙 丙
(1)b极上的电极反应式为__,甲电池的总反应化学方程式是__。
(2)在粗铜的电解过程中,图中c电极的材料是__(填“粗铜板”或“纯铜板”);在d电极上发生的电
极反应为__;若粗铜中还含有Au、Ag、Fe等杂质,则沉积在电解槽底部(阳极泥)的杂质是__,电解一
段时间后,电解液中的金属离子有__。
(3)如果要在铁制品上镀镍(二价金属),则e电极的材料是__(填“铁制品”或“镍块”,下同),f
电极的材料是__。
(4)若e电极的质量变化118 g,则a电极上产生的气体在标准状况下的体积为__。
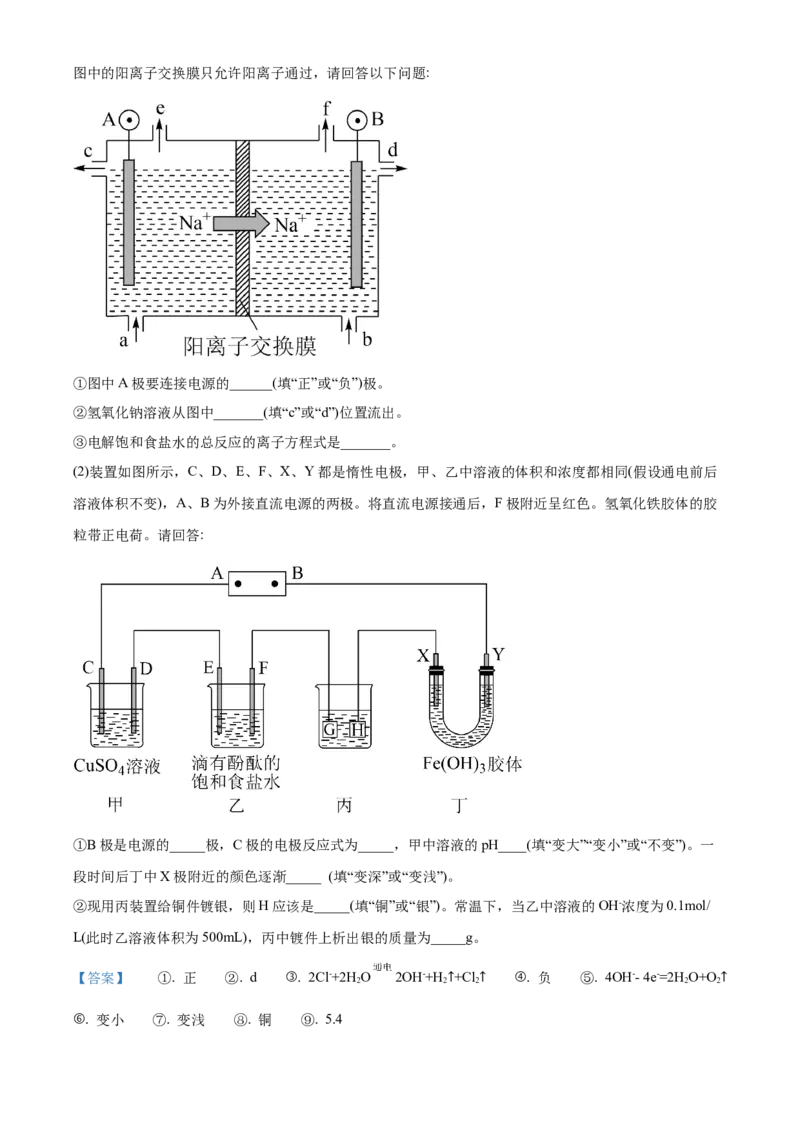
18. (1)电解饱和食盐水是氯碱工业的基础。目前比较先进的方法是阳离子交换膜法,电解装置如图所示,
图中的阳离子交换膜只允许阳离子通过,请回答以下问题:
①图中A极要连接电源的______(填“正”或“负”)极。
②氢氧化钠溶液从图中_______(填“c”或“d”)位置流出。
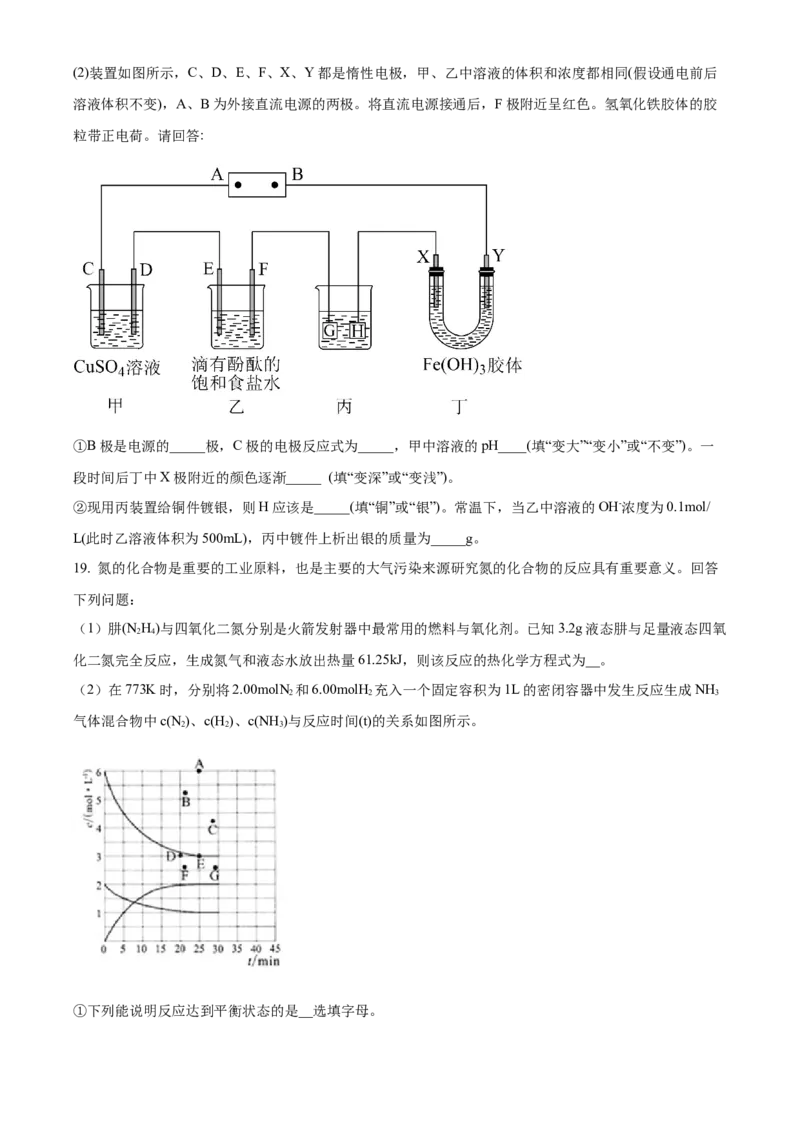
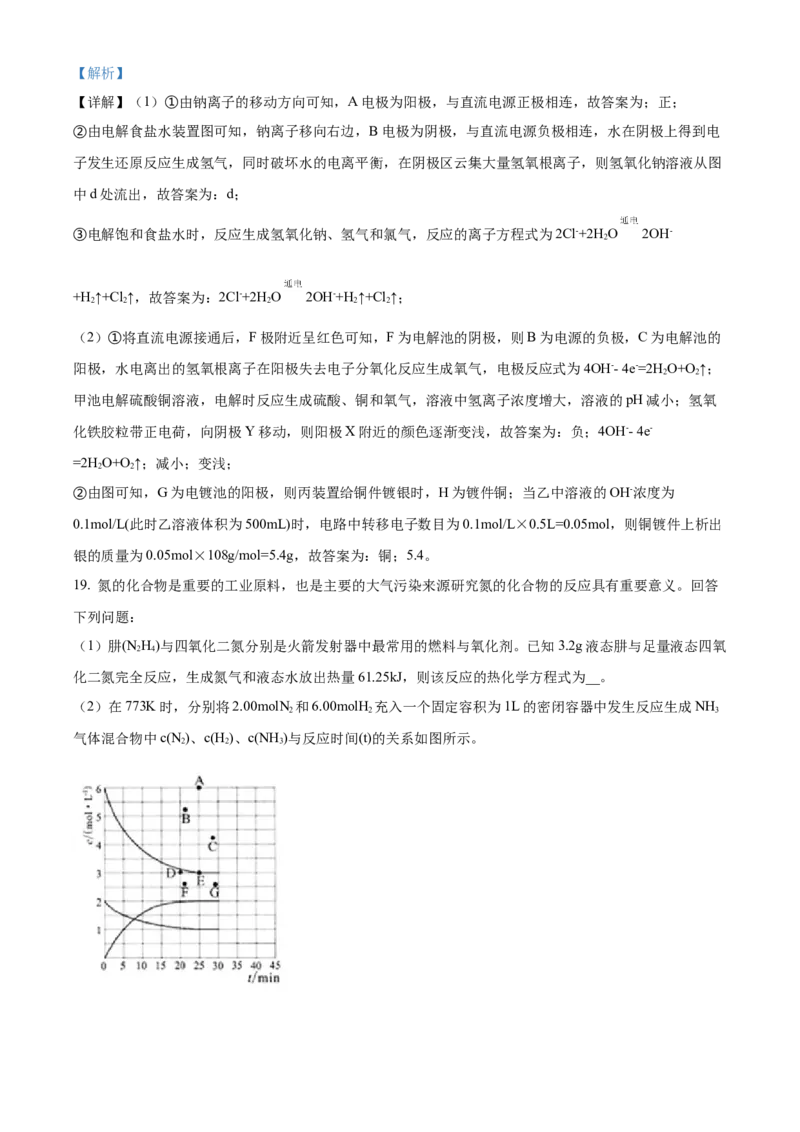
③电解饱和食盐水的总反应的离子方程式是_______。(2)装置如图所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后
溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。氢氧化铁胶体的胶
粒带正电荷。请回答:
①B极是电源的_____极,C极的电极反应式为_____,甲中溶液的pH____(填“变大”“变小”或“不变”)。一
段时间后丁中X极附近的颜色逐渐_____ (填“变深”或“变浅”)。
②现用丙装置给铜件镀银,则H应该是_____(填“铜”或“银”)。常温下,当乙中溶液的OH-浓度为0.1mol/
L(此时乙溶液体积为500mL),丙中镀件上析出银的质量为_____g。
19. 氮的化合物是重要的工业原料,也是主要的大气污染来源研究氮的化合物的反应具有重要意义。回答
下列问题:
(1)肼(N H)与四氧化二氮分别是火箭发射器中最常用的燃料与氧化剂。已知3.2g液态肼与足量液态四氧
2 4
化二氮完全反应,生成氮气和液态水放出热量61.25kJ,则该反应的热化学方程式为__。
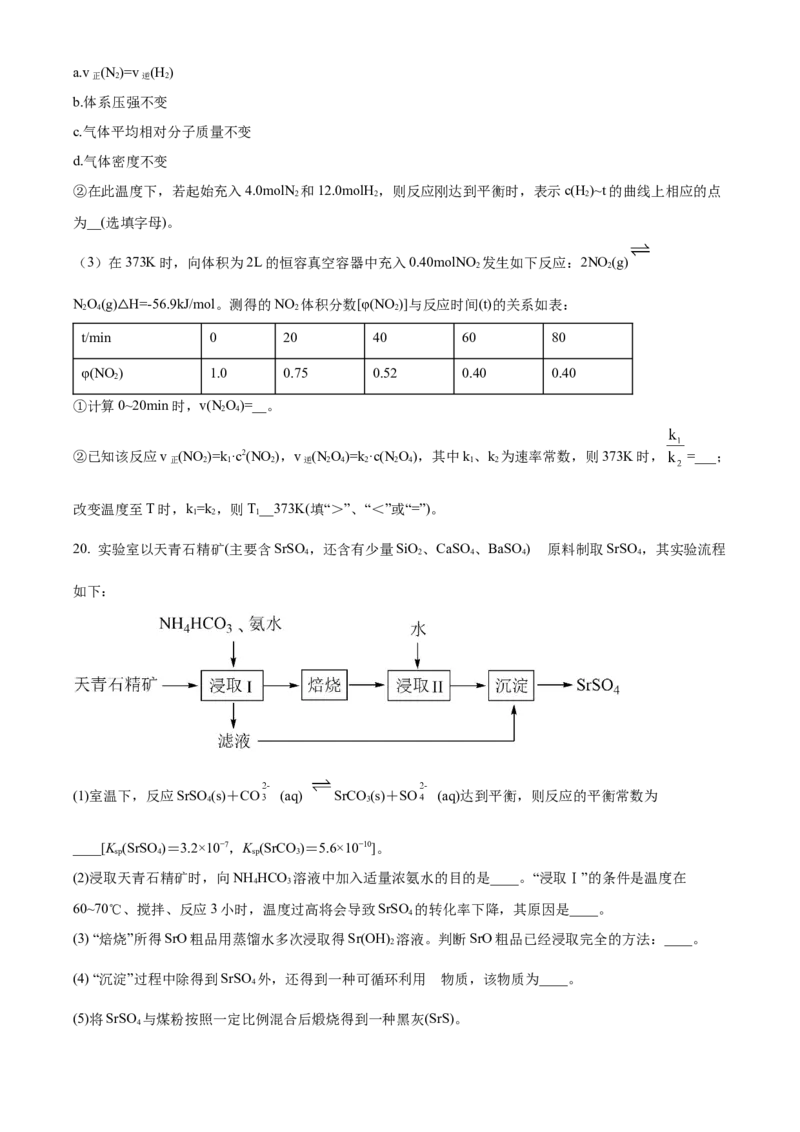
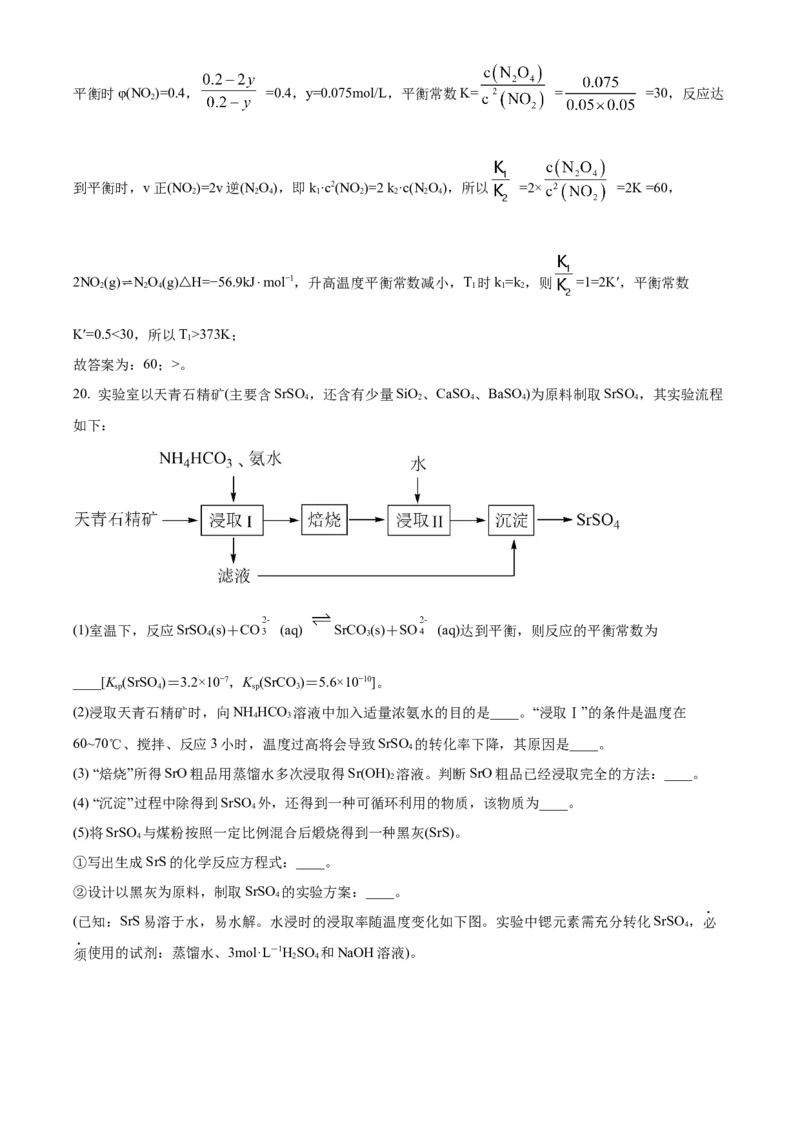
(2)在773K时,分别将2.00molN 和6.00molH 充入一个固定容积为1L的密闭容器中发生反应生成NH
2 2 3
气体混合物中c(N)、c(H)、c(NH )与反应时间(t)的关系如图所示。
2 2 3
①下列能说明反应达到平衡状态的是__选填字母。a.v (N )=v (H )
正 2 逆 2
b.体系压强不变
c.气体平均相对分子质量不变
d.气体密度不变
②在此温度下,若起始充入4.0molN 和12.0molH,则反应刚达到平衡时,表示c(H)~t的曲线上相应的点
2 2 2
为__(选填字母)。
(3)在373K时,向体积为2L的恒容真空容器中充入0.40molNO 发生如下反应:2NO (g)
2 2
NO(g) H=-56.9kJ/mol。测得的NO 体积分数[φ(NO )]与反应时间(t)的关系如表:
2 4 2 2
t/min △ 0 20 40 60 80
φ(NO ) 1.0 0.75 0.52 0.40 0.40
2
①计算0~20min时,v(N O)=__。
2 4
②已知该反应v (NO )=k ·c2(NO ),v (N O)=k ·c(NO),其中k、k 为速率常数,则373K时, =___;
正 2 1 2 逆 2 4 2 2 4 1 2
改变温度至T时,k=k,则T__373K(填“>”、“<”或“=”)。
1 2 1
为
20. 实验室以天青石精矿(主要含SrSO ,还含有少量SiO、CaSO、BaSO) 原料制取SrSO ,其实验流程
4 2 4 4 4
如下:
(1)室温下,反应SrSO (s)+CO (aq) SrCO (s)+SO (aq)达到平衡,则反应的平衡常数为
4 3
____[K (SrSO )=3.2×10−7,K (SrCO )=5.6×10−10]。
sp 4 sp 3
(2)浸取天青石精矿时,向NH HCO 溶液中加入适量浓氨水的目的是____。“浸取Ⅰ”的条件是温度在
4 3
60~70℃、搅拌、反应3小时,温度过高将会导致SrSO 的转化率下降,其原因是____。
4
(3) “焙烧”所得SrO粗品用蒸馏水多次浸取得Sr(OH) 溶液。判断SrO粗品已经浸取完全的方法:____。
2
的
(4) “沉淀”过程中除得到SrSO 外,还得到一种可循环利用 物质,该物质为____。
4
(5)将SrSO 与煤粉按照一定比例混合后煅烧得到一种黑灰(SrS)。
4①写出生成SrS的化学反应方程式:____。
②设计以黑灰为原料,制取SrSO 的实验方案:____。
4
(已知:SrS易溶于水,易水解。水浸时的浸取率随温度变化如下图。实验中锶元素需充分转化SrSO ,必
4
须使用的试剂:蒸馏水、3mol·L-1HSO 和NaOH溶液)。
2 42024 年兰州市高二级第一学期期中学业质量检测卷(2)
化学
时长:75分钟 总分:100分
一、单选题(每题3分,共48分)
1. 如图是家用消毒液发生器,下列分析错误的是
A. 碳棒a是阴极
B. 反应中碳棒b附近溶液显酸性
C. 电子由碳棒a经溶液流向碳棒b
D. 发生器中的总反应:NaCl+HO NaClO+H↑
2 2
【答案】C
【解析】
【分析】家用消毒液发生器制取NaClO,所以a电极应生成OH-和H,b电极应生成Cl,由此确定b电极
2 2
为阳极,发生反应2Cl--2e- ==Cl ↑;a电极为阴极,发生反应2HO+2e- ==2OH- +H ↑。
2 2 2
【详解】A.由以上分析知,碳棒a是阴极,A正确;
B.反应中碳棒b附近生成Cl,Cl+H O=H++Cl- +HClO,溶液显酸性,B正确;
2 2 2
C.电子不能经过溶液流动,只能沿导线移动,C错误;
D.发生器中发生反应:2NaCl+2H O 2NaOH+Cl ↑+H ↑,Cl+2NaOH NaCl+NaClO+H O,总反应为
2 2 2 2 2
NaCl+HO NaClO+H↑,D正确;
2 2
故选C。
2. 对于可逆反应M+N Q达到平衡时,下列说法正确的是
⇌A. M、N、Q三种物质的浓度一定相等 B. M、N全部变成了Q
C. 反应混合物中各组分的浓度不再变化 D. 反应已经停止
【答案】C
【解析】
【详解】A.反应达到平衡时,各物质浓度保持不变,M、N、Q三种物质的浓度不一定相等,故A错误;
B.可逆反应是有限度的,M、N不可能全部变成Q,故B错误;
C.反应混合物中各组分的浓度不再变化,反应达到平衡状态,故C正确;
D.反应达到平衡状态,正逆反应速率相等,但不等于0,反应没有停止,故D错误;
选C。
3. 在一个不传热的固定容积的容器中,对于反应 A(g)+2B(g) 3C(g)(正反应为吸热反应),下列叙述为
平衡状态标志的是
①体系的温度不再变化 ②外界条件不变时,A、B、C浓度保持不变 ③气体平均分子量不再变化 ④体
系的压强不再变化 ⑤气体密度不再变化 ⑥3 v (B)=2 v (C) ⑦单位时间内消耗1 mol A(g)的同时生成
正 逆
3 mol C(g)
A. ①②⑥ B. ①②③⑤ C. ②③④⑤ D. ①②④⑤⑦
【答案】A
【解析】
【分析】反应达到平衡状态时,正逆反应速率相等,平衡时各种物质的物质的量、浓度等不再发生变化。
【详解】①体系温度不再变化,说明正逆反应速率相等,反应达到平衡状态,故①符合题意;
②外界条件不变时,A,B,C浓度不随时间变化,说明正逆反应速率相等,反应达到平衡状态,故②符合
题意;
③该反应前后气体物质的量相等,M = ,m和n均不变,故M 始终不变,气体平均分子量不
(平均) (平均)
再变化不能说明达到平衡,故③不符合题意;
④该反应前后气体物质的量相等,即分子总数保持恒定,故压强也保持恒定,压强不再变化不能说明达到
平衡,故④不符合题意;
⑤容器体积固定,反应物和生成物都是气体,故气体密度始终恒定,气体密度不再变化不能说明达到平衡,
故⑤不符合题意;
⑥反应速率3 v正(B)=2 v逆(C),描述了正、逆反应方向,且速率之比等于计量数之比,故能说明达到平衡,
故⑥符合题意;
⑦单位时间内消耗1 mol A(g)的同时生成3 mol C(g),只描述了正反应反方向,故不能说明达平衡,故⑦不符合题意。
综上分析,能说明达到平衡的有①②⑥。
答案选A。
【点睛】本题考查化学平衡状态的判断,明确化学平衡状态的特征为解答关键,试题培养了学生的灵活应
用能力。
4. 溶液与 溶液发生反应:
,达到平衡。下列说法不正确的是
A. 加入苯,振荡,平衡正向移动
B. 经苯2次萃取分离后,在水溶液中加入 ,溶液呈血红色,表明该化学反应存在限度
C. 加入 固体,平衡逆向移动
D. 该反应的平衡常数
【答案】D
【解析】
【详解】A.加入苯振荡,苯将I 萃取到苯层,水溶液中c(I)减小,平衡正向移动,A正确;
2 2
B.将5mL0.1mol/LKI溶液与1mL0.1mol/LFeCl 溶液混合,参与反应的Fe3+与I-物质的量之比为1:1,反应后
3
I-一定过量,经苯2次萃取分离后,在水溶液中加入KSCN溶液呈血红色,说明水溶液中仍含有Fe3+,即
Fe3+没有完全消耗,表明该化学反应存在限度,B正确;
C.加入FeSO 固体溶于水电离出Fe2+,c(Fe2+)增大,平衡逆向移动,C正确;
4
D.该反应的平衡常数K= ,D错误;
答案选D。
5. 下列是教材中常规电化学示意图,其标注完全正确的是( )
A. B.C D.
.
【答案】D
【解析】
【详解】A. 该装置中发生的反应为Zn+2H+=Zn2++H ↑,Zn发生失电子的氧化反应,为负极,铜为正极,
2
故A错误;
B. 该原电池装置中,Zn电极所在的电解质溶液应为ZnSO 溶液,Cu电极所在的电解质溶液应为CuSO 溶
4 4
液,故B错误;
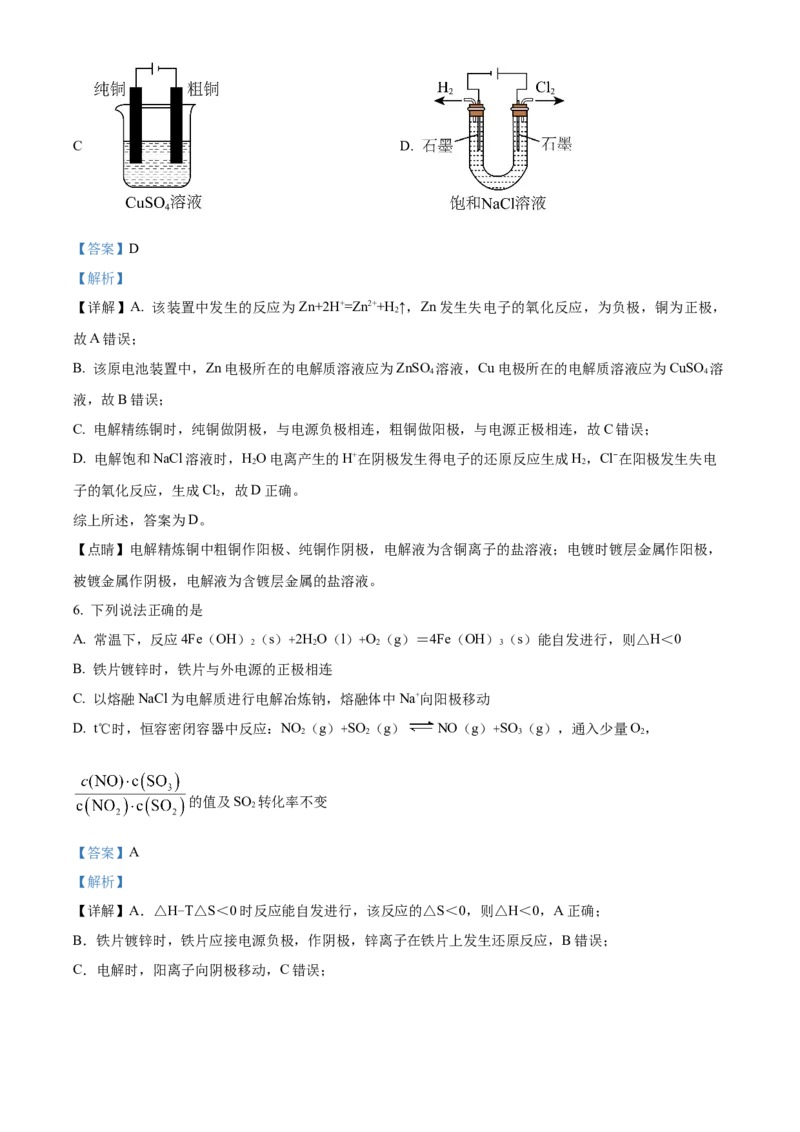
C. 电解精练铜时,纯铜做阴极,与电源负极相连,粗铜做阳极,与电源正极相连,故C错误;
D. 电解饱和NaCl溶液时,HO电离产生的H+在阴极发生得电子的还原反应生成H,Cl−在阳极发生失电
2 2
子的氧化反应,生成Cl,故D正确。
2
综上所述,答案为D。
【点睛】电解精炼铜中粗铜作阳极、纯铜作阴极,电解液为含铜离子的盐溶液;电镀时镀层金属作阳极,
被镀金属作阴极,电解液为含镀层金属的盐溶液。
6. 下列说法正确的是
A. 常温下,反应4Fe(OH)(s)+2HO(l)+O(g)=4Fe(OH)(s)能自发进行,则△H<0
2 2 2 3
B. 铁片镀锌时,铁片与外电源的正极相连
C. 以熔融NaCl为电解质进行电解冶炼钠,熔融体中Na+向阳极移动
D. t℃时,恒容密闭容器中反应:NO (g)+SO (g) NO(g)+SO (g),通入少量O,
2 2 3 2
的值及SO 转化率不变
2
【答案】A
【解析】
【详解】A.△H-T△S<0时反应能自发进行,该反应的△S<0,则△H<0,A正确;
B.铁片镀锌时,铁片应接电源负极,作阴极,锌离子在铁片上发生还原反应,B错误;
C.电解时,阳离子向阴极移动,C错误;D.通入氧气与NO反应,c(NO)减小,平衡正向移动,SO 转化率增大, 是平衡常数,
2
温度不变,平衡常数不变,D错误。
答案选A。
7. 全世界每年因钢铁锈蚀造成了巨大的损失,下列有关说法不正确的是
A. 钢铁腐蚀时化学能不能全部转化为电能
B. 钢铁腐蚀的负极反应式为Fe-2e-=Fe2+
C. 如图所示,将导线与金属锌相连可保护地下铁管
D. 如图所示,将导线与外接电源的正极相连可保护地下铁管
【答案】D
【解析】
【详解】A. 钢铁腐蚀时,化学能不能全部转化为电能,还转化为热能,故A正确;
B.钢铁腐蚀时,铁作负极被损耗,电极反应式为Fe-2e-=Fe2+,故B正确;
C.锌的金属性强于铁,锌、铁和电解质溶液可形成原电池,锌作负极,铁作正极,锌的腐蚀可保护地下
铁管,故C正确;
D.采用外加电流的阴极保护法时,被保护金属与直流电源的负极相连,与外加直流电源的正极相连,地
下铁管作阳极,更易被腐蚀,故D错误;
故选D。
【点睛】地下铁管易被腐蚀是因为在潮湿的土壤中形成了原电池而被腐蚀,要保护地下铁管不被腐蚀,则
钢管应该与电源的负极相连或作原电池的正极。
8. 为减缓钢铁设施在如图所示的情境中腐蚀速率,下列说法正确的是
A. 此装置设计符合电解池的工作原理B. 金属 的还原性应该比 的还原性弱
C. 当水体环境呈较强酸性时,钢铁设施表面会有气泡冒出
D. 当水体环境呈中性时,发生的反应有
【答案】C
【解析】
【分析】
【详解】A.该装置为牺牲阳极的阴极保护法,符合原电池的工作原理,A错误;
B.金属 的还原性应该比 的还原性强,才能优先失去电子,从而保护铁不被腐蚀,B错误;
C.当水体环境呈较强酸性时,H+向钢铁设施一极移动,得到电子生成氢气,钢铁设施表面会有气泡冒出,
C正确;
D.当水体环境呈中性时,发生吸氧腐蚀,O 得到电子,反应为 ,D错误;
2
答案选C。
9. 设N 为阿伏加德罗常数的值。已知反应:
A
(1)CH (g)+2O(g)=CO(g)+2HO(l) △H=akJ/mol
4 2 2 2
(2)CH (g)+2O(g)=CO(g)+2HO(g) △H=bkJ/mol 其。他数据如表:
4 2 2 2
化学键 C‒O O‒O C‒H O‒H
键能/(kJ•mol‒1) 798 x 413 463
下列说法正确 的是( )
A. 上表中x=
B. HO(g)=HO(l)的△S<0,△H=(a-b)kJ/mol
2 2
C. 当有4N 个C‒H键断裂时,反应放出的热量一定为akJ
A
D. a>b且甲烷燃烧热为bkJ/mol
【答案】A
【解析】
【详解】A.根据反应热键能计算,反应(2)的 △H=
,解得x=
,A项正确;B.根据盖斯定律,由反应 可得:HO(g)=HO(l) △H= kJ/mol,水从气态到液态、从液态
2 2
到固态的变化均是熵减的过程,故正反应为熵减小的反应,B项错误;
C.当有4N 个C‒H键断裂时,1molCH 反应,若生成HO(l)放出akJ热量,若生成HO(g),则放出bkJ热
A 4 2 2
量,C项错误;
D.CH 燃烧为放热反应,a、b均小于零。且反应物相同时,生成同种液态物质放出的热量比生成等量的
4
气态物质放出的热量多,故a<b。根据燃烧热的定义,燃烧热所生成的产物一定是稳定的。则水应为液态,
故甲烷燃烧热为akJ/mol;D项错误;
答案选A。
10. 已知常温下 溶液 ,说法正确的是
A. 溶液中:
.
B 溶液中:
C. 溶液中:
D. 溶液中加入少量 溶液发生反应:
【答案】B
【解析】
【分析】
溶液中存在平衡, 、 、
,由于常温下 溶液 ,说明电离大于水解,
据此解答问题。
【详解】A.溶液中 会发生水解和电离,因此 ,A错误;
B.由上述分析可知, 溶液中 的电离大于水解,但电离、水解均是少量的,因此
,B正确;C.溶液中存在电荷守恒: ,C错误;
D.溶液中加入少量 溶液发生反应: ,D错误;
答案选B。
11. 某温度下,恒容密闭容器中进行可逆反应:X(g) + Y(g) 2Z(g) + W(s) ΔH>0,下列说法正确的
⇌
是
A. 容器中混合气体的平均摩尔质量不再变化时,反应达到平衡
B. 平衡后加入 X,平衡正向移动,X、Y 的转化率均增大
C. 平衡后升高温度,平衡正向移动,ΔH 增大
D. 平衡后加入少量 W,逆反应速率增大
【答案】A
【解析】
【详解】A.该反应前后气体总质量减小,混合气体的物质的量不变,则混合气体平均摩尔质量在反应前
后减小,当容器中混合气体的平均摩尔质量不再变化时,正逆反应速率相等,反应达到平衡状态,故A正
确;
B.平衡后加入X,平衡正向移动,但是消耗X的增加量小于加入X的量,所以X转化率减小,但是Y转
化率增大,故B错误;
C.焓变只与反应物和生成物能量差有关,与反应条件、平衡移动方向无关,故C错误;
D.W是固体,不影响化学反应速率,所以平衡后加入少量W,逆反应速率不变,故D错误;
故答案选A。
12. 已知:2CO(g)+O(g) =2CO (g) ΔH=−566 kJ·mol−1;NaO(s)+CO(g) = Na CO(s)+ O(g) ΔH=−226
2 2 2 2 2 2 3 2
kJ·mol−1
根据以上热化学方程式和图象判断,下列说法正确的是
A. CO的燃烧热为283 kJ
B. 上图可表示由1 mol CO生成CO 的反应过程和能量关系
2C. 2NaO(s)+2CO(s)=2Na CO(s)+O(g) ΔH < −452 kJ·mol−1
2 2 2 2 3 2
D. 根据以上热化学方程式可以求算NaO(s)+CO(g)=Na CO(s)的反应热
2 2 2 3
【答案】D
【解析】
【详解】A. CO的燃烧热为283 kJ·mol−1,单位错了,A错误;
B.图中的CO(g)+O2(g)系数不等于方程式的化学计量数,不能表示由1 mol CO生成CO 的反应过程和能
2
量关系,B错误;
C.ΔH跟化学计量数成正比,化学计量数扩大2倍,ΔH也扩大2倍,ΔH变为−452 kJ·mol−1,但是选项中
CO 为固态,变化为气体二氧化碳需要吸热,焓变放热是负值,ΔH −452 kJ·mol−1,C错误;
2
D.根据盖斯定律,式① 式②可以求出Na
2
O
2
(s)+CO(g)=Na
2
CO
3
(s>)的反应热,D正确;故选D。
13. 部分弱酸的电离平衡÷常2数+如表所示:
弱酸 HCOOH HCN HCO HSO
2 3 2 3
K =4.3×10-7 K =1.54×10-2
a1 a1
电离平衡(25℃) K=1.77×10-4 K=4.9×10-10
a a
K =5.6×10-11 K =1.02×10-7
a2 a2
下列选项错误的是( )
A. 等体积等浓度的HCOONa和NaCN溶液中所含阴离子总数前者大于后者
B. 少量SO 通入NaCO 溶液中:SO +H O+ = +H CO
2 2 3 2 2 2 3
C. 中和等体积等pH的HCOOH和HCN消耗NaOH的量前者小于后者
D. CN-+H O+CO=HCN+
2 2
【答案】B
【解析】
【详解】A. 电离平衡常数HCOOH> HCN则酸性:HCOOH >HCN,等体积等浓度的HCOONa和NaCN溶
液中pH,HCOONaNaCN,由电荷守恒
, 可知,所含阴离子总数前者大
于后者,故A正确;
B. 由HSO 和HCO 电离平衡常数可知,则酸性 ,所以少量SO 通入
2 3 2 3 2
NaCO 溶液中发生反应:SO +H O+ = + ,故B错误;
2 3 2 2
C. 等pH的HCOOH和HCN溶液,酸的物质的量:HCOOHc(H+),所以c(Na+)>c(Cl−)
+c(ClO−),故C错误;
D.G点为完全反应生成NaClO,溶液呈碱性,ClO−水解,新制氯水中起始时是等量的HCl和HClO,所以
有c(Na+)>c(Cl-)>c(ClO-)>c(OH- )>c(H+),故D正确。
故答案选:D。
16. 可逆反应mA(固)+nB(气) pC(气)+qD(气),反应过程中其它条件不变时C的百分含量C%
⇌
与温度(T)和压强(P)的关系如图所示,下列叙述中正确的是A. 达到平衡后,使用催化剂,C%将增大
B. 达到平衡后,若升高温度、化学平衡向逆反应方向移动
C. 方程式中n>p+q
D. 达到平衡后,增加A的量有利于化学平衡向正反应方向移动
【答案】B
【解析】
【详解】可逆反应,当其他条件一定时,温度越高,反应速率越大,达到平衡所用的时间越短。由图象(1)可知
T>T,温度越高,平衡时C的体积分数φ(C)越小,故此反应的正反应为放热反应;
1 2
当其他条件一定时,压强越高,反应速率越大,达到平衡所用的时间越短。由图(2)可知P>P ,压强越大,
2 1
平衡时C的体积分数φ(C)越小,可知正反应为气体物质的量增大的反应,即n
【解析】 ⋅
【分析】(1)液态肼与液态四氧化二氮反应生成氮气和液态水的方程式为2NH(l)+N O(l)=3N (g)
2 4 2 4 2
+4H O,3.2g液态肼即0.1molNH 完全反应放出热量61.25kJ,则2molN H 完全反应放出热量
2 2 4 2 4
61.25kJ×20=1225kJ,结合物质的凝聚状态写出热化学方程式;
(2)①反应达到平衡状态时,正逆反应速率相等,各物质的浓度、含量不变,以及由此衍生的一些量也不
发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到不变时,
说明可逆反应到达平衡状态;
②若起始充入4.00molN 和12.00molH 是充入2.00 molN 和6.00 molH 的2倍,相当加压、反应速率加快、
2 2 2 2
达到平衡状态的时间缩短,但合成氨的正反应是气体体积减小的反应,增大压强、平衡正向移动,据此分
析解答;
(3)①根据v= 计算0~20min时,v(NO);
2 4②反应达到平衡时,v (NO )=2v (NO),即k•c2(NO )=2k•c(NO),所以 =2×
正 2 逆 2 4 1 2 2 2 4
=2K,根据反应三段式计算平衡时[φ(NO )=0.4]各物质的平衡浓度,代入平衡常数K= 中计算
2
K;该反应正向放热,升高温度,K减小,降低温度K增大。
【详解】(1)液态肼与液态四氧化二氮反应生成氮气和液态水的方程式为2NH(l)+N O(l)=3N (g)+4HO
2 4 2 4 2 2
(l),3.2g液态肼即0.1molNH 完全反应放出热量61.25kJ,则2molN H 完全反应放出热量
2 4 2 4
61.25kJ×20=1225kJ,热化学方程式为
;
(2)①a.3v正(N )=v逆(H )的状态是平衡状态,所以v正(N )=v逆(H )的状态不是平衡状态,故a错误;
2 2 2 2
b.该反应正向体积减小,恒温恒容条件下,反应正向进行、气体物质的量减小、压强降低,所以体系压强
不变时达到平衡状态,故b正确;
c.体系中各物质均为气体,气体质量不变,该反应正向体积减小,恒温恒容条件下,反应正向进行、气体
物质的量减小,气体平均相对分子质量增大,所以气体平均相对分子质量不变时达到平衡状态,故c正确;
d.体系中各物质均为气体,气体质量不变,恒温恒容条件下,气体密度始终不变,所以气体密度不变不能
判定反应达到平衡状态,故d错误;
故答案为:bc;
②由图可知,将2.00molN 和6.00molH 充入1L密闭容器中,达到平衡时,c(H)=3mol/L,即E点;若起始
2 2 2
充入4.00molN 和12.00molH,是恒容容器中充入的2.00 molN 和6.00 molH 的2倍,相当于加压过程、反
2 2 2 2
应速率加快、先达到平衡状态,但加压时平衡正向移动,使c(H)小于6mol/L,故为B点;
2
故答案为:B;
(3)①设 c(NO)=x,2NO (g) NO(g),则 c(NO )=2x,起始时c(NO )=0.2mol/L,20min时
2 4 2 2 4 2 2
△ ⇌ △
[φ(NO )]=0.75,即 =0.75,x=0.04mol/L,0∼20min时,
2
v(N O)=0.04mol/L 20min=2×10−3mol/(L⋅min);
2 4
÷
②平衡时φ(NO )=0.4, =0.4,y=0.075mol/L,平衡常数K= = =30,反应达
2
到平衡时,v正(NO )=2v逆(N O),即k·c2(NO )=2 k·c(NO),所以 =2× =2K =60,
2 2 4 1 2 2 2 4
2NO
2
(g)⇌N
2
O
4
(g)△H=−56.9kJ⋅mol−1,升高温度平衡常数减小,T
1
时k
1
=k
2
,则 =1=2K′,平衡常数
K′=0.5<30,所以T>373K;
1
故答案为:60;>。
20. 实验室以天青石精矿(主要含SrSO ,还含有少量SiO、CaSO、BaSO)为原料制取SrSO ,其实验流程
4 2 4 4 4
如下:
(1)室温下,反应SrSO (s)+CO (aq) SrCO (s)+SO (aq)达到平衡,则反应的平衡常数为
4 3
____[K (SrSO )=3.2×10−7,K (SrCO )=5.6×10−10]。
sp 4 sp 3
(2)浸取天青石精矿时,向NH HCO 溶液中加入适量浓氨水的目的是____。“浸取Ⅰ”的条件是温度在
4 3
60~70℃、搅拌、反应3小时,温度过高将会导致SrSO 的转化率下降,其原因是____。
4
(3) “焙烧”所得SrO粗品用蒸馏水多次浸取得Sr(OH) 溶液。判断SrO粗品已经浸取完全的方法:____。
2
(4) “沉淀”过程中除得到SrSO 外,还得到一种可循环利用的物质,该物质为____。
4
(5)将SrSO 与煤粉按照一定比例混合后煅烧得到一种黑灰(SrS)。
4
①写出生成SrS的化学反应方程式:____。
②设计以黑灰为原料,制取SrSO 的实验方案:____。
4
(已知:SrS易溶于水,易水解。水浸时的浸取率随温度变化如下图。实验中锶元素需充分转化SrSO ,必
4
须使用的试剂:蒸馏水、3mol·L-1HSO 和NaOH溶液)。
2 4【答案】 ①. 571.4 ②. 将HCO 转化为CO ,增大溶液中CO 的浓度 ③. 温度过高将会导致
NH HCO 的分解及氨水的分解挥发 ④. 取最后一次浸取液,向其中滴加几滴酚酞,溶液不变红 ⑤.
4 3
氨水 ⑥. SrSO +2C=SrS+2CO↑(或SrSO +4C=SrS+4CO↑) ⑦. 取适量的黑灰用90℃的热水浸取
4 2 4
2~3次,将产生的气体用NaOH溶液充分吸收,所得浸取液合并后滴加稍过量的3mol·L-1HSO ,将所得沉
2 4
淀过滤、洗涤、烘干
【解析】
【分析】天青石精矿(主要含SrSO ,还含有少量SiO、CaSO、BaSO),加入碳酸氢铵溶液和氨水浸取,
4 2 4 4
可将SrSO 转化为SrCO ,过滤后滤渣含有SiO、CaCO 、BaSO、SrCO 滤液中含有NH ,滤渣经过焙烧,
4 3 2 3 4 3
“焙烧”所得SrO粗品用蒸馏水多次浸取得Sr(OH) 溶液,再和第一步浸取的滤液反应生成SrSO ,以此解答。
2 4
【详解】(1)室温下,反应SrSO (s)+CO (aq) SrCO (s)+SO (aq)达到平衡,则溶液中 =
4 3
= =571.4,故答案为:571.4;
(2)一水合氨可以和碳酸氢根反应生成碳酸根,浸取天青石精矿时,向NH HCO 溶液中加入适量浓氨水的
4 3
目的是:将HCO 转化为CO ,增大溶液中CO 的浓度;NH HCO 加热易分解,温度过高将会导致
4 3
NH HCO 的分解及氨水的分解挥发,所以“浸取Ⅰ”的条件是温度在60~70℃、搅拌、反应3小时,温度过
4 3
高将会导致SrSO 的转化率下降,故答案为:将HCO 转化为CO ,增大溶液中CO 的浓度;温度过高
4
将会导致NH HCO 的分解及氨水的分解挥发;
4 3
(3) SrO粗品已经浸取完全时,浸取后的溶液中不再有Sr(OH) ,取最后一次浸取液,向其中滴加几滴酚酞,
2
溶液不变红说明浸取完全,故答案为:取最后一次浸取液,向其中滴加几滴酚酞,溶液不变红;(4)第一步浸取滤液中含有NH ,在沉淀过程中会生成NH HO,可循环利用,故答案为:氨水;
3 2
(5)①SrSO 与C发生氧化还原反应生成SrS和二氧化碳或一氧化碳,根据得失电子守恒和质量守恒配平方
4
为
程式 :SrSO +2C=SrS+2CO↑(或SrSO +4C=SrS+4CO↑),故答案为:SrSO +2C=SrS+2CO↑(或
4 2 4 4 2
SrSO +4C=SrS+4CO↑);
4
②由图可知,90℃是Sr(OH) 的浸取率最高,取适量的黑灰用90℃的热水浸取2~3次,将产生的气体用
2
NaOH溶液充分吸收,所得浸取液合并后滴加稍过量的3mol·L-1HSO ,将所得沉淀过滤、洗涤、烘干,
2 4
故答案为:取适量的黑灰用90℃的热水浸取2~3次,将产生的气体用NaOH溶液充分吸收,所得浸取液合
并后滴加稍过量的3mol·L-1HSO ,将所得沉淀过滤、洗涤、烘干。
2 4