文档内容
1
学科网(北京)股份有限公司2
学科网(北京)股份有限公司3
学科网(北京)股份有限公司4
学科网(北京)股份有限公司5
学科网(北京)股份有限公司6
学科网(北京)股份有限公司7
学科网(北京)股份有限公司8
学科网(北京)股份有限公司2024 年高三 9 月起点考试高三化学试题答案和给分标准
1-15.(每题 3分,共45分)
1.D 2.A 3.D 4.B 5.C 6.A 7.C 8.D 9.B 10.C
11.C 12.B 13.D 14.A 15.C
16.(共14分)
(1) 3d74s2 (1分) 第四周期VIII 族 (2 分,周期和族各 1分,不互相牵连)
+3 (1 分)
(2)abc (2分,选对两个得 1分,有错或只选对 1个 0分)
(3) 2LiCoO +H C O +8Cl 6H+ 2 CoCl 2 2CO +4H O+2Li (2分,
2 2 2 4 4 2 2
要么0分要么 2分)
(4) 9.44×10-3 (2 分,没有用科学计数法或者没有保留 3位有效数字者不得分)
(5) 1:4 (2 分) 降低反应温度或带走过多热量,反应速率减慢 (2 分,合
理即得分)
17. (共14分)
(1) CH (g) +CO (g) 2CO(g) + 2H (g) ΔH=+247.4kJ·mol-1 (2 分,ΔH 的值
4 2 2
没有标明正号者不扣分,无单位或者没配平、没写状态者无分)
(2) ① 0.025(2 分) ② AC (2 分,只写对一个得 1分,有错者无分)
(3) ①< (2 分) ② (2 分)
k k
(4) ①< (2 分) ② 1 3 (2 分)
k k
2 4
{#{QQABCYAAoggIQJBAARgCQwmICAKQkAGACQgOwBAEIAAAgAFABAA=}#}18.(共13分)
(1) CuH O Cu(OH) (2 分,没有沉淀符号者得 1分) ; Cu2e Cu2(1 分)
2 2 2
(2) CuH O H SO CuSO 2H O(2分,若写成离子方程式,写对了,得 1分);
2 2 2 4 4 2
产生的铜离子催化了过氧化氢分解 (1分)
(3) 对于 Cu2e Cu2,加入氨水,氨水与 Cu2形成 CuNH
2
,使c
Cu2
减小,
3 4
提高了Cu的还原性 (2 分,合理即得 2分);
向U型管右侧溶液中滴加硫酸(1 分,没说清楚是右侧者不得分)
(4) 在还原反应或氧化反应(半反应)中,增大反应物浓度或降低生成物浓度,氧
化剂(还原剂)的氧化性(还原性)增强。(2 分,合理即得 2分)
(5) 溶解度AglAgBrAgCl, I、 Br、Cl均可使氧化反应Age Ag中的c Ag
降低,提高Ag的还原性,其中只有 I能使Ag的还原性提高到能将 H还原。(2
分,合理即得 2分)
19.(共14分)
(1) 间甲基苯酚(或3-甲基苯酚)(2 分) 9(2 分)
(2)b(2 分)
(3)保护氨基(使其暂不参加反应,只让酚羟基参加反应)(2 分,合理即得 2分)
(4) 或 (CH ) NCH CH Cl(2 分)
3 2 2 2
(5) N HCl(各1分,共 2分,不互相牵连)
2
(6)
(2分,没写条件不扣分,方程式有错者不得分)
{#{QQABCYAAoggIQJBAARgCQwmICAKQkAGACQgOwBAEIAAAgAFABAA=}#}2024 年高三 9 月起点考试高三化学试题答案详解
1.【答案】D
【详解】A.丙烷、丁烷等燃烧热值高、化学性质稳定,能够在不同环境下稳定燃烧。A正
确,不符合题意;
B.麻黄碱、杜冷丁、吗啡等属于国际奥委会规定的违禁药物。有的直接刺激中枢神经系统,
提高运动表现;有的可以缓解疼痛,但会抑制神经系统;有的像雄性激素的衍生物,有助于
肌肉生长和恢复。兴奋剂的滥用破坏了体育竞赛的公平性,对运动员的身心健康造成极大的
危害。绝大多数复方感冒制剂、止咳平喘药以及部分胃肠系统药里都含有麻黄碱成分,其含
量没有超出国家规定标准,可在医生指导下合理用药。B正确,不符合题意;
C.合成纤维是运动装备中最常见的化学材料之一。例如,聚酯纤维(如涤纶)因其良好的
弹性、耐磨性和抗皱性而被广泛用于运动服装和运动鞋的制造。C正确,不符合题意;
D.钢材是由铁和碳等元素组成的合金,具有高强度、耐磨损、耐腐蚀等特性。混凝土
是由水泥、骨料(如砂、石等)和水按照一定比例混合而成的。玻璃的主要成分是硅酸盐和
二氧化硅的混合物。D错误,符合题意;
综上所述,本题选D。
2.【答案】A
【详解】A.H S属于二元弱酸,应该分步电离:H S H++HS- ,HS- H++S2- 。A
2 2
选项描述错误,符合题意;
B.HCl中的共价键是由氢原子提供的未成对电子的1s原子轨道和氯原子提供的未成对电子
的3p原子轨道“头碰头”重叠而成s-pσ键。B选项描述正确,不符合题意;
C.2p 与2p 两个原子轨道能层均为L层,能级均为2p亚层,原子轨道的能量一样只不过
x y
空间伸展方向不同,1s22s22p 1→ls22s22p 1过程中不存在电子由较高能级跃回到较低能级释
x y
放能量的可能,故不能形成发射光谱。C选项描述正确,不符合题意;
D.N,N-二甲基苯甲酰胺的结构简式正确。D选项描述正确,不符合题意;
综上所述,本题选A。
3. 【答案】D
【详解】A.乙醇与水的沸点本身比较接近,当乙醇中含有少量水时更是会形成共沸混合液,
形成的液体具有恒定沸点,不能用蒸馏的方法将二者分离。应该先加入氧化钙进行加热回流,
再进行蒸馏可得99.5%的无水酒精。A选项描述错误;不符合题意
B.重结晶是提纯固体有机物常用的方法。乙酸乙酯为液体,去除其中含有的少量乙酸可以
1
{#{QQABCYAAoggIQJBAARgCQwmICAKQkAGACQgOwBAEIAAAgAFABAA=}#}先加入饱和碳酸钠溶液,充分振荡后再进行分液等操作进行提纯。B选项描述错误;不符合
题意;
C.去除硝酸钾中少量食盐,应该利用氯化钠的溶解度随温度升高变化极小,而硝酸钾的溶
解度随温度升高急剧增大的性质区别。将样品配成溶液,蒸发浓缩至液体表面出现晶膜,缓
慢降温结晶(所得晶体为大块的硝酸钾晶体,氯化钠杂质以离子形式存在于滤液中),随后
进行过滤洗涤等其他操作。C选项描述错误;不符合题意;
D.在选三教材62页彩图3-12可看到苯酚钠滴入盐酸后产生的苯酚为液态和NaCl水溶液
不互溶。虽然苯酚熔点为43℃,但在水溶液中,苯酚中含水,熔点下降,含水苯酚常温下
为液体,故应用分液的方法分离。D选项描述正确,符合题意;
综上所述,本题选D。
4.【答案】B
【详解】A.用FeS固体除去污水中的Hg2+,反应生成更难溶的HgS,反应离子方程式为
FeSHg2 HgSFe2。A选项错误;不符合题意;
B.某管道疏通剂遇水苛性钠溶解生成氢氧化钠同时大量放热,铝粉与热的氢氧化钠溶液剧
烈反应,对应离子方程式为: 。B选项正确,
符合题意;
C.乙醛和新制Cu(OH) 共热出现Cu O砖红色浑浊,反应方程式为
2 2
CH CHO2CuOH NaOHCH COONaCu O3H O 。C选项错误,不符合题意;
3 2 3 2 2
D.乙醇中的碳碳单键比较牢固。乙醇被酸性高锰酸钾氧化生成的不是二氧化碳而是乙酸,
(教材必修二79页),正确的方程式为:5CH CH OH+4KMnO +6H SO 5CH COOH
3 2 4 2 4 3
+4MnSO +2K SO +11H O。D选项错误,不符合题意;
4 2 4 2
综上所述,本题选B。
5.【答案】C
【分析】由图可知,a为H S,b为S,c为SO ,d为SO ,e为H SO ,f为NH ,g为NO,
2 2 3 2 4 3
h为NO ,i为HNO 以此解题;
2 3
【解析】A.二氧化硫和二氧化氮同时通入水中,会生成硫酸,加入氯化钡会生成硫酸钡白
色沉淀.A推断合理,不符合题意;
B.c为SO ,d为SO 。SO 与过氧化钠会生成硫酸钠和氧气;过氧化钠有强氧化性,与SO
2 3 3 2
也会有硫酸钠生成。B推断合理,不符合题意;
2
{#{QQABCYAAoggIQJBAARgCQwmICAKQkAGACQgOwBAEIAAAgAFABAA=}#}C.e的浓溶液(浓硫酸)具有强氧化性和酸性会与还原性气体a(H S)和f(NH )反应,但是气体
2 3
c(SO )中硫元素化合价与浓硫酸中硫的价态相邻,不能发生氧化还原反应,故SO 可以用浓
2 2
硫酸来干燥。C推断不合理,符合题意;
D.i 的浓溶液(浓硝酸)有强氧化性,常温下遇金属铝、铁发生“钝化”现象,因而无剧烈
反应。D推断合理,不符合题意;
综上所述,本题选C。
6.【答案】A
【详解】A.VSEPR模型是价层电子对的空间结构模型,而分子的空间结构指的是成键电
子对的空间结构,不包括孤电子对,当中心原子无孤电子对时,两者空间结构相同,当中心
原子有孤电子对时,两者空间结构不同。A正确;符合题意;
B.元素的性质随着原子序数的递增呈现周期性的变化,这一规律叫元素周期律,元素性质
的周期性的变化是元素原子的核外电子排布周期性变化的必然结果。B错误;不符合题意;
C.化合物具有相同分子式,但是据有不同结构的现象称为同分异构现象。C错误;不符合
题意;
D.气态中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量叫作第一电离
能。第一电离大小与元素的金属性、非金属性没有必然联系,比如镁的第一电离能比铝要高,
事实上镁的金属性比铝要强。D错误,不符合题意;
综上所述,本题选A。
7.【答案】C
【详解】A.H O分子间存在氢键会使得H O的沸点较高,H O很稳定是因为氧氢键键能较
2 2 2
大,两者不存在对应因果关系。A错误,不符合题意;
B.HClO具有强氧化性,能使蛋白质变性,可作杀菌消毒剂,与其具有酸性无关。B错误,
不符合题意;
C.三氟乙酸中的-CF 与乙酸中的-CH 相比是吸电子基,吸电子效应使羧基中羟基极性增大,
3 3
三氟乙酸的酸性强于乙酸。C正确,符合题意;
D.可溶性钡离子有剧毒,可以导致蛋白质变性,破坏人体中各种酶,使一系列生理活动被
破坏,BaSO 可用作“钡餐造影剂”是因为BaSO 难溶于水且不溶于胃里的强酸。D错误,
4 4
不符合题意;
综上所述,本题选C。
8.【答案】D
3
{#{QQABCYAAoggIQJBAARgCQwmICAKQkAGACQgOwBAEIAAAgAFABAA=}#}【详解】A.该有机物结构简式含有酯基、羟基、碳碳双键3种官能团。A正确,不符合题
意;
B.有机物M中 标有红色五角星的三处的碳原子为手性碳原子。B正确,不
符合题意;
C.有机物M一个羟基氢可与酯基的氧原子形成分子内氢键,由于有机物M含有羟基,也
可以形成分子间氢键。C正确,不符合题意;
D.有机物M中的酯基可与氢氧化钠水溶液反应,醇羟基不能反应。D错误,符合题意;
综上所述,本题选D。
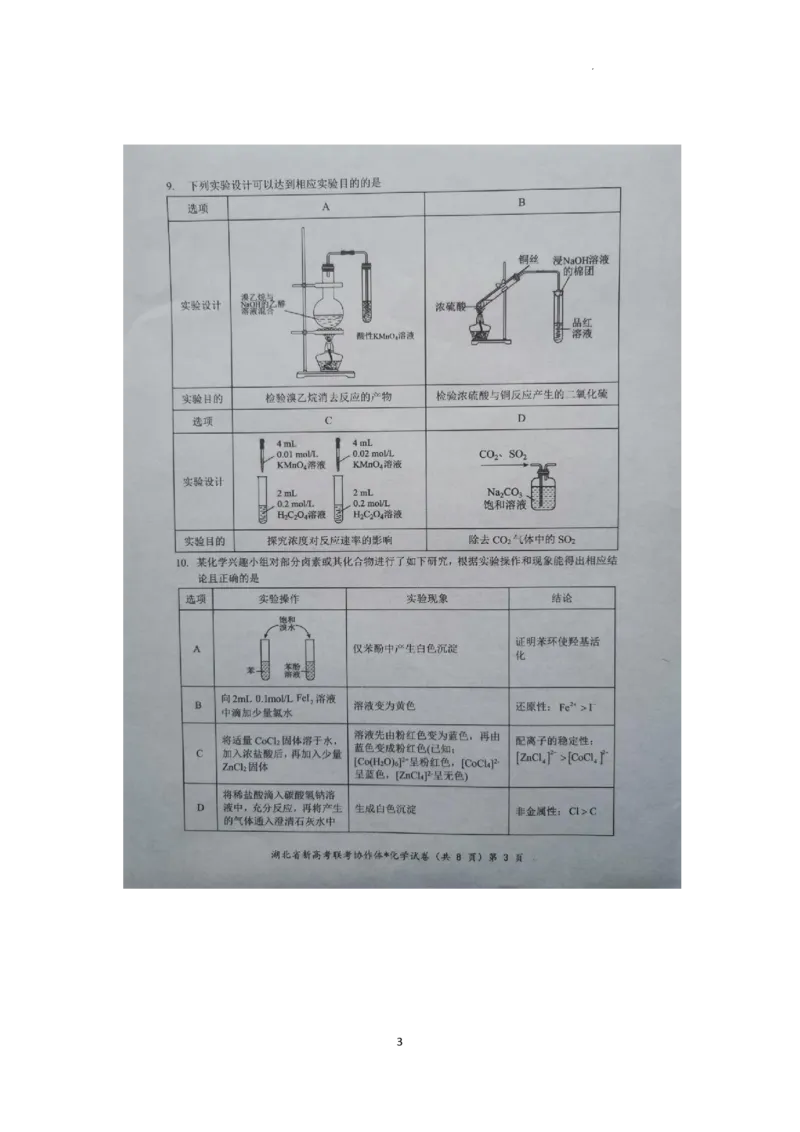
9.【答案】B
【详解】A.溴乙烷与氢氧化钠的乙醇溶液共热发生消去反应的产物是乙烯,可使酸性高锰
酸钾溶液褪色,但是乙醇有挥发性,也可以使酸性高锰酸钾溶液褪色,对实验目的有干扰。
A不能达到相应实验目的,不符合题意;
B.图示的装置及药品来自教材原图,可检验浓硫酸与铜反应产生的二氧化硫,B符合题意;
C.本实验设计没有很好的实现变量控制。依据高锰酸钾紫红色褪色快慢来判断反应的快慢
就应该让两试管中高锰酸钾溶液的浓度一样,而去设置不同草酸溶液的浓度。C 不能达到
相应实验目的,不符合题意;
D.饱和Na CO 溶液既能吸收SO 也能吸收CO ,用饱和Na CO 溶液除去CO 气体中的
2 3 2 2 2 3 2
SO 可能导致CO 损失。D不能达到相应实验目的,不符合题意;
2 2
综上所述,本题选B。
10.【答案】C
【详解】A.该现象证明的是羟基使苯环活化,A不能得出相应结论,不符合题意;
B.碘水和含铁离子的溶液均显黄色,无法证明是Fe2+先被氧化,B对应的实验操作和现象
不能得出相应结论,况且该结论也不正确,B不符合题意;
C.溶液先由粉红色变为蓝色发生的反应为:Co(H O) 2 +4Cl- CoCl 2 +6H O ;
2 6 4 2
再由蓝色变成粉红色发生的反应为:CoCl 2 +Zn2++6H O Co(H O) 2 + ZnCl 2,
4 2 2 6 4
第二个反应说明配离子的稳定性: ZnCl 2 CoCl 2 ,C对应的实验操作和现象能得出
4 4
相应结论,C符合题意;
D.对应的实验操作和现象证明盐酸的酸性强于碳酸,但是不能推理出氯元素的非金属性比
碳强。如果用高氯酸溶液代替盐酸来做这个实验就可以。D对应的实验操作和现象不能得出
相应结论,D不符合题意;
综上所述,本题选C。
11.【答案】C
4
{#{QQABCYAAoggIQJBAARgCQwmICAKQkAGACQgOwBAEIAAAgAFABAA=}#}【分析】A、W、M、X、Y、Z六种主族元素,原子序数依次增大,W原子最外层电子数
是内层电子数的2倍,W是C,W与Z相邻,Z是Si,MA 常用作制冷剂,说明 M是N
3
元素,A是H元素,X是周期表中非金属性最强的元素,说明X是F。基态Y原子的s能级
与p能级电子数相等且原子序数比F原子的更大,(1s22s22p63s2),Y是Mg,据此作答。
【详解】A.N H 中N原子为sp3杂化,杂化轨道中s轨道占的分数为1/4;N H 中N原子
2 4 2 2
为sp2杂化,杂化轨道中s轨道占的分数为1/3,sp2-sσ键的键长短于sp3-sσ键的键长。A
正确,不符合题意;
B.NF 为三角锥形,极性分子,CF ,正四面体,非极性分子,所以分子的极性NF CF 。
3 4 3 4
B正确;不符合题意;
C.Mg和C的电负性相差大于Si,所以离子键成分的百分数Mg C>Mg Si。C错误,C符
2 2
合题意;
D.工业上用电解熔融氯化镁的方式来制取金属镁单质。D正确,不符合题意;
综上所述,本题选C。
12.【答案】B
【详解】A.由晶胞结构必须满足“无隙并置”的要求可知图示结构是一个晶胞。A正确,
不符合题意;
B.观察图示正中心的BH- ,距离BH- 最近的Na+有8个,该晶体中BH- 的配位数为8,那
4 4 4
么Na+的配位数也为8。B错误,符合题意;
C.由VSEPR理论知BH- 中B原子的价层电子对为4对,B原子采取等性sp3杂化,则BH-
4 4
为正四面体结构。C正确,不符合题意;
1 1 1 1
D.一个晶胞中:BH- 个数8 4 14,Na+个数4 6 4,N 为阿伏加德罗常
4 8 2 4 2 A
数的值,1nm=10-7cm,则硼氢化钠晶体的密度
nM 438
76
m N N 1021 g·cm-3。故D正确,不符合
A A a3N
V V a107cma107cm2a107cm A
题意。
综上所述,本题选B。
13.【答案】D
【分析】乙醛与氢氰酸(HCN,弱酸)能发生加成反应,氧原子的电负性较大,所以醛基中的
5
{#{QQABCYAAoggIQJBAARgCQwmICAKQkAGACQgOwBAEIAAAgAFABAA=}#}碳原子带部分正电荷,与CN-作用,产物结合氢离子,生成2-羟基丙腈,据此作答。
【详解】A.氧原子的电负性较大,电子对偏向O原子,则醛基中的碳原子带部分正电荷,
与CN-作用,故A正确;
B.2-羟基丙腈先后经历消去反应得到丙烯腈,再经过加聚反应可以生成腈纶(聚丙烯腈纤
维),故B正确;
C.对于间硝基苯甲醛,醛基的间位上连有吸电子基-NO 会使得醛基中的碳原子带有更多正
2
电荷,更有利于与CN-作用。对于间甲基苯甲醛,醛基的间位上连有供电子基-CH ,使得醛
3
基中的碳原子带有较少正电荷,不利于与CN-作用,故C正确;
D.酸性条件下利于生成HCN,HCN易挥发且有剧毒是原因之一。酸性条件下HCN很难
电离出较大浓度的CN-,第一步反应难以进行,故D错误,符合题意;
综上所述,本题选D。
14.【答案】A
【详解】A.乙醇不是电解质,并且乙醇会与金属钙反应,故A错误,符合题意;
B.原电池中,阳离子向正极移动,故Ca2向a极迁移,故B正确,不符合题意;
C.准状况下22.4LO 物质的量约为1mol,由图示可知,氧元素化合价从0价降低为-1价,
2
故1mol氧气得2mol电子,故理论上转移2mol电子,C正确,不符合题意;
1 2
D.单位质量的金属锂失去电子 比等质量的金属钙失去电子 多,故D正确,不符
7 40
合题意;
综上所述,本题选A。
15.【答案】C
【分析】在溶液中存在CH COOAg和CH COOH的电离平衡:
3 3
CH COOAg(aq)Ag+(aq)+CH COO-(aq)(①)、CH COOHCH COO-+H+(②),
3 3 3 3
Ag+的水解平衡Ag++H OAgOH+H+(③)。可以估算与①相比②③的平衡常数较小。随
2
着pH的增大,c(H+)减小,平衡②③正向移动,c(CH COOH)与c(Ag+)减小,c(CH COO-)增
3 3
大。对于①平衡移动的讨论:pH较小时(约小于7.8),c(CH COO-)增大的影响大于c(Ag+)
3
减小的影响,c(CH COOAg)增大;pH较大时(约大于7.8),c(CH COO-)增大的影响小于
3 3
Ag+浓度减小的影响,c(CH COOAg)减小,故线Ⅰ表示CH COOH的摩尔分数随pH变化的关
3 3
系,线Ⅱ表示CH COO-的摩尔分数随pH变化的关系,线Ⅲ表示CH COOAg随pH变化的关
3 3
系。
6
{#{QQABCYAAoggIQJBAARgCQwmICAKQkAGACQgOwBAEIAAAgAFABAA=}#}【详解】A.根据分析,线Ⅱ表示CH COO-的变化情况,A项正确,不符合题意;
3
B.由图可知,当c(CH COOH)=c(CH COO-)相等时(即线Ⅰ和线Ⅱ的交点),溶液的pH=m,
3 3
c(H+)c(CH COO-)
则CH COOH的电离平衡常数K = 3 =10-m,B项正确,不符合题意;
3 a
c(CH COOH)
3
c(H+)c(CH COO-) 10-mc(CH COOH)
C.pH=n时 3 =10-m,c(CH COO-)= 3 =10n-mc(CH COOH),
c(CH COOH) 3 c(H+) 3
3
CH COOAg(aq)Ag+(aq)+CH COO-(aq)的K= ,
3 3
c(Ag+) = ,由图可知pH=n时,c(CH COOH) =c(CH COOAg),代入
3 3
整理得c(Ag+)=K·10m-nmol/L,C项错误,符合题意;
D.pH=12时,如果AgOH没有大量沉淀且假设溶液体积没有增大,由物料守恒可得溶液中
c(Ag+)+c(CH COOAg)+c(AgOH)=0.08mol/L,那么:c(Ag+)+c(CH COOAg)<0.08mol/L,
3 3
况且上述两项假设均不成立,则D项正确,不符合题意;
综上所述,本题选C。
16.(14分)【答案】
(1) 3d74s2 (1分) 第四周期VIII族 (2分) +3(1分)
(2)abc(2分)
(3) 2LiCoO +H C O +8Cl6H+ 2 CoCl 22CO +4H O +2Li (2分)
2 2 2 4 4 2 2
(4) 9.44×10-3(2分)
(5) 1:4(2分) 降低反应温度,反应速率减慢 (2分)
【分析】氯化胆碱-草酸和LiCoO 微波共熔的过程中,Co被还原为+2价,经过水浸滤液中
2
Co以[CoCl ]2-存在,加入氢氧化钠沉钴,得到Co(OH) 沉淀和含有锂离子的溶液,Co(OH)
4 2 2
固体经过煅烧得到Co O 固体,含有锂离子的溶液中加入碳酸钠溶液生成碳酸锂沉淀,碳酸
3 4
锂和Co O 高温烧结(通入空气氧化)得到LiCoO 产品,以此分析解答。
3 4 2
【详解】(1)钴是27号元素,价层电子排布式为:3d74s2,Co在周期表中的位置为第四周
期VIII族,LiCoO 中Li为+1价,O为-2价,因此Co为+3价;
2
(2)由题中的介绍知道低共熔溶剂可以只溶解离子化合物不溶解杂质中的单质。其熔点低、
难挥发,与有大体积的阴阳离子的离子液体很相似。选择性必修2第89页介绍的离子液体
7
{#{QQABCYAAoggIQJBAARgCQwmICAKQkAGACQgOwBAEIAAAgAFABAA=}#}正是有机胺正离子和甲酸跟负离子,并且本题需要还原剂把+3价的钴还原为+2价,氯化胆
碱[HOCH CH N+(CH ) ·C1-]与草酸混合可以很好满足本题中低共熔溶剂的要求。故本题选
2 2 3 3
abc
(3)低共熔溶剂中含有一定量的草酸,草酸中的C为+3价,具有还原性,其作用为作为还
原剂,水浸”操作中得到较浓的滤液(pH=2)呈深蓝色的[CoCl ]2-,同时有CO 气体逸出,其
4 2
总离子方程式为2LiCoO +H C O +8Cl6H+ 2 CoCl 22CO +4H O +2Li
2 2 2 4 4 2 2
(4)常温下,K
sp
CoOH
2
1.61015,
c Co2
K
sp
CoOH
2
1.61015
mol/L1.6107mol/L
c
OH2
(
1014
)2
,
1010
Co2+的质量体积浓度为:
c(Co2)59103mg/L1.610759103mg/L9.44103mg/L
(5)碳酸锂和Co O 高温烧结(通入空气氧化)得到产品LiCoO ,结合质量守恒还生成二
3 4 2
8
氧化碳气体,反应中Co O 中钴表观平均化合价由+ 变为+3、氧气中氧化合价由0变为-2,
3 4 3
结合电子守恒可知,“高温烧结”发生反应的化学方程式为
高温
4Co O +O +Li CO 12LiCoO +6CO,该反应中氧化剂与还原剂物质的量之比为1:4;
3 4 2 2 3 2 2
若通入空气过多过快,造成的不利影响是降低反应温度,反应速率减慢。
17.(14分)【答案】
(1) CH
4
(g)+CO
2
(g)=2CO(g)+2H
2
(g) ΔH=+247.4kJ·mol-1 (2分)
(2) ① 0.025(2分) ② AC(2分)
(3) ①< (2分) ② (2分)
8
{#{QQABCYAAoggIQJBAARgCQwmICAKQkAGACQgOwBAEIAAAgAFABAA=}#}k k
(4) ①<(2分) ② 1 3 (2分)
k k
2 4
【详解】
(1) CH 与CO 转化为合成气(H 和CO)的化学反应为CH (g)+CO (g)=2CO(g)+2H (g)。
4 2 2 4 2 2
由能量-反应进程曲线得热化学方程式:
CH (g)+H O(g)=CO(g)+3H (g)ΔH=+206.2kJ·mol-1(i)
4 2 2
CO (g)+4H (g)=CH (g)+2H O(g)ΔH=-165kJ·mol-1(ii)
2 2 4 2
(i)×2+(ii)得过程I的热化学方程式:CH (g)+CO (g)=2CO(g)+2H (g) ΔH=+247.4kJ·mol-1
4 2 2
(2) 详解
①
0.15mol
v(CH ) 0.025molL1min1
4 2L3min
②A.该反应为气体分子数减小的反应,且为吸热反应,故高温低压有利于平衡正向移动,
可以提高CH 的平衡转化率,A正确,符合题意;
4
B.使用催化剂,活化能降低,反应速率加快,但平衡不移动,不能提高CO 的平衡转化率,
2
B错误,不符合题意;
C.该反应是在恒容密闭容器中进行的反应前后气体分子数增大的反应,若容器内的总压强
不再变化,说明气体的物质的量不变,反应达到平衡状态,C正确,符合题意;
D.该反应在恒容密闭容器中进行,反应混合物都是气体,气体的质量不变,容器的容积不
变,则反应混合气体的密度始终不变,因此不能据此判断反应是否处于平衡状态,D错误,
不符合题意;
故选AC;
(3)①T 对应的阴影部分的面积更大,说明活化分子百分数更高,温度越高,活化分子百分
2
数越大,故T