文档内容
C.常温,pH=11的溶液中:CO2-、Na+、NH+、NO-
3 4 3
高二化学试卷(二) D.含有NaHCO 的溶液:Cl-、NO-、OH-、Ba2+
3 3
4.设N 为阿伏加德罗常数的值,下列说法正确的是 ( )
(本试卷满分100分,考试时间75分钟) A
A.1molN 与过量H 充分反应可生成NH 数目为2N
注意事项:1.答题前,考生务必用黑色字迹的签字笔或钢笔将自己的姓名、准考证号分别填写 2 2 3 A
在试卷和答题卡规定的位置上。 B.常温下,1L0.1mol·L-1的NHNO 溶液中NH+数目小于0.1N
4 3 4 A
2.答选择题时,选出每小题答案后,用2B铅笔把答题卡对应题目的答案涂黑,如需 C.0.1mol·L-1HClO溶液含有的H+数目为小于0.1N
A
改动,用橡皮擦干净后,再涂其它答案。非选择题的答案必须用黑色字迹的签字
D.1molNaHSO 在熔融状态下电离出的阴、阳离子总数目为3N
4 A
笔或钢笔写在答题卡上相应的区域内,写在本试卷上无效。
5.下列操作可以使水的离子积常数K 增大的是 ( )
w
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Cu-64
A.通入少量氨气 B.加入少量稀HCl
一 、选 择 题 : 本 题 共 15 小 题 ,每 小 题 3分 , 共 4 5分 。 在 每 小 题 给 出 的 四 个选项中,只有一项符
C.加热 D.加入少量醋酸钠固体
合题目要求。
6.一定温度下,在恒容密闭容器中发生反应2AlO(s)+6Cl(g)幑幐4AlCl(g)+3O(g),下
1.化学与生产、生活和科技息息相关,下列说法正确的是 ( ) 2 3 2 3 2
A.燃油汽车上的三元催化器中的催化剂提高了反应物中活化分子百分数,加快了反应速率 列叙述能表明该反应已达到平衡状态的是 ( )
B.“酒曲”的酿酒工艺,是利用了催化剂使平衡正向移动的原理 ①混合气体的密度不变 ②n(Cl)∶n(AlCl)∶n(O)=6∶4∶3
2 3 2
C.工业合成氨温度控制在700K左右可以用勒夏特列原理解释 ③容器内物质的总质量不变 ④AlO 的质量不变
2 3
D.骨头中含有的碳酸钙属于弱电解质
⑤混合气体的平均相对分子质量不变 ⑥v(Cl)=2v(O)
正 2 正 2
2.下列叙述正确的是 ( )
A.①③④⑤ B.①④⑤⑥ C.①④⑤ D.①②③⑥
A.甲烷的燃烧热为890kJ/mol,则表示甲烷燃烧热的热化学方程式为CH(g)+2O(g)
4 2
7.下列说法及相关方程式书写均正确的是 ( )
CO(g)+2HO(g) ΔH=-890kJ/mol
2 2
A.水是弱电解质:2HO幑幐HO++OH-
2 3
B.在一定条件下将1molSO 和0.5molO 置于密闭容器中充分反应,放出热量79.2kJ,则
2 2
B.硫酸氢钠在水中电离:NaHSO →Na++HSO-
反应的热化学方程式为2SO(g)+O(g)幑幐2SO(g) ΔH=-158.4kJ/mol 4 4
2 2 3
1 C.碳酸氢钠在水中水解:HCO-+HO幑幐HO++CO2-
C.已知C(s)+O(g)CO(g) ΔH=akJ/mol,C(s)+ O(g)CO(g) ΔH=bkJ/mol, 3 2 3 3
2 2 2 2
D.醋酸铵在水中部分电离:CHCOONH 幑幐CHCOO-+NH+
3 4 3 4
则a<b
8.下列说法中正确的是 ( )
D.已知中和热ΔH=-57.3kJ/mol,则HSO(aq)+Ba(OH)(aq)BaSO(s)+2HO(l)
2 4 2 4 2
A.在100℃时,pH约为6的纯水呈中性
ΔH=-114.6kJ/mol
3.常温下,下列各组离子在指定溶液中能大量共存的是 ( ) B.将pH=2的盐酸和醋酸各1mL分别稀释至100mL,所得醋酸的pH略大
A.滴加几滴KSCN溶液显红色的溶液中:K+、Na+、SO2-、OH- C.将1mL1×10-6mol·L-1盐酸稀释至1000mL,所得溶液的pH为9
4
B.能使甲基橙变红的溶液中:Cu2+、Mg2+、SO2-、Cl- D.强电解质溶液的导电能力一定比弱电解质溶液的强
4
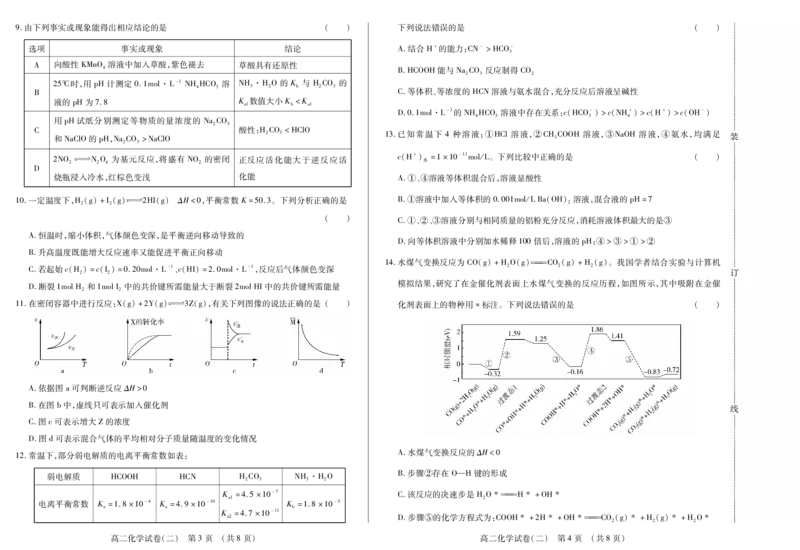
高二化学试卷(二) 第1页 (共8页) 高二化学试卷(二) 第2页 (共8页)9.由下列事实或现象能得出相应结论的是 ( ) 下列说法错误的是 ( )
选项 事实或现象 结论 A.结合H+的能力:CN->HCO-
3
A 向酸性KMnO 溶液中加入草酸,紫色褪去 草酸具有还原性
4 B.HCOOH能与NaCO 反应制得CO
2 3 2
25℃时,用 pH计测定0.1mol·L-1NHHCO 溶 NH·HO的 K 与 HCO 的
4 3 3 2 b 2 3
B C.等体积、等浓度的HCN溶液与氨水混合,充分反应后溶液呈碱性
液的pH为7.8 K 数值大小K <K
a1 b a1
D.0.1mol·L-1的NHHCO 溶液中存在关系:c(HCO-)>c(NH+)>c(H+)>c(OH-)
4 3 3 4
用pH试纸分别测定等物质的量浓度的 NaCO
2 3
C 酸性:HCO <HClO
2 3 13.已知常温下 4种溶液:①HCl溶液,②CHCOOH溶液,③NaOH溶液,④氨水,均满足
和NaClO的pH,NaCO >NaClO 3
2 3
c(H+) =1×10-11mol/L。下列比较中正确的是 ( )
2NO 幑幐NO 为基元反应,将盛有 NO 的密闭 正反应活化能大于逆反应活 水
2 2 4 2
D
烧瓶浸入冷水,红棕色变浅 化能 A.①、④溶液等体积混合后,溶液显酸性
10.一定温度下,H(g)+I(g)幑幐2HI(g) ΔH<0,平衡常数K=50.3。下列分析正确的是 B.①溶液中加入等体积的0.001mol/LBa(OH)溶液,混合液的pH=7
2 2 2
( ) C.①、②、③溶液分别与相同质量的铝粉充分反应,消耗溶液体积最大的是③
A.恒温时,缩小体积,气体颜色变深,是平衡逆向移动导致的
D.向等体积溶液中分别加水稀释100倍后,溶液的pH:④>③>①>②
B.升高温度既能增大反应速率又能促进平衡正向移动
14.水煤气变换反应为CO(g)+HO(g)CO(g)+H(g)。我国学者结合实验与计算机
C.若起始c(H)=c(I)=0.20mol·L-1、c(HI)=2.0mol·L-1,反应后气体颜色变深 2 2 2
2 2
模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催
D.断裂1molH 和1molI中的共价键所需能量大于断裂2molHI中的共价键所需能量
2 2
11.在密闭容器中进行反应:X(g)+2Y(g)幑幐3Z(g),有关下列图像的说法正确的是 ( ) 化剂表面上的物种用标注。下列说法错误的是 ( )
A.依据图a可判断逆反应ΔH>0
B.在图b中,虚线只可表示加入催化剂
C.图c可表示增大Z的浓度
D.图d可表示混合气体的平均相对分子质量随温度的变化情况
A.水煤气变换反应的ΔH<0
12.常温下,部分弱电解质的电离平衡常数如表:
B.步骤②存在O—H键的形成
弱电解质 HCOOH HCN HCO NH·HO
2 3 3 2
K =4.5×10-7 C.该反应的决速步是HOH +OH
a1 2
电离平衡常数 K=1.8×10-4 K=4.9×10-10 K =1.8×10-5
a a b
K =4.7×10-11
a2 D.步骤⑤的化学方程式为:COOH +2H +OHCO(g) +H(g) +HO
2 2 2
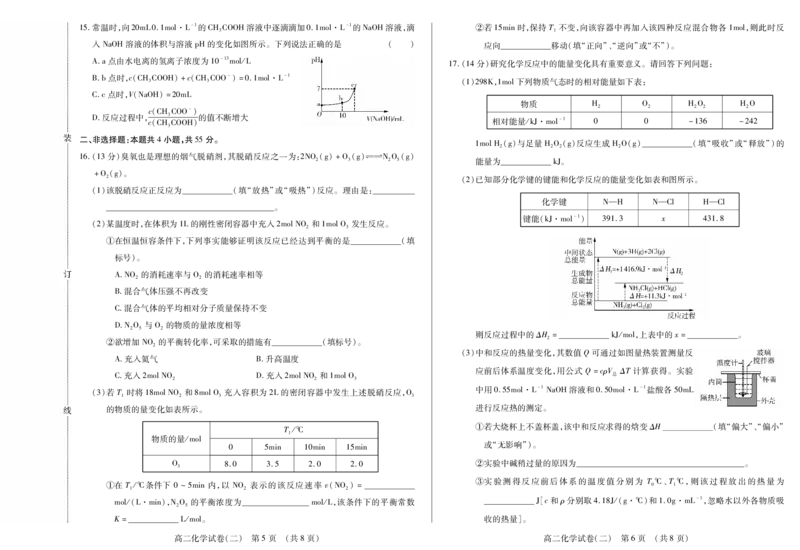
高二化学试卷(二) 第3页 (共8页) 高二化学试卷(二) 第4页 (共8页)15.常温时,向20mL0.1mol·L-1的CHCOOH溶液中逐滴滴加0.1mol·L-1的NaOH溶液,滴 ②若15min时,保持T不变,向该容器中再加入该四种反应混合物各1mol,则此时反
3 1
入NaOH溶液的体积与溶液pH的变化如图所示。下列说法正确的是 ( ) 应向 移动(填“正向”、“逆向”或“不”)。
A.a点由水电离的氢离子浓度为10-13mol/L
17.(14分)研究化学反应中的能量变化具有重要意义。请回答下列问题:
B.b点时,c(CHCOOH)+c(CHCOO-)=0.1mol·L-1
3 3 (1)298K,1mol下列物质气态时的相对能量如下表:
C.c点时,V(NaOH)=20mL
物质 H O HO HO
c(CHCOO-) 2 2 2 2 2
D.反应过程中, 3 的值不断增大
c(CHCOOH) 相对能量/kJ·mol-1 0 0 -136 -242
3
二、非选择题:本题共4小题,共55分。
1molH(g)与足量HO(g)反应生成HO(g) (填“吸收”或“释放”)的
2 2 2 2
16.(13分)臭氧也是理想的烟气脱硝剂,其脱硝反应之一为:2NO(g)+O(g)幑幐NO(g)
2 3 2 5 能量为 kJ。
+O(g)。
2 (2)已知部分化学键的键能和化学反应的能量变化如表和图所示。
(1)该脱硝反应正反应为 (填“放热”或“吸热”)反应。理由是:
化学键 N—H N—Cl H—Cl
。
键能(kJ·mol-1) 391.3 x 431.8
(2)某温度时,在体积为1L的刚性密闭容器中充入2molNO 和1molO 发生反应。
2 3
①在恒温恒容条件下,下列事实能够证明该反应已经达到平衡的是 (填
标号)。
A.NO 的消耗速率与O 的消耗速率相等
2 2
B.混合气体压强不再改变
C.混合气体的平均相对分子质量保持不变
D.NO 与O 的物质的量浓度相等
2 5 2
则反应过程中的ΔH = kJ/mol,上表中的x= 。
2
②欲增加NO 的平衡转化率,可采取的措施有 (填标号)。
2
(3)中和反应的热量变化,其数值 Q可通过如图量热装置测量反
A.充入氦气 B.升高温度
应前后体系温度变化,用公式 Q=cρV ΔT计算获得。实验
C.充入2molNO D.充入2molNO 和1molO 总
2 2 3
中用0.55mol·L-1NaOH溶液和0.50mol·L-1盐酸各50mL
(3)若T时将18molNO 和8molO 充入容积为2L的密闭容器中发生上述脱硝反应,O
1 2 3 3
的物质的量变化如表所示。 进行反应热的测定。
①若大烧杯上不盖杯盖,该中和反应求得的焓变ΔH (填“偏大”、“偏小”
T/℃
1
物质的量/mol
0 5min 10min 15min 或“无影响”)。
O 8.0 3.5 2.0 2.0 ②实验中碱稍过量的原因为 。
3
③实验测得反应前后体系的温度值分别为 T℃、T℃,则该过程放出的热量为
①在T/℃条件下 0~5min内,以 NO 表示的该反应速率 v(NO)= 0 1
1 2 2
mol/(L·min),NO 的平衡浓度为 mol/L,该条件下的平衡常数
J[c和ρ分别取4.18J/(g·℃)和1.0g·mL-1,忽略水以外各物质吸
2 5
K= L/mol。 收的热量]。
高二化学试卷(二) 第5页 (共8页) 高二化学试卷(二) 第6页 (共8页)④关于中和热的测定实验,下列说法正确的是 (填标号)。 ①滴定达终点时的现象为 。
A.向内筒加入稀碱液时,应当缓慢分批加入 ②样品中铜的质量分数为 (写字母表达式)。
B.实验中,应记录初始温度与反应过程中达到的最高温度 ③步骤1中若没有除尽未反应的 HNO,则导致测定结果 (填“偏高”、
3
C.实验中,测量酸液的初始温度后,可使用同一支温度计直接测量碱液的初始温度 “偏低”或“无影响”)。
D.实验过程中,若使用铁质搅拌棒,会导致测得的中和热ΔH偏小 19.(15分)Ⅰ.常温下,如果取0.2mol/LCHCOOH溶液与0.2mol/LNaOH溶液等体积混合
3
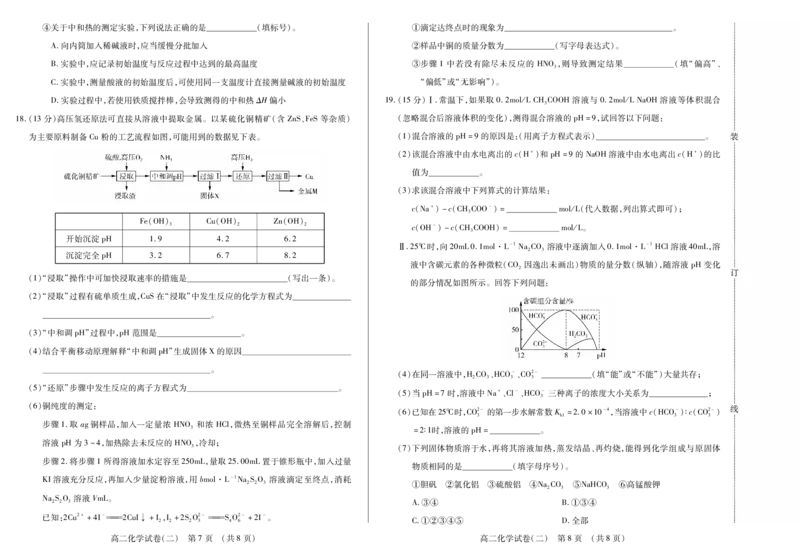
18.(13分)高压氢还原法可直接从溶液中提取金属。以某硫化铜精矿(含 ZnS、FeS等杂质) (忽略混合后溶液体积的变化),测得混合溶液的pH=9,试回答以下问题:
为主要原料制备Cu粉的工艺流程如图,可能用到的数据见下表。 (1)混合溶液的pH=9的原因是:(用离子方程式表示) 。
(2)该混合溶液中由水电离出的c(H+)和pH=9的NaOH溶液中由水电离出c(H+)的比
值为 。
(3)求该混合溶液中下列算式的计算结果:
c(Na+)-c(CHCOO-)= mol/L(代入数据,列出算式即可);
3
Fe(OH) Cu(OH) Zn(OH)
3 2 2 c(OH-)-c(CHCOOH)= mol/L。
3
开始沉淀pH 1.9 4.2 6.2
Ⅱ.25℃时,向20mL0.1mol·L-1NaCO 溶液中逐滴加入0.1mol·L-1HCl溶液40mL,溶
2 3
沉淀完全pH 3.2 6.7 8.2
液中含碳元素的各种微粒(CO 因逸出未画出)物质的量分数(纵轴),随溶液 pH变化
2
(1)“浸取”操作中可加快浸取速率的措施是 (写出一条)。
的部分情况如图所示。回答下列问题:
(2)“浸取”过程有硫单质生成,CuS在“浸取”中发生反应的化学方程式为
。
(3)“中和调pH”过程中,pH范围是 。
(4)结合平衡移动原理解释“中和调pH”生成固体X的原因
。
(4)在同一溶液中,HCO、HCO-、CO2- (填“能”或“不能”)大量共存;
2 3 3 3
(5)“还原”步骤中发生反应的离子方程式为 。
(5)当pH=7时,溶液中Na+、Cl-、HCO-三种离子的浓度大小关系为 ;
3
(6)铜纯度的测定:
(6)已知在25℃时,CO2-的第一步水解常数K =2.0×10-4,当溶液中c(HCO-)∶c(CO2-)
3 h1 3 3
步骤1.取ag铜样品,加入一定量浓 HNO 和浓 HCl,微热至铜样品完全溶解后,控制
3 =2∶1时,溶液的pH= 。
溶液pH为3~4,加热除去未反应的HNO,冷却;
3 (7)下列固体物质溶于水,再将其溶液加热,蒸发结晶、再灼烧,能得到化学组成与原固体
步骤2.将步骤1所得溶液加水定容至250mL,量取25.00mL置于锥形瓶中,加入过量
物质相同的是 (填字母序号)。
KI溶液充分反应,再加入少量淀粉溶液,用 bmol·L-1NaSO 溶液滴定至终点,消耗
2 2 3 ①胆矾 ②氯化铝 ③硫酸铝 ④NaCO ⑤NaHCO ⑥高锰酸钾
2 3 3
NaSO 溶液VmL。
2 2 3 A.③④ B.①③④
已知:2Cu2++4I-2CuI↓+I,I+2SO2-SO2-+2I-。
2 2 2 3 4 6 C.①②③④⑤ D.全部
高二化学试卷(二) 第7页 (共8页) 高二化学试卷(二) 第8页 (共8页)