文档内容
2023—2024 学年度下学期 2022 级
7 月月考化学试卷
命题人:文智丽 审题人:蔡艳
考试时间:2024年7月26日
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Cl 35.5 Sc 45
一、单选题(本题共15小题,每小题3分,共15分。在每小题给出的四个选项中,只有一项符
合题目要求)
1.新材料助力嫦娥六号探月挖“宝”,下列有关说法正确的是
A.“挖宝”所用钻杆由碳化硅增强铝基复合材料制造,碳化硅属于共价晶体
B.月面国旗由超细玄武岩纤维纺织而成,玄武岩纤维属于有机高分子
C.登月中,所用北斗系统的导航卫星,其计算机的芯片材料是高纯度二氧化硅
D.制造一同启程的小卫星“思源二号”,采用了特种镁合金与碳纤维,碳纤维属于纤维素
2.《梦溪笔谈》是北宋科学家沈括(1031~1095)的著作,书中详细记载了我国劳动人民在科学技
术方面的卓越贡献和他自己的研究成果,被称为“中国科学史的里程碑”,沈括则被称为“中国整
部科学史中的卓越人物”。下列工艺不可能被记载的是
A.湿法炼铜 B.炼铁 C.电解法冶炼铝 D.海水晒盐
3.由下列实验操作和现象得出结论正确的是
选项 实验操作和现象 结论
A 向可能混有苯酚的甲苯中滴加饱和溴水,未出现白色沉淀 甲苯中未混有苯酚
向淀粉溶液中加入适量稀硫酸,加热煮沸后,加入过量
B 淀粉已经完全水解
NaOH溶液,再加入少量碘水,溶液不变蓝
花生油在水中的溶解度
C 将花生油与NaOH溶液混合,充分加热后分层消失
随温度升高而增大
1-溴丁烷和NaOH乙醇溶液共热,将产生的气体通入溴水
D 反应有1-丁烯生成
中,溴水褪色
A.A B.B C.C D.D
1
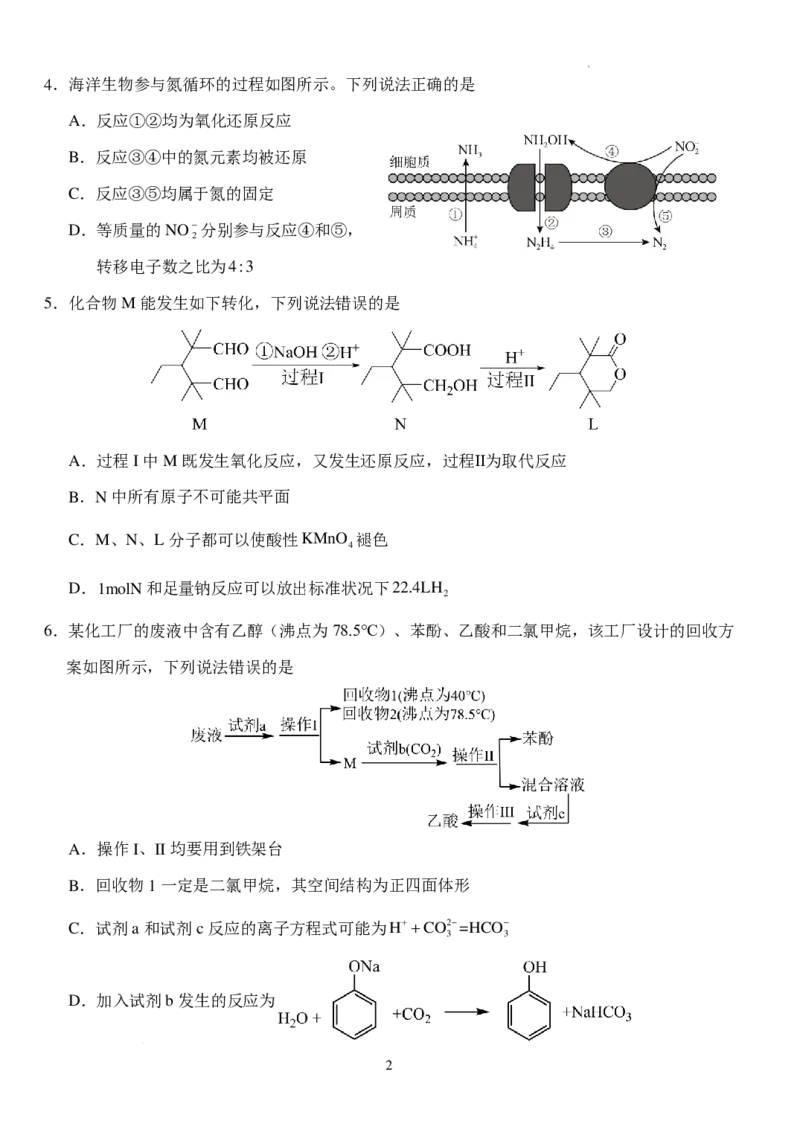
学科网(北京)股份有限公司4.海洋生物参与氮循环的过程如图所示。下列说法正确的是
A.反应①②均为氧化还原反应
B.反应③④中的氮元素均被还原
C.反应③⑤均属于氮的固定
D.等质量的NO−分别参与反应④和⑤,
2
转移电子数之比为4:3
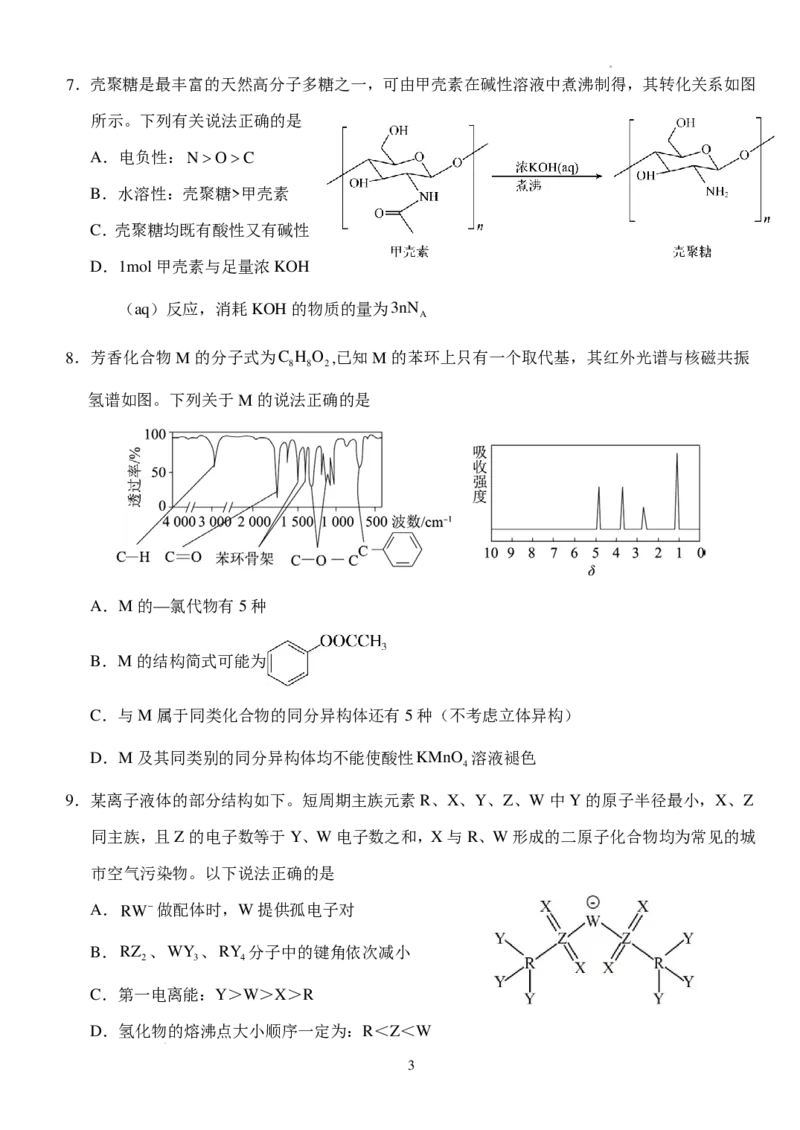
5.化合物M能发生如下转化,下列说法错误的是
A.过程I中M既发生氧化反应,又发生还原反应,过程Ⅱ为取代反应
B.N中所有原子不可能共平面
C.M、N、L分子都可以使酸性KMnO 褪色
4
D.1molN和足量钠反应可以放出标准状况下22.4LH
2
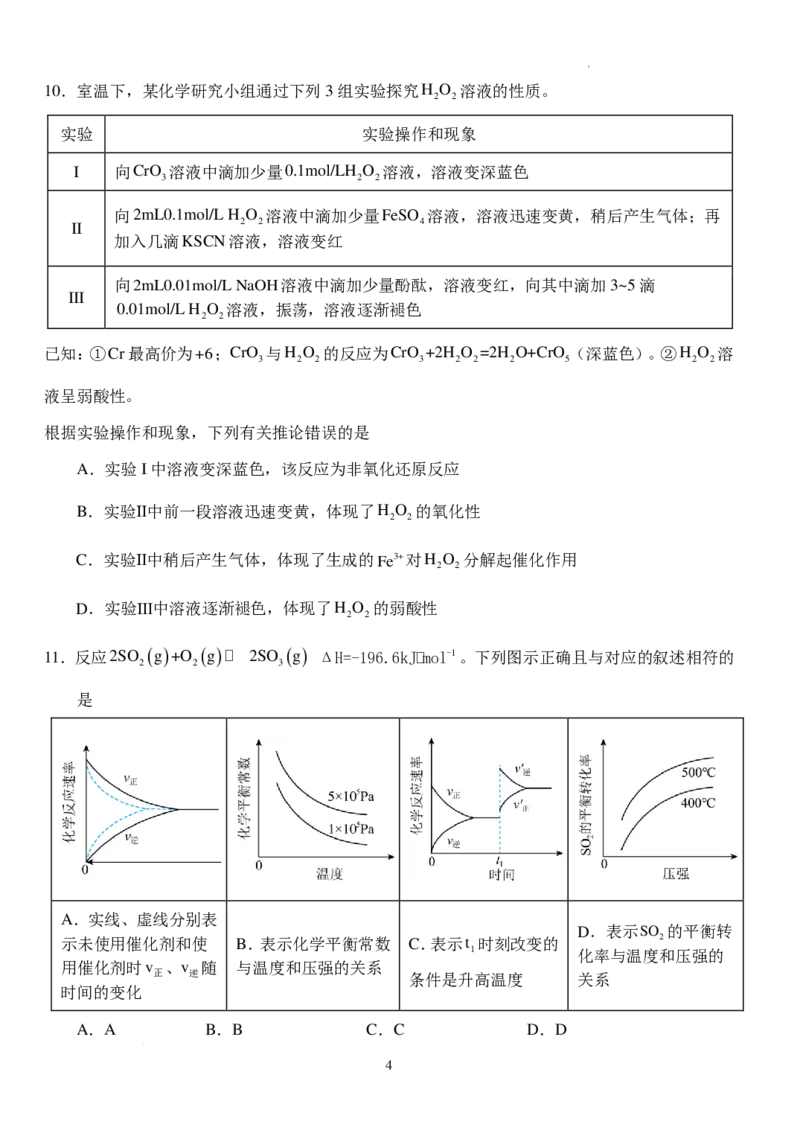
6.某化工厂的废液中含有乙醇(沸点为78.5℃)、苯酚、乙酸和二氯甲烷,该工厂设计的回收方
案如图所示,下列说法错误的是
A.操作I、II均要用到铁架台
B.回收物1一定是二氯甲烷,其空间结构为正四面体形
C.试剂a和试剂c反应的离子方程式可能为H+ +CO2−=HCO−
3 3
D.加入试剂b发生的反应为
2
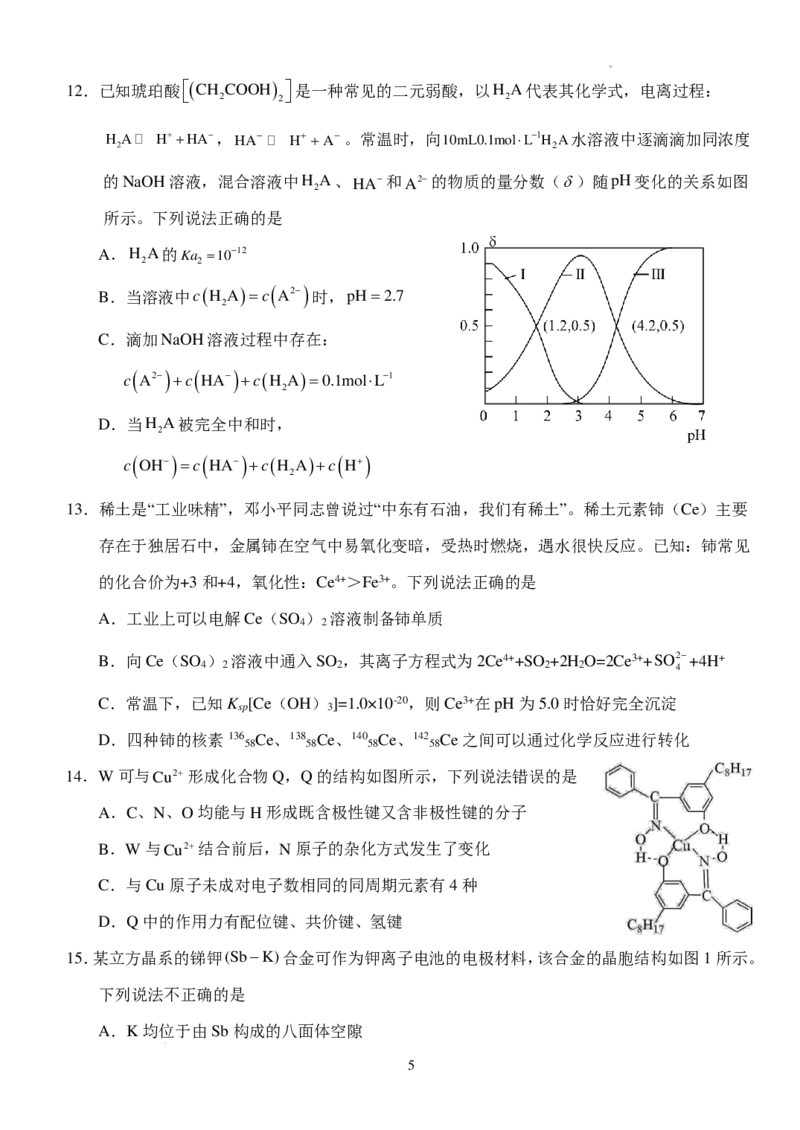
学科网(北京)股份有限公司7.壳聚糖是最丰富的天然高分子多糖之一,可由甲壳素在碱性溶液中煮沸制得,其转化关系如图
所示。下列有关说法正确的是
A.电负性:N>O>C
B.水溶性:壳聚糖>甲壳素
C.壳聚糖均既有酸性又有碱性
D.1mol甲壳素与足量浓KOH
(aq)反应,消耗KOH的物质的量为3nN
A
8.芳香化合物M的分子式为C H O ,已知M的苯环上只有一个取代基,其红外光谱与核磁共振
8 8 2
氢谱如图。下列关于M的说法正确的是
A.M的—氯代物有5种
B.M的结构简式可能为
C.与M属于同类化合物的同分异构体还有5种(不考虑立体异构)
D.M及其同类别的同分异构体均不能使酸性KMnO 溶液褪色
4
9.某离子液体的部分结构如下。短周期主族元素R、X、Y、Z、W中Y的原子半径最小,X、Z
同主族,且Z的电子数等于Y、W电子数之和,X与R、W形成的二原子化合物均为常见的城
市空气污染物。以下说法正确的是
A.RW−做配体时,W提供孤电子对
B.RZ 、WY 、RY 分子中的键角依次减小
2 3 4
C.第一电离能:Y>W>X>R
D.氢化物的熔沸点大小顺序一定为:R<Z<W
3
学科网(北京)股份有限公司10.室温下,某化学研究小组通过下列3组实验探究H O 溶液的性质。
2 2
实验 实验操作和现象
I 向CrO 溶液中滴加少量0.1mol/LH O 溶液,溶液变深蓝色
3 2 2
向2mL0.1mol/L H O 溶液中滴加少量FeSO 溶液,溶液迅速变黄,稍后产生气体;再
2 2 4
II
加入几滴KSCN溶液,溶液变红
向2mL0.01mol/L NaOH溶液中滴加少量酚酞,溶液变红,向其中滴加3~5滴
III
0.01mol/L H O 溶液,振荡,溶液逐渐褪色
2 2
已知:①Cr最高价为+6;CrO 与H O 的反应为CrO +2H O =2H O+CrO(深蓝色)。②H O 溶
3 2 2 3 2 2 2 5 2 2
液呈弱酸性。
根据实验操作和现象,下列有关推论错误的是
A.实验I中溶液变深蓝色,该反应为非氧化还原反应
B.实验Ⅱ中前一段溶液迅速变黄,体现了H O 的氧化性
2 2
C.实验Ⅱ中稍后产生气体,体现了生成的Fe3+对H O 分解起催化作用
2 2
D.实验Ⅲ中溶液逐渐褪色,体现了H O 的弱酸性
2 2
11.反应2SO (g)+O (g) 2SO (g) ΔH=-196.6kJmol-1。下列图示正确且与对应的叙述相符的
2 2 3
是
A.实线、虚线分别表
D.表示SO 的平衡转
示未使用催化剂和使 B.表示化学平衡常数 C.表示t 时刻改变的 2
1 化率与温度和压强的
用催化剂时v 、v 随 与温度和压强的关系
正 逆 条件是升高温度 关系
时间的变化
A.A B.B C.C D.D
4
学科网(北京)股份有限公司12.已知琥珀酸
(CH
2
COOH)
2
是一种常见的二元弱酸,以H
2
A代表其化学式,电离过程:
H A H++HA−,HA− H+ +A−。常温时,向10mL0.1mol⋅L−1H A水溶液中逐滴滴加同浓度
2 2
的NaOH溶液,混合溶液中H A、HA−和A2−的物质的量分数(δ)随pH变化的关系如图
2
所示。下列说法正确的是
A.H A的Ka =10−12
2 2
B.当溶液中c(H A)=c ( A2−) 时,pH=2.7
2
C.滴加NaOH溶液过程中存在:
c ( A2−) +c ( HA−) +c(H A)=0.1mol⋅L−1
2
D.当H A被完全中和时,
2
c ( OH−) =c ( HA−) +c(H A)+c ( H+)
2
13.稀土是“工业味精”,邓小平同志曾说过“中东有石油,我们有稀土”。稀土元素铈(Ce)主要
存在于独居石中,金属铈在空气中易氧化变暗,受热时燃烧,遇水很快反应。已知:铈常见
的化合价为+3和+4,氧化性:Ce4+>Fe3+。下列说法正确的是
A.工业上可以电解Ce(SO ) 溶液制备铈单质
4 2
B.向Ce(SO ) 溶液中通入SO ,其离子方程式为2Ce4++SO +2H O=2Ce3++SO2−+4H+
4 2 2 2 2 4
C.常温下,已知K [Ce(OH) ]=1.0×10-20,则Ce3+在pH为5.0时恰好完全沉淀
sp 3
D.四种铈的核素136 Ce、138 Ce、140 Ce、142 Ce之间可以通过化学反应进行转化
58 58 58 58
14.W可与Cu2+形成化合物Q,Q的结构如图所示,下列说法错误的是
A.C、N、O均能与H形成既含极性键又含非极性键的分子
B.W与Cu2+结合前后,N原子的杂化方式发生了变化
C.与Cu原子未成对电子数相同的同周期元素有4种
D.Q中的作用力有配位键、共价键、氢键
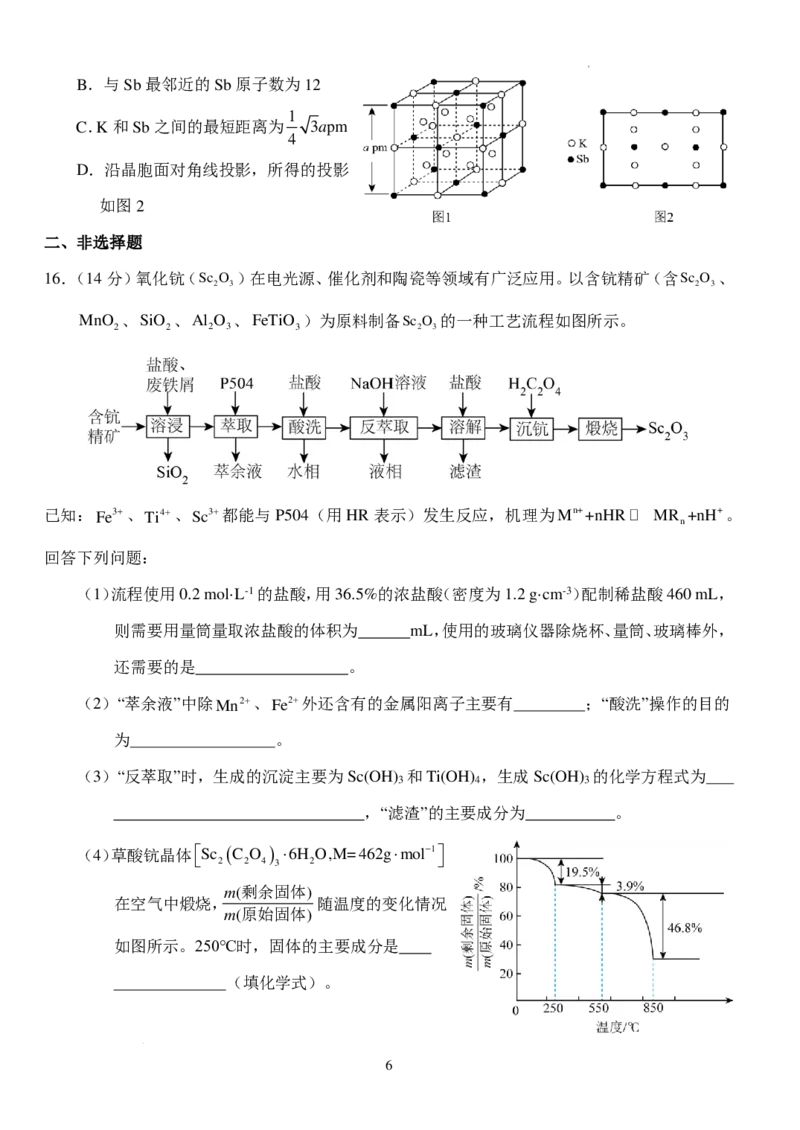
15.某立方晶系的锑钾(Sb−K)合金可作为钾离子电池的电极材料,该合金的晶胞结构如图1所示。
下列说法不正确的是
A.K均位于由Sb构成的八面体空隙
5
学科网(北京)股份有限公司B.与Sb最邻近的Sb原子数为12
1
C.K和Sb之间的最短距离为 3apm
4
D.沿晶胞面对角线投影,所得的投影
如图2
二、非选择题
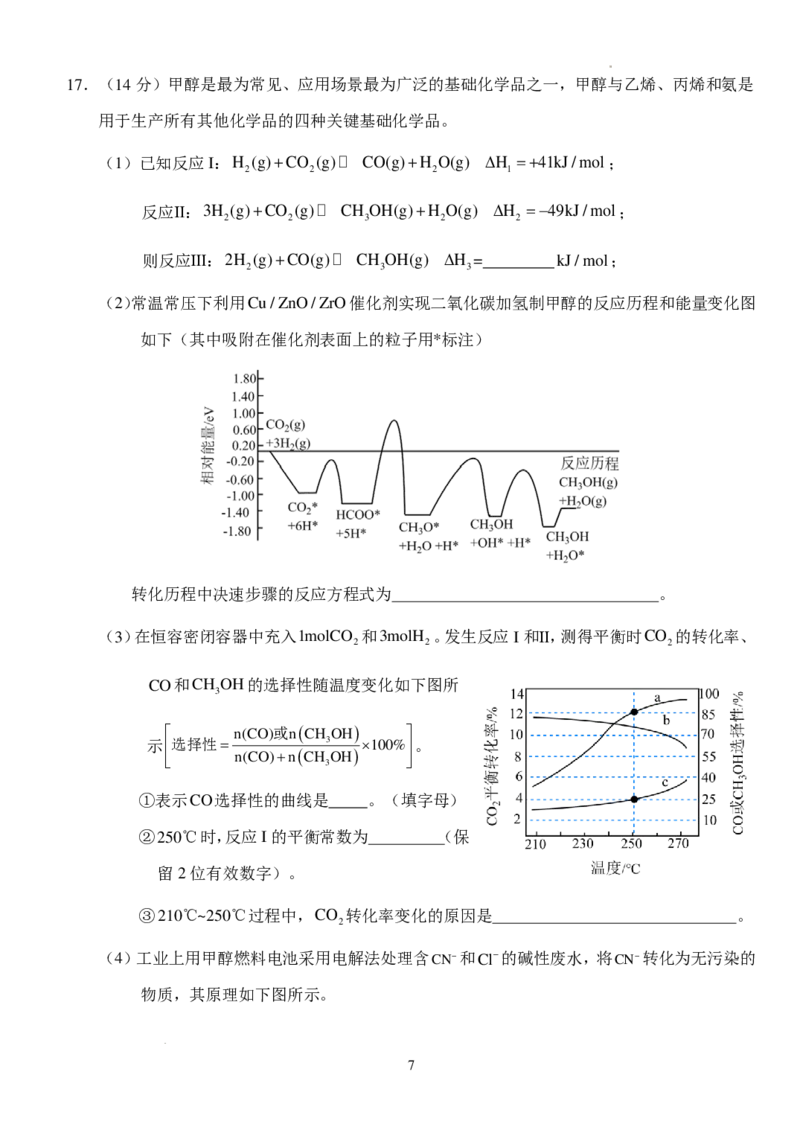
16.(14分)氧化钪(Sc O )在电光源、催化剂和陶瓷等领域有广泛应用。以含钪精矿(含Sc O 、
2 3 2 3
MnO 、SiO 、Al O 、FeTiO )为原料制备Sc O 的一种工艺流程如图所示。
2 2 2 3 3 2 3
已知:Fe3+、Ti4+、Sc3+都能与P504(用HR表示)发生反应,机理为Mn++nHR MR +nH+。
n
回答下列问题:
(1)流程使用0.2 mol·L-1的盐酸,用36.5%的浓盐酸(密度为1.2 g·cm-3)配制稀盐酸460 mL,
则需要用量筒量取浓盐酸的体积为 mL,使用的玻璃仪器除烧杯、量筒、玻璃棒外,
还需要的是 。
(2)“萃余液”中除Mn2+、Fe2+外还含有的金属阳离子主要有 ;“酸洗”操作的目的
为 。
(3)“反萃取”时,生成的沉淀主要为Sc(OH) 和Ti(OH) ,生成Sc(OH) 的化学方程式为
3 4 3
,“滤渣”的主要成分为 。
(4)草酸钪晶体
Sc
2
(C
2
O
4
)
3
⋅6H
2
O,M=462g⋅mol−1
m(剩余固体)
在空气中煅烧, 随温度的变化情况
m(原始固体)
如图所示。250℃时,固体的主要成分是
(填化学式)。
6
学科网(北京)股份有限公司17.(14分)甲醇是最为常见、应用场景最为广泛的基础化学品之一,甲醇与乙烯、丙烯和氨是
用于生产所有其他化学品的四种关键基础化学品。
(1)已知反应I:H (g)+CO (g) CO(g)+H O(g) ∆H =+41kJ/mol;
2 2 2 1
反应Ⅱ:3H (g)+CO (g) CH OH(g)+H O(g) ∆H =−49kJ/mol;
2 2 3 2 2
则反应Ⅲ:2H (g)+CO(g) CH OH(g) ∆H = kJ/mol;
2 3 3
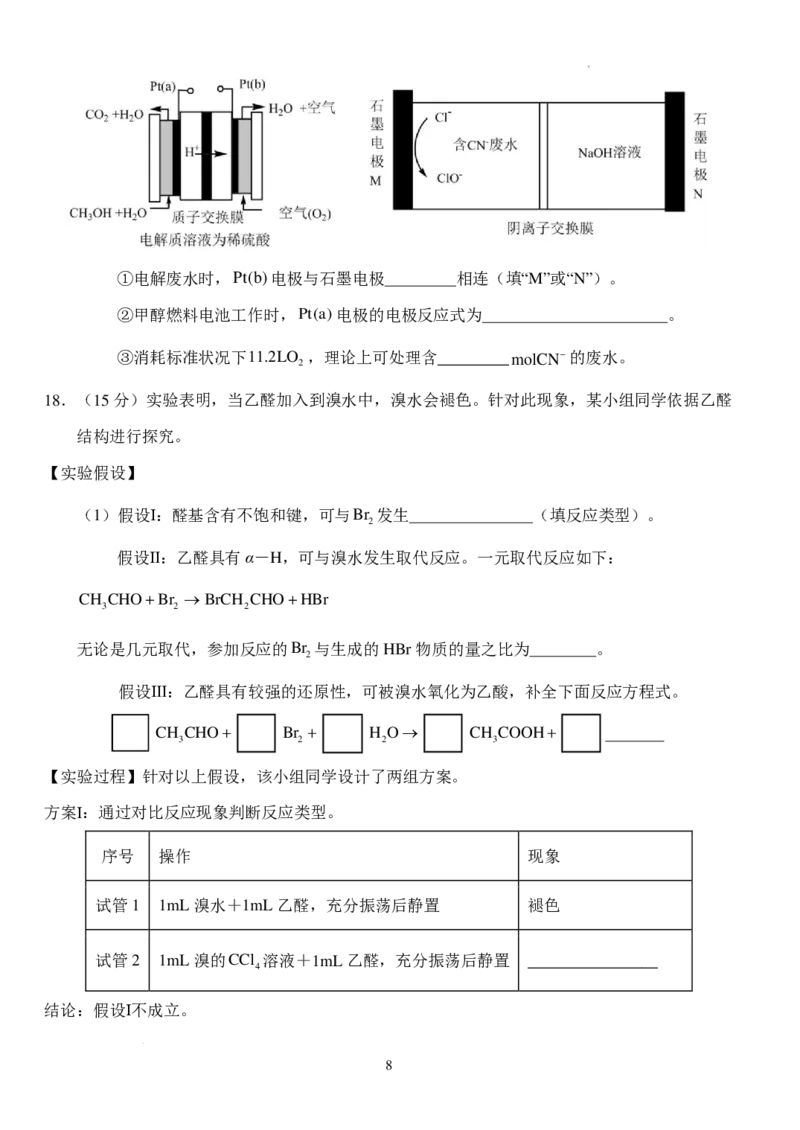
(2)常温常压下利用Cu/ZnO/ZrO催化剂实现二氧化碳加氢制甲醇的反应历程和能量变化图
如下(其中吸附在催化剂表面上的粒子用*标注)
转化历程中决速步骤的反应方程式为 。
(3)在恒容密闭容器中充入1molCO 和3molH 。发生反应I和Ⅱ,测得平衡时CO 的转化率、
2 2 2
CO和CH OH的选择性随温度变化如下图所
3
n(CO)或n(CH OH)
示选择性= 3 ×100%。
n(CO)+n(CH
3
OH)
①表示CO选择性的曲线是 。(填字母)
②250℃时,反应I的平衡常数为 ( 保
留2位有效数字)。
③210℃~250℃过程中,CO 转化率变化的原因是 。
2
(4)工业上用甲醇燃料电池采用电解法处理含CN−和Cl−的碱性废水,将CN−转化为无污染的
物质,其原理如下图所示。
7
学科网(北京)股份有限公司①电解废水时,Pt(b)电极与石墨电极 相连(填“M”或“N”)。
②甲醇燃料电池工作时,Pt(a)电极的电极反应式为 。
③消耗标准状况下11.2LO ,理论上可处理含 molCN−的废水。
2
18.(15分)实验表明,当乙醛加入到溴水中,溴水会褪色。针对此现象,某小组同学依据乙醛
结构进行探究。
【实验假设】
(1)假设Ⅰ:醛基含有不饱和键,可与Br 发生 (填反应类型)。
2
假设Ⅱ:乙醛具有α-H,可与溴水发生取代反应。一元取代反应如下:
CH CHO+Br →BrCH CHO+HBr
3 2 2
无论是几元取代,参加反应的Br 与生成的HBr物质的量之比为 。
2
假设Ⅲ:乙醛具有较强的还原性,可被溴水氧化为乙酸,补全下面反应方程式。
CH CHO+ Br + H O→ CH COOH+
3 2 2 3
【实验过程】针对以上假设,该小组同学设计了两组方案。
方案Ⅰ:通过对比反应现象判断反应类型。
序号 操作 现象
试管1 1mL溴水+1mL乙醛,充分振荡后静置 褪色
试管2 1mL溴的CCl 溶液+1mL乙醛,充分振荡后静置 ________________
4
结论:假设Ⅰ不成立。
8
学科网(北京)股份有限公司(2)试管2中的实验现象为 。
方案Ⅱ:通过测定反应后混合液的pH判断反应类型。
序号 操作 pH
加入20mL溴水,再加入10mL苯酚溶液,待完全反应后 1.85
试管1
(苯酚过量),测定混合液pH [c ( H+) =1×10−1.85mol⋅L−1]
加入20mL相同浓度的溴水,再加入10mL 20%的乙醛溶
试管2 ____________
液(乙醛过量),3min后完全褪色,测定混合液pH
注:苯酚和乙酸的电离及温度变化对混合液pH的影响可忽略。
(3)写出苯酚与溴水反应的化学方程式: 。
(4)若试管2中反应后混合液的pH=1.85,则证明乙醛与溴水的反应类型为 ;
若pH接近 ,则证明为氧化反应(lg2≈0.3);若pH介于两者之间,则证明两种反
应类型皆有。
【实验结论与反思】
(5)根据实验数据得出结论:乙醛与溴水发生氧化反应。查阅资料,乙醛并非直接与Br 发
2
生反应,而是与次溴酸(HBrO)反应,从平衡移动的角度解释乙醛使溴水褪色的原
因: 。
(6)已知柠檬醛的结构如图,结合上述实验,检验柠檬醛分子中存在碳碳双键的合理方法为
(填字母序号)。
A.向酸性高锰酸钾溶液中加适量柠檬醛,观察其
是否褪色
B.向溴水中加适量柠檬醛,观察其是否褪色
C.向溴的CCl 溶液中加适量柠檬醛,观察其是
4
否褪色
D.向新制氢氧化铜悬浊液中加适量柠檬醛,加热,冷却后取上层清液再加溴水,观察
其是否褪色
9
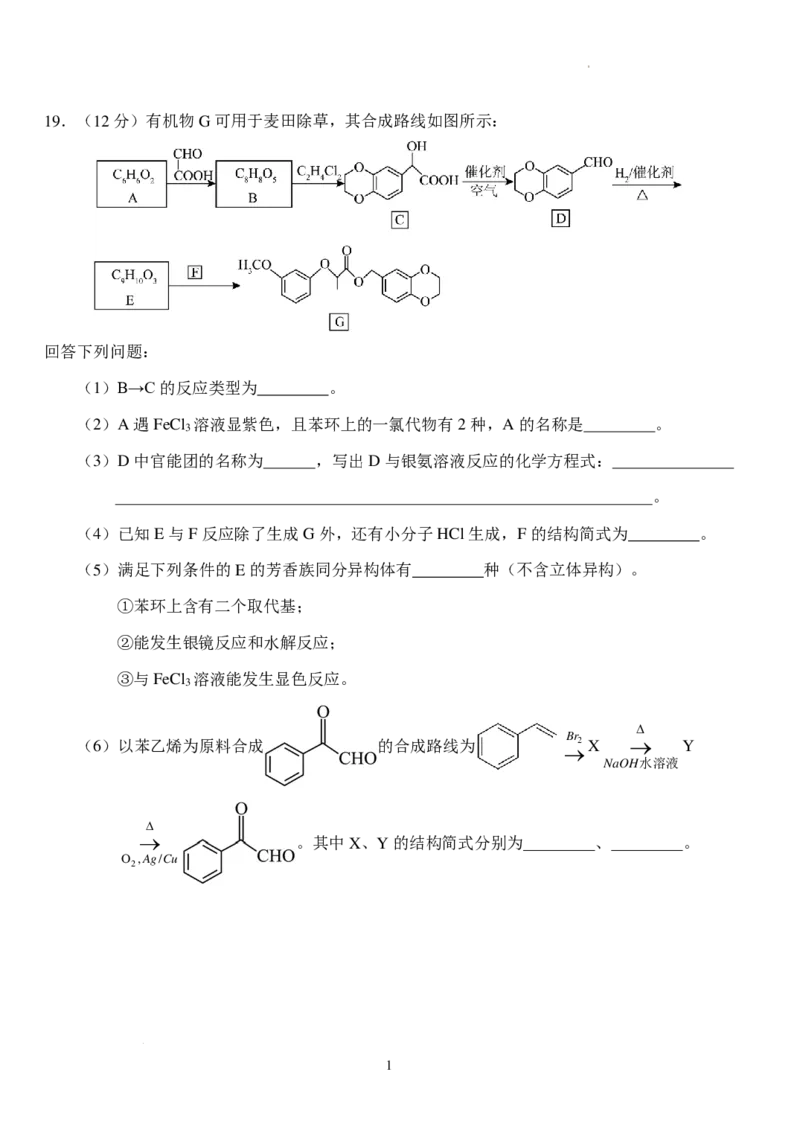
学科网(北京)股份有限公司19.(12分)有机物G可用于麦田除草,其合成路线如图所示:
回答下列问题:
(1)B→C的反应类型为 。
(2)A遇FeCl 溶液显紫色,且苯环上的一氯代物有2种,A的名称是 。
3
(3)D中官能团的名称为 ,写出D与银氨溶液反应的化学方程式:
。
(4)已知E与F反应除了生成G外,还有小分子HCl生成,F的结构简式为 。
(5)满足下列条件的E的芳香族同分异构体有 种(不含立体异构)。
①苯环上含有二个取代基;
②能发生银镜反应和水解反应;
③与FeCl 溶液能发生显色反应。
3
∆
Br
(6)以苯乙烯为原料合成 的合成路线为 → 2 X → Y
NaOH水溶液
∆
→ 。其中X、Y的结构简式分别为 、 。
O ,Ag/Cu
2
1
学科网(北京)股份有限公司化学参考答案
1-5 ACDDC 6-10 BBCCD 11-15 CBBBA
16.(14分,每空2分)
(1)8.3 500mL容量瓶、胶头滴管
(2)Al3+ 除去Fe3+
(3)ScR +3NaOH=Sc(OH) ↓+3NaR Ti(OH)
3 3 4
(4)Sc (C O ) ⋅H O
2 2 4 3 2
17.(14分,除标注外每空2分)
(1)-90 (1分)
(2)HCOO*+5H*=CH O*+H O+H*(或合理答案)(1分)
3 2
(3)c 0.0015 升高温度对反应Ⅰ的影响大于反应Ⅱ(或合理答案)
(4)M CH OH−6e−+H O=CO +6H+ 0.4
3 2 2
18.(15分,除标注外每空2分)
(1)加成反应(1分) 1:1 (1分) CH CHO+Br +H O=CH COOH+2HBr(1分)
3 2 2 3
(2)溴的CCl 溶液不褪色
4
(3)
(4)取代反应 1.55
(5)乙醛与HBrO反应,使得Br +H O HBr+HBrO平衡正向移动,消耗Br ,溶液褪色
2 2 2
(6)C
1
学科网(北京)股份有限公司19.(12分,除标注外,每空2分)
(1)取代反应(1分)
(2)邻苯二酚或1,2-苯二酚(1分)
(3)醚键、醛基
Δ
+2[Ag(NH
3
)
2
]OH→ +2Ag↓+3NH
3
+H
2
O
(4)
(5)6
(6) (1分) (1分)
1
学科网(北京)股份有限公司