文档内容
2024~2025 学年第一学期期中调研考试
高二化学试卷
试卷总分:100分 考试时长:75分钟
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Mg-24 S-32 Cl-35.5 Ca-40 Mn-55
Fe-56 Cu-64 Ag-108
一、单项选择题:共13题,每小题3分,共39分。每题只有一个选项最符合题意。
1.下列民俗、诗句、谚语等包含吸热反应的是( )
A.民间焰火——打铁花 B.千锤万凿出深山,烈火焚烧若等闲(石灰吟)
C.只要功夫深,铁杵磨成针 D.冰,水为之,而寒于水
2.生活中常见的金属防腐的方法很多。下列措施不能起到防腐作用的是( )
A.健身器材刷油漆 B.衣架和电线的外面包上一层塑料层
C.在轮船船身上镶上一定数量的铜块 D.地下钢铁管道连接镁块
3.下列根据热化学反应方程式的推导正确的( )
A.已知 ,则 的燃烧热为
B.已知 红磷, 白磷, ,则可推得红磷稳定性比白磷差
C.已知 下,将 和 充分反应能放出19.3kJ的热量,则该反应的热化学方程
式为
D.已知 ; ,则
4.下表是几种弱酸常温下的电离平衡常数:
则下列说法中不正确的是( )
A.多元弱酸的酸性主要由第一步电离决定
B.常温下,加水稀释醋酸, 减小
C.向弱酸溶液中加入少量的NaOH溶液,电离平衡常数发生改变
D.常温下, 溶液的所有离子中, 的物质的量浓度最大5.铅蓄电池的两极分别为 ,电解质溶液为 。已知 难溶于稀硫酸,下列结论正确
的是( )
A.铅蓄电池属于一次电池 B.电池放电时,Pb电极发生还原反应
C.电池放电时,两极板质量均减轻 D.电池充电时, 电极接电源的正极
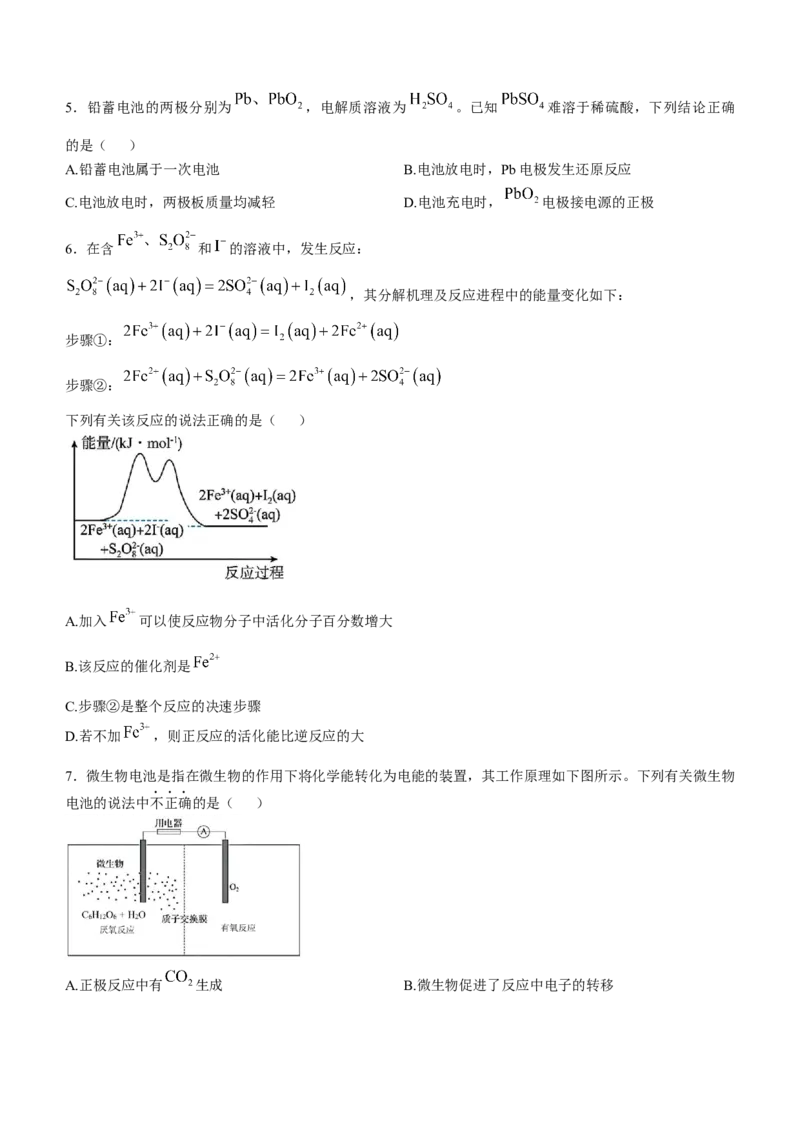
6.在含 和 的溶液中,发生反应:
,其分解机理及反应进程中的能量变化如下:
步骤①:
步骤②:
下列有关该反应的说法正确的是( )
A.加入 可以使反应物分子中活化分子百分数增大
B.该反应的催化剂是
C.步骤②是整个反应的决速步骤
D.若不加 ,则正反应的活化能比逆反应的大
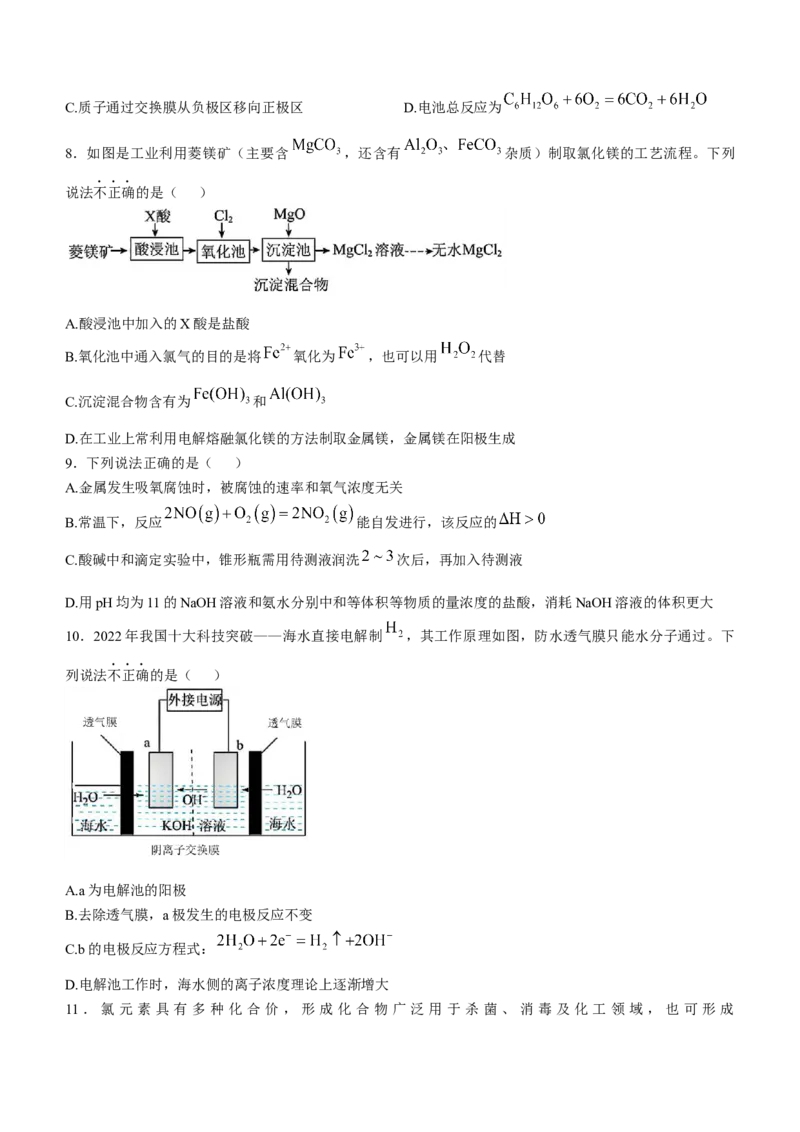
7.微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如下图所示。下列有关微生物
电池的说法中不正确的是( )
A.正极反应中有 生成 B.微生物促进了反应中电子的转移C.质子通过交换膜从负极区移向正极区 D.电池总反应为
8.如图是工业利用菱镁矿(主要含 ,还含有 杂质)制取氯化镁的工艺流程。下列
说法不正确的是( )
A.酸浸池中加入的X酸是盐酸
B.氧化池中通入氯气的目的是将 氧化为 ,也可以用 代替
C.沉淀混合物含有为 和
D.在工业上常利用电解熔融氯化镁的方法制取金属镁,金属镁在阳极生成
9.下列说法正确的是( )
A.金属发生吸氧腐蚀时,被腐蚀的速率和氧气浓度无关
B.常温下,反应 能自发进行,该反应的
C.酸碱中和滴定实验中,锥形瓶需用待测液润洗 次后,再加入待测液
D.用pH均为11的NaOH溶液和氨水分别中和等体积等物质的量浓度的盐酸,消耗NaOH溶液的体积更大
10.2022年我国十大科技突破——海水直接电解制 ,其工作原理如图,防水透气膜只能水分子通过。下
列说法不正确的是( )
A.a为电解池的阳极
B.去除透气膜,a极发生的电极反应不变
C.b的电极反应方程式:
D.电解池工作时,海水侧的离子浓度理论上逐渐增大
11 . 氯 元 素 具 有 多 种 化 合 价 , 形 成 化 合 物 广 泛 用 于 杀 菌 、 消 毒 及 化 工 领 域 , 也 可 形 成和 等离子,在一定条件下还能发生相互转化。在新型催化剂 作用下,
氧化HCl可获得 对于该反应下列说法正确的
是( )
A.该反应
B.4molHCl与 反应转移电子数约为
C. 的使用能降低该反应的焓变
D.反应的平衡常数
12.室温下,通过下列实验探究 溶液的性质。
实验1:实验测得 溶液pH为8.6。
实验2:向溶液中滴加等体积 溶液,pH由8.6降为4.8。
实验3:向溶液中加入等体积 溶液,出现白色沉淀。
实验4:向稀硫酸酸化的 溶液中滴加 溶液至溶液褪色。
已知室温时 ,下列说法正确的是( )
A. 溶液中满足:
B.实验2滴加盐酸过程中不可能满足:
C.实验3所得上层清液中
D.实验4发生反应离子方程式为:
13. 和 联合重整能减少温室气体的排放。重整时发生如下反应:
反应Ⅰ:
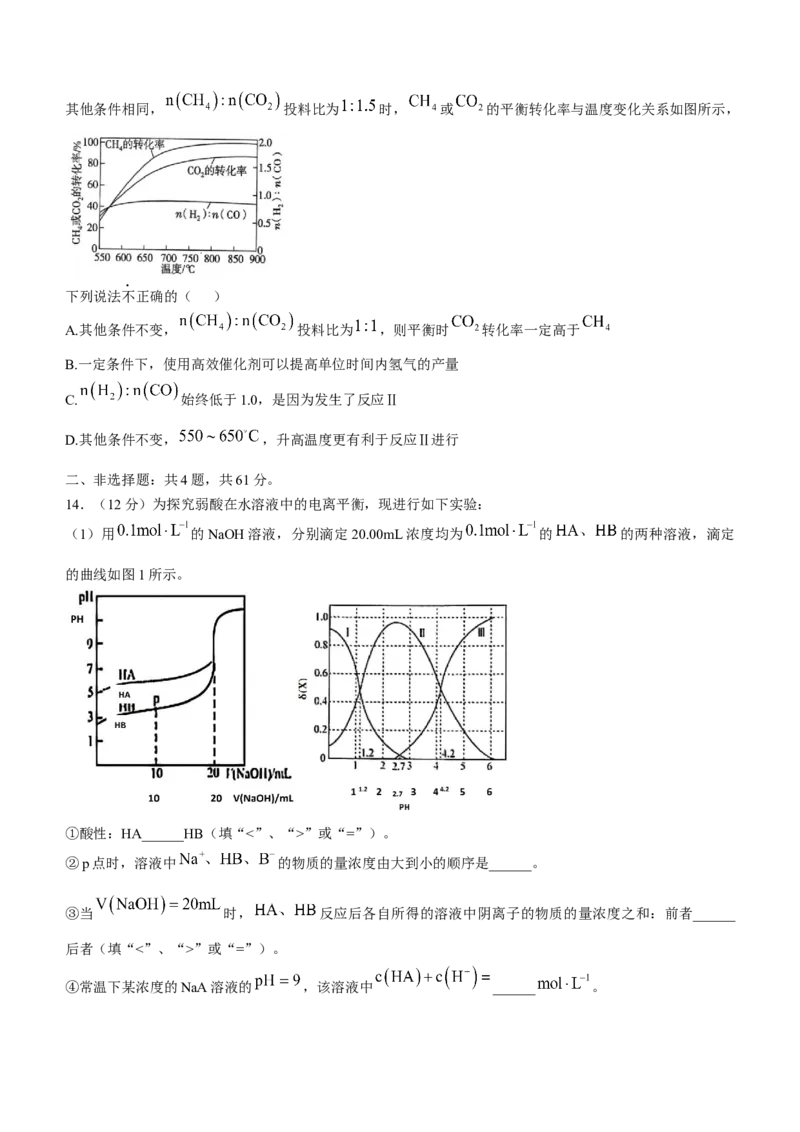
反应Ⅱ:其他条件相同, 投料比为 时, 或 的平衡转化率与温度变化关系如图所示,
下列说法不正确的( )
A.其他条件不变, 投料比为 ,则平衡时 转化率一定高于
B.一定条件下,使用高效催化剂可以提高单位时间内氢气的产量
C. 始终低于1.0,是因为发生了反应Ⅱ
D.其他条件不变, ,升高温度更有利于反应Ⅱ进行
二、非选择题:共4题,共61分。
14.(12分)为探究弱酸在水溶液中的电离平衡,现进行如下实验:
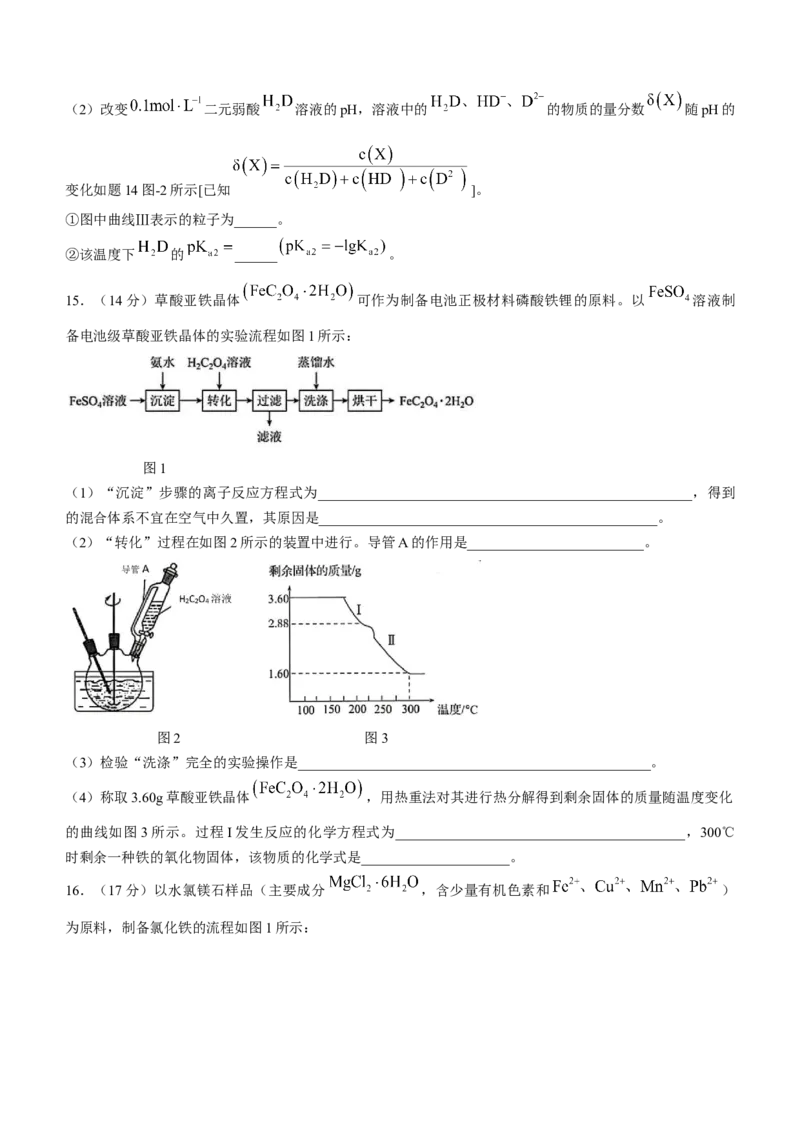
(1)用 的NaOH溶液,分别滴定20.00mL浓度均为 的 的两种溶液,滴定
的曲线如图1所示。
①酸性:HA______HB(填“<”、“>”或“=”)。
②p点时,溶液中 的物质的量浓度由大到小的顺序是______。
③当 时, 反应后各自所得的溶液中阴离子的物质的量浓度之和:前者______
后者(填“<”、“>”或“=”)。
④常温下某浓度的NaA溶液的 ,该溶液中 ______ 。(2)改变 二元弱酸 溶液的pH,溶液中的 的物质的量分数 随pH的
变化如题14图-2所示[已知 ]。
①图中曲线Ⅲ表示的粒子为______。
②该温度下 的 ______ 。
15.(14分)草酸亚铁晶体 可作为制备电池正极材料磷酸铁锂的原料。以 溶液制
备电池级草酸亚铁晶体的实验流程如图1所示:
图1
(1)“沉淀”步骤的离子反应方程式为_____________________________________________________,得到
的混合体系不宜在空气中久置,其原因是________________________________________________。
(2)“转化”过程在如图2所示的装置中进行。导管A的作用是_________________________。
图2 图3
(3)检验“洗涤”完全的实验操作是__________________________________________________。
(4)称取3.60g草酸亚铁晶体 ,用热重法对其进行热分解得到剩余固体的质量随温度变化
的曲线如图3所示。过程I发生反应的化学方程式为_________________________________________,300℃
时剩余一种铁的氧化物固体,该物质的化学式是_____________________。
16.(17分)以水氯镁石样品(主要成分 ,含少量有机色素和 )
为原料,制备氯化铁的流程如图1所示:图1 图2
(1)脱色
①此过程中 能产生 (羟基自由基),可使部分有机色素转化为 和 。 体现的性质是
______。
②相同时间内,测得不同温度下脱色率的变化如图 2所示。50℃后脱色率随着温度升高而下降,原因是
______。
(2)沉淀
①加氨水调节pH时, 转化成 的离子方程式为______。加入 之前需加热使多余的
分解,原因是______。
(2)已知: 室温下 ,溶液中离子浓度小于 或等于
即认为已经除尽。除 离子时, 均沉淀完全,此时需控制溶液中
不低于______。
(3)测定产品中 含量的实验方案如下:
取一定量样品溶于水,加水定容至 500mL。取 10.00mL 所得溶液于锥形瓶中,滴加 的
溶液20.00mL,充分反应后,过滤。向滤液中加入指示剂,用 溶液滴定至
终点。重复上述实验3次,平均消耗的 溶液10.00mL。
已知:
①实验过程中不需要的实验仪器有____________________。
a.胶头滴管 b.250mL容量瓶 c.酸式滴定管 d.锥形瓶
②样品中 的物质的量为____________。(写出计算过程)17.(18分)我国力争在2060年前实现“碳中和”,体现了中国对解决气候问题的大国担当。为此我国制
定了实现“碳中和”和“温室气体净零排放”的长期战略目标。 的转化、回收和重整受到越来越多的关
注,它是有效应对全球气候变化、促进低碳社会构建的重要方法。
(1)热化学转化法。科学家研究利用回收的 制取甲酸 。
(1)已知:Ⅰ: ;
Ⅱ. ;
Ⅲ.
则反应Ⅳ: 的 ______。
②查阅资料可知在过渡金属催化剂存在下, 和 合成 的反应分两步进行:
已知第二步反应的方程式为 ;则第一步反应的方程式为______。
③工业上利用 ,合成甲醚。向一绝热恒容密闭
容器中,加入 和 发生上述反应,能够说明该反应达到平衡状态的是______(填字母)
a.
b.容器内气体的密度保持不变
c.容器内温度保持不变
d.容器内 比值保持不变
(2)催化还原法
图1 图2
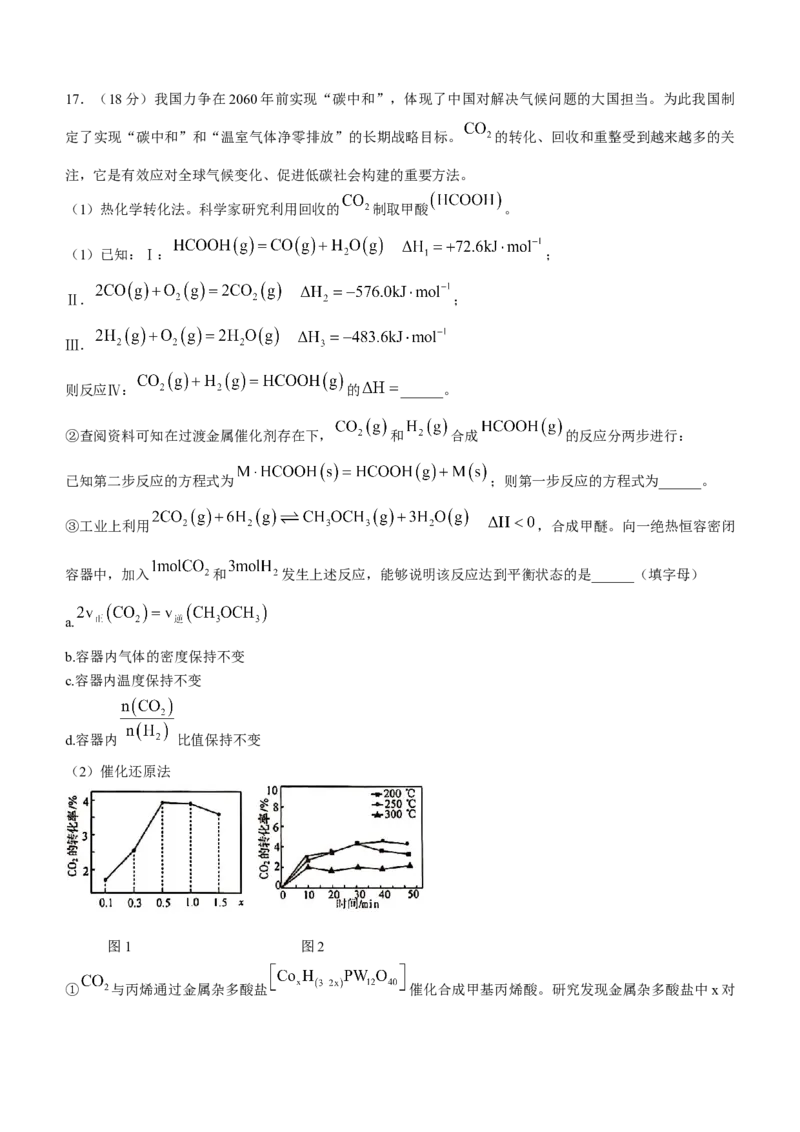
① 与丙烯通过金属杂多酸盐 催化合成甲基丙烯酸。研究发现金属杂多酸盐中x对转化率的影响如图1所示,由图1得出催化效果最好的金属杂多酸盐化学式是______。
②催化剂在温度不同时对 转化率的影响如图2所示, 催化效果远不如 和 的原因
____________。
(3)电化学法
催化加氢制甲醇有利于减少 的排放,我国科研团队在 电化学还原反应机理的研究上取得新突
破,明确两电子转移 电化学还原反应的控速步骤为 吸附过程。 电化学还原法中采用 纳米
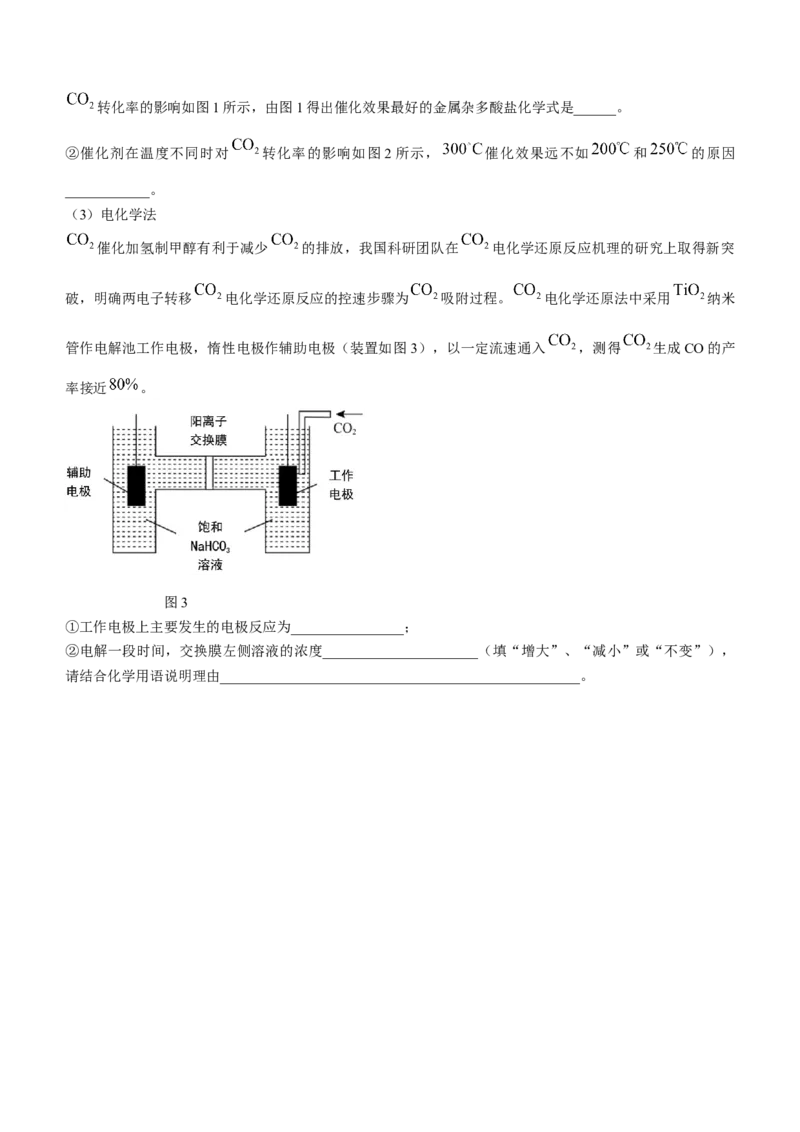
管作电解池工作电极,惰性电极作辅助电极(装置如图3),以一定流速通入 ,测得 生成CO的产
率接近 。
图3
①工作电极上主要发生的电极反应为________________;
②电解一段时间,交换膜左侧溶液的浓度______________________(填“增大”、“减小”或“不变”),
请结合化学用语说明理由___________________________________________________。高二化学试题参考答案
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1.B 2.C 3.D 4.C 5.D 6.A 7.A 8.D 9.D 10.B 11.A 12.C1 3.D
二、非选择题:共4题,共61分。
14.(12分)
(1)① (2分) ② (2分) ③ (2分) ④ (2分)
(2)① (2分) ②4.2(2分)
15.(14分)
(1) (3分)
在空气中容易被氧气氧化为 ,导致草酸亚铁产率降低。(2分)
(2)平衡气压,使 溶液顺利滴入三颈烧瓶中。(2分)
(3)取最后一次洗涤滤液少许于试管中,先滴加盐酸酸化,再滴加氯化钡溶液,若无白色沉淀,则已经洗涤
干净。(2分)
(4) (3分)
16.(17分)
(1)①氧化性(2分) ②温度过高,双氧水受热分解生成水和氧气(2分)
(2)① 或
(3分) 防止多余的 氧化 ,增加 消
耗量。(2分)
② (2分)
(3)①b(2分) ② (共4分,结果2分,计算过程2分)(写出计算过程)
17.(18分)
(1)① ② ③c(2分)
(2)① 或 (2分)
②温度过高,可能会导致催化剂失活(2分)
(3)① ②减小阳极电极反应式为 ,同时发生反应 减小,
而 通过阳离子交换膜从左侧向右侧移动,所以左侧溶液浓度减小(2分)