文档内容
重庆八中 2024-2025 学年度(上)高二年级第一次月考
化 学 试 题
命题:谢苏菲 杨利敏 审核:林培龙 打印:谢苏菲 校对:杨利敏
可能用到的相对原子质量:H-1 C-12 O-16 V-51
一. 选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有
一项是符合题目要求的。
1. 化学与社会、生产、生活密切相关,下列说法错误的是
A.废旧钢材焊接前,可用饱和NH Cl溶液处理焊点的铁锈
4
B.生活中常用明矾净水,可加速水中悬浮物沉降
C.将草木灰与NH Cl混合施用,可更好为植物全面提供N、K两种营养元素
4
D.加热纯碱溶液可以增强其去油污的能力
2. 下列事实能说明醋酸是弱电解质的是
①醋酸与水能以任意比互溶 ②常温下0.1 mol/L醋酸钠溶液的pH=8.9
③醋酸溶液中存在醋酸分子 ④同温下,0.1 mol/L醋酸的pH比0.1 mol/L盐酸的pH大
⑤醋酸溶液能导电
A.①⑤ B.②③④ C.③④⑤ D.①②
3. 25℃时,将pH=4的NH Cl溶液加水稀释过程中,下列说法正确的是
4
A.能使NH Cl的水解常数K 增大 B.溶液中c(H+)•c(OH-)不变
4 h
C.能使溶液中n(NH +)增大 D.此过程中,溶液中所有离子浓度均减小
4
4. 下列事实能用勒夏特列原理解释的是
A.工业合成氨选择500 ℃
B.SO 氧化成SO ,需要使用催化剂
2 3
C.光照新制氯水时,溶液的颜色逐渐变浅
D.由NO (g)和N O (g)组成的平衡体系,加压后颜色加深
2 2 4
5. 常温下,下列溶液中各组离子一定能大量共存的是
A.由水电离产生的c(H+)=10-12 mol/L的溶液:K+、SO 2-、CO 2-、Cl-
4 3
B.K / c(H+)=0.1mol/L的溶液:Na+、K+、CO 2-、NO -
w 3 3
C.pH=7的溶液中,Na+、Fe3+、CO 2-、Cl-
3
D.含有S2-的溶液:Cu2+、H+、MnO -、SO 2-
4 4
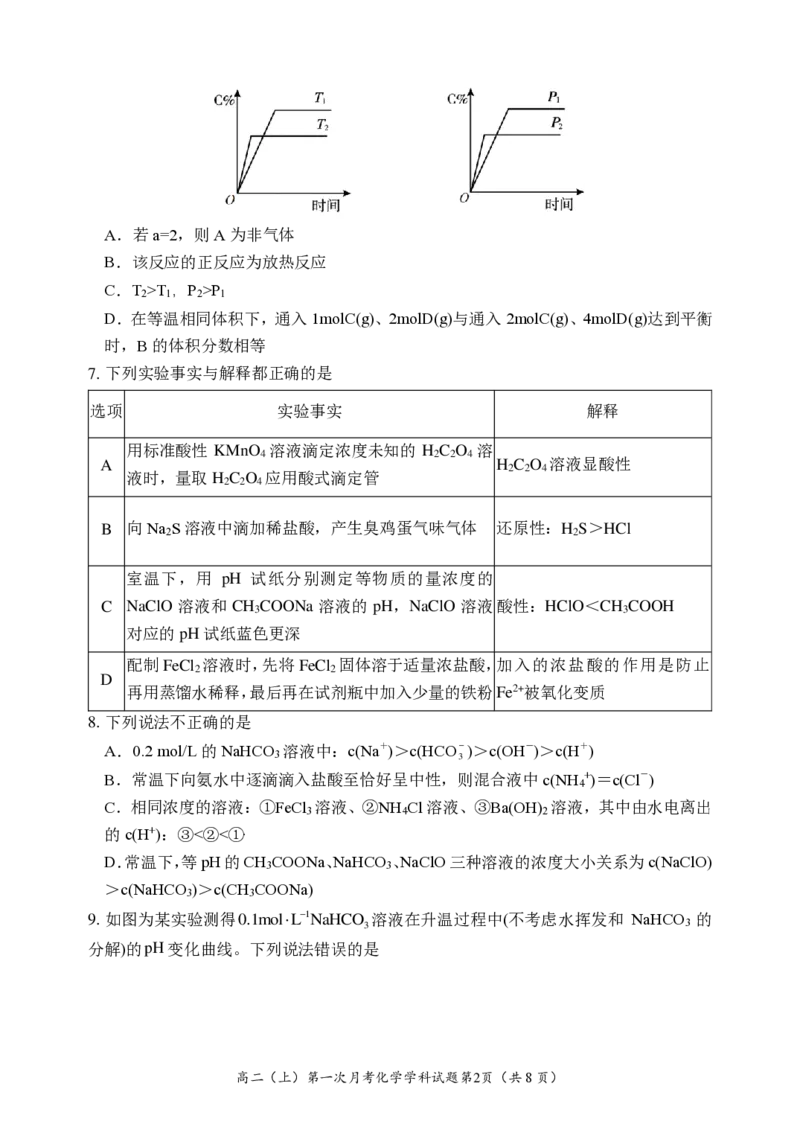
6. 可逆反应A(?)+aB(g) C(g)+2D(g)(a为正整数)。反应过程中,当其他条件不变时,C
的百分含量与温度(T)和压强(P)的关系如图所示。下列说法不正确的是
高二(上)第一次月考化学学科试题第1页(共8页)A.若a=2,则A为非气体
B.该反应的正反应为放热反应
C.T >T ,P >P
2 1 2 1
D.在等温相同体积下,通入1molC(g)、2molD(g)与通入2molC(g)、4molD(g)达到平衡
时,B的体积分数相等
7. 下列实验事实与解释都正确的是
选项 实验事实 解释
用标准酸性 KMnO 溶液滴定浓度未知的 H C O 溶
4 2 2 4
A H C O 溶液显酸性
2 2 4
液时,量取H C O 应用酸式滴定管
2 2 4
B 向Na S溶液中滴加稀盐酸,产生臭鸡蛋气味气体 还原性:H S>HCl
2 2
室温下,用 pH 试纸分别测定等物质的量浓度的
C NaClO 溶液和 CH COONa 溶液的 pH,NaClO 溶液酸性:HClO<CH COOH
3 3
对应的pH试纸蓝色更深
配制FeCl 溶液时,先将FeCl 固体溶于适量浓盐酸,加入的浓盐酸的作用是防止
2 2
D
再用蒸馏水稀释,最后再在试剂瓶中加入少量的铁粉 Fe2+被氧化变质
8. 下列说法不正确的是
A.0.2 mol/L的NaHCO 溶液中:c(Na+)>c(HCO
3
高二(上)第一次月考化学学科试题第2页(共8页)
−3 )>c(OH-)>c(H+)
B.常温下向氨水中逐滴滴入盐酸至恰好呈中性,则混合液中c(NH +)=c(Cl-)
4
C.相同浓度的溶液:①FeCl 溶液、②NH Cl溶液、③Ba(OH) 溶液,其中由水电离出
3 4 2
的c(H+):③<②<①
D.常温下,等pH的CH COONa、NaHCO 、NaClO三种溶液的浓度大小关系为c(NaClO)
3 3
>c(NaHCO )>c(CH COONa)
3 3
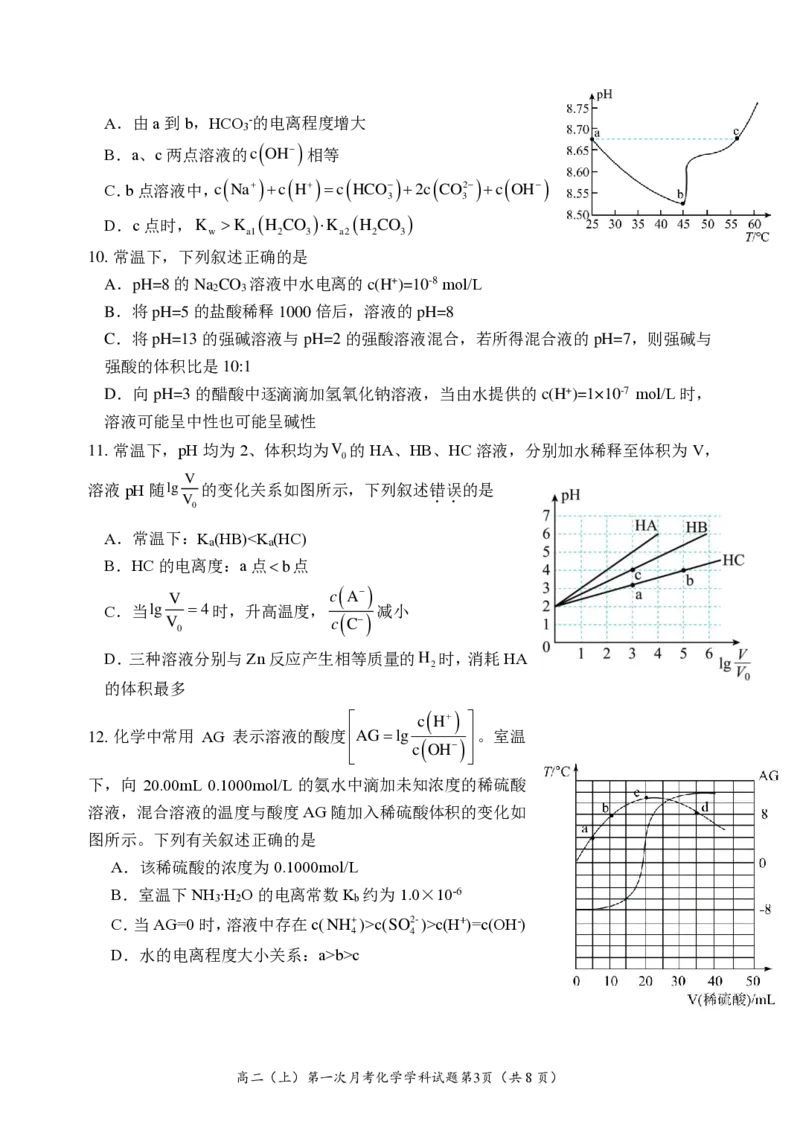
9. 如图为某实验测得 0 .1 m o l L − 1 N a H C O
3
溶液在升温过程中(不考虑水挥发和 NaHCO 的
3
分解)的pH变化曲线。下列说法错误的是A.由a到b,HCO -的电离程度增大
3
B.a、c两点溶液的
高二(上)第一次月考化学学科试题第3页(共8页)
c ( O H − ) 相等
C.b点溶液中, c ( N a + ) + c ( H + ) = c ( H C O −3 ) + 2 c ( C O 23 − ) + c ( O H − )
D.c点时, K
w
K
a1
( H
2
C O
3
) K
a 2
( H
2
C O
3
)
10. 常温下,下列叙述正确的是
A.pH=8的Na CO 溶液中水电离的c(H+)=10-8 mol/L
2 3
B.将pH=5的盐酸稀释1000倍后,溶液的pH=8
C.将pH=13的强碱溶液与pH=2的强酸溶液混合,若所得混合液的pH=7,则强碱与
强酸的体积比是 10:1
D.向pH=3的醋酸中逐滴滴加氢氧化钠溶液,当由水提供的c(H+)=1×10-7 mol/L时,
溶液可能呈中性也可能呈碱性
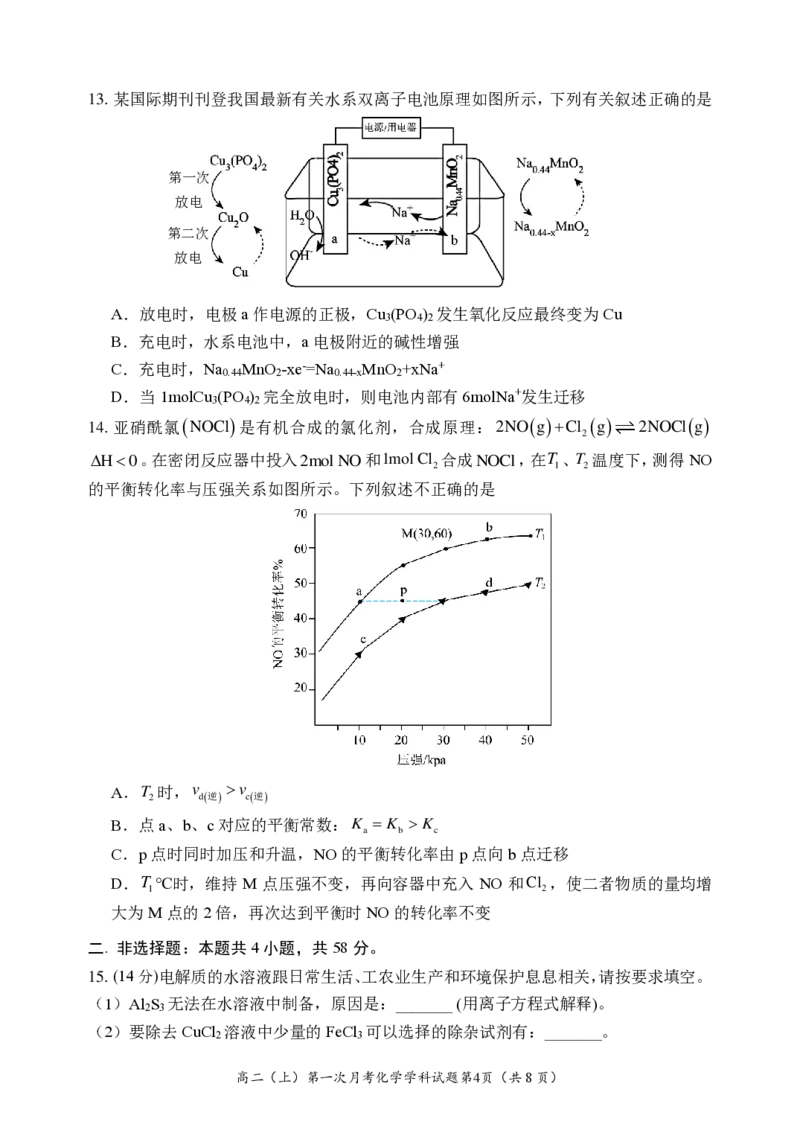
11. 常温下,pH均为 2、体积均为V 的HA、HB、HC 溶液,分别加水稀释至体积为V,
0
V
溶液pH随lg 的变化关系如图所示,下列叙述错误的是
V ..
0
A.常温下:K (HB)c(
4
S O 24 - )>c(H+)=c(OH-)
D.水的电离程度大小关系:a>b>c13. 某国际期刊刊登我国最新有关水系双离子电池原理如图所示,下列有关叙述正确的是
A.放电时,电极a作电源的正极,Cu (PO ) 发生氧化反应最终变为Cu
3 4 2
B.充电时,水系电池中,a电极附近的碱性增强
C.充电时,Na MnO -xe-=Na MnO +xNa+
0.44 2 0.44-x 2
D.当1molCu (PO ) 完全放电时,则电池内部有6molNa+发生迁移
3 4 2
14. 亚硝酰氯
高二(上)第一次月考化学学科试题第4页(共8页)
( N O C l ) 是有机合成的氯化剂,合成原理:
H 0
2 N O ( g ) + C l
2
( g ) 2 N O C l ( g )
。在密闭反应器中投入2mol NO和 1 m o l C l
2
合成 N O C l ,在 T
1
、 T
2
温度下,测得NO
的平衡转化率与压强关系如图所示。下列叙述不正确的是
A. T
2
时,v v
d(逆) c(逆)
B.点a、b、c对应的平衡常数:K =K K
a b c
C.p点时同时加压和升温,NO的平衡转化率由p点向b点迁移
D. T
1
℃时,维持 M 点压强不变,再向容器中充入 NO 和 C l
2
第一次
放电
第二次
放电
,使二者物质的量均增
大为M点的2倍,再次达到平衡时NO的转化率不变
二. 非选择题:本题共4小题,共58分。
15. (14分)电解质的水溶液跟日常生活、工农业生产和环境保护息息相关,请按要求填空。
(1)Al S 无法在水溶液中制备,原因是:_______ (用离子方程式解释)。
2 3
(2)要除去CuCl 溶液中少量的FeCl 可以选择的除杂试剂有:_______。
2 3A.NaOH B.Cu(OH) C.NH ·H O D.Cu (OH) CO
2 3 2 2 2 3
(3)从MgCl 溶液中得到MgCl 固体的操作是_______。
2 2
(4)蒸干并灼烧Ca(ClO) 溶液,得到的产物是_______(填化学式)。
2
(5)已知25°C时,
高二(上)第一次月考化学学科试题第5页(共8页)
C H
3
C O O H 的 K
a
= 1 .8 1 0 − 5 ; H
2
C O
3
的: K
a1
= 4 .3 1 0 − 7 , K
a 2
= 5 .6 1 0 − 1 1 ;
HCN的 K
a
= 6 .2 1 0 − 1 0 ,回答下列问题:
①25°C时,向NaCN溶液中通入少量CO ,反应的离子方程式为 。
2
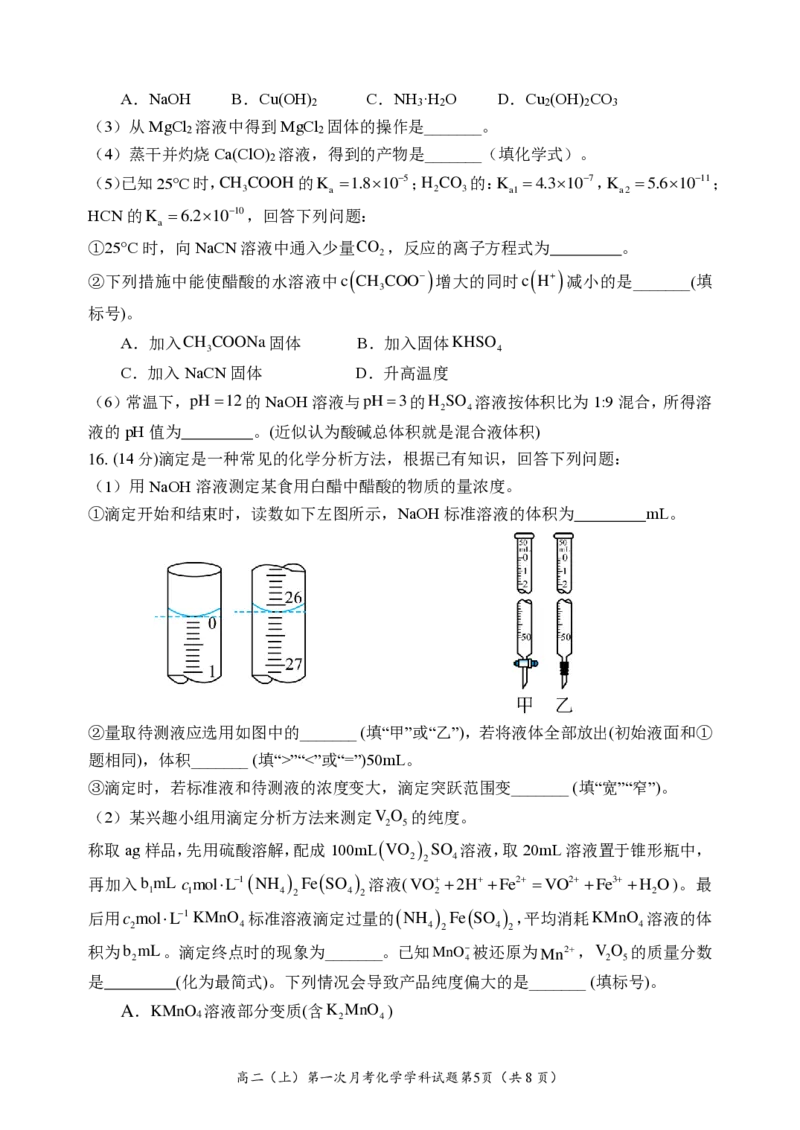
②下列措施中能使醋酸的水溶液中c
(
CH
COO−)
增大的同时c
( H+)
减小的是_______(填
3
标号)。
A.加入 C H
3
C O O N a 固体 B.加入固体 K H S O
4
C.加入NaCN固体 D.升高温度
(6)常温下, p H = 1 2 的NaOH溶液与 p H = 3 的 H
2
S O
4
溶液按体积比为1:9混合,所得溶
液的pH值为 。(近似认为酸碱总体积就是混合液体积)
16. (14分)滴定是一种常见的化学分析方法,根据已有知识,回答下列问题:
(1)用NaOH溶液测定某食用白醋中醋酸的物质的量浓度。
①滴定开始和结束时,读数如下左图所示,NaOH标准溶液的体积为 mL。
②量取待测液应选用如图中的_______ (填“甲”或“乙”),若将液体全部放出(初始液面和①
题相同),体积_______ (填“>”“<”或“=”)50mL。
③滴定时,若标准液和待测液的浓度变大,滴定突跃范围变_______ (填“宽”“窄”)。
(2)某兴趣小组用滴定分析方法来测定 V
2
O
5
的纯度。
称取ag样品,先用硫酸溶解,配成100mL ( V O
2
)
2
S O
4
溶液,取20mL溶液置于锥形瓶中,
再加入bmL
1
c
1
m o l L − 1 ( N H
4
)
2
F e ( S O
4
)
2
溶液(VO++2H++Fe2+ =VO2++Fe3++H O )。最
2 2
后用c molL−1
2
K M n O
4
标准溶液滴定过量的(NH ) Fe(SO ) ,平均消耗
4 2 4 2
K M n O
4
溶液的体
积为b mL。滴定终点时的现象为_______。已知MnO−被还原为Mn2+,VO 的质量分数
2 4 2 5
是 (化为最简式)。下列情况会导致产品纯度偏大的是_______ (填标号)。
A.KMnO 溶液部分变质(含K MnO )
4 2 4B.滴定达终点时,仰视刻度线读数
C.滴定终点时,滴定管尖嘴内有气泡生成
D.
高二(上)第一次月考化学学科试题第6页(共8页)
( N H
4
)
2
F e ( S O
4
)
2
溶液因露空放置太久而变质
E.酸式滴定管未用 K M n O
4
标准溶液润洗
17. (14分)为更有效处理工业废气中排放的氮氧化物(NO )、SO 等,减少大气污染。科学
x 2
家不断对相关反应进行研究尝试。
(1)下列溶液中,能吸收SO 的有_______(填序号)。
2
a.饱和NaHSO 溶液 b.酸性KMnO 溶液 c.Na CO 溶液 d. 品红溶液
3 4 2 3
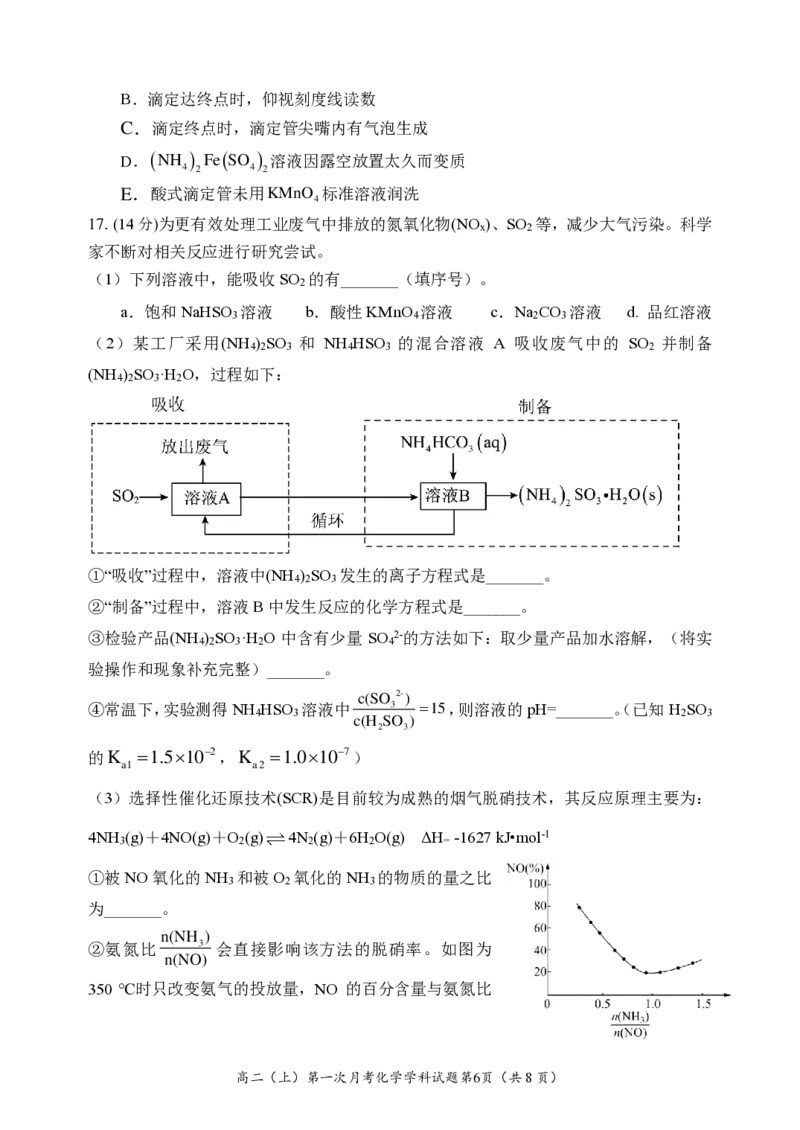
(2)某工厂采用(NH ) SO 和 NH HSO 的混合溶液 A 吸收废气中的 SO 并制备
4 2 3 4 3 2
(NH ) SO ·H O,过程如下:
4 2 3 2
①“吸收”过程中,溶液中(NH ) SO 发生的离子方程式是_______。
4 2 3
②“制备”过程中,溶液B中发生反应的化学方程式是_______。
③检验产品(NH ) SO ·H O 中含有少量 SO 2-的方法如下:取少量产品加水溶解,(将实
4 2 3 2 4
验操作和现象补充完整)_______。
④常温下,实验测得NH HSO 溶液中
4 3
c ( S
c ( H
O
S2
2- )
3O
)
3
= 1 5 ,则溶液的pH=_______。(已知H SO
2 3
的 K
a 1
= 1 .5 1 0 − 2 , K
a 2
= 1 . 0 1 0 − 7 )
(3)选择性催化还原技术(SCR)是目前较为成熟的烟气脱硝技术,其反应原理主要为:
4NH (g)+4NO(g)+O (g) 4N (g)+6H O(g) ΔH -1627 kJ•mol-1
3 2 2 2 =
①被NO氧化的NH 和被O 氧化的NH 的物质的量之比
3 2 3
为_______。
n(NH )
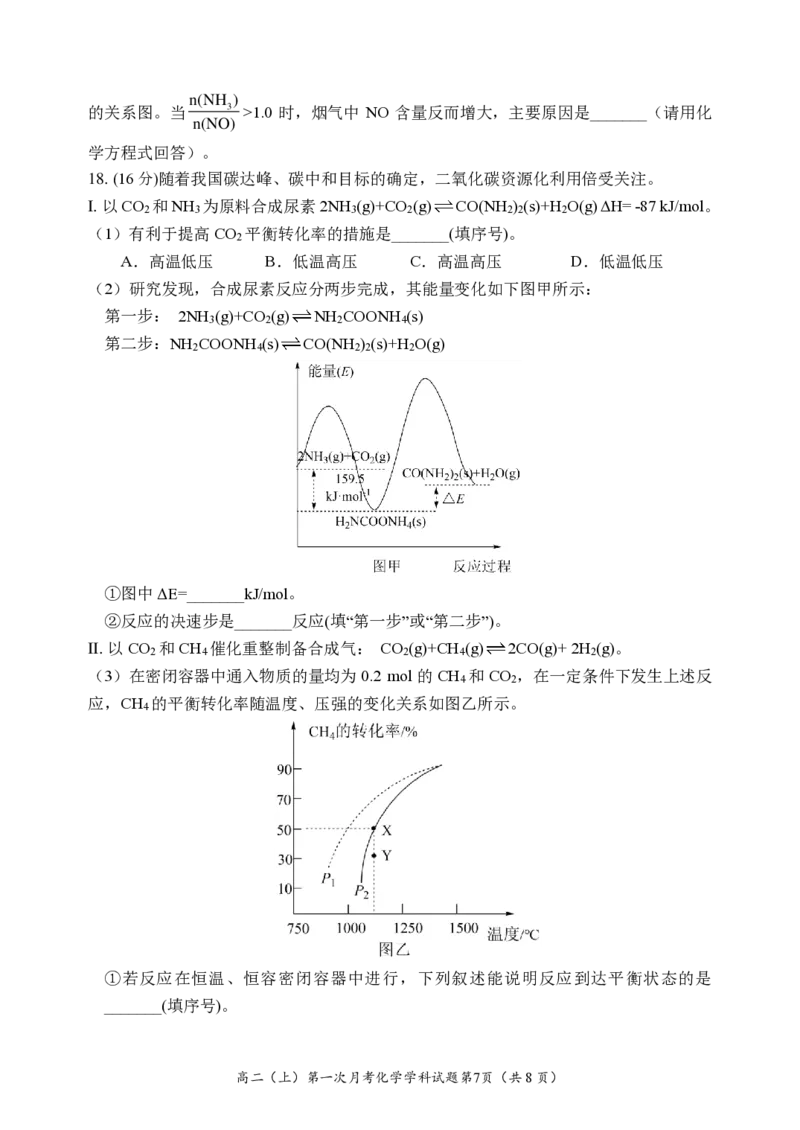
②氨氮比 3 会直接影响该方法的脱硝率。如图为
n(NO)
350 ℃时只改变氨气的投放量,NO 的百分含量与氨氮比的关系图。当
高二(上)第一次月考化学学科试题第7页(共8页)
n
n
( N
( N
H
O
)
3) >1.0 时,烟气中 NO 含量反而增大,主要原因是_______(请用化
学方程式回答)。
18. (16分)随着我国碳达峰、碳中和目标的确定,二氧化碳资源化利用倍受关注。
I. 以CO 和NH 为原料合成尿素2NH (g)+CO (g) CO(NH ) (s)+H O(g) ∆H= -87 kJ/mol。
2 3 3 2 2 2 2
(1)有利于提高CO 平衡转化率的措施是_______(填序号)。
2
A.高温低压 B.低温高压 C.高温高压 D.低温低压
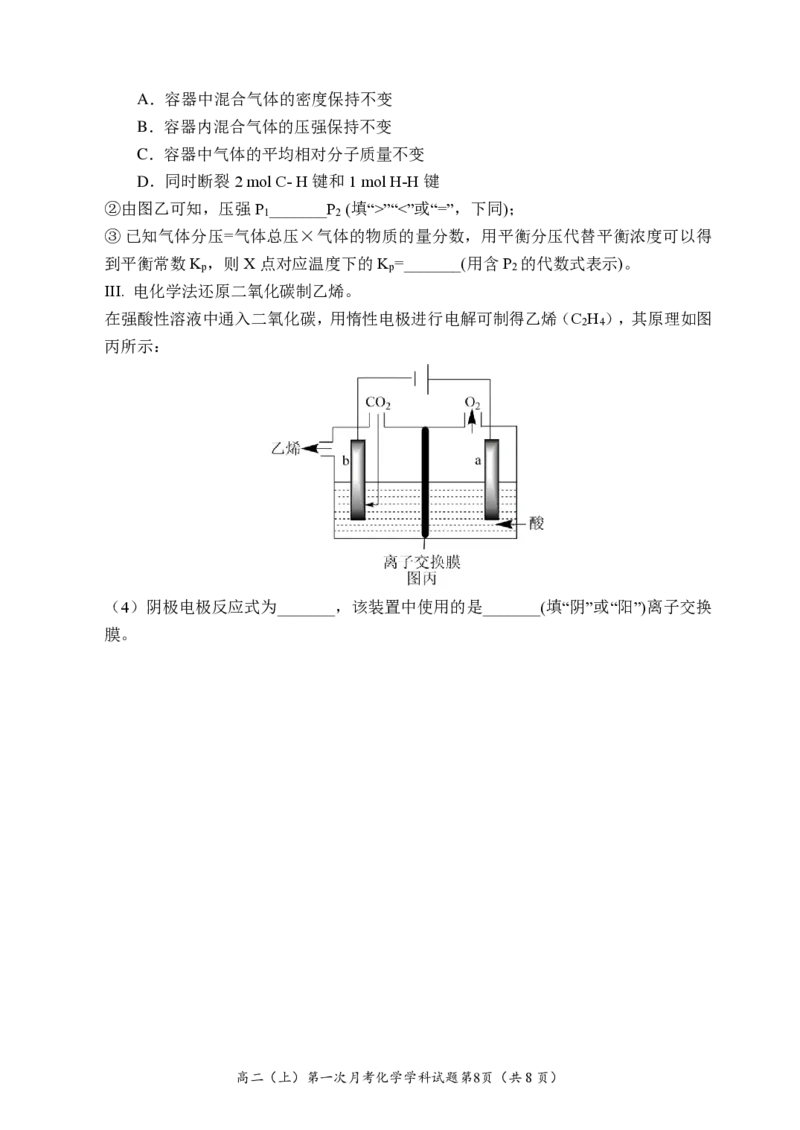
(2)研究发现,合成尿素反应分两步完成,其能量变化如下图甲所示:
第一步: 2NH (g)+CO (g) NH COONH (s)
3 2 2 4
第二步:NH COONH (s) CO(NH ) (s)+H O(g)
2 4 2 2 2
①图中ΔE=_______kJ/mol。
②反应的决速步是_______反应(填“第一步”或“第二步”)。
II. 以CO 和CH 催化重整制备合成气: CO (g)+CH (g) 2CO(g)+ 2H (g)。
2 4 2 4 2
(3)在密闭容器中通入物质的量均为0.2 mol的CH 和CO ,在一定条件下发生上述反
4 2
应,CH 的平衡转化率随温度、压强的变化关系如图乙所示。
4
①若反应在恒温、恒容密闭容器中进行,下列叙述能说明反应到达平衡状态的是
_______(填序号)。A.容器中混合气体的密度保持不变
B.容器内混合气体的压强保持不变
C.容器中气体的平均相对分子质量不变
D.同时断裂2 mol C- H键和1 mol H-H键
②由图乙可知,压强P _______P (填“>”“<”或“=”,下同);
1 2
③ 已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得
到平衡常数K ,则X点对应温度下的K =_______(用含P 的代数式表示)。
p p 2
III. 电化学法还原二氧化碳制乙烯。
在强酸性溶液中通入二氧化碳,用惰性电极进行电解可制得乙烯(C H ),其原理如图
2 4
丙所示:
(4)阴极电极反应式为_______,该装置中使用的是_______(填“阴”或“阳”)离子交换
膜。
高二(上)第一次月考化学学科试题第8页(共8页)