文档内容
(在此卷上答题无效)
福建省漳州市 2025 届高三毕业班第一次教学质量检测
化学试题
本试题卷共6页,14题.满分100分,考试用时75分钟.
可能用到的相对原子质量:
一、选择题:本题共10小题,每小题4分,共40分.在每小题给出的四个选项中,只有一项
是符合题目要求的.
1.《本草纲目》中记载“冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”.下列说法错误的是( )
A.“薪柴”主要含纤维素等有机物
B.“薪柴之灰”可用作农用肥,但不宜与铵态氮肥混用
C.“以灰淋汁”涉及的分离操作有溶解、分液
D.“取碱浣衣”与水解反应有关
2.对乙酰氨基酚是一种用于治疗疼痛与发热的药物,其分子结构如图示.下列有关对乙酰氨基酚的说法错误
的是( )
A.分子式为
B.能发生氧化反应和取代反应
C.分子中所有原子不可能共平面
D. 对乙酰氨基酚最多能与 发生反应
3.短周期主族元素X、Y、Z、W的原子序数依次增大,X的一种核素没有中子,基态Y原子的p轨道半充
满,Z元素的一种单质是植物光合作用的产物之一,W与Z同主族.下列说法正确的是( )
A、元素的第一电离能: B.简单氢化物的键角:
C.简单氢化物的沸点: D.由X、Y、Z三种元素组成的化合物的水溶液均显酸性
4.侯氏制碱法制取 的反应原理为 .设 为阿
伏加德罗常数的值,下列说法正确的是( )
A. 晶体中含离子数目为
B.标准状况下, 含σ键数目为C. 溶液中, 数目为
D. 与足量 充分反应生成 ,转移电子数目为
5.关于反应 (浓) ,下列说法正确的是( )
A.该反应中浓硫酸仅体现强氧化性
B.氧化剂与还原剂的物质的量之比为
C.浓硫酸的氧化性强于硫酸铜
D. 浓硫酸与足量 反应,转移 电子
6.下列离子方程式正确的是( )
A. 与 反应:
B. 溶液与 反应:
C. 与 溶液反应:
D. 溶液与过量浓氨水反应:
7.室温下,下列各组离子在指定溶液中能大量共存的是( )
A. 的溶液:
B. 溶液:
C.含大量 的溶液:
D.无色溶液:
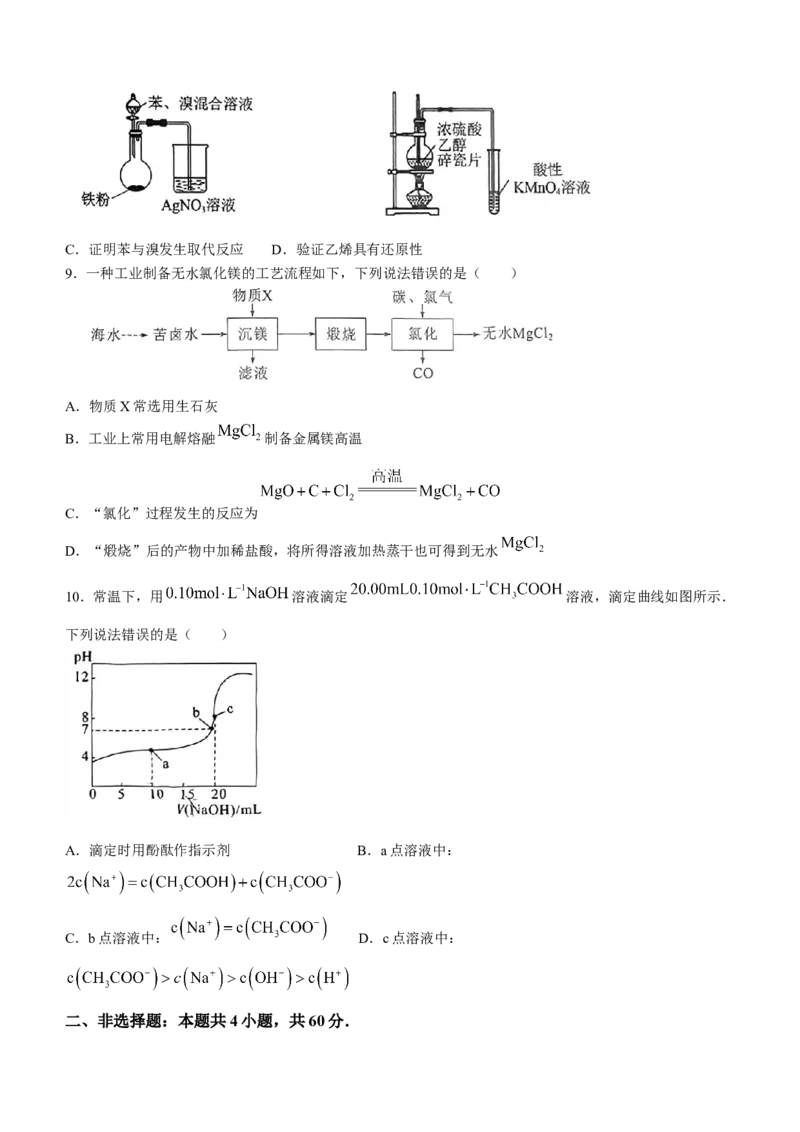
8.下列装置能达到实验目的的是( )
A.制备乙酸乙酯 B.验证 溶解性C.证明苯与溴发生取代反应 D.验证乙烯具有还原性
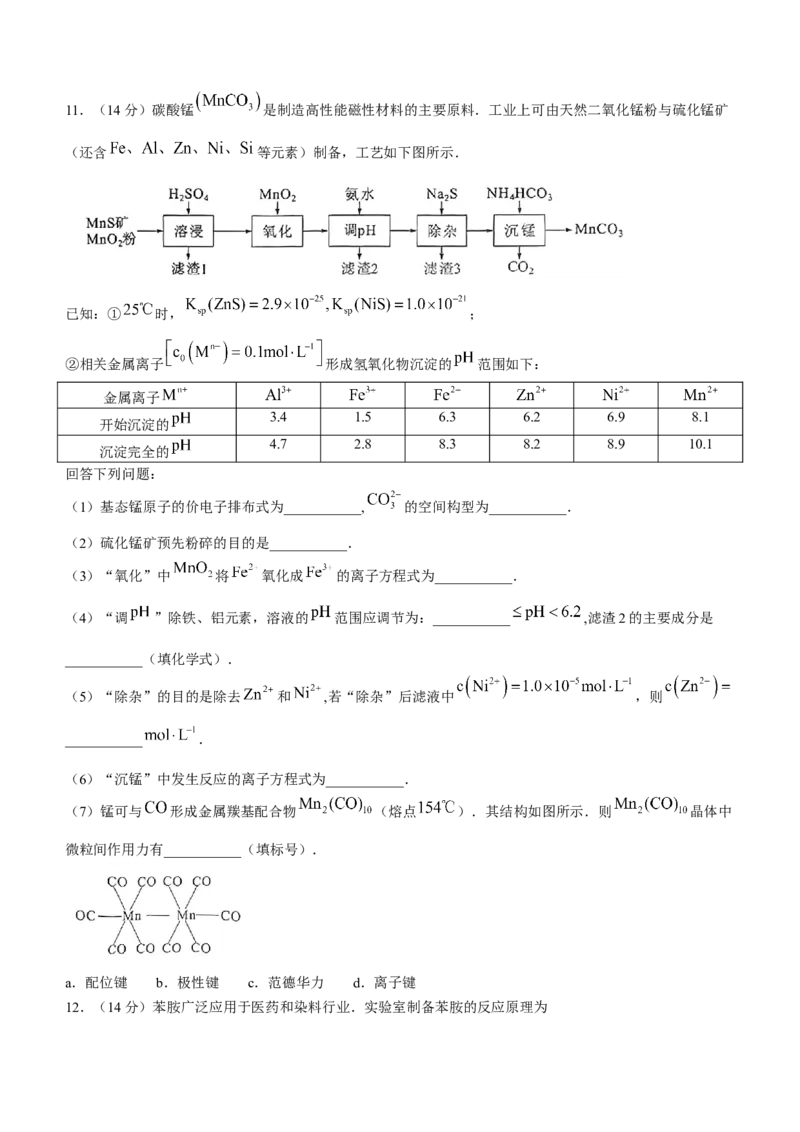
9.一种工业制备无水氯化镁的工艺流程如下,下列说法错误的是( )
A.物质X常选用生石灰
B.工业上常用电解熔融 制备金属镁高温
C.“氯化”过程发生的反应为
D.“煅烧”后的产物中加稀盐酸,将所得溶液加热蒸干也可得到无水
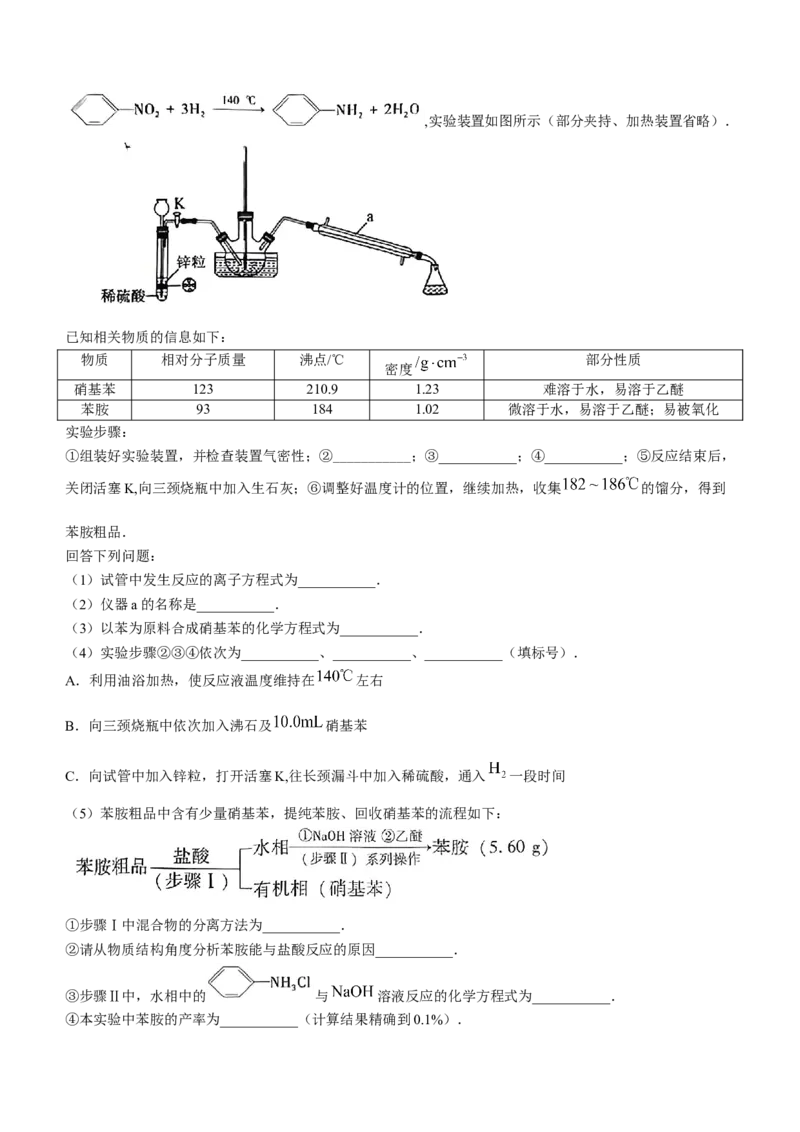
10.常温下,用 溶液滴定 溶液,滴定曲线如图所示.
下列说法错误的是( )
A.滴定时用酚酞作指示剂 B.a点溶液中:
C.b点溶液中: D.c点溶液中:
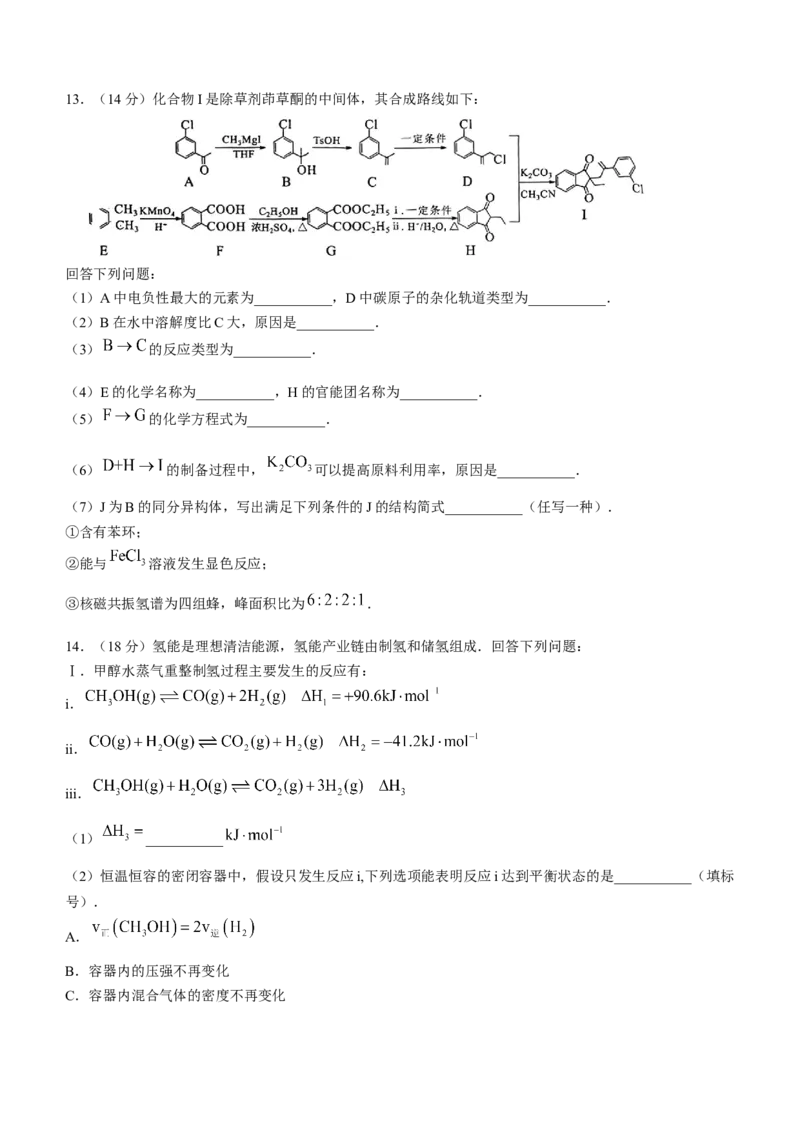
二、非选择题:本题共4小题,共60分.11.(14分)碳酸锰 是制造高性能磁性材料的主要原料.工业上可由天然二氧化锰粉与硫化锰矿
(还含 等元素)制备,工艺如下图所示.
已知:① 时, ;
②相关金属离子 形成氢氧化物沉淀的 范围如下:
金属离子
3.4 1.5 6.3 6.2 6.9 8.1
开始沉淀的
4.7 2.8 8.3 8.2 8.9 10.1
沉淀完全的
回答下列问题:
(1)基态锰原子的价电子排布式为___________, 的空间构型为___________.
(2)硫化锰矿预先粉碎的目的是___________.
(3)“氧化”中 将 氧化成 的离子方程式为___________.
(4)“调 ”除铁、铝元素,溶液的 范围应调节为:___________ ,滤渣2的主要成分是
___________(填化学式).
(5)“除杂”的目的是除去 和 ,若“除杂”后滤液中 ,则
___________ .
(6)“沉锰”中发生反应的离子方程式为___________.
(7)锰可与 形成金属羰基配合物 (熔点 ).其结构如图所示.则 晶体中
微粒间作用力有___________(填标号).
a.配位键 b.极性键 c.范德华力 d.离子键
12.(14分)苯胺广泛应用于医药和染料行业.实验室制备苯胺的反应原理为,实验装置如图所示(部分夹持、加热装置省略).
已知相关物质的信息如下:
物质 相对分子质量 沸点/℃ 部分性质
密度
硝基苯 123 210.9 1.23 难溶于水,易溶于乙醚
苯胺 93 184 1.02 微溶于水,易溶于乙醚;易被氧化
实验步骤:
①组装好实验装置,并检查装置气密性;②___________;③___________;④___________;⑤反应结束后,
关闭活塞K,向三颈烧瓶中加入生石灰;⑥调整好温度计的位置,继续加热,收集 的馏分,得到
苯胺粗品.
回答下列问题:
(1)试管中发生反应的离子方程式为___________.
(2)仪器a的名称是___________.
(3)以苯为原料合成硝基苯的化学方程式为___________.
(4)实验步骤②③④依次为___________、___________、___________(填标号).
A.利用油浴加热,使反应液温度维持在 左右
B.向三颈烧瓶中依次加入沸石及 硝基苯
C.向试管中加入锌粒,打开活塞K,往长颈漏斗中加入稀硫酸,通入 一段时间
(5)苯胺粗品中含有少量硝基苯,提纯苯胺、回收硝基苯的流程如下:
①步骤Ⅰ中混合物的分离方法为___________.
②请从物质结构角度分析苯胺能与盐酸反应的原因___________.
③步骤Ⅱ中,水相中的 与 溶液反应的化学方程式为___________.
④本实验中苯胺的产率为___________(计算结果精确到0.1%).13.(14分)化合物I是除草剂茚草酮的中间体,其合成路线如下:
回答下列问题:
(1)A中电负性最大的元素为___________,D中碳原子的杂化轨道类型为___________.
(2)B在水中溶解度比C大,原因是___________.
(3) 的反应类型为___________.
(4)E的化学名称为___________,H的官能团名称为___________.
(5) 的化学方程式为___________.
(6) 的制备过程中, 可以提高原料利用率,原因是___________.
(7)J为B的同分异构体,写出满足下列条件的J的结构简式___________(任写一种).
①含有苯环;
②能与 溶液发生显色反应;
③核磁共振氢谱为四组蜂,峰面积比为 .
14.(18分)氢能是理想清洁能源,氢能产业链由制氢和储氢组成.回答下列问题:
Ⅰ.甲醇水蒸气重整制氢过程主要发生的反应有:
i.
ii.
iii.
(1) ___________
(2)恒温恒容的密闭容器中,假设只发生反应i,下列选项能表明反应i达到平衡状态的是___________(填标
号).
A.
B.容器内的压强不再变化
C.容器内混合气体的密度不再变化D.单位时间内,断裂 键的同时生成 键
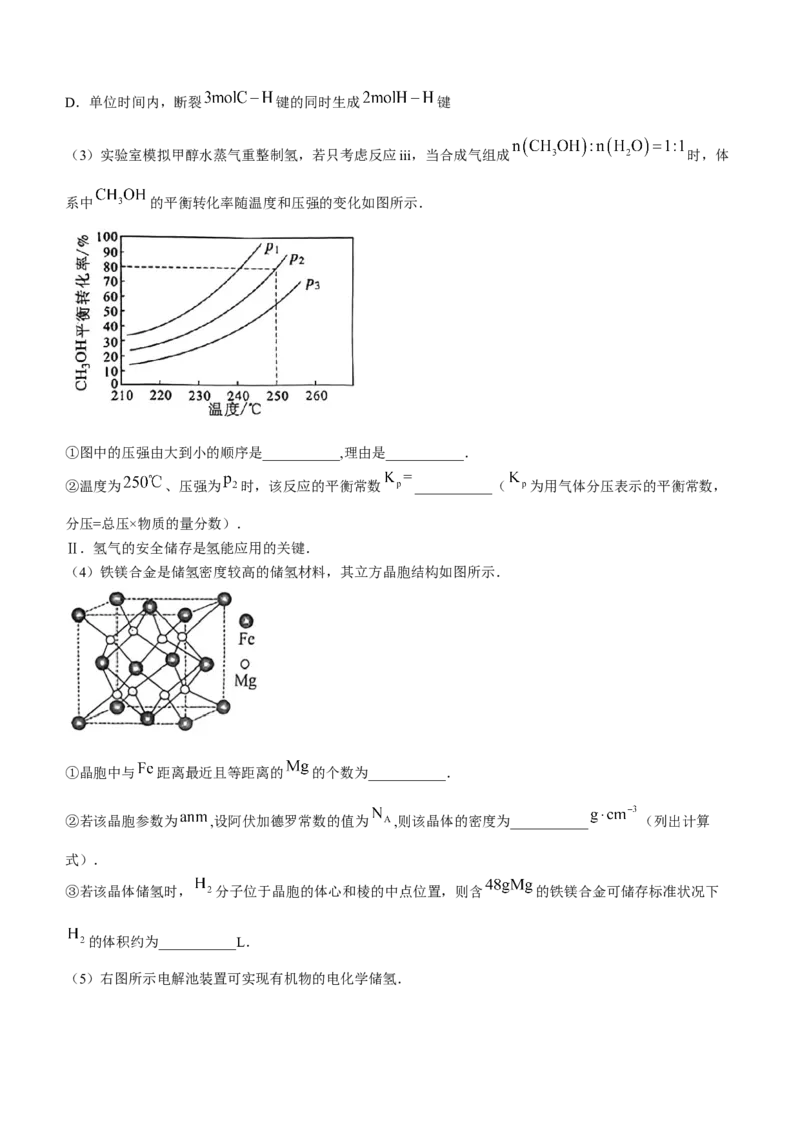
(3)实验室模拟甲醇水蒸气重整制氢,若只考虑反应iii,当合成气组成 时,体
系中 的平衡转化率随温度和压强的变化如图所示.
①图中的压强由大到小的顺序是___________,理由是___________.
②温度为 、压强为 时,该反应的平衡常数 ___________( 为用气体分压表示的平衡常数,
分压=总压×物质的量分数).
Ⅱ.氢气的安全储存是氢能应用的关键.
(4)铁镁合金是储氢密度较高的储氢材料,其立方晶胞结构如图所示.
①晶胞中与 距离最近且等距离的 的个数为___________.
②若该晶胞参数为 ,设阿伏加德罗常数的值为 ,则该晶体的密度为___________ (列出计算
式).
③若该晶体储氢时, 分子位于晶胞的体心和棱的中点位置,则含 的铁镁合金可储存标准状况下
的体积约为___________L.
(5)右图所示电解池装置可实现有机物的电化学储氢.①电极B为电解池的___________(填“阴极”或“阳极”).
②电解池工作时 向___________移动(填“电极A”或“电极B”).
③电极A的电极反应式为___________.福建省漳州市 2025 届高三毕业班第一次教学质量检测
化学参考答案
评分说明:
1.考生若写出其它合理答案,可参照评分标准给分
2.化学方程式和离子方程式未正确配平、未正确标注反应条件、“↑”“↓”等总扣1分.
一、选择题:本题共10小题,每小题4分,共40分.在每小题给出的四个选项中,只有一项
是符合题目要求的.
题号 1 2 3 4 5 6 7 8 9 10
答案 C A C B C A B B D D
二、非选择题:本题共4小题,共60分.
11.(14分)
(1) (1分) 平面三角形(1分)
(2)增大接触面积,加快溶浸速率(1分)
(3) (2分)
(4)4.7(1分) (2分)
(5) (2分)
(6) (2分)
(7)a b c(2分)
12.(14分)
(1) (2分)
(2)直形冷凝管(1分)
(3) (2分)
(4)B C A(2分)
(5)①分液(1分)
②苯胺分子中的N原子有孤电子对,可与提供空轨道的 形成配位键(2分)
③ (2分)
④60.2%(2分)
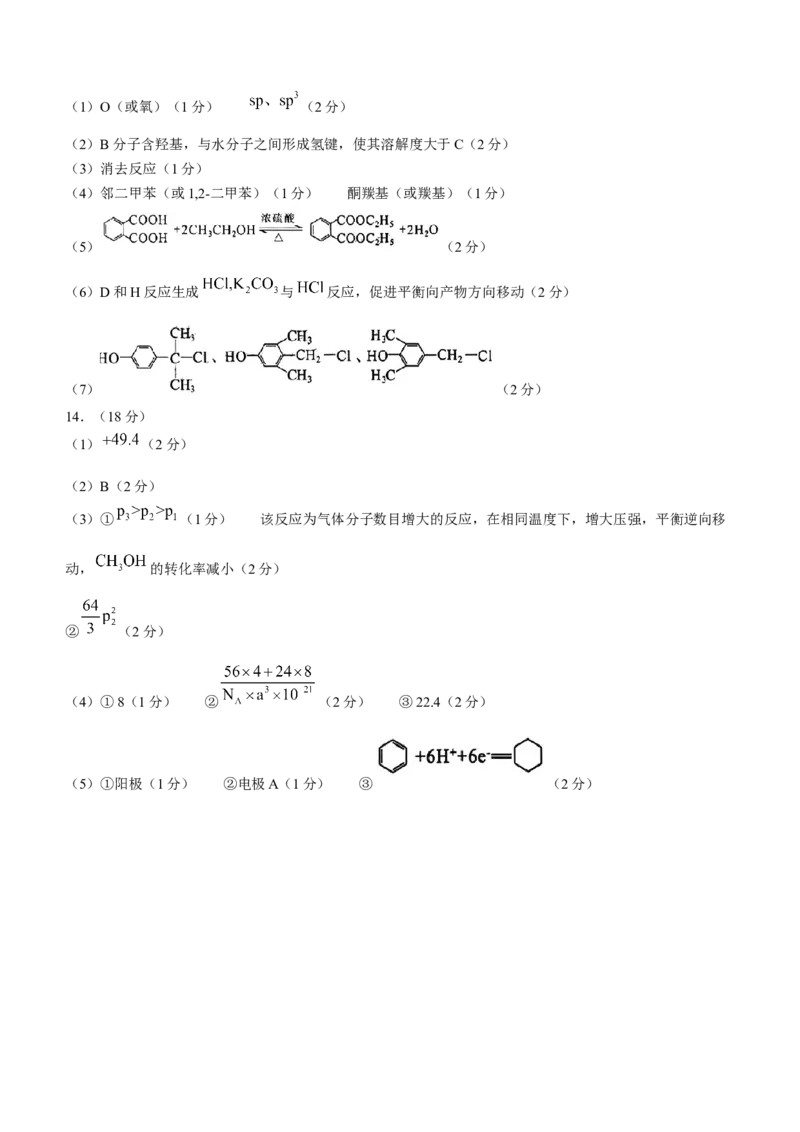
13.(14分)(1)O(或氧)(1分) (2分)
(2)B分子含羟基,与水分子之间形成氢键,使其溶解度大于C(2分)
(3)消去反应(1分)
(4)邻二甲苯(或1,2-二甲苯)(1分) 酮羰基(或羰基)(1分)
(5) (2分)
(6)D和H反应生成 与 反应,促进平衡向产物方向移动(2分)
(7) (2分)
14.(18分)
(1) (2分)
(2)B(2分)
(3)① (1分) 该反应为气体分子数目增大的反应,在相同温度下,增大压强,平衡逆向移
动, 的转化率减小(2分)
② (2分)
(4)①8(1分) ② (2分) ③22.4(2分)
(5)①阳极(1分) ②电极A(1分) ③ (2分)