文档内容
保密★启用前
塘沽一中 2025 届高三毕业班第二次月考
化学
本试卷分为第I卷(选择题)和第Ⅱ卷(非选择题)两部分,共100分,考试用时60分钟。第I卷
1至4页,第Ⅱ卷5至8页。
答卷前,考生务必将自己的姓名、考生号、考场号和座位号填写在答题卡上,并在规定位置
粘贴考试用条形码。答卷时,考生务必将答案涂写在答题卡上,答在试卷上的无效。考试结
束后,将本试卷和答题卡一并交回。
祝各位考生考试顺利!
第I卷
注意事项:
1.每题选出答案后,用铅笔将答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净
后,再选涂其他答案标号。
2.本卷共12题,每题3分,共36分。在每题给出的四个选项中,只有一项是最符合题目要求
的。
可能用到的相对原子质量:H1 O16 Na23 S32 Fe56
1. 下列说法错误的是
A. 自行车采用T1100碳纤维材料打造,车架仅有1150克,这是一种复合材料
B. 摔跤运动垫面层应用了纳米防污抗菌涂层技术,涂层颗粒是纳米级别,属于胶体
C. 可实时采集运动员运动信息的智能芯片技术,其材料离不开硅单质
D. 奥运会火炬火焰利用了部分金属元素特征的焰色试验,该反应属于物理变化
2. 下列化学用语或图示正确的是
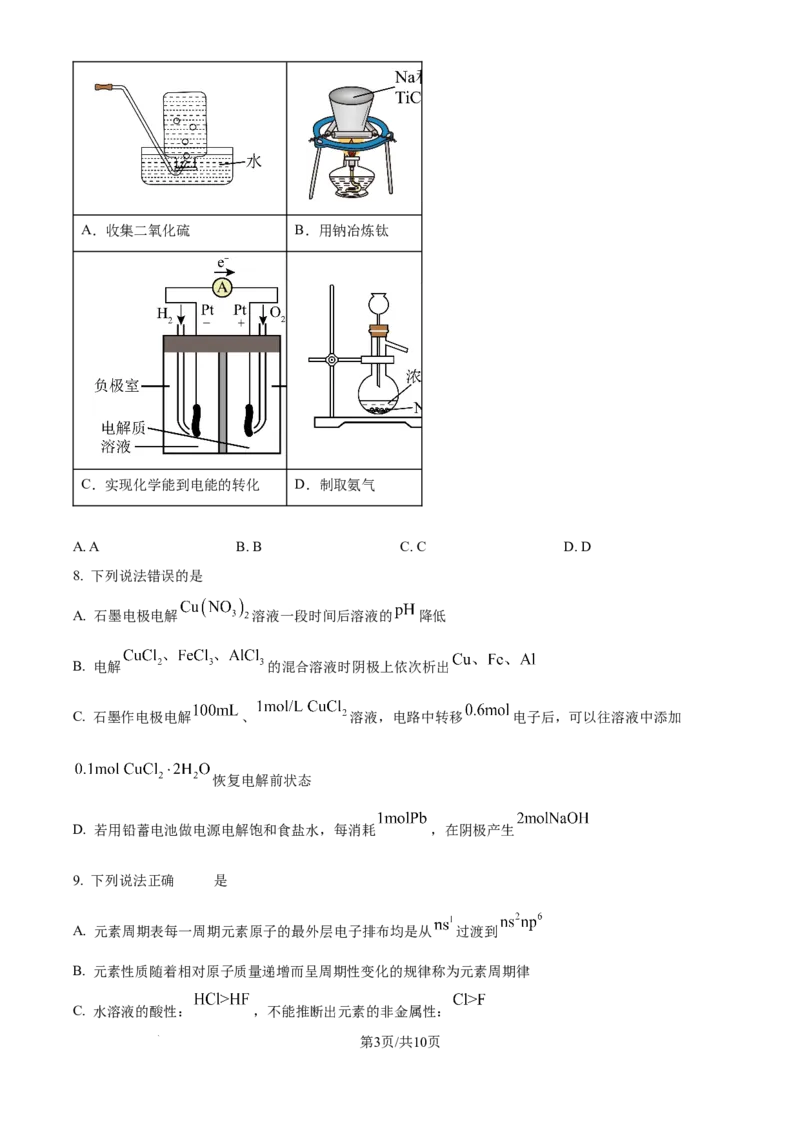
A. 激发态H原子的轨道表示式:
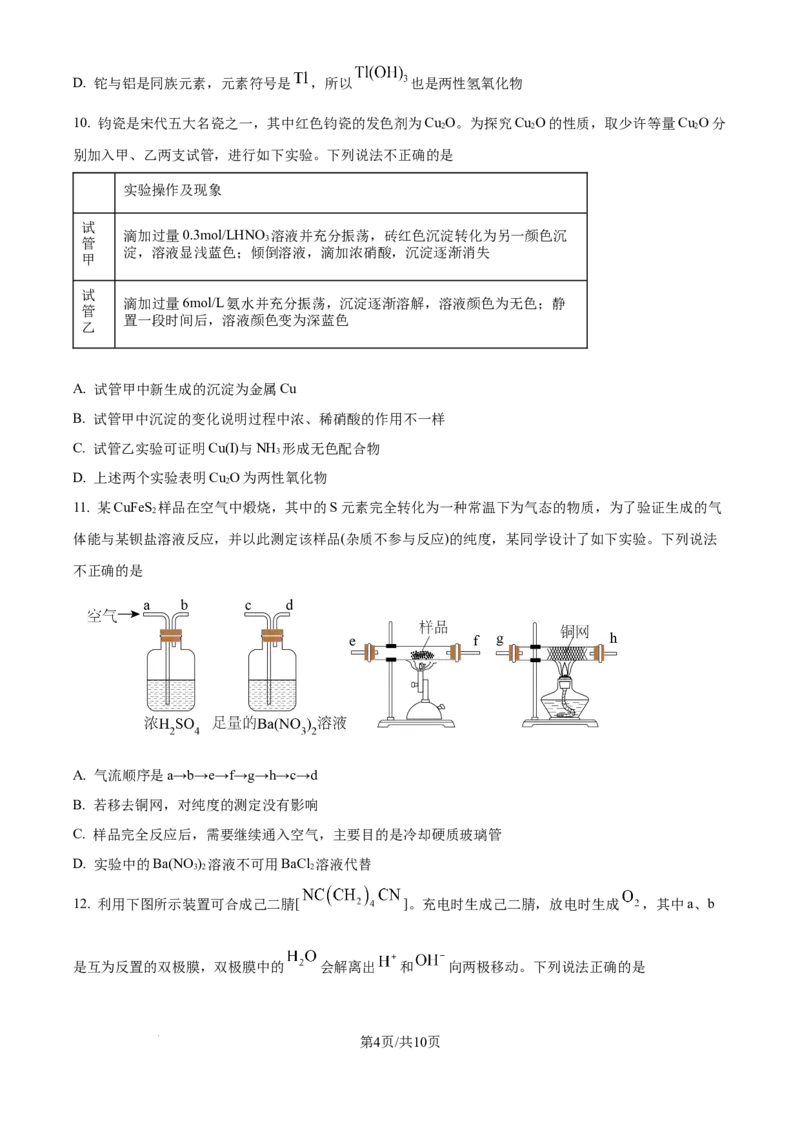
B. 基态Ge原子的简化电子排布式为:
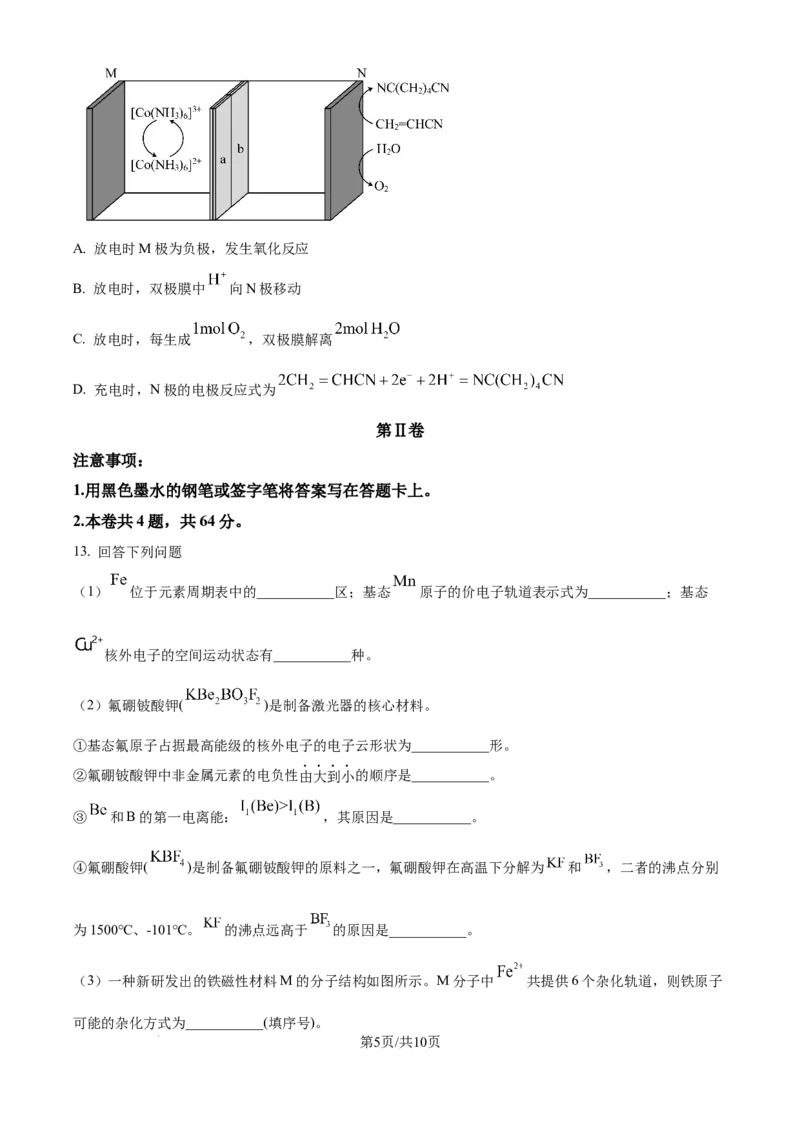
C. 溶液中的水合离子:
第1页/共10页
学科网(北京)股份有限公司D. 分子中 键的形成:
3. 下列叙述正确的是
A. 共价键的极性: B. 沸点:
C. 最高正化合价: D. 碱性:
4. 下列过程对应的离子方程式正确的是
A. 用氢氟酸刻蚀玻璃:
B. 惰性电极电解 水溶液:
C. 硫酸酸化的淀粉碘化钾溶液久置后变蓝:
D. 澄清石灰水中通入过量 :
5. 设 为阿伏加德罗常数的值,下列说法正确的是
A. 常温常压下, 的 约含有的质子数为
B. 白磷分子( )呈正四面体结构, 白磷中约含有 键的数目为
C. 中B原子最外层电子数为
D. 在足量的氧气中充分燃烧,转移的电子的数目为
6. X、Y、Z、W为原子序数依次增大的短周期主族元素,单质X 可用作粮仓中的粮食保护气,Y、Z原子
2
的最外层电子数之和等于W原子的最外层电子数,Z原子的核外电子总数是W原子的最外层电子数的2倍,
Y、Z、W处于同一周期,Z的氧化物可用来生产光导纤维。下列说法错误的是
A. 原子半径:Y>Z>W>X
B. 简单氢化物的稳定性:X>Z
C. 最高正化合价:W>X>Z>Y
D. 最高价氧化物对应的水化物的酸性:Z>W
7. 下列实验方案中,实验设计能达成实验目的的是
第2页/共10页
学科网(北京)股份有限公司A.收集二氧化硫 B.用钠冶炼钛
C.实现化学能到电能的转化 D.制取氨气
A. A B. B C. C D. D
8. 下列说法错误的是
A. 石墨电极电解 溶液一段时间后溶液的 降低
B. 电解 的混合溶液时阴极上依次析出
C. 石墨作电极电解 、 溶液,电路中转移 电子后,可以往溶液中添加
恢复电解前状态
D. 若用铅蓄电池做电源电解饱和食盐水,每消耗 ,在阴极产生
的
9. 下列说法正确 是
A. 元素周期表每一周期元素原子的最外层电子排布均是从 过渡到
B. 元素性质随着相对原子质量递增而呈周期性变化的规律称为元素周期律
C. 水溶液的酸性: ,不能推断出元素的非金属性:
第3页/共10页
学科网(北京)股份有限公司D. 铊与铝是同族元素,元素符号是 ,所以 也是两性氢氧化物
10. 钧瓷是宋代五大名瓷之一,其中红色钧瓷的发色剂为Cu O。为探究Cu O的性质,取少许等量Cu O分
2 2 2
别加入甲、乙两支试管,进行如下实验。下列说法不正确的是
实验操作及现象
试
滴加过量0.3mol/LHNO 溶液并充分振荡,砖红色沉淀转化为另一颜色沉
管 3
淀,溶液显浅蓝色;倾倒溶液,滴加浓硝酸,沉淀逐渐消失
甲
试
滴加过量6mol/L氨水并充分振荡,沉淀逐渐溶解,溶液颜色为无色;静
管
置一段时间后,溶液颜色变为深蓝色
乙
A. 试管甲中新生成的沉淀为金属Cu
B. 试管甲中沉淀的变化说明过程中浓、稀硝酸的作用不一样
C. 试管乙实验可证明Cu(Ⅰ)与NH 形成无色配合物
3
D. 上述两个实验表明Cu O为两性氧化物
2
11. 某CuFeS 样品在空气中煅烧,其中的S元素完全转化为一种常温下为气态的物质,为了验证生成的气
2
体能与某钡盐溶液反应,并以此测定该样品(杂质不参与反应)的纯度,某同学设计了如下实验。下列说法
不正确的是
A. 气流顺序是a→b→e→f→g→h→c→d
B. 若移去铜网,对纯度的测定没有影响
C. 样品完全反应后,需要继续通入空气,主要目的是冷却硬质玻璃管
D. 实验中的Ba(NO ) 溶液不可用BaCl 溶液代替
3 2 2
12. 利用下图所示装置可合成己二腈[ ]。充电时生成己二腈,放电时生成 ,其中a、b
是互为反置的双极膜,双极膜中的 会解离出 和 向两极移动。下列说法正确的是
第4页/共10页
学科网(北京)股份有限公司A. 放电时M极为负极,发生氧化反应
B. 放电时,双极膜中 向N极移动
C. 放电时,每生成 ,双极膜解离
D. 充电时,N极的电极反应式为
第Ⅱ卷
注意事项:
1.用黑色墨水的钢笔或签字笔将答案写在答题卡上。
2.本卷共4题,共64分。
13. 回答下列问题
(1) 位于元素周期表中的___________区;基态 原子的价电子轨道表示式为___________;基态
核外电子的空间运动状态有___________种。
(2)氟硼铍酸钾( )是制备激光器的核心材料。
①基态氟原子占据最高能级的核外电子的电子云形状为___________形。
②氟硼铍酸钾中非金属元素的电负性由大到小的顺序是___________。
③ 和B的第一电离能: ,其原因是___________。
④氟硼酸钾( )是制备氟硼铍酸钾的原料之一,氟硼酸钾在高温下分解为 和 ,二者的沸点分别
为1500℃、-101℃。 的沸点远高于 的原因是___________。
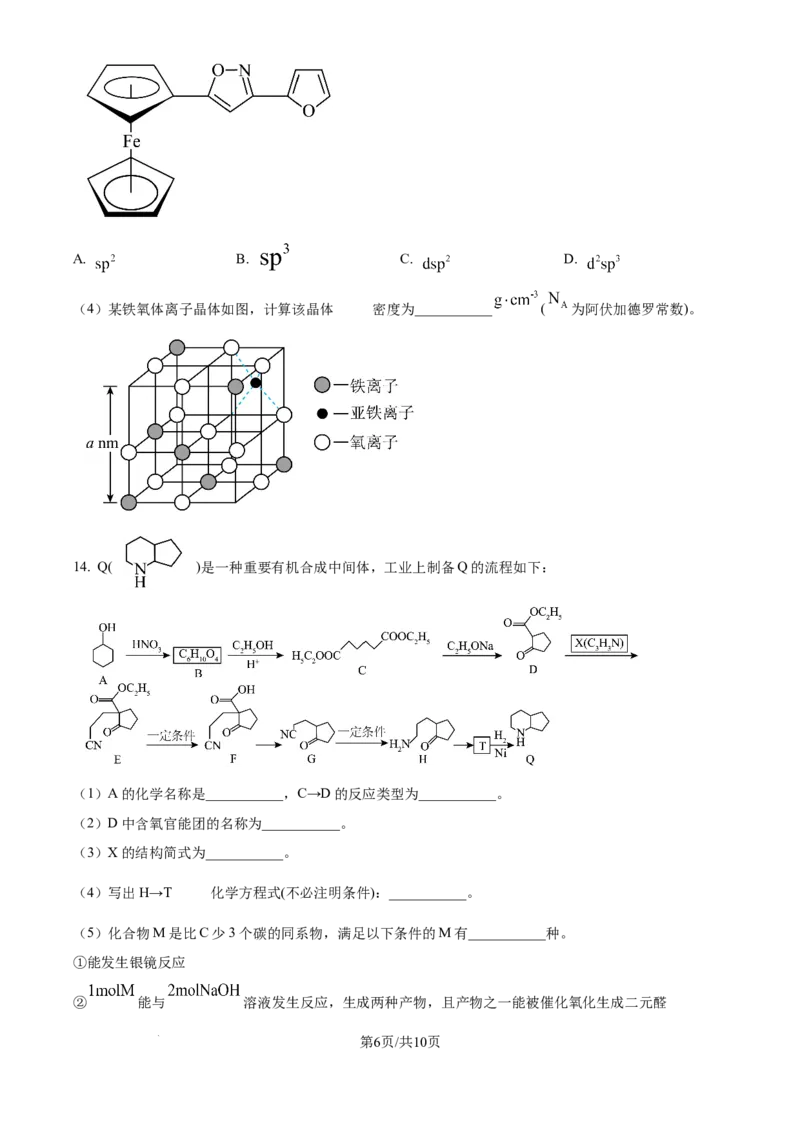
(3)一种新研发出的铁磁性材料M的分子结构如图所示。M分子中 共提供6个杂化轨道,则铁原子
可能的杂化方式为___________(填序号)。
第5页/共10页
学科网(北京)股份有限公司A. B. C. D.
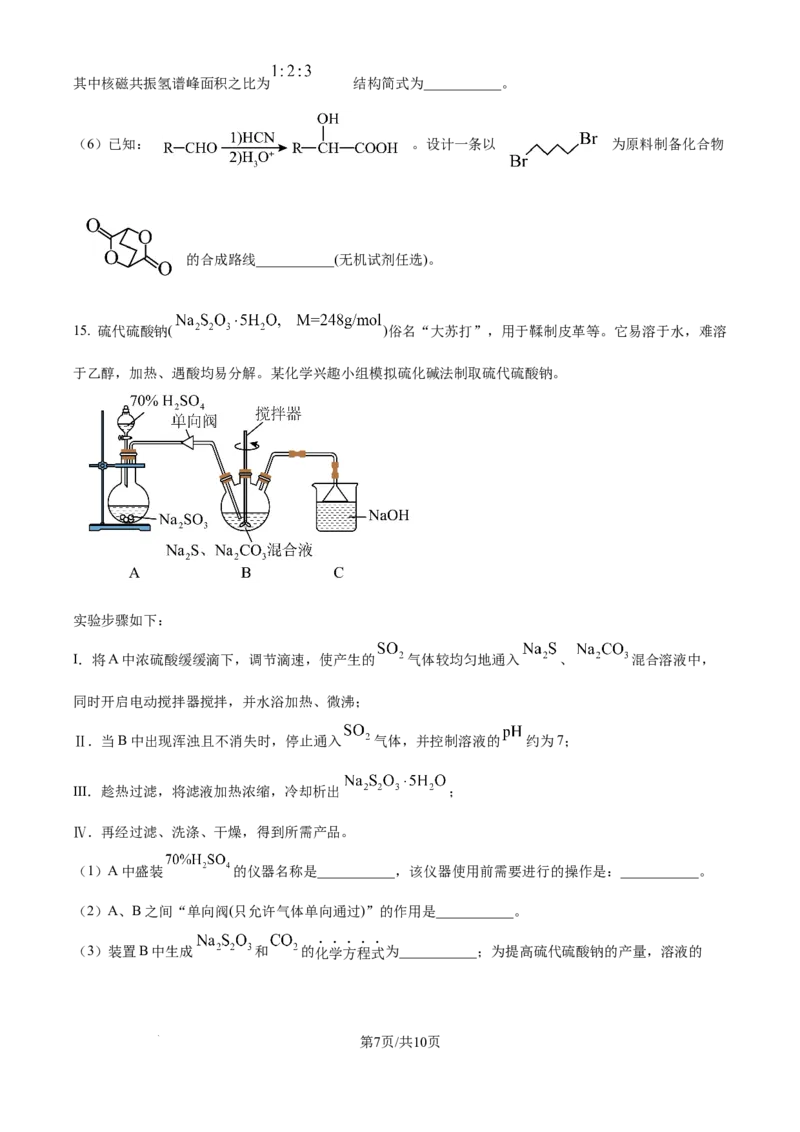
的
(4)某铁氧体离子晶体如图,计算该晶体 密度为___________ ( 为阿伏加德罗常数)。
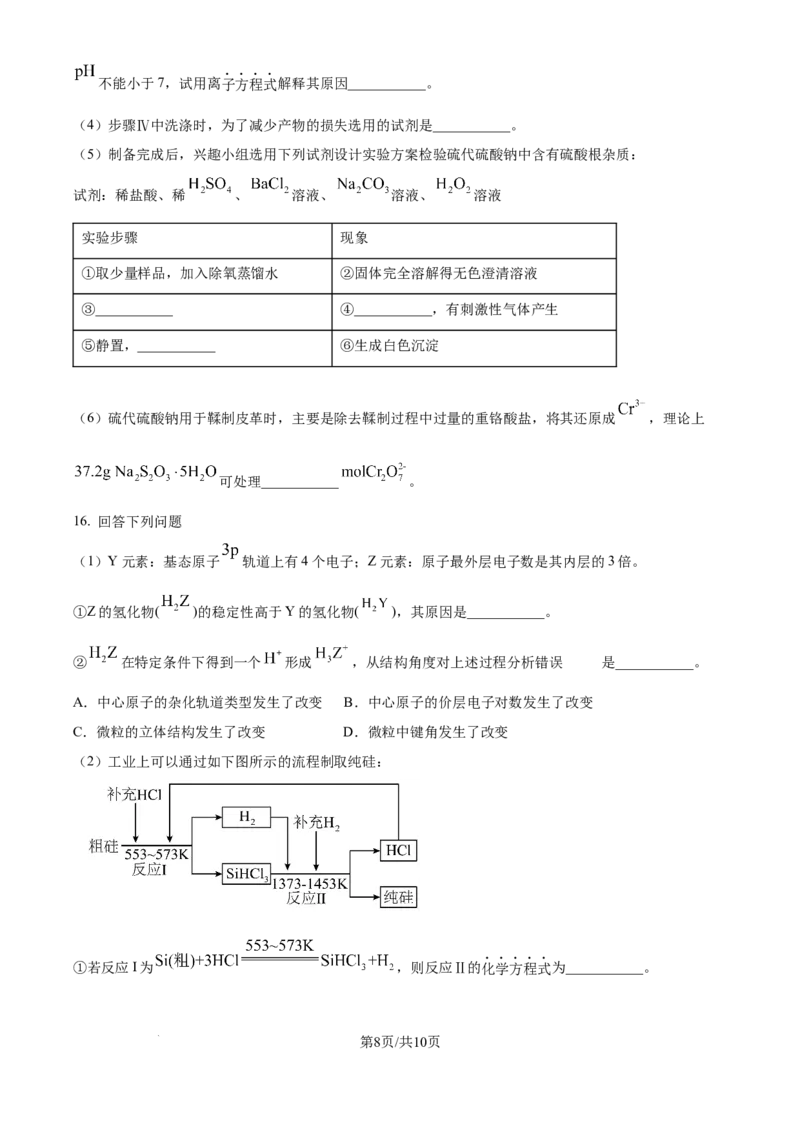
14. Q( )是一种重要有机合成中间体,工业上制备Q的流程如下:
(1)A的化学名称是___________,C→D的反应类型为___________。
(2)D中含氧官能团的名称为___________。
(3)X的结构简式为___________。
的
(4)写出H→T 化学方程式(不必注明条件):___________。
(5)化合物M是比C少3个碳的同系物,满足以下条件的M有___________种。
①能发生银镜反应
② 能与 溶液发生反应,生成两种产物,且产物之一能被催化氧化生成二元醛
第6页/共10页
学科网(北京)股份有限公司的
其中核磁共振氢谱峰面积之比为 结构简式为___________。
(6)已知: 。设计一条以 为原料制备化合物
的合成路线___________(无机试剂任选)。
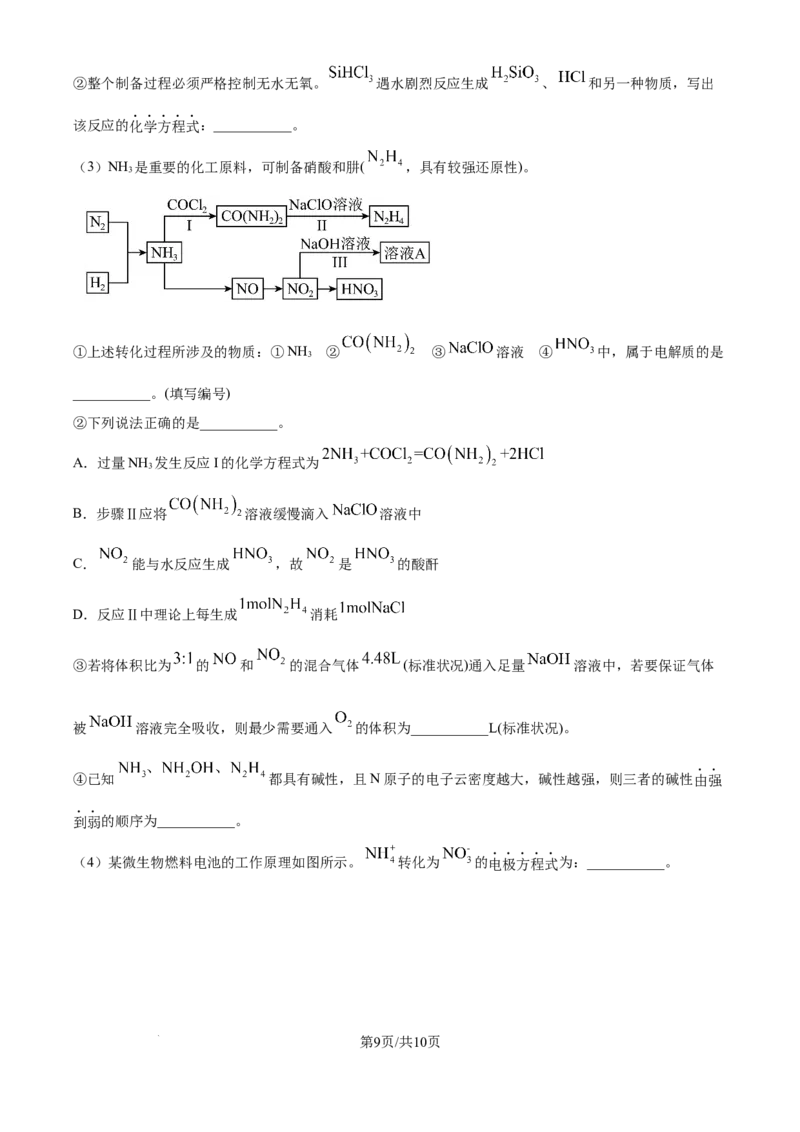
15. 硫代硫酸钠( )俗名“大苏打”,用于鞣制皮革等。它易溶于水,难溶
于乙醇,加热、遇酸均易分解。某化学兴趣小组模拟硫化碱法制取硫代硫酸钠。
实验步骤如下:
I.将A中浓硫酸缓缓滴下,调节滴速,使产生的 气体较均匀地通入 、 混合溶液中,
同时开启电动搅拌器搅拌,并水浴加热、微沸;
Ⅱ.当B中出现浑浊且不消失时,停止通入 气体,并控制溶液的 约为7;
III.趁热过滤,将滤液加热浓缩,冷却析出 ;
Ⅳ.再经过滤、洗涤、干燥,得到所需产品。
(1)A中盛装 的仪器名称是___________,该仪器使用前需要进行的操作是:___________。
(2)A、B之间“单向阀(只允许气体单向通过)”的作用是___________。
(3)装置B中生成 和 的化学方程式为___________;为提高硫代硫酸钠的产量,溶液的
第7页/共10页
学科网(北京)股份有限公司不能小于7,试用离子方程式解释其原因___________。
(4)步骤Ⅳ中洗涤时,为了减少产物的损失选用的试剂是___________。
(5)制备完成后,兴趣小组选用下列试剂设计实验方案检验硫代硫酸钠中含有硫酸根杂质:
试剂:稀盐酸、稀 、 溶液、 溶液、 溶液
实验步骤 现象
①取少量样品,加入除氧蒸馏水 ②固体完全溶解得无色澄清溶液
③___________ ④___________,有刺激性气体产生
⑤静置,___________ ⑥生成白色沉淀
(6)硫代硫酸钠用于鞣制皮革时,主要是除去鞣制过程中过量的重铬酸盐,将其还原成 ,理论上
可处理___________ 。
16. 回答下列问题
(1)Y元素:基态原子 轨道上有4个电子;Z元素:原子最外层电子数是其内层的3倍。
①Z的氢化物( )的稳定性高于Y的氢化物( ),其原因是___________。
的
② 在特定条件下得到一个 形成 ,从结构角度对上述过程分析错误 是___________。
A.中心原子的杂化轨道类型发生了改变 B.中心原子的价层电子对数发生了改变
C.微粒的立体结构发生了改变 D.微粒中键角发生了改变
(2)工业上可以通过如下图所示的流程制取纯硅:
①若反应I为 ,则反应Ⅱ的化学方程式为___________。
第8页/共10页
学科网(北京)股份有限公司②整个制备过程必须严格控制无水无氧。 遇水剧烈反应生成 、 和另一种物质,写出
该反应的化学方程式:___________。
(3)NH 是重要的化工原料,可制备硝酸和肼( ,具有较强还原性)。
3
①上述转化过程所涉及的物质:①NH ② ③ 溶液 ④ 中,属于电解质的是
3
___________。(填写编号)
②下列说法正确的是___________。
A.过量NH 发生反应I的化学方程式为
3
B.步骤Ⅱ应将 溶液缓慢滴入 溶液中
C. 能与水反应生成 ,故 是 的酸酐
D.反应Ⅱ中理论上每生成 消耗
③若将体积比为 的 和 的混合气体 (标准状况)通入足量 溶液中,若要保证气体
被 溶液完全吸收,则最少需要通入 的体积为___________L(标准状况)。
④已知 都具有碱性,且N原子的电子云密度越大,碱性越强,则三者的碱性由强
到弱的顺序为___________。
(4)某微生物燃料电池的工作原理如图所示。 转化为 的电极方程式为:___________。
第9页/共10页
学科网(北京)股份有限公司第10页/共10页
学科网(北京)股份有限公司