文档内容
湖北省部分高中协作体2025—2026学年上学期10月联考
高二化学试题
本试卷共8页,19题,全卷满分100分,考试用时75分钟。
★祝考试顺利★
注意事项:
1、答题前,请将自己的姓名、准考证号、考场号、座位号填写在试卷和答题卡上,并
将准考证号条形码粘贴在答题卡上的制定位置。
2、选择题的作答:每小题选出答案后,用 2B铅笔把答题卡上对应题目的答案标号涂
黑,写在试卷、草稿纸和答题卡上的非答题区域均无效。
3、非选择题作答:用黑色签字笔直接答在答题卡对应的答题区域内,写在试卷、草稿
纸和答题卡上的非答题区域均无效。
4、考试结束后,请将答题卡上交。
一、选择题:本题共15小题,每题3分,共45分,每小题仅有一项是符合题意。
1.下列关于热化学方程式的说法正确的是( )
A.若 H 的燃烧热为 a kJ·mol-1,则 H 燃烧的热化学方程式为 H(g)+
2 2 2
Cl(g)===2HCl(g) ΔH=-a kJ·mol-1
2
B.若 1 mol SO 和 0.5 mol O 反应放热 98.3 kJ,则热化学方程式为 2SO (g)+
2 2 2
O(g)2SO (g) ΔH=-196.6 kJ·mol-1
2 3
C.若H+(aq)+OH-(aq)===H O(l) ΔH=-57.3 kJ·mol-1,则稀硫酸与稀Ba(OH) 溶液
2 2
反应的热化学方程式为 HSO (aq)+Ba(OH) (aq)===BaSO (s)+2HO(l) ΔH=-114.6
2 4 2 4 2
kJ·mol-1
D.若31 g白磷的能量比31 g红磷多b kJ,则白磷转化为红磷的热化学方程式为P(白
4
磷,s)===4P(红磷,s) ΔH=-4b kJ·mol-1
2.某温度下,在体积一定的密闭容器中进行如下反应:2X(g)+Y(g)Z(g)+W(s)
ΔH>0,下列叙述正确的是( )
A.加入少量W,逆反应速率增大
B.升高温度,正反应和逆反应速率都增大
C.在容器中加入氦气,压强增大,反应速率增大
D.将容器的体积压缩,可增大活化分子的百分数,有效碰撞次数增大
3.据文献报道,某反应的反应历程如图所示:下列有关该历程的说法错误的是( )
A.总反应化学方程式为4NH +3O=====2N+6HO
3 2 2 2
B.Ti4+…NH —N===O是中间产物
2
C.Ti4+是催化剂
D.Ti4+…NH —N===O―→Ti4++N+HO属于分解反应
2 2 2
4.将4 mol A(g)和2 mol B(g)在2 L的恒容密闭容器中混合并在一定条件下发生反应:
2A(g)+B(g)2C(g) ΔH<0,反应2 s后测得C的浓度为0.6 mol·L-1。下列说法正确的是
( )
A.2 s后物质A的转化率为15%
B.当v(C)=2v(B)时,该反应达到了平衡状态
C.达到平衡状态时,增加A的物质的量,会提高B的转化率
D.达到平衡状态时,升高温度,平衡逆向移动,同时化学平衡常数不变
5.已知 T 温度下在容积为 10 L 的密闭容器中发生可逆反应 X(g)+Y(g)2Z(g)+
1
2W(s) ΔH,起始时充入15 mol X与15 mol Y,10 min时反应达到平衡状态,测得平均速
率v(Z)=0.12 mol·L-1·min-1。下列有关说法正确的是( )
A.T 温度下该反应的平衡常数为2.56
1
B.平衡时再充入一定量的X,平衡正向移动,X的转化率增大
C.若T>T,T 时K=1.52,则该反应的ΔH>0
2 1 2
D.若其他条件不变,T 温度下,K=1.96,则Y的平衡转化率约为41.3%
3
6.CO 催化加氢制取甲醇的研究,对于环境、能源问题都具有重要的意义。反应如
2
下:
反应ⅰ CO(g)+3H(g)CHOH(g)+HO(g) ΔH=-58 kJ·mol-1;
2 2 3 2 1
反应ⅱ CO(g)+H(g)CO(g)+HO(g) ΔH=+42 kJ·mol-1。
2 2 2 2
下列说法不正确的是( )
A.增大氢气浓度能提高二氧化碳的转化率
B.增大压强,有利于反应向生成甲醇的方向进行,反应ⅰ的平衡常数增大
C.升高温度,生成甲醇的速率增大,反应ⅱ的限度同时增大
D.选用理想的催化剂可以提高甲醇在最终产物中的比例
7.下列图示与对应的叙述相符的是( )
图1 图2
图3 图4A.图1表示反应mA(s)+nB(g)pC(g)在一定温度下达到平衡时B的转化率与压强
变化的关系,x点的正反应速率比y点的快
B.图2表示反应A(g)+B(s)C(s)+D(g)的速率-时间图像,在t 时刻改变的条件可
1
能是加入催化剂或增大压强
C.图3表示反应mA(g)+nB(g)pC(g)+qD(g)中A的百分含量与温度(T)的变化情
况,则该反应的ΔH>0
D.图4所示图中的阴影部分面积的含义是(v正 -v逆 )
8.一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所
示,下列说法正确的是( )
A.a、b、c三点溶液的pH:cc(K+)>c(Ag+)>c(H+)>c(OH-)
C.该温度下,K (Ag CrO)=4.0×10-12
sp 2 4
D.相同实验条件下,若改为0.05 mol/L的KCl和KCrO 溶液,则曲线L 中N点移到
2 4 2
Q点
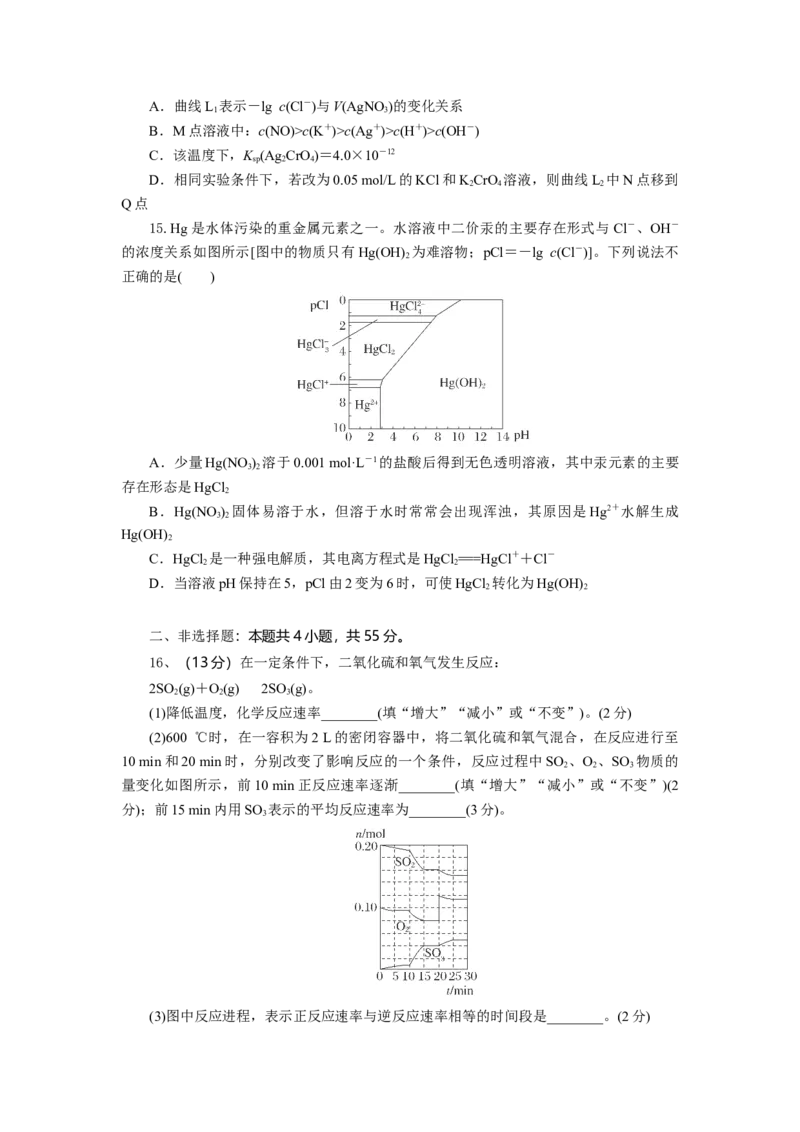
15.Hg是水体污染的重金属元素之一。水溶液中二价汞的主要存在形式与 Cl-、OH-
的浓度关系如图所示[图中的物质只有Hg(OH) 为难溶物;pCl=-lg c(Cl-)]。下列说法不
2
正确的是( )
A.少量Hg(NO) 溶于0.001 mol·L-1的盐酸后得到无色透明溶液,其中汞元素的主要
3 2
存在形态是HgCl
2
B.Hg(NO ) 固体易溶于水,但溶于水时常常会出现浑浊,其原因是Hg2+水解生成
3 2
Hg(OH)
2
C.HgCl 是一种强电解质,其电离方程式是HgCl ===HgCl++Cl-
2 2
D.当溶液pH保持在5,pCl由2变为6时,可使HgCl 转化为Hg(OH)
2 2
二、非选择题:本题共4小题,共55分。
16、(13分)在一定条件下,二氧化硫和氧气发生反应:
2SO (g)+O(g)2SO (g)。
2 2 3
(1)降低温度,化学反应速率________(填“增大”“减小”或“不变”)。(2分)
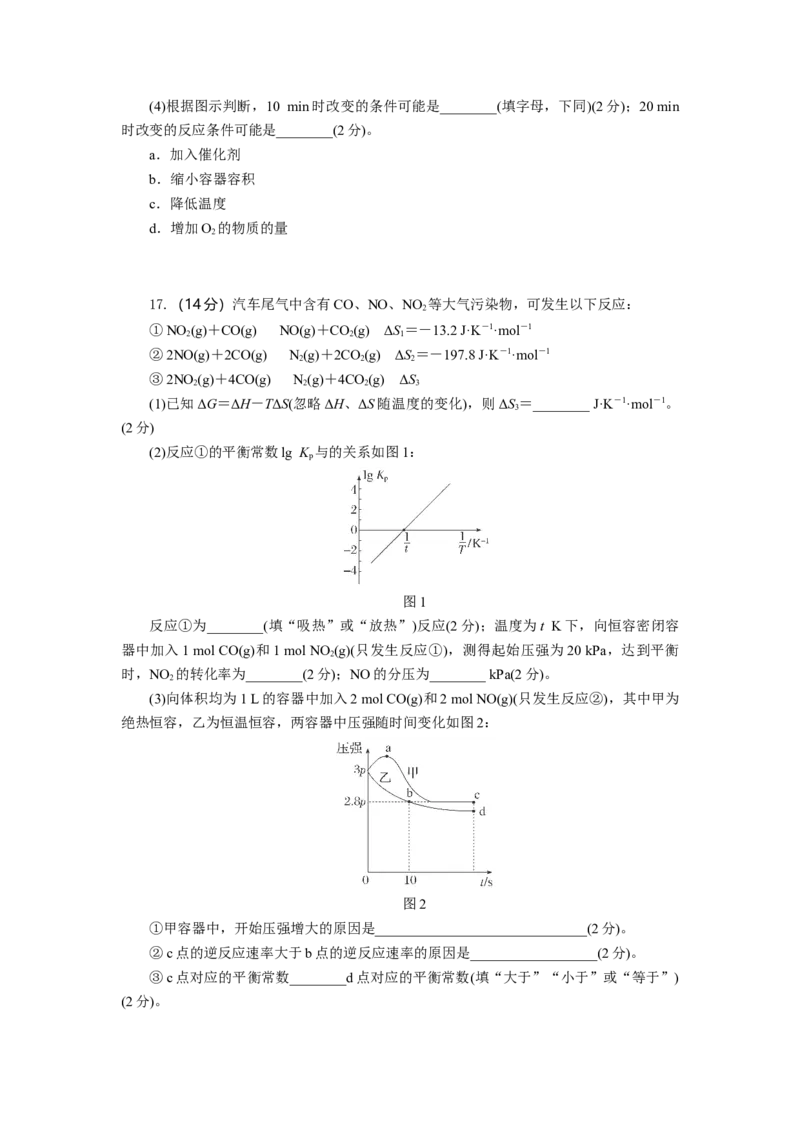
(2)600 ℃时,在一容积为2 L的密闭容器中,将二氧化硫和氧气混合,在反应进行至
10 min和20 min时,分别改变了影响反应的一个条件,反应过程中SO 、O 、SO 物质的
2 2 3
量变化如图所示,前10 min正反应速率逐渐________(填“增大”“减小”或“不变”)(2
分);前15 min内用SO 表示的平均反应速率为________(3分)。
3
(3)图中反应进程,表示正反应速率与逆反应速率相等的时间段是________。(2分)(4)根据图示判断,10 min时改变的条件可能是________(填字母,下同)(2分);20 min
时改变的反应条件可能是________(2分)。
a.加入催化剂
b.缩小容器容积
c.降低温度
d.增加O 的物质的量
2
17.(14分)汽车尾气中含有CO、NO、NO 等大气污染物,可发生以下反应:
2
①NO (g)+CO(g)NO(g)+CO(g) ΔS=-13.2 J·K-1·mol-1
2 2 1
②2NO(g)+2CO(g)N(g)+2CO(g) ΔS=-197.8 J·K-1·mol-1
2 2 2
③2NO (g)+4CO(g)N(g)+4CO(g) ΔS
2 2 2 3
(1)已知ΔG=ΔH-TΔS(忽略ΔH、ΔS随温度的变化),则ΔS =________ J·K-1·mol-1。
3
(2分)
(2)反应①的平衡常数lg K 与的关系如图1:
p
图1
反应①为________(填“吸热”或“放热”)反应(2分);温度为t K下,向恒容密闭容
器中加入1 mol CO(g)和1 mol NO (g)(只发生反应①),测得起始压强为20 kPa,达到平衡
2
时,NO 的转化率为________(2分);NO的分压为________ kPa(2分)。
2
(3)向体积均为1 L的容器中加入2 mol CO(g)和2 mol NO(g)(只发生反应②),其中甲为
绝热恒容,乙为恒温恒容,两容器中压强随时间变化如图2:
图2
①甲容器中,开始压强增大的原因是______________________________(2分)。
②c点的逆反应速率大于b点的逆反应速率的原因是__________________(2分)。
③c点对应的平衡常数________d点对应的平衡常数(填“大于”“小于”或“等于”)
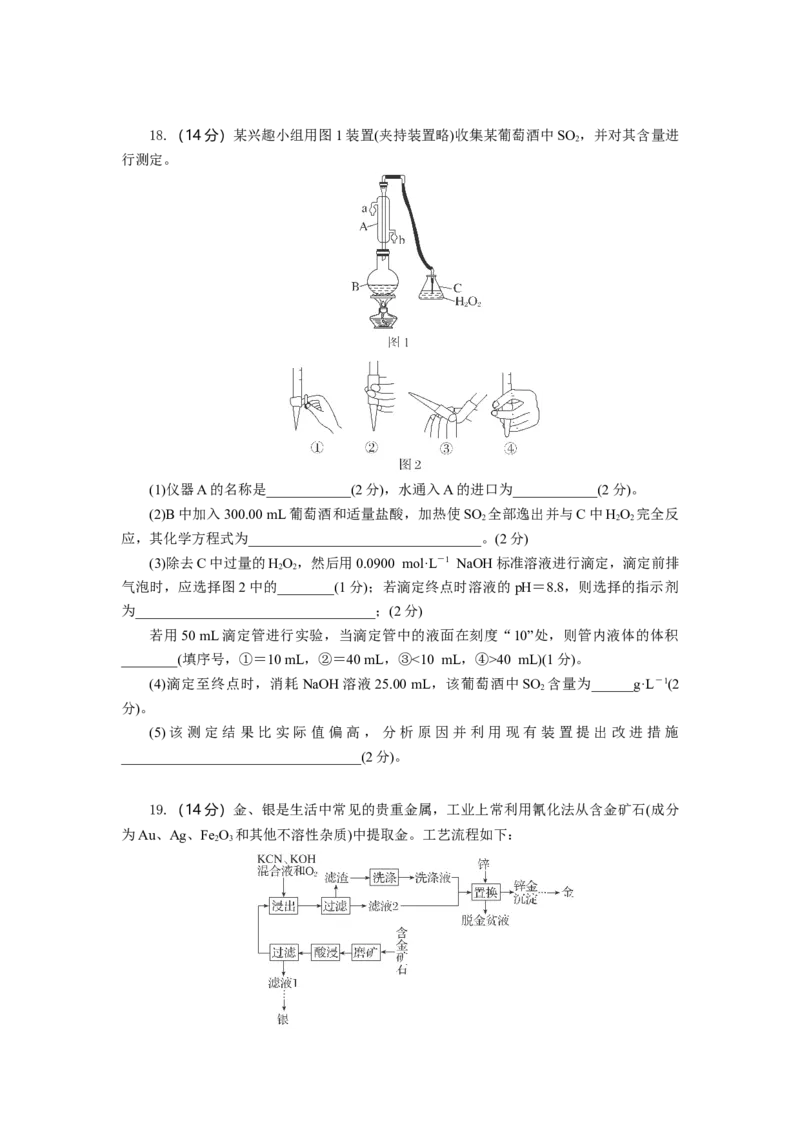
(2分)。18.(14分)某兴趣小组用图1装置(夹持装置略)收集某葡萄酒中SO ,并对其含量进
2
行测定。
(1)仪器A的名称是____________(2分),水通入A的进口为____________(2分)。
(2)B中加入300.00 mL葡萄酒和适量盐酸,加热使SO 全部逸出并与C中HO 完全反
2 2 2
应,其化学方程式为_________________________________。(2分)
(3)除去C中过量的HO,然后用0.0900 mol·L-1 NaOH标准溶液进行滴定,滴定前排
2 2
气泡时,应选择图2中的________(1分);若滴定终点时溶液的pH=8.8,则选择的指示剂
为__________________________________;(2分)
若用50 mL滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积
________(填序号,①=10 mL,②=40 mL,③<10 mL,④>40 mL)(1分)。
(4)滴定至终点时,消耗NaOH溶液25.00 mL,该葡萄酒中SO 含量为______g·L-1(2
2
分)。
(5)该测定结果比实际值偏高,分析原因并利用现有装置提出改进措施
__________________________________(2分)。
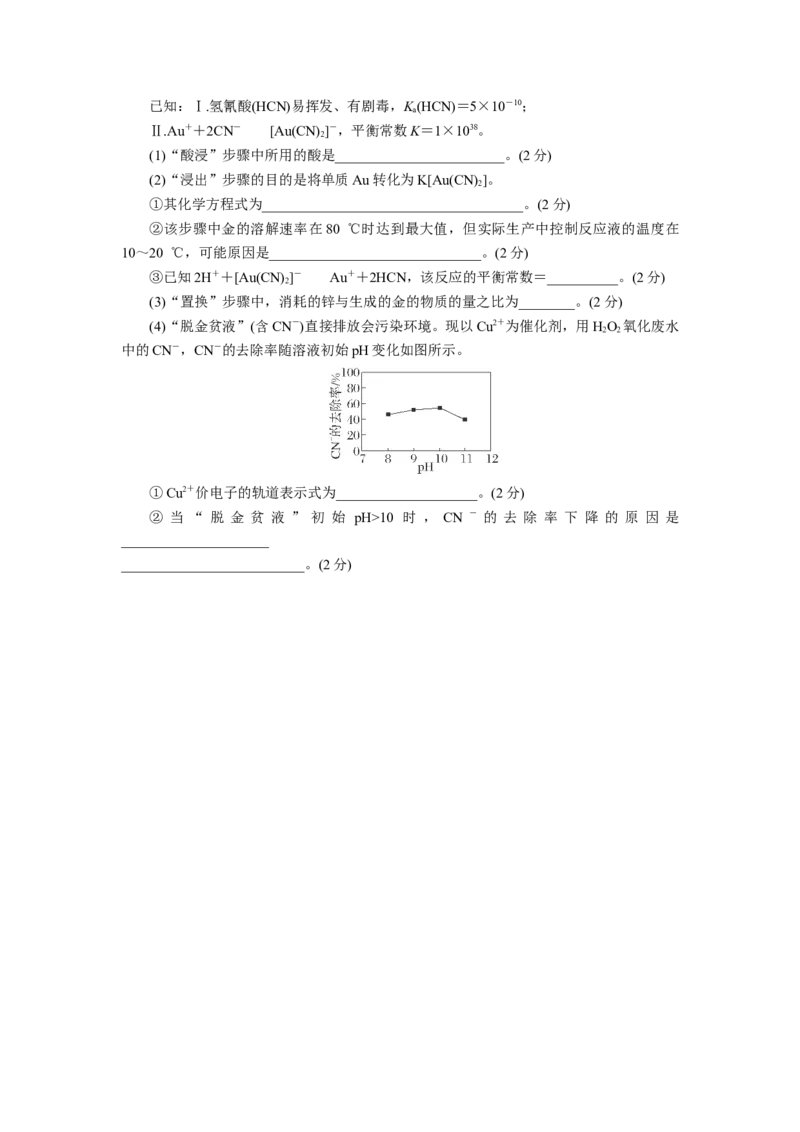
19.(14分)金、银是生活中常见的贵重金属,工业上常利用氰化法从含金矿石(成分
为Au、Ag、Fe O 和其他不溶性杂质)中提取金。工艺流程如下:
2 3已知:Ⅰ.氢氰酸(HCN)易挥发、有剧毒,K(HCN)=5×10-10;
a
Ⅱ.Au++2CN-[Au(CN) ]-,平衡常数K=1×1038。
2
(1)“酸浸”步骤中所用的酸是________________________。(2分)
(2)“浸出”步骤的目的是将单质Au转化为K[Au(CN) ]。
2
①其化学方程式为_____________________________________。(2分)
②该步骤中金的溶解速率在80 ℃时达到最大值,但实际生产中控制反应液的温度在
10~20 ℃,可能原因是______________________________。(2分)
③已知2H++[Au(CN) ]-Au++2HCN,该反应的平衡常数=__________。(2分)
2
(3)“置换”步骤中,消耗的锌与生成的金的物质的量之比为________。(2分)
(4)“脱金贫液”(含CN-)直接排放会污染环境。现以Cu2+为催化剂,用HO 氧化废水
2 2
中的CN-,CN-的去除率随溶液初始pH变化如图所示。
①Cu2+价电子的轨道表示式为____________________。(2分)
② 当 “ 脱 金 贫 液 ” 初 始 pH>10 时 , CN - 的 去 除 率 下 降 的 原 因 是
_____________________
__________________________。(2分)