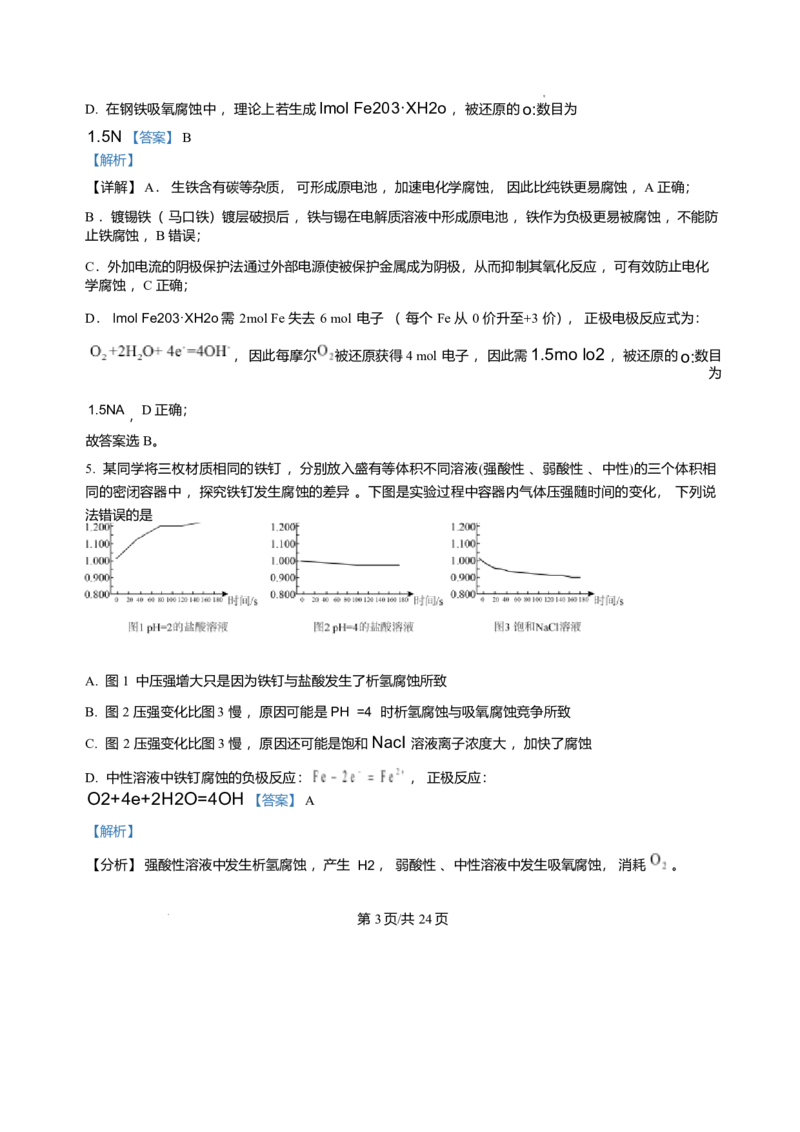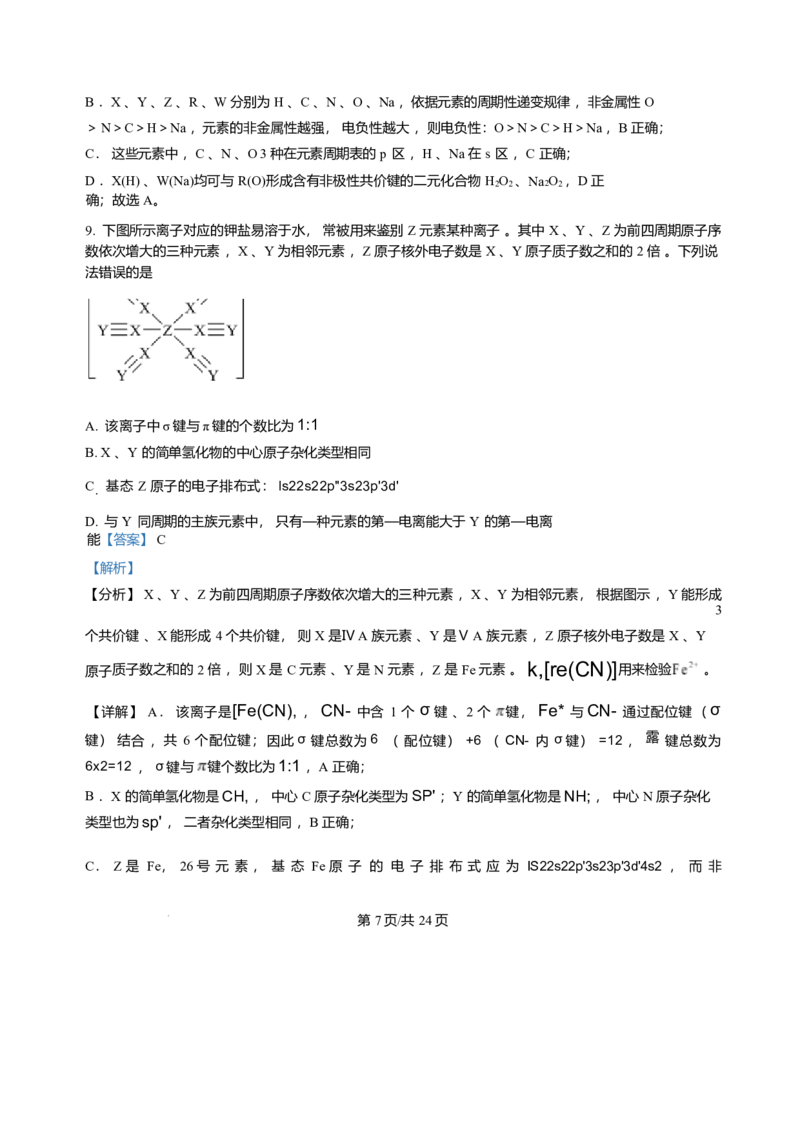文档内容
哈三中 2025—2026 学年度上学期高二学年期末考试
化学试卷
本试卷分第 Ⅰ 卷(选择题)和第Ⅱ卷(非选择题)两部分, 共 100 分,考试用时 75 分
钟可能用到的相对原子质量:H-1 N-14 Na-23 Cl-35.5
第 Ⅰ 卷(选择题 共 45 分)
一 、单选题: 共 15 个小题, 每题有且仅有一个选项符合题意, 每题 3 分, 共 45 分。
1. 下列化学用语表示正确的是
A. 的 VSEPR 模型:
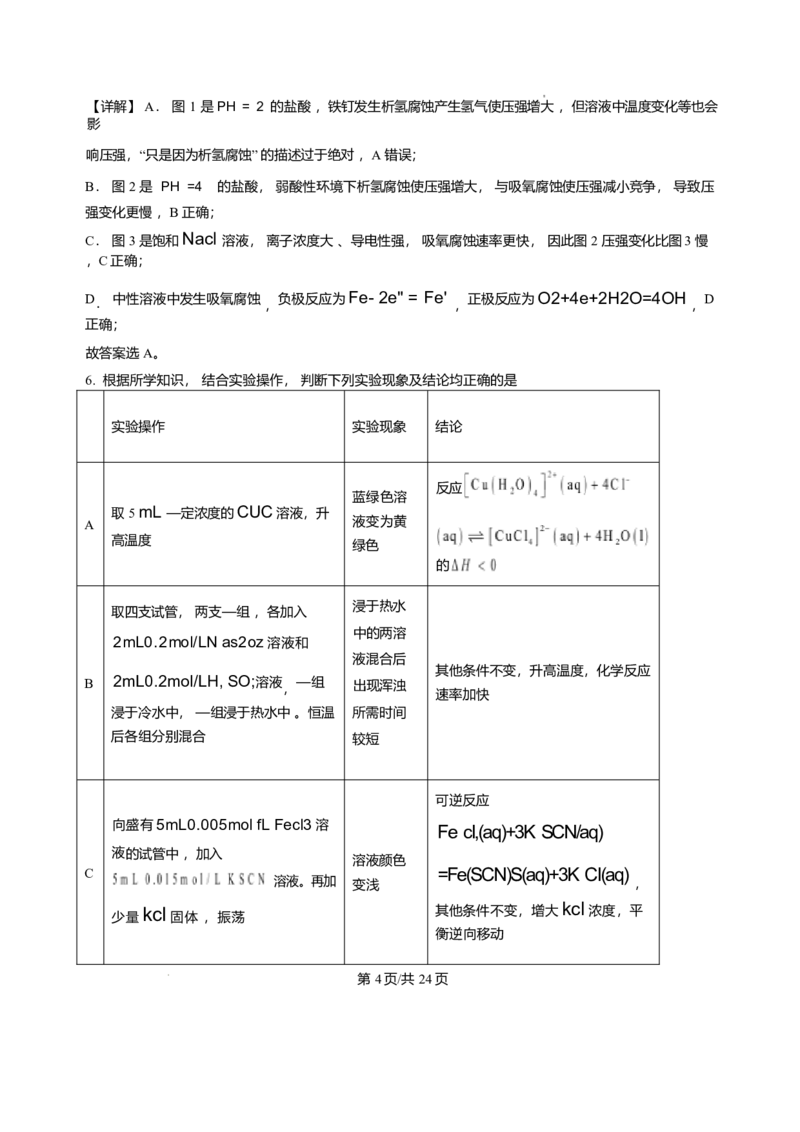
B. 电子式:
C. 基态锗原子的简化电子排布式: [Ar]4s24p2
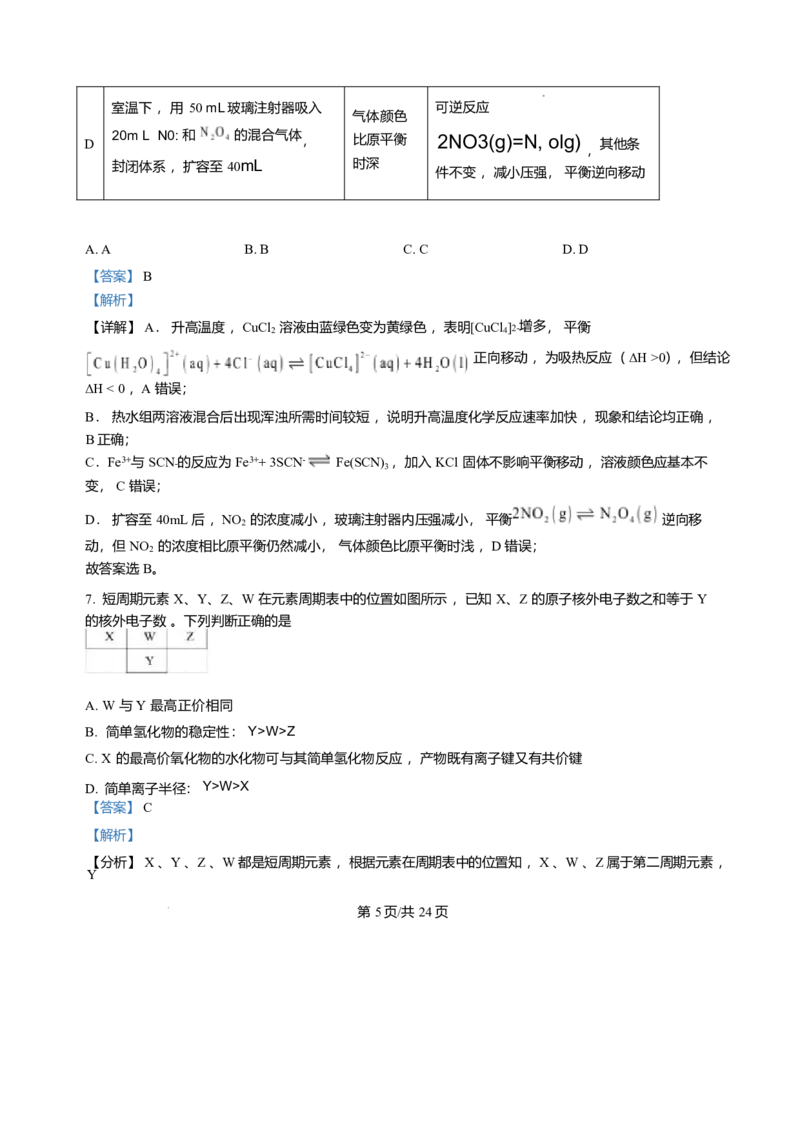
D. 用电子式表示HCI的形成过程:
2. 关于化工生产原理的描述中正确的是
A. 在给铁制品上镀铜时 ,应用铁做阳极
B. 工业上电解熔融的氧化镁来获得镁单质
C. 在氯碱工业中, 电解池中 阴极产生的是 H ,NaOH 在阳极附近产生
2
D. 电解精炼铜时 ,应用粗铜作阳极 、精铜作阴极, 可用 CuSO 溶液作电解质溶液
4
3. 下列分子或离子的空间结构和中心原子的杂化方式均正确的是
A. ASHY 平面三角形 sp'杂化 B. H,o' 平面三角形 sp'杂化
C. H,se V 形 sp'杂化 D. 三角锥形 sp'杂化
4. 金属的电化学腐蚀是金属腐蚀中最普遍且危害最严重的类型, 下列说法错误的是
A. 生铁比纯铁更易腐蚀
B. 镀锡铁(俗称马口铁)表面镀层破损后 ,仍可防止铁发生腐蚀
C. 为防止金属发生电化学腐蚀, 可采用外加电流的阴极保护法
D. 在钢铁吸氧腐蚀中 ,理论上若生成lmol Fe203·XH,o ,被还原的 数目为1.5NA
5. 某同学将三枚材质相同的铁钉 ,分别放入盛有等体积不同溶液(强酸性 、弱酸性 、中性)的三个体积相
同
第 1页/共 11页的密闭容器中 ,探究铁钉发生腐蚀的差异 。下图是实验过程中容器内气体压强随时间的变化, 下列说法
错误的是
A. 图 1 中压强增大只是因为铁钉与盐酸发生了析氢腐蚀所致
B. 图 2 压强变化比图3 慢 ,原因可能 PHl =4 时析氢腐蚀与吸氧腐蚀竞争所致
C. 图 2 压强变化比图3 慢 ,原因还可能是饱和NacI 溶液离子浓度大 ,加快了腐蚀
D. 中性溶液中铁钉腐蚀的负极反应: Fe- 2t" = Fe'
,
正极反应: O2+4e+2H2O=4OH
6. 根据所学知识, 结合实验操作, 判断下列实验现象及结论均正确的是
实验操作 实验现象 结论
反应
蓝绿色溶
取 5 mL —定浓度的CUC溶液,升
A 液变为黄
高温度
绿色
的
浸于热水
取四支试管, 两支—组 ,各加入
中的两溶
2mL0.2moli LN as, oz溶液和
液混合后
其他条件不变,升高温度,化学反应
B 2mL0.2molL H, SO4溶液 , —组 出现浑浊
速率加快
浸于冷水中, —组浸于热水中 。恒温 所需时间
后各组分别混合 较短
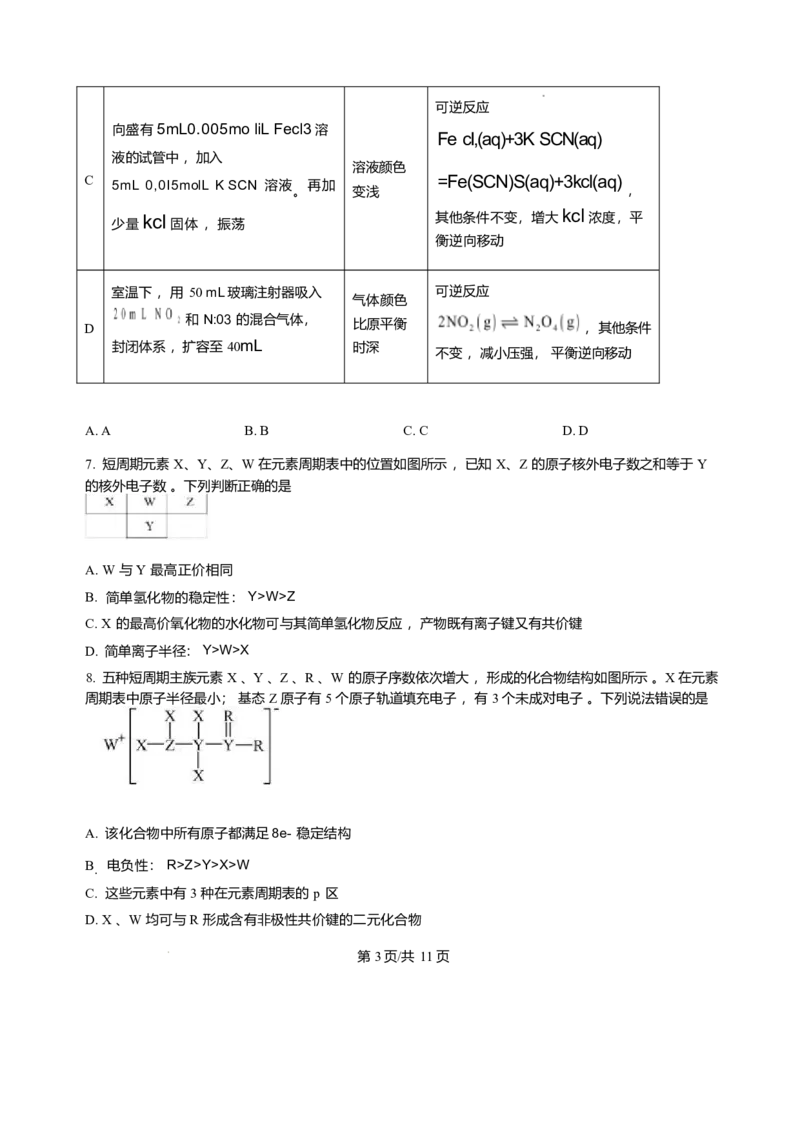
第 2页/共 11页可逆反应
向盛有5mL0.005mo liL Fecl3溶
Fe cI,(aq)+3K SCN(aq)
液的试管中 ,加入
溶液颜色
C =Fe(SCN)S(aq)+3kcl(aq)
5mL 0,0I5molL K SCN 溶液 再加
。 变浅 ,
kcl
kcl 其他条件不变,增大 浓度,平
少量 固体 ,振荡
衡逆向移动
室温下 ,用 50 mL玻璃注射器吸入 可逆反应
气体颜色
D 和 N:03 的混合气体, 比原平衡 , 其他条件
封闭体系 ,扩容至 40mL 时深
不变 ,减小压强, 平衡逆向移动
A. A B. B C. C D. D
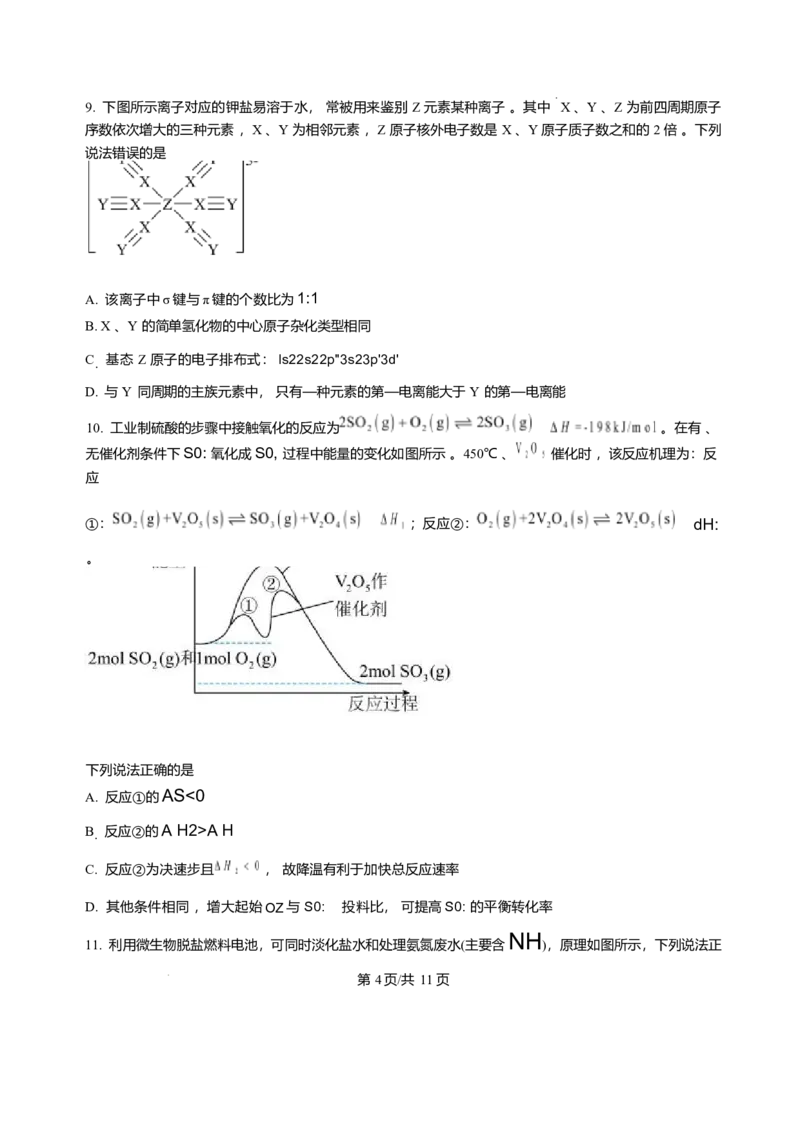
7. 短周期元素 X、Y、Z、W 在元素周期表中的位置如图所示 ,已知 X、Z 的原子核外电子数之和等于 Y
的核外电子数 。下列判断正确的是
A. W 与Y 最高正价相同
B. 简单氢化物的稳定性: Y>W>Z
C. X 的最高价氧化物的水化物可与其简单氢化物反应 ,产物既有离子键又有共价键
D. 简单离子半径: Y>W>X
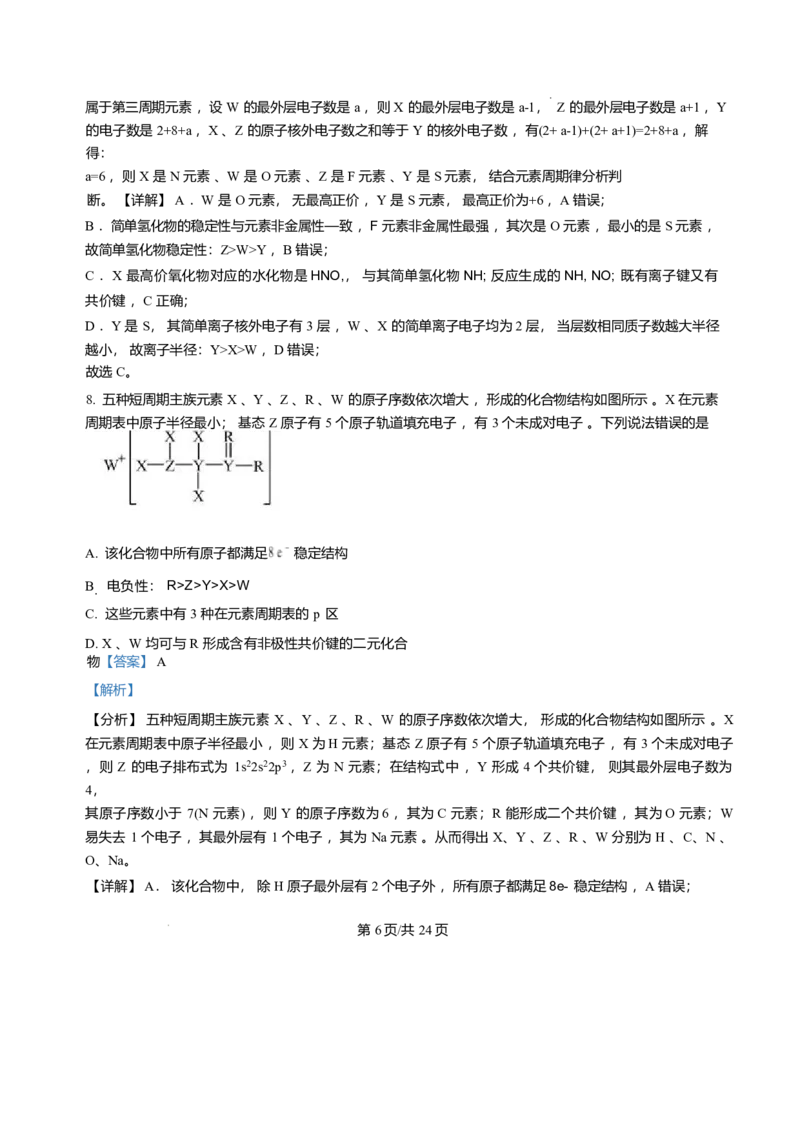
8. 五种短周期主族元素 X 、Y 、Z 、R 、W 的原子序数依次增大 ,形成的化合物结构如图所示 。X 在元素
周期表中原子半径最小; 基态 Z 原子有 5 个原子轨道填充电子 ,有 3 个未成对电子 。下列说法错误的是
A. 该化合物中所有原子都满足8e- 稳定结构
B. 电负性: R>Z>Y>X>W
C. 这些元素中有 3 种在元素周期表的 p 区
D. X 、W 均可与R 形成含有非极性共价键的二元化合物
第 3页/共 11页·
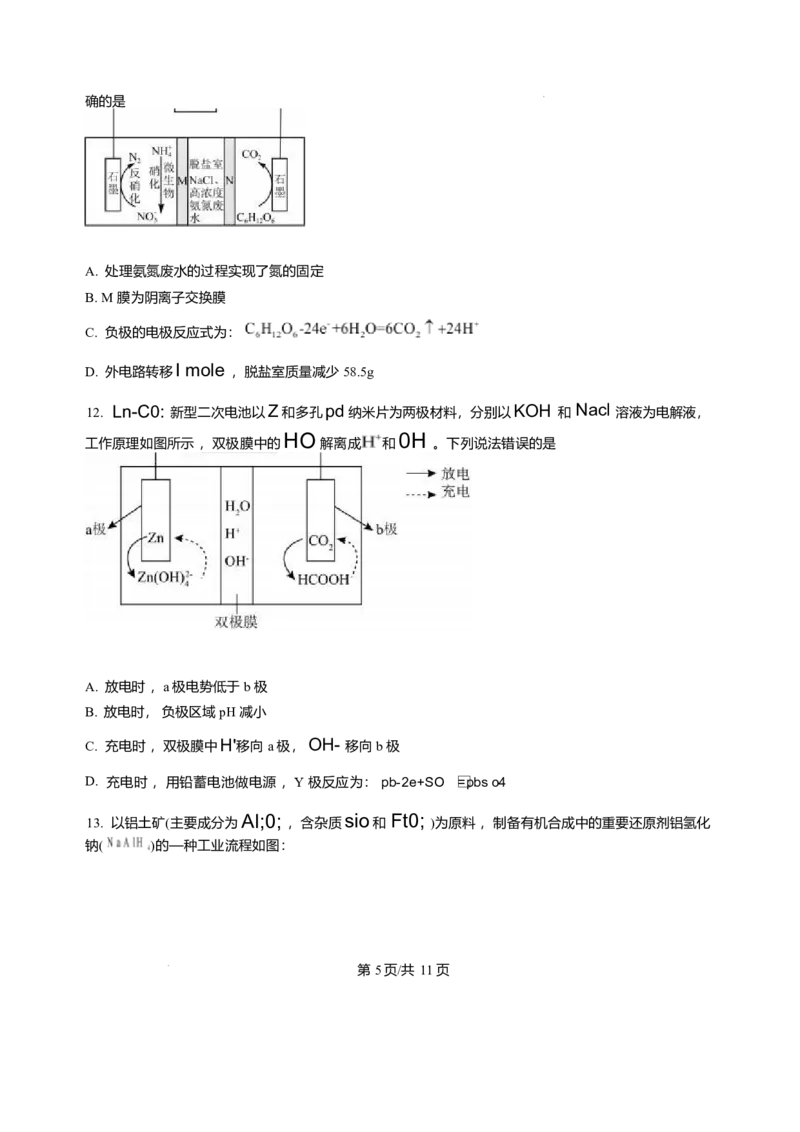
9. 下图所示离子对应的钾盐易溶于水, 常被用来鉴别 Z 元素某种离子 。其中 X 、Y 、Z 为前四周期原子
序数依次增大的三种元素 ,X 、Y 为相邻元素 ,Z 原子核外电子数是 X 、Y 原子质子数之和的 2 倍 。下列
说法错误的是
A. 该离子中σ键与π键的个数比为1:1
B. X 、Y 的简单氢化物的中心原子杂化类型相同
C. 基态 Z 原子的电子排布式: ls22s22p"3s23p'3d'
D. 与 Y 同周期的主族元素中, 只有—种元素的第—电离能大于 Y 的第—电离能
10. 工业制硫酸的步骤中接触氧化的反应为 。在有 、
无催化剂条件下S0: 氧化成S0, 过程中能量的变化如图所示 。450℃ 、 催化时 ,该反应机理为:反
应
①: ;反应②: dH:
。
下列说法正确的是
A. 反应①的AS<0
B. 反应②的A H2>A H
C. 反应②为决速步且 , 故降温有利于加快总反应速率
D. 其他条件相同 ,增大起始OZ与 S0: 投料比, 可提高S0: 的平衡转化率
NH
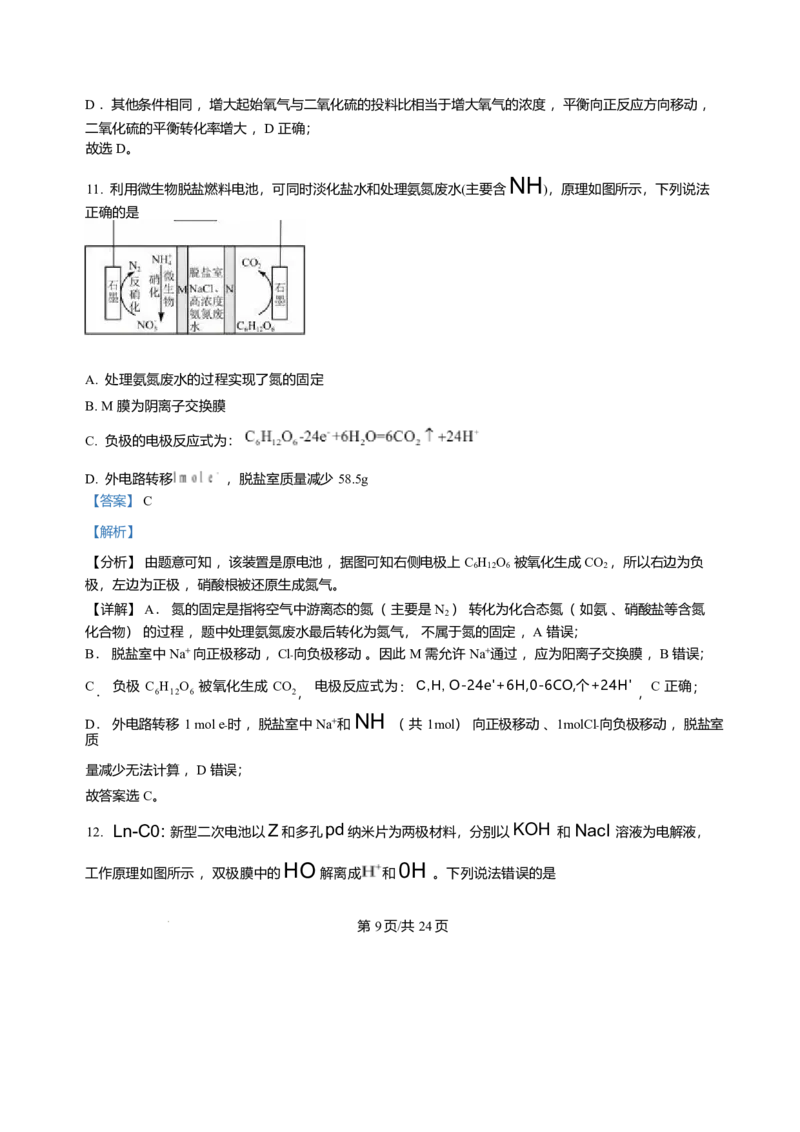
11. 利用微生物脱盐燃料电池,可同时淡化盐水和处理氨氮废水(主要含 ),原理如图所示,下列说法正
第 4页/共 11页确的是
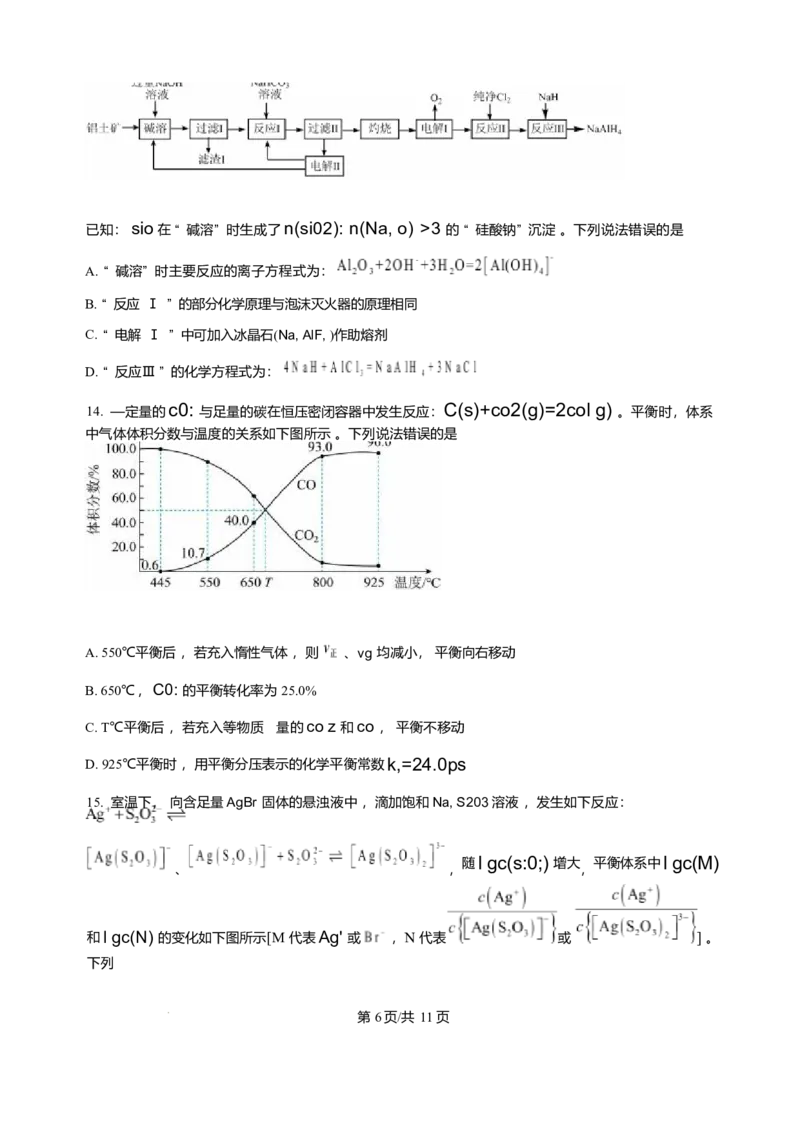
A. 处理氨氮废水的过程实现了氮的固定
B. M 膜为阴离子交换膜
C. 负极的电极反应式为:
D. 外电路转移 I mole ,脱盐室质量减少 58.5g
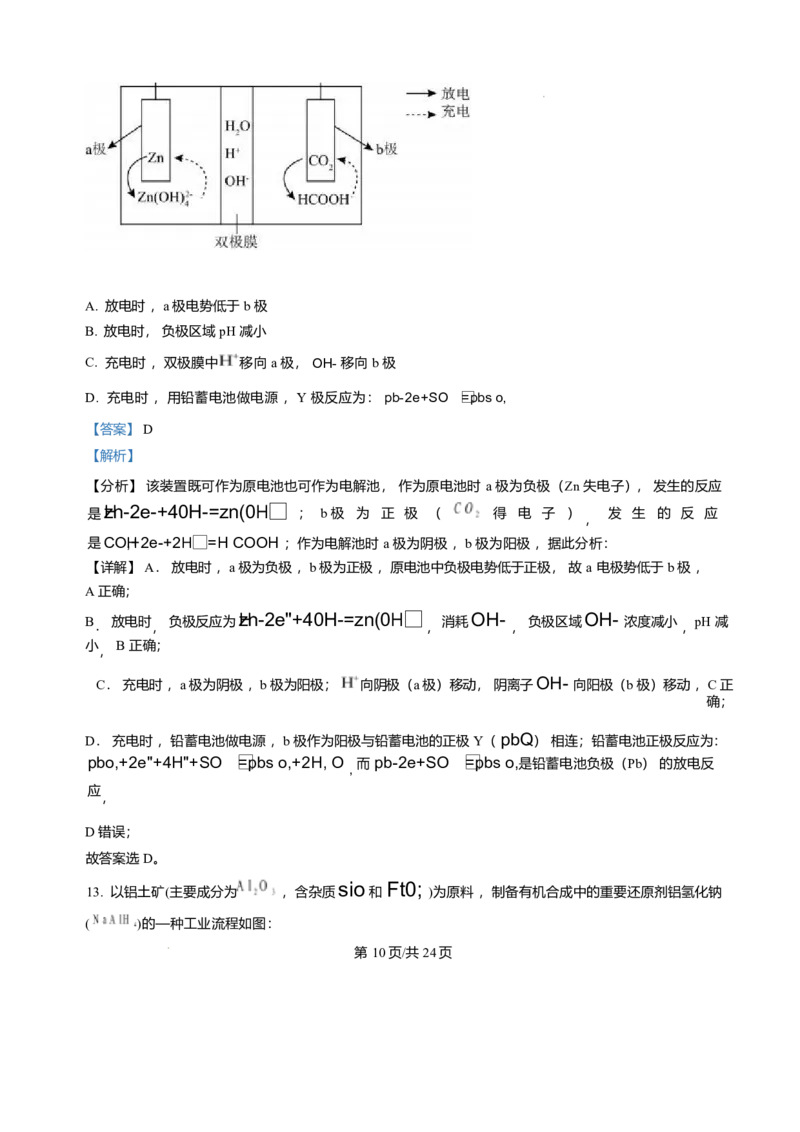
12. Ln-C0: 新型二次电池以Z和多孔pd纳米片为两极材料,分别以KOH 和 Nacl 溶液为电解液,
HO 0H
工作原理如图所示 ,双极膜中的 解离成 和 。下列说法错误的是
A. 放电时 ,a 极电势低于 b 极
B. 放电时, 负极区域 pH 减小
C. 充电时 ,双极膜中H'移向 a 极, OH- 移向 b 极
D. 充电时 ,用铅蓄电池做电源 ,Y 极反应为: pb-2e+SO =(cid:1)pbs o4
AI;0; sio Ft0;
13. 以铝土矿(主要成分为 ,含杂质 和 )为原料 ,制备有机合成中的重要还原剂铝氢化
钠( )的—种工业流程如图:
第 5页/共 11页已知: sio在 “ 碱溶” 时生成了n(si02): n(Na, o) >3 的 “ 硅酸钠” 沉淀 。下列说法错误的是
A. “ 碱溶” 时主要反应的离子方程式为:
B. “ 反应 Ⅰ ” 的部分化学原理与泡沫灭火器的原理相同
C. “ 电解 Ⅰ ” 中可加入冰晶石(Na, AlF, )作助熔剂
D. “ 反应Ⅲ ” 的化学方程式为:
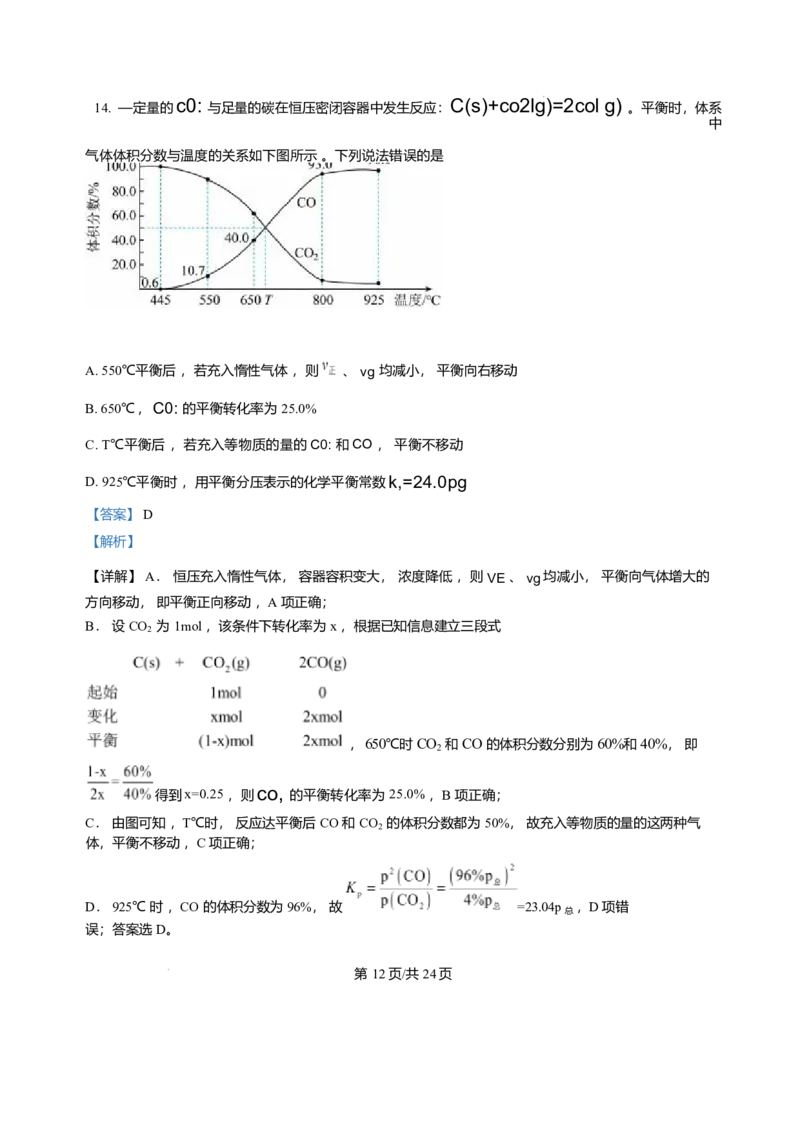
14. —定量的 c0: 与足量的碳在恒压密闭容器中发生反应: C(s)+co2(g)=2col g) 。平衡时,体系
中气体体积分数与温度的关系如下图所示 。下列说法错误的是
A. 550℃平衡后 ,若充入惰性气体 ,则 、vg 均减小, 平衡向右移动
B. 650℃ , C0: 的平衡转化率为 25.0%
C. T℃平衡后 ,若充入等物质 量的co z 和co , 平衡不移动
D. 925℃平衡时 ,用平衡分压表示的化学平衡常数k,=24.0ps
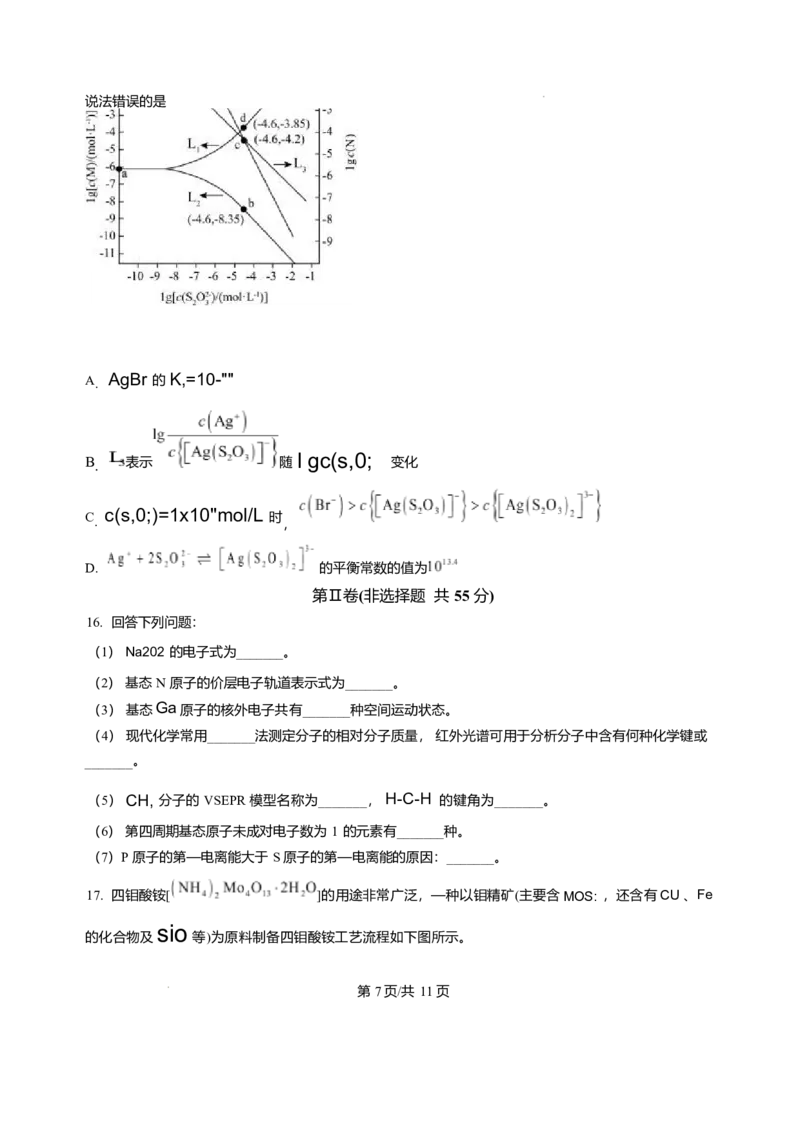
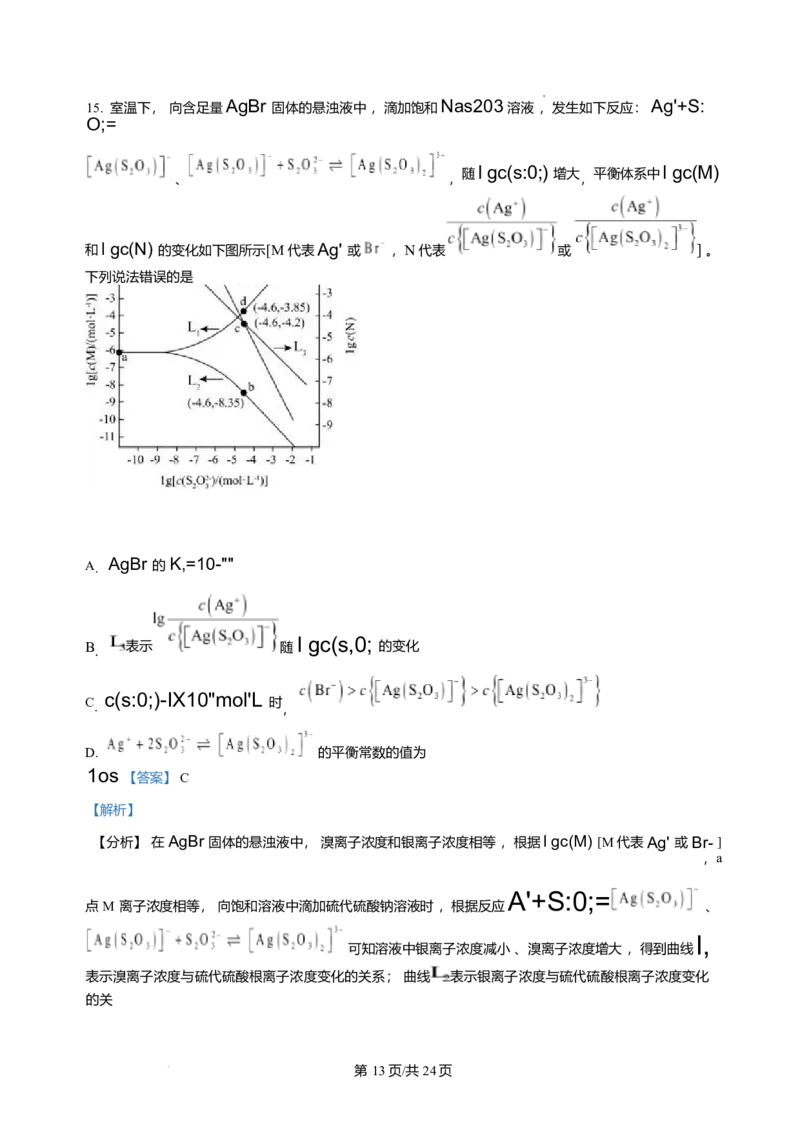
15. 室温下, 向含足量AgBr 固体的悬浊液中 ,滴加饱和Na, S203溶液 ,发生如下反应:
随l gc(s:0;) 增大 平衡体系中l gc(M)
、 , ,
和l gc(N) 的变化如下图所示[M 代表Ag' 或 ,N 代表 或 ] 。
下列
第 6页/共 11页说法错误的是
A. AgBr 的 K,=10-""
l gc(s,0;
B. 表示 随 变化
c(s,0;)=1x10"mol/L
C 时
. ,
D. 的平衡常数的值为
第Ⅱ卷(非选择题 共 55 分)
16. 回答下列问题:
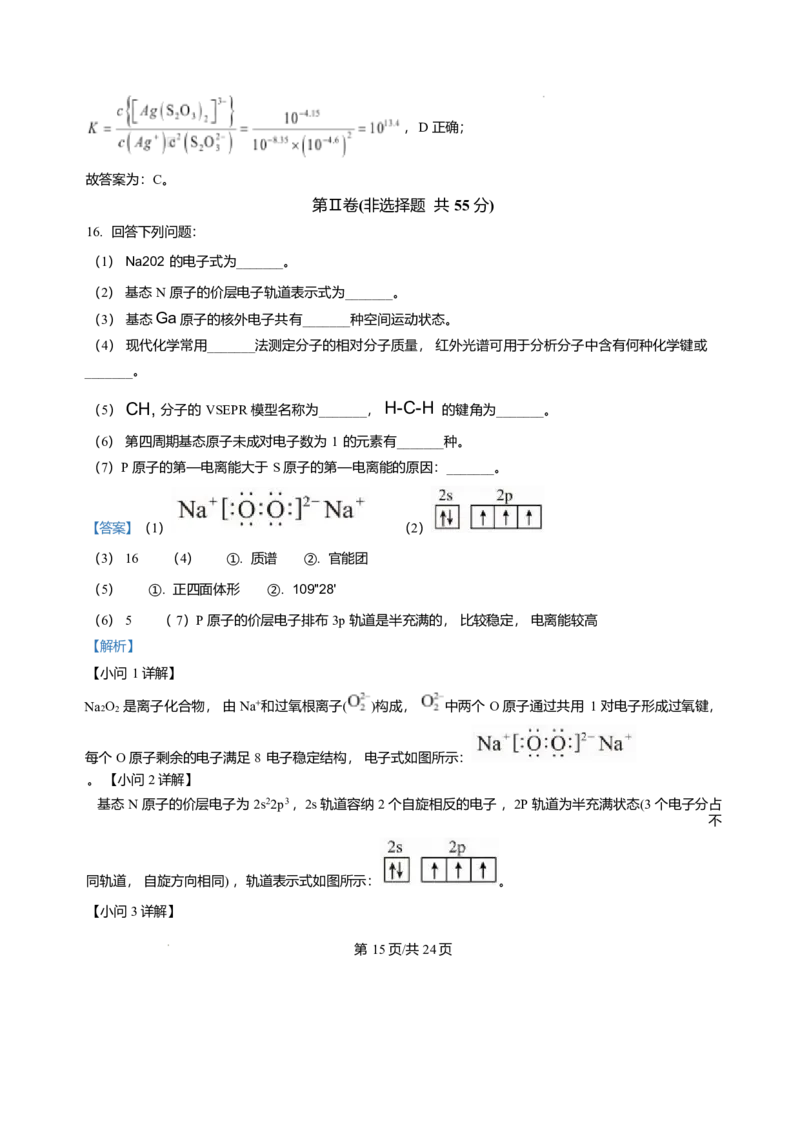
(1) Na202 的电子式为_______。
(2) 基态 N 原子的价层电子轨道表示式为_______。
(3) 基态Ga原子的核外电子共有_______种空间运动状态。
(4) 现代化学常用_______法测定分子的相对分子质量, 红外光谱可用于分析分子中含有何种化学键或
_______。
(5) CH, 分子的 VSEPR 模型名称为_______, H-C-H 的键角为_______。
(6) 第四周期基态原子未成对电子数为 1 的元素有_______种。
(7)P 原子的第—电离能大于 S 原子的第—电离能的原因:_______。
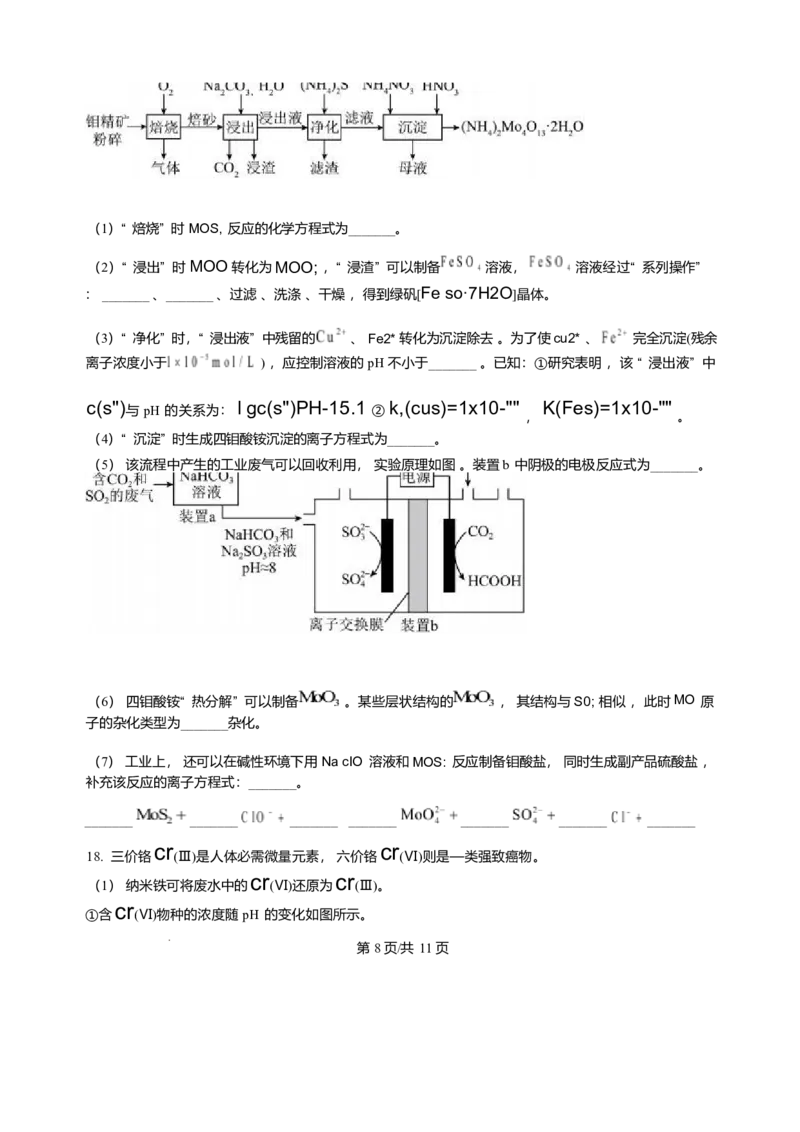
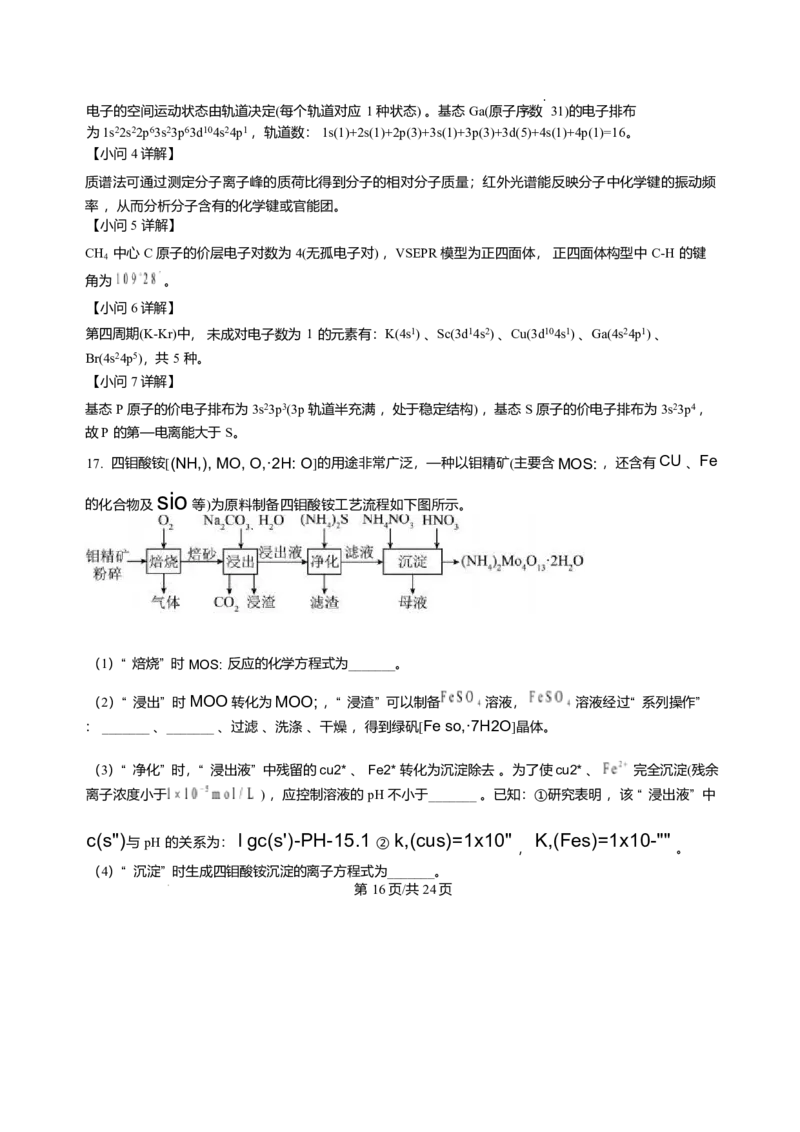
17. 四钼酸铵[ ]的用途非常广泛,—种以钼精矿(主要含MOS: ,还含有CU 、Fe
sio
的化合物及 等)为原料制备四钼酸铵工艺流程如下图所示。
第 7页/共 11页(1)“ 焙烧” 时 MOS, 反应的化学方程式为_______。
(2)“ 浸出” 时 MOO转化为MOO; ,“ 浸渣” 可以制备 溶液, 溶液经过“ 系列操作”
: _______ 、_______ 、过滤 、洗涤 、干燥 ,得到绿矾[Fe so·7H2O]晶体。
(3)“ 净化” 时,“ 浸出液” 中残留的 、 Fe2* 转化为沉淀除去 。为了使cu2* 、 完全沉淀(残余
离子浓度小于 ) ,应控制溶液的 pH 不小于_______ 。已知:①研究表明 ,该 “ 浸出液” 中
c(s") l gc(s")PH-15.1 k,(cus)=1x10-"" K(Fes)=1x10-""
与 pH 的关系为: ②
, 。
(4)“ 沉淀” 时生成四钼酸铵沉淀的离子方程式为_______。
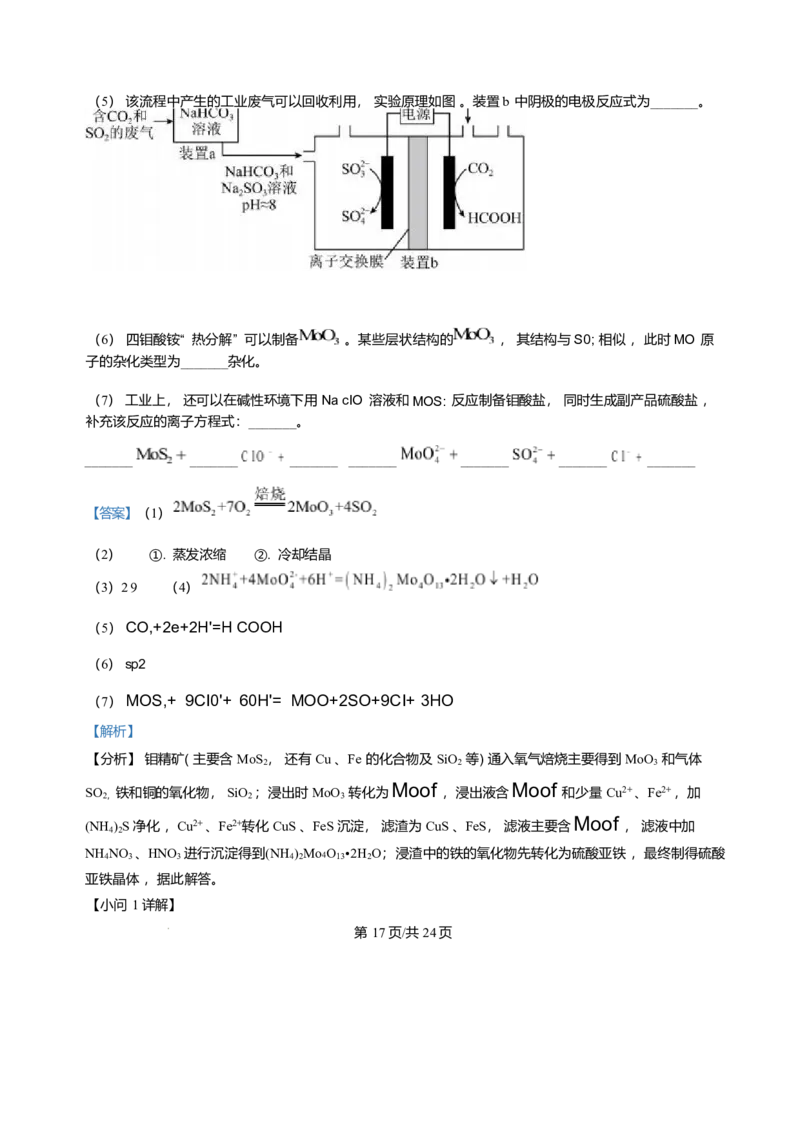
(5) 该流程中产生的工业废气可以回收利用, 实验原理如图 。装置b 中阴极的电极反应式为_______。
(6) 四钼酸铵“ 热分解” 可以制备 。某些层状结构的 , 其结构与S0; 相似 ,此时MO 原
子的杂化类型为_______杂化。
(7) 工业上, 还可以在碱性环境下用 Na cIO 溶液和MOS: 反应制备钼酸盐, 同时生成副产品硫酸盐 ,
补充该反应的离子方程式:_______。
_______ _______ _______ _______ _______ _______ _______
cr cr
18. 三价铬 (Ⅲ)是人体必需微量元素, 六价铬 (Ⅵ)则是—类强致癌物。
cr cr
(1) 纳米铁可将废水中的 (Ⅵ)还原为 (Ⅲ)。
cr
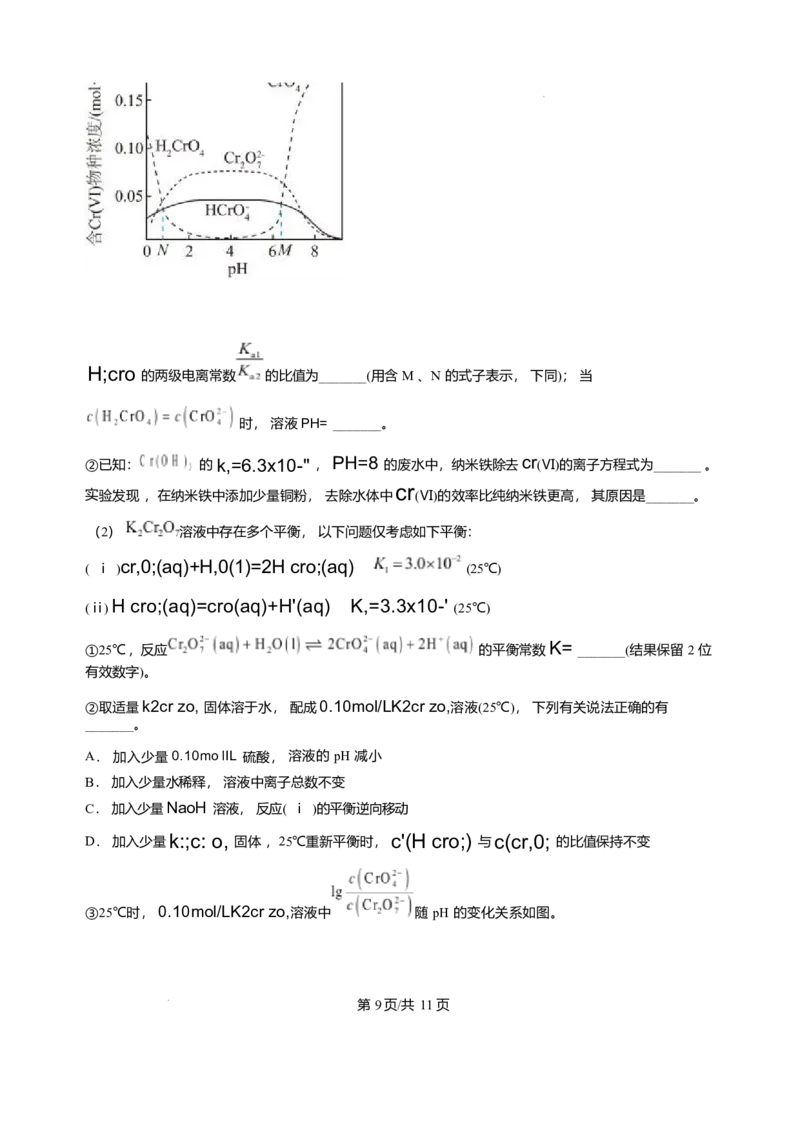
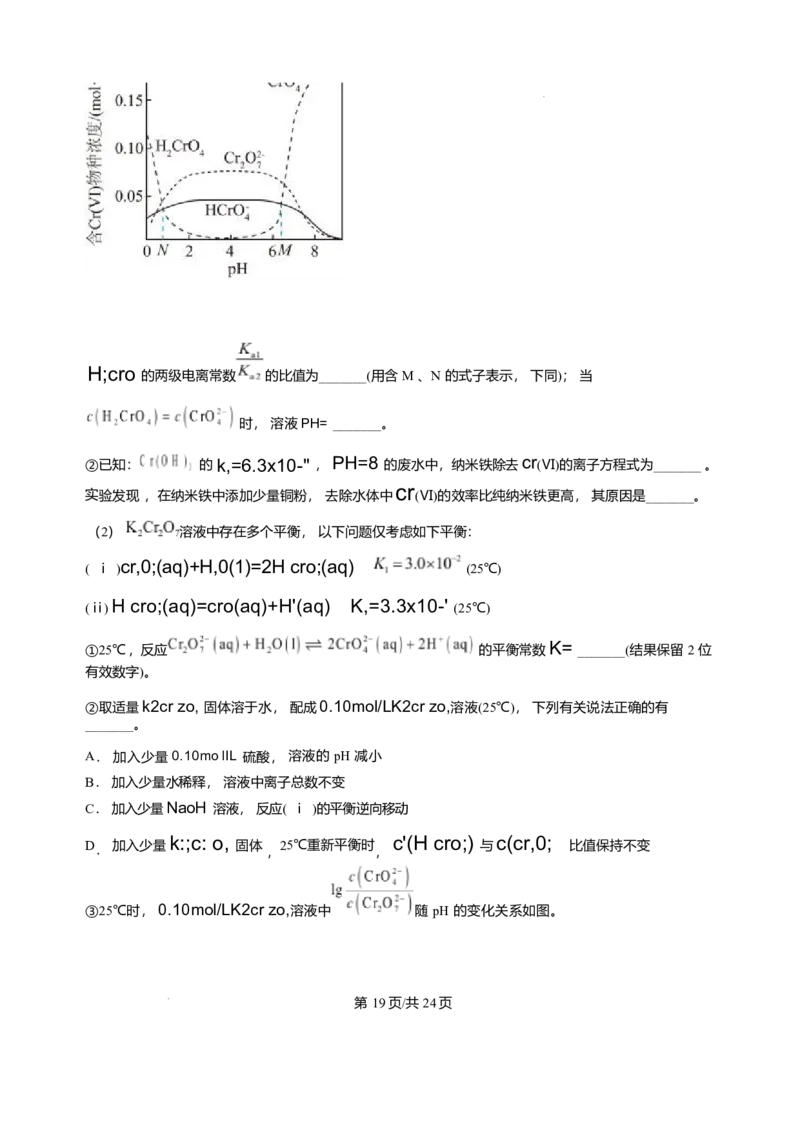
①含 (Ⅵ)物种的浓度随 pH 的变化如图所示。
·
第 8页/共 11页H;cro
的两级电离常数 的比值为_______(用含 M 、N 的式子表示, 下同); 当
时, 溶液PH= _______。
②已知: 的 k,=6.3x10-" , PH=8 的废水中,纳米铁除去 cr (Ⅵ)的离子方程式为_______ 。
cr
实验发现 ,在纳米铁中添加少量铜粉, 去除水体中 (Ⅵ)的效率比纯纳米铁更高, 其原因是_______。
(2) 溶液中存在多个平衡, 以下问题仅考虑如下平衡:
cr,0;(aq)+H,0(1)=2H cro;(aq)
( ⅰ ) (25℃)
H cro;(aq)=cro(aq)+H'(aq) K,=3.3x10-'
(ⅱ) (25℃)
K=
①25℃ , 反应 的平衡常数 _______(结果保留 2 位
有效数字)。
②取适量k2cr zo, 固体溶于水, 配成0.10mol/LK2cr zo,溶液(25℃), 下列有关说法正确的有
_______。
A. 加入少量0.10mo lIL 硫酸, 溶液的 pH 减小
B. 加入少量水稀释, 溶液中离子总数不变
C. 加入少量NaoH 溶液, 反应( ⅰ )的平衡逆向移动
D. 加入少量 k:;c: o, 固体 ,25℃重新平衡时, c'(H cro;) 与c(cr,0; 的比值保持不变
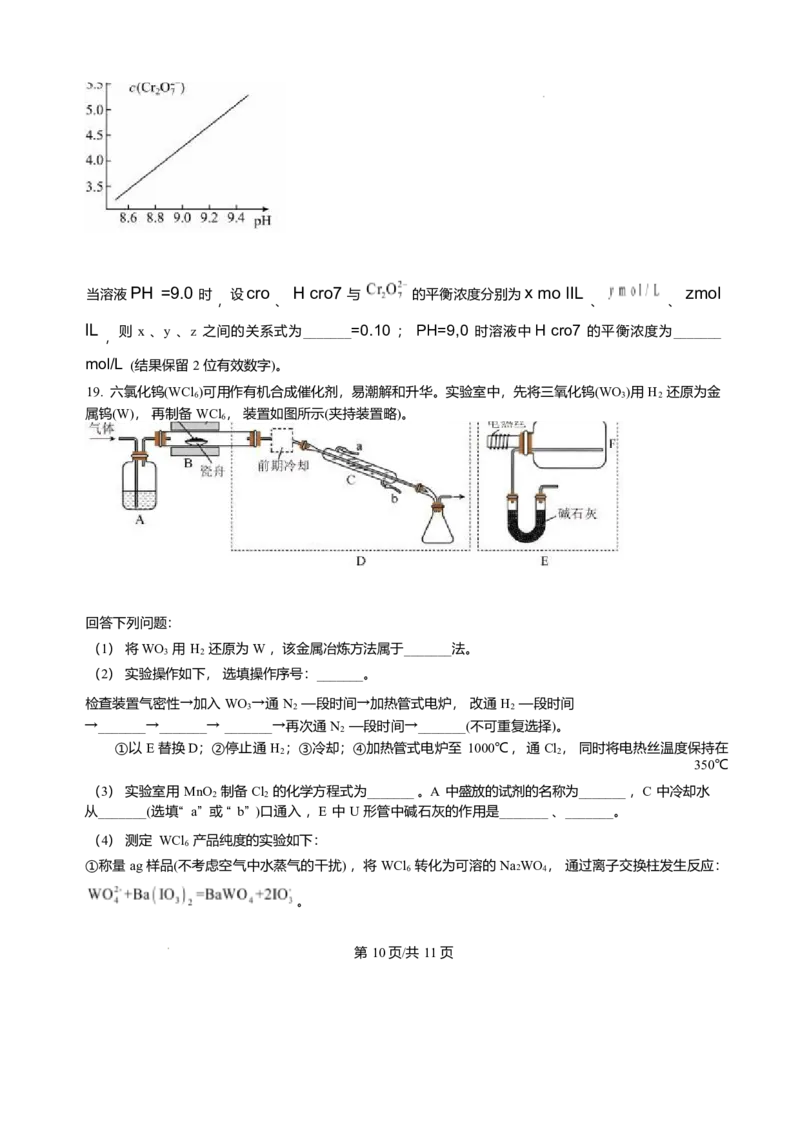
③25℃时, 0.10mol/LK2cr zo,溶液中 随 pH 的变化关系如图。
第 9页/共 11页当溶液PH =9.0 时 设cro H cro7 与 的平衡浓度分别为 x mo lIL zmol
, 、 、 、
lL 则 x 、y 、z 之间的关系式为_______=0.10 ; PH=9,0 时溶液中H cro7 的平衡浓度为_______
,
mol/L (结果保留 2 位有效数字)。
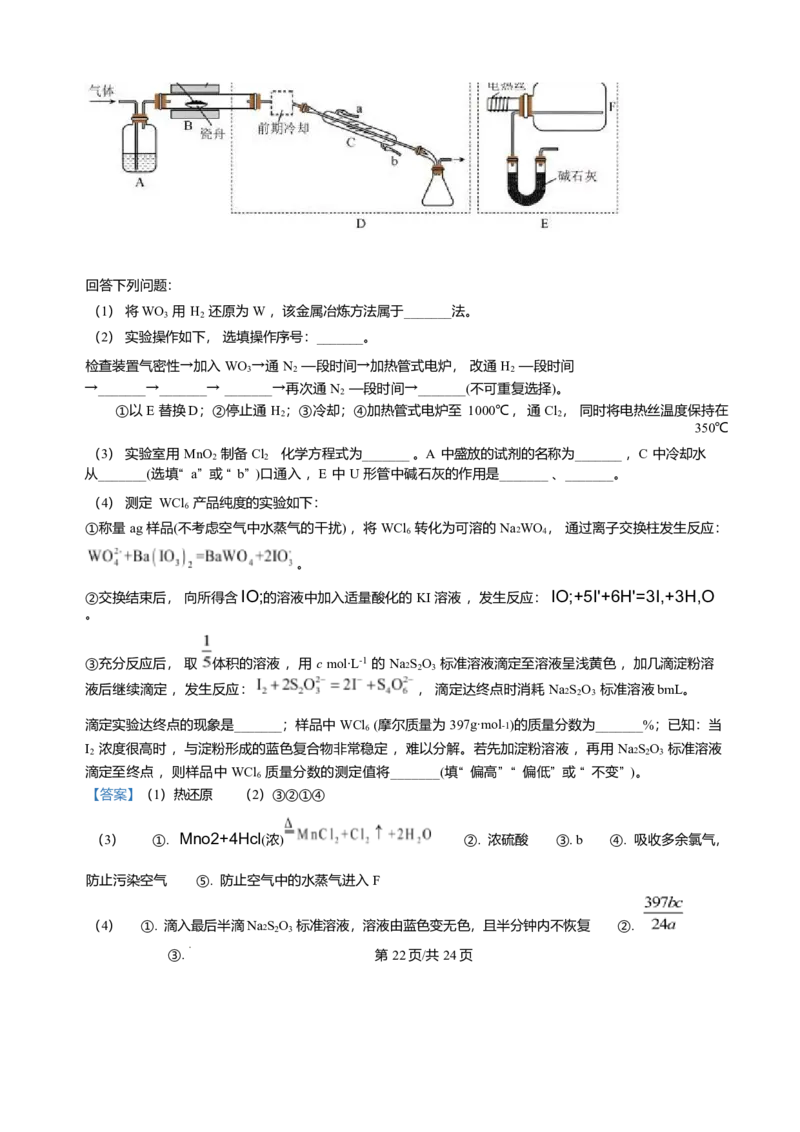
19. 六氯化钨(WCl )可用作有机合成催化剂,易潮解和升华。实验室中,先将三氧化钨(WO )用 H 还原为金
6 3 2
属钨(W), 再制备 WCl , 装置如图所示(夹持装置略)。
6
回答下列问题:
(1) 将 WO 用 H 还原为 W ,该金属冶炼方法属于_______法。
3 2
(2) 实验操作如下, 选填操作序号:_______。
检查装置气密性→加入 WO →通 N —段时间→加热管式电炉, 改通 H —段时间
3 2 2
→_______→_______→ _______→再次通 N —段时间→_______(不可重复选择)。
2
①以 E 替换D;②停止通 H ;③冷却;④加热管式电炉至 1000℃ , 通 Cl , 同时将电热丝温度保持在
2 2
350℃
(3) 实验室用 MnO 制备 Cl 的化学方程式为_______ 。A 中盛放的试剂的名称为_______ ,C 中冷却水
2 2
从_______(选填“ a” 或 “ b” )口通入 ,E 中 U 形管中碱石灰的作用是_______ 、_______。
(4) 测定 WCl 产品纯度的实验如下:
6
①称量 ag 样品(不考虑空气中水蒸气的干扰) ,将 WCl
6
转化为可溶的 Na2WO
4
, 通过离子交换柱发生反应:
。
第 10页/共 11页②交换结束后, 向所得含IO;的溶液中加入适量酸化的 KI 溶液 ,发生反应: IO;+5I+6H'=3I,+3H,O
。
③充分反应后, 取 体积的溶液 ,用 c mol∙L-1 的 Na2S
2
O
3
标准溶液滴定至溶液呈浅黄色 ,加几滴淀粉溶
液后继续滴定 ,发生反应: , 滴定达终点时消耗 Na2S
2
O
3
标准溶液bmL。
滴定实验达终点的现象是_______;样品中 WCl
6
(摩尔质量为 397g∙mol-1)的质量分数为_______%;已知:当
I
2
浓度很高时 ,与淀粉形成的蓝色复合物非常稳定 ,难以分解。若先加淀粉溶液 ,再用 Na2S
2
O
3
标准溶液
滴定至终点 ,则样品中 WCl 质量分数的测定值将_______(填“ 偏高” “ 偏低” 或 “ 不变” )。
6
第 11页/共 11页哈三中 2025—2026 学年度上学期高二学年期末考试
化学试卷
本试卷分第 Ⅰ 卷(选择题)和第Ⅱ卷(非选择题)两部分, 共 100 分,考试用时 75 分
钟可能用到的相对原子质量:H-1 N-14 Na-23 Cl-35.5
第 Ⅰ 卷(选择题 共 45 分)
一 、单选题: 共 15 个小题, 每题有且仅有一个选项符合题意, 每题 3 分, 共 45 分。
1. 下列化学用语表示正确的是
A. 的 VSEPR 模型:
B. 电子式:
C. 基态锗原子的简化电子排布式: [Ar]4s24p2
D. 用电子式表示HCI的形成过程:
【答案】 A
【解析】
【详解】 A .N 与2 个 O 形成σ键, 故σ键电子对数为2, 中心 N 原子的价电子数为 5, 带—个单
位负
电荷 ,价电子总数为 ,孤电子对数= ,价层电子对数为 ,VSEPR 模型为
平面三角形 ,A 正确;
…
B. 的电子式应为: ,B 错误;
C. 基态锗原子的简化电子排布式应为:[Ar]3d"4s24p2 ,C 错误;
D. HCl 是共价化合物, 其生成过程如图所示: ,D 错
误;故选 A。
2. 关于化工生产原理的描述中正确的是
A. 在给铁制品上镀铜时 ,应用铁做阳极
第 1页/共 24页B. 工业上电解熔融的氧化镁来获得镁单质
C. 在氯碱工业中, 电解池中的阴极产生的是 H ,NaOH 在阳极附近产生
2
D. 电解精炼铜时 ,应用粗铜作阳极 、精铜作阴极, 可用 CuSO 溶液作电解质溶
4
液【答案】 D
【解析】
【详解】 A. 电镀时 ,镀层金属作阳极 ,待镀件作阴极 ,铁制品镀铜应使用铜阳极 ,A 错误;
B. 工业制镁电解的是熔融氯化镁而非氧化镁, 因 MgO 熔点过高 ,B 错误;
C. 氯碱工业中, 阴极析出 H
2
,OH-在阴极积累生成 NaOH, 而非阳极附近 ,C 错误;
D. 电解精炼铜时 ,粗铜为阳极(溶解) 、精铜为阴极(析出) ,CuSO 溶液作电解质 ,D 正
4
确;故答案为:D。
3. 下列分子或离子的空间结构和中心原子的杂化方式均正确的是
A. ASH; 平面三角形 sP'杂化 B. H,O' 平面三角形 sP杂化
C. H,se V 形 sp'杂化 D. 三角锥形 sp'杂化
【答案】 C
【解析】
【详解】 A .AsH 中心原子的价层电子对数=3+ (5-3×1)=4, 为 sp3 ,有—对孤电子对, 立体构型为三角
3
锥形 ,A 错误;
B .H O+ 的中心原子的价层电子对数=3+ (6-1-3×1)=4 ,为 sp3 ,有—对孤电子对 ,立体构型为三角锥形
3
,B错误;
C. H Se 中心原子的价层电子对数 为 sp3 ,有两对孤电子对, 立体构型为V 形 ,C 正
2
确;
D. 中心原子的价层电子对数=3+ (4+2-3×2)=3, 为 sp2 ,没有孤电子对, 立体构型为平面三角形 ,
D错误;
故答案为:C。
4. 金属的电化学腐蚀是金属腐蚀中最普遍且危害最严重的类型, 下列说法错误的是
A. 生铁比纯铁更易腐蚀
B. 镀锡铁(俗称马口铁)表面镀层破损后 ,仍可防止铁发生腐蚀
C. 为防止金属发生电化学腐蚀, 可采用外加电流的阴极保护法
第 2页/共 24页D. 在钢铁吸氧腐蚀中 ,理论上若生成lmol Fe203·XH2o ,被还原的o:数目为
1.5N 【答案】 B
【解析】
【详解】 A. 生铁含有碳等杂质, 可形成原电池 ,加速电化学腐蚀, 因此比纯铁更易腐蚀 ,A 正确;
B .镀锡铁( 马口铁)镀层破损后 ,铁与锡在电解质溶液中形成原电池 ,铁作为负极更易被腐蚀 ,不能防
止铁腐蚀 ,B 错误;
C.外加电流的阴极保护法通过外部电源使被保护金属成为阴极,从而抑制其氧化反应 ,可有效防止电化
学腐蚀 ,C 正确;
D. lmol Fe203·XH2o需 2mol Fe 失去 6 mol 电子 ( 每个 Fe 从 0 价升至+3 价), 正极电极反应式为:
, 因此每摩尔 被还原获得4 mol 电子 ,因此需1.5mo lo2 ,被还原的o:数目
为
1.5NA D 正确;
,
故答案选 B。
5. 某同学将三枚材质相同的铁钉 ,分别放入盛有等体积不同溶液(强酸性 、弱酸性 、中性)的三个体积相
同的密闭容器中 ,探究铁钉发生腐蚀的差异 。下图是实验过程中容器内气体压强随时间的变化, 下列说
法错误的是
A. 图 1 中压强增大只是因为铁钉与盐酸发生了析氢腐蚀所致
B. 图 2 压强变化比图3 慢 ,原因可能是PH =4 时析氢腐蚀与吸氧腐蚀竞争所致
C. 图 2 压强变化比图3 慢 ,原因还可能是饱和NacI 溶液离子浓度大 ,加快了腐蚀
D. 中性溶液中铁钉腐蚀的负极反应: , 正极反应:
O2+4e+2H2O=4OH 【答案】 A
【解析】
【分析】 强酸性溶液中发生析氢腐蚀 ,产生 H2 , 弱酸性 、中性溶液中发生吸氧腐蚀, 消耗 。
第 3页/共 24页【详解】 A. 图 1 是PH = 2 的盐酸 ,铁钉发生析氢腐蚀产生氢气使压强增大 ,但溶液中温度变化等也会
影
响压强,“只是因为析氢腐蚀” 的描述过于绝对 ,A 错误;
B. 图 2 是 PH =4 的盐酸, 弱酸性环境下析氢腐蚀使压强增大, 与吸氧腐蚀使压强减小竞争, 导致压
强变化更慢 ,B 正确;
Nacl
C. 图 3 是饱和 溶液, 离子浓度大 、导电性强, 吸氧腐蚀速率更快, 因此图 2 压强变化比图3 慢
,C正确;
D 中性溶液中发生吸氧腐蚀 负极反应为Fe- 2e" = Fe' 正极反应为O2+4e+2H2O=4OH D
. , , ,
正确;
故答案选 A。
6. 根据所学知识, 结合实验操作, 判断下列实验现象及结论均正确的是
实验操作 实验现象 结论
反应
蓝绿色溶
取 5 mL —定浓度的CUC溶液,升
A 液变为黄
高温度
绿色
的
浸于热水
取四支试管, 两支—组 ,各加入
中的两溶
2mL0.2mol/LN as2oz溶液和
液混合后
其他条件不变,升高温度,化学反应
B 2mL0.2mol/LH, SO;溶液 , —组 出现浑浊
速率加快
浸于冷水中, —组浸于热水中 。恒温 所需时间
后各组分别混合 较短
可逆反应
向盛有5mL0.005mol fL Fecl3溶
Fe cI,(aq)+3K SCN/aq)
液的试管中 ,加入
溶液颜色
C =Fe(SCN)S(aq)+3K CI(aq)
溶液。再加 变浅 ,
kcl
kcl 其他条件不变,增大 浓度,平
少量 固体 ,振荡
衡逆向移动
第 4页/共 24页室温下 ,用 50 mL玻璃注射器吸入 可逆反应
气体颜色
D 20m L N0: 和 的混合气体 , 比原平衡 2NO3(g)=N, olg) 其他条
,
封闭体系 ,扩容至 40mL 时深
件不变 ,减小压强, 平衡逆向移动
A. A B. B C. C D. D
【答案】 B
【解析】
【详解】 A. 升高温度 ,CuCl
2
溶液由蓝绿色变为黄绿色 ,表明[CuCl
4
]2-增多, 平衡
正向移动 ,为吸热反应 ( ΔH >0),但结论
ΔH < 0 ,A 错误;
B. 热水组两溶液混合后出现浑浊所需时间较短 ,说明升高温度化学反应速率加快 ,现象和结论均正确 ,
B正确;
C.Fe3+与 SCN-的反应为 Fe3++ 3SCN- Fe(SCN)
3
,加入 KCl 固体不影响平衡移动 ,溶液颜色应基本不
变, C 错误;
D. 扩容至 40mL 后 ,NO 的浓度减小 ,玻璃注射器内压强减小, 平衡 逆向移
2
动,但 NO 的浓度相比原平衡仍然减小, 气体颜色比原平衡时浅 ,D 错误;
2
故答案选 B。
7. 短周期元素 X、Y、Z、W 在元素周期表中的位置如图所示 ,已知 X、Z 的原子核外电子数之和等于 Y
的核外电子数 。下列判断正确的是
A. W 与Y 最高正价相同
B. 简单氢化物的稳定性: Y>W>Z
C. X 的最高价氧化物的水化物可与其简单氢化物反应 ,产物既有离子键又有共价键
D. 简单离子半径: Y>W>X
【答案】 C
【解析】
【分析】 X 、Y 、Z 、W 都是短周期元素 ,根据元素在周期表中的位置知 ,X 、W 、Z 属于第二周期元素 ,
Y
第 5页/共 24页·
属于第三周期元素 ,设 W 的最外层电子数是 a ,则 X 的最外层电子数是 a-1, Z 的最外层电子数是 a+1 ,Y
的电子数是 2+8+a ,X 、Z 的原子核外电子数之和等于 Y 的核外电子数 ,有(2+ a-1)+(2+ a+1)=2+8+a ,解
得:
a=6 ,则 X 是 N 元素 、W 是 O 元素 、Z 是 F 元素 、Y 是 S 元素, 结合元素周期律分析判
断。 【详解】 A .W 是 O 元素, 无最高正价 ,Y 是 S 元素, 最高正价为+6 ,A 错误;
B .简单氢化物的稳定性与元素非金属性—致 ,F 元素非金属性最强 ,其次是 O 元素 ,最小的是 S 元素 ,
故简单氢化物稳定性:Z>W>Y ,B 错误;
C .X 最高价氧化物对应的水化物是HNO,, 与其简单氢化物NH; 反应生成的NH, NO; 既有离子键又有
共价键 ,C 正确;
D .Y 是 S, 其简单离子核外电子有 3 层 ,W 、X 的简单离子电子均为2 层, 当层数相同质子数越大半径
越小, 故离子半径:Y>X>W ,D 错误;
故选 C。
8. 五种短周期主族元素 X 、Y 、Z 、R 、W 的原子序数依次增大 ,形成的化合物结构如图所示 。X 在元素
周期表中原子半径最小; 基态 Z 原子有 5 个原子轨道填充电子 ,有 3 个未成对电子 。下列说法错误的是
A. 该化合物中所有原子都满足 稳定结构
B. 电负性: R>Z>Y>X>W
C. 这些元素中有 3 种在元素周期表的 p 区
D. X 、W 均可与R 形成含有非极性共价键的二元化合
物【答案】 A
【解析】
【分析】 五种短周期主族元素 X 、Y 、Z 、R 、W 的原子序数依次增大, 形成的化合物结构如图所示 。X
在元素周期表中原子半径最小 ,则 X 为H 元素;基态 Z 原子有 5 个原子轨道填充电子 ,有 3 个未成对电子
,则 Z 的电子排布式为 1s22s22p3 ,Z 为 N 元素;在结构式中 ,Y 形成 4 个共价键, 则其最外层电子数为
4,
其原子序数小于 7(N 元素) ,则 Y 的原子序数为6 ,其为C 元素;R 能形成二个共价键 ,其为O 元素;W
易失去 1 个电子 ,其最外层有 1 个电子 ,其为 Na 元素 。从而得出 X、Y 、Z 、R 、W 分别为 H 、C、N 、
O、Na。
【详解】 A. 该化合物中, 除 H 原子最外层有 2 个电子外 ,所有原子都满足8e- 稳定结构 ,A 错误;
第 6页/共 24页B .X 、Y 、Z 、R 、W 分别为 H 、C 、N 、O 、Na ,依据元素的周期性递变规律 ,非金属性 O
> N>C>H>Na ,元素的非金属性越强, 电负性越大 ,则电负性:O>N>C>H>Na ,B 正确;
C. 这些元素中 ,C 、N 、O 3 种在元素周期表的 p 区 ,H 、Na 在 s 区 ,C 正确;
D .X(H) 、W(Na)均可与 R(O)形成含有非极性共价键的二元化合物 H
2
O
2
、Na2 O
2
,D 正
确;故选 A。
9. 下图所示离子对应的钾盐易溶于水, 常被用来鉴别 Z 元素某种离子 。其中 X 、Y 、Z 为前四周期原子序
数依次增大的三种元素 ,X 、Y 为相邻元素 ,Z 原子核外电子数是 X 、Y 原子质子数之和的 2 倍 。下列说
法错误的是
A. 该离子中σ键与π键的个数比为1:1
B. X 、Y 的简单氢化物的中心原子杂化类型相同
C. 基态 Z 原子的电子排布式: ls22s22p"3s23p'3d'
D. 与 Y 同周期的主族元素中, 只有—种元素的第—电离能大于 Y 的第—电离
能【答案】 C
【解析】
【分析】 X 、Y 、Z 为前四周期原子序数依次增大的三种元素 ,X 、Y 为相邻元素, 根据图示 ,Y 能形成
3
个共价键 、X 能形成 4 个共价键, 则 X 是ⅣA 族元素 、Y 是ⅤA 族元素 ,Z 原子核外电子数是 X 、Y
原子质子数之和的 2 倍 ,则 X 是 C 元素 、Y 是 N 元素 ,Z 是 Fe 元素 。 k,[re(CN)] 用来检验 。
【详解】 A. 该离子是[Fe(CN), , CN- 中含 1 个 σ 键 、2 个 键, Fe* 与CN- 通过配位键 ( σ
键) 结合 ,共 6 个配位键;因此σ 键总数为6 ( 配位键) +6 ( CN- 内 σ键) =12 , 露 键总数为
6x2=12 , σ键与 键个数比为1:1 ,A 正确;
B .X 的简单氢化物是CH, , 中心 C 原子杂化类型为SP' ;Y 的简单氢化物是NH; , 中心 N 原子杂化
类型也为sp' , 二者杂化类型相同 ,B 正确;
C. Z 是 Fe, 26 号 元 素 , 基 态 Fe 原 子 的 电 子 排 布 式 应 为 IS22s22p'3s23p'3d'4s2 , 而 非
第 7页/共 24页( 是 Fe" 的排布),C 错误;
D. Y 是 N, 第二周期元素, 同周期主族元素中, 核电荷数增大, 第—电离能增大, 但 N 的电子排布式
为IS'2s'2p' , 2p能级有 3 个电子 ,形成半充满稳定结构, 因此 N 的第—电离能大于 O ,则只有 F 元素
的第—电离能大于 N 的第—电离能 ,D 正确;
故答案选 C。
10. 工业制硫酸的步骤中接触氧化的反应为 。在有 、
无催化剂条件下S0: 氧化成S0, 过程中能量的变化如图所示 。450℃ 、 催化时 ,该反应机理为:反
应
①: ;反应②: dH:
。
下列说法正确的是
A. 反应①的AS<0
B. 反应②的A H2>A H
C. 反应②为决速步且山H: < I , 故降温有利于加快总反应速率
D. 其他条件相同 ,增大起始OZ与 S0: 的投料比, 可提高S0: 的平衡转
化率【答案】 D
【解析】
【详解】A. 由图可知 ,反应①为吸热反应,450℃条件下反应能自发进行 ,说明反应ΔH—TΔS<0 ,则反
应的熵变ΔS 大于 0 ,A 错误;
B. 由盖斯定律可知, 反应①× 2+反应②=总反应 ,则反应ΔH=2ΔH +ΔH , 由图可知, 反应①为吸热反
1 2
应、反应②和总反应为放热反应 ,所以反应②的烩变小于总反应的烩变 ,B 错误;
C. 降低温度, 反应① 、反应② 、总反应的反应速率均减小 ,C 错误;
第 8页/共 24页D .其他条件相同 ,增大起始氧气与二氧化硫的投料比相当于增大氧气的浓度 ,平衡向正反应方向移动 ,
二氧化硫的平衡转化率增大 ,D 正确;
故选 D。
NH
11. 利用微生物脱盐燃料电池,可同时淡化盐水和处理氨氮废水(主要含 ),原理如图所示,下列说法
正确的是
A. 处理氨氮废水的过程实现了氮的固定
B. M 膜为阴离子交换膜
C. 负极的电极反应式为:
D. 外电路转移 ,脱盐室质量减少 58.5g
【答案】 C
【解析】
【分析】 由题意可知 ,该装置是原电池 ,据图可知右侧电极上 C H O 被氧化生成 CO ,所以右边为负
6 12 6 2
极,左边为正极 ,硝酸根被还原生成氮气。
【详解】 A. 氮的固定是指将空气中游离态的氮( 主要是 N ) 转化为化合态氮( 如氨 、硝酸盐等含氮
2
化合物) 的过程 ,题中处理氨氮废水最后转化为氮气, 不属于氮的固定 ,A 错误;
B. 脱盐室中 Na+ 向正极移动 ,Cl-向负极移动 。因此 M 需允许 Na+通过 ,应为阳离子交换膜 ,B 错误;
C 负极 C H O 被氧化生成 CO 电极反应式为: C,H, O-24e'+6H,0-6CO,个+24H' C 正确;
. 6 12 6 2, ,
NH
D. 外电路转移 1 mol e-时 ,脱盐室中 Na+和 ( 共 1mol) 向正极移动 、1molCl-向负极移动 ,脱盐室
质
量减少无法计算 ,D 错误;
故答案选 C。
12. Ln-C0: 新型二次电池以Z和多孔 pd 纳米片为两极材料,分别以 KOH 和 NacI 溶液为电解液,
HO 0H
工作原理如图所示 ,双极膜中的 解离成 和 。下列说法错误的是
第 9页/共 24页A. 放电时 ,a 极电势低于 b 极
B. 放电时, 负极区域 pH 减小
C. 充电时 ,双极膜中 移向 a 极, OH- 移向 b 极
D. 充电时 ,用铅蓄电池做电源 ,Y 极反应为: pb-2e+SO =(cid:1)pbs o,
【答案】 D
【解析】
【分析】 该装置既可作为原电池也可作为电解池, 作为原电池时 a 极为负极(Zn 失电子), 发生的反应
是 zH⃞n-2e-+40H-=zn(0H⃞(cid:1) ; b 极 为 正 极 ( 得 电 子 ) 发 生 的 反 应
,
是CO,H⃞+2e-+2H⃞(cid:1)=H COOH ;作为电解池时 a 极为阴极 ,b 极为阳极 ,据此分析:
【详解】 A. 放电时 ,a 极为负极 ,b 极为正极 ,原电池中负极电势低于正极, 故 a 电极势低于 b 极 ,
A 正确;
B 放电时 负极反应为
zH⃞n-2e"+40H-=zn(0H⃞(cid:1)
消耗
OH-
负极区域
OH-
浓度减小 pH 减
. , , , ,
小 B 正确;
,
C. 充电时 ,a 极为阴极 ,b 极为阳极; 向阴极(a 极)移动, 阴离子OH- 向阳极(b 极)移动 ,C 正
确;
D. 充电时 ,铅蓄电池做电源 ,b 极作为阳极与铅蓄电池的正极 Y( pbQ) 相连;铅蓄电池正极反应为:
pbo,+2e"+4H"+SO =(cid:1)pbs o,+2H, O 而 pb-2e+SO =(cid:1)pbs o,是铅蓄电池负极(Pb) 的放电反
,
应
,
D 错误;
故答案选 D。
sio Ft0;
13. 以铝土矿(主要成分为 ,含杂质 和 )为原料 ,制备有机合成中的重要还原剂铝氢化钠
( )的—种工业流程如图:
第 10页/共 24页已知: sio在 “ 碱溶” 时生成了n(si02): n(Na, o) >3 的 “ 硅酸钠” 沉淀 。下列说法错误的是
A. “ 碱溶” 时主要反应的离子方程式为:
B. “ 反应 Ⅰ ” 部分化学原理与泡沫灭火器的原理相同
C. “ 电解 Ⅰ ” 中可加入冰晶石(Na, AlF, )作助熔剂
D. “ 反应Ⅲ ” 的化学方程式为:
【答案】 B
【解析】
AI;0; sio
【分析】以铝土矿(主要成分为 ,含杂质 和 )为原料,制备有机合成中的重要还原剂铝氢
化钠( )的—种工业流程。“ 碱溶” 在过量 NaOH 溶液下将A1,0, 转化为NO[a1on1.] 、 sio 转
化为Nasi0; 通过过滤 1 得到的滤渣 1 为 Ft0; ;往滤液中加NaHCO;溶液 NO[A1on1.] 可与
, ,
NaHCO;反应生成Al(OH,沉淀和 ,电解 溶液阴极生成氢气和氢氧化钠,阳极生成氧
气和 NaHCO; ,氢氧化钠 、碳酸氢钠可返回至“ 碱溶” 、“ 反应 Ⅰ ” 阶段循环利用,“ 过滤 Ⅱ ” 得到的氢
氧化铝灼烧后生成氧化铝, 电解氧化铝生成金属铝 ,铝和氯气反应生成氯化铝 ,氯化铝和 NaH 反应可生
成
和氯化钠。
【详解】 A “ 碱溶” 时主要反应的离子方程式为A4,03+20H+3H:0=2Al1(OH), I A 正确;
. ,
B “ 反应 Ⅰ ” 是 与 NaHCO;反应生成Al(OH沉淀和Na, C0, 是[Al(OH),
. ,
I与HCO之间的中和反应, 而泡沫灭火器利用了 与 HCQ之间双水解, 故两者原理不同 ,B
错误;
C.“ 电解 I” 是电解氧化铝, 由于其熔点较高 ,加入冰晶石降低其熔点 ,C 正确;
D.“ 反应Ⅲ ” 是氯化铝和 NaH 反应可生成氯氢化钠和氯化钠, 方程式表示
为4NaH+Alcl,-Na Al H;+3Nacl D 正确;
,
故选 B。
第 11页/共 24页c0: C(s)+co2lg)=2col g)
14. —定量的 与足量的碳在恒压密闭容器中发生反应: 。平衡时,体系
中
气体体积分数与温度的关系如下图所示 。下列说法错误的是
A. 550℃平衡后 ,若充入惰性气体 ,则 、 vg 均减小, 平衡向右移动
B. 650℃ , C0: 的平衡转化率为 25.0%
C. T℃平衡后 ,若充入等物质的量的C0: 和CO , 平衡不移动
D. 925℃平衡时 ,用平衡分压表示的化学平衡常数k,=24.0pg
【答案】 D
【解析】
【详解】 A. 恒压充入惰性气体, 容器容积变大, 浓度降低 ,则 VE 、 vg均减小, 平衡向气体增大的
方向移动, 即平衡正向移动 ,A 项正确;
B. 设 CO 为 1mol ,该条件下转化率为 x ,根据已知信息建立三段式
2
, 650℃时 CO 和 CO 的体积分数分别为 60%和40%, 即
2
得到x=0.25 ,则 co, 的平衡转化率为 25.0% ,B 项正确;
C. 由图可知 ,T℃时, 反应达平衡后 CO 和 CO 的体积分数都为 50%, 故充入等物质的量的这两种气
2
体,平衡不移动 ,C 项正确;
D. 925℃ 时 ,CO 的体积分数为 96%, 故 =23.04p ,D 项错
总
误;答案选 D。
第 12页/共 24页15. 室温下, 向含足量 AgBr 固体的悬浊液中 ,滴加饱和 Nas203 溶液 ,发生如下反应: Ag'+S:
O;=
l gc(s:0;) l gc(M)
随 增大 平衡体系中
、 , ,
和l gc(N) 的变化如下图所示[M 代表Ag' 或 ,N 代表 或 ] 。
下列说法错误的是
A. AgBr 的 K,=10-""
l gc(s,0;
B. 表示 随 的变化
c(s:0;)-IX10"mol'L
C . 时 ,
D. 的平衡常数的值为
1os
【答案】 C
【解析】
【分析】 在 AgBr 固体的悬浊液中, 溴离子浓度和银离子浓度相等 ,根据l gc(M) [M 代表Ag' 或 Br- ]
,a
A'+S:0;=
点 M 离子浓度相等, 向饱和溶液中滴加硫代硫酸钠溶液时 ,根据反应 、
l,
可知溶液中银离子浓度减小 、溴离子浓度增大 ,得到曲线
表示溴离子浓度与硫代硫酸根离子浓度变化的关系; 曲线 表示银离子浓度与硫代硫酸根离子浓度变化
的关
第 13页/共 24页系;再根据l gc(N) [N 代表 或 ],溴化银与硫代硫酸钠溶液开始反
[Ag(S:0,]
应时, 溴化银主要转化为 ,然后才继续转化为 ,则有溶
液中
. l gc(s:0;
小于 ,则直线 表示 随 变化的关
系、
直线 表示 随l gc(s:0;) 变化的关系;据此分析解答。
l gc(s:0;)=-4.6 c(s,0;)-10"mol1'
【详解】A 由图可知 溶液中 即 时 溶液中溴离子和
. , , ,
银离子浓度分别为 和 ,则溴化银的溶度积常数
K,IA gbr)=c(Ag")o(Br)-10-""x10"=10-""
A 正确;
,
B. 根据分析, 直线 表示 随l gc(s:0;) 变化的关系 ,B 正确;
c(s:0;)-IX10"mol'L l gc(Br) > >
C . 根据图中曲线可知 , 当 时 , 有
, 可得到 > , 因c(Ag') 相同 ,则有
, 最后得到浓度大小关系为:
, C 错误;
c(s,0;)-10"mol1'
D 当溶液中 时 此时有 同时根据 c 点有
. , ,
, 得到此时溶液中的 ,最后得到
反应 的平衡常数为
·
第 14页/共 24页, D 正确;
故答案为:C。
第Ⅱ卷(非选择题 共 55 分)
16. 回答下列问题:
(1) Na202 的电子式为_______。
(2) 基态 N 原子的价层电子轨道表示式为_______。
(3) 基态Ga原子的核外电子共有_______种空间运动状态。
(4) 现代化学常用_______法测定分子的相对分子质量, 红外光谱可用于分析分子中含有何种化学键或
_______。
(5) CH, 分子的 VSEPR 模型名称为_______, H-C-H 的键角为_______。
(6) 第四周期基态原子未成对电子数为 1 的元素有_______种。
(7)P 原子的第—电离能大于 S 原子的第—电离能的原因:_______。
【答案】(1) (2)
(3) 16 (4) ①. 质谱 ②. 官能团
(5) ①. 正四面体形 ②. 109"28'
(6) 5 ( 7)P 原子的价层电子排布 3p 轨道是半充满的, 比较稳定, 电离能较高
【解析】
【小问 1 详解】
Na2 O
2
是离子化合物, 由 Na+和过氧根离子( )构成, 中两个 O 原子通过共用 1 对电子形成过氧键,
每个 O 原子剩余的电子满足 8 电子稳定结构, 电子式如图所示:
。 【小问 2 详解】
基态 N 原子的价层电子为 2s22p3 ,2s 轨道容纳 2 个自旋相反的电子 ,2P 轨道为半充满状态(3 个电子分占
不
同轨道, 自旋方向相同) ,轨道表示式如图所示: 。
【小问 3 详解】
第 15页/共 24页·
电子的空间运动状态由轨道决定(每个轨道对应 1 种状态) 。基态 Ga(原子序数 31)的电子排布
为1s22s22p63s23p63d104s24p1 ,轨道数: 1s(1)+2s(1)+2p(3)+3s(1)+3p(3)+3d(5)+4s(1)+4p(1)=16。
【小问 4 详解】
质谱法可通过测定分子离子峰的质荷比得到分子的相对分子质量;红外光谱能反映分子中化学键的振动频
率 ,从而分析分子含有的化学键或官能团。
【小问 5 详解】
CH 中心 C 原子的价层电子对数为 4(无孤电子对) ,VSEPR 模型为正四面体, 正四面体构型中 C-H 的键
4
角为 。
【小问 6 详解】
第四周期(K-Kr)中, 未成对电子数为 1 的元素有:K(4s1) 、Sc(3d14s2) 、Cu(3d104s1) 、Ga(4s24p1) 、
Br(4s24p5),共 5 种。
【小问 7 详解】
基态 P 原子的价电子排布为 3s23p3(3p 轨道半充满 ,处于稳定结构) ,基态 S 原子的价电子排布为 3s23p4 ,
故P 的第—电离能大于 S。
17. 四钼酸铵[(NH,), MO, O,·2H: O]的用途非常广泛,—种以钼精矿(主要含MOS: ,还含有CU 、Fe
sio
的化合物及 等)为原料制备四钼酸铵工艺流程如下图所示。
(1)“ 焙烧” 时 MOS: 反应的化学方程式为_______。
(2)“ 浸出” 时 MOO转化为MOO; ,“ 浸渣” 可以制备 溶液, 溶液经过“ 系列操作”
: _______ 、_______ 、过滤 、洗涤 、干燥 ,得到绿矾[Fe so,·7H2O]晶体。
(3)“ 净化” 时,“ 浸出液” 中残留的cu2* 、 Fe2* 转化为沉淀除去 。为了使cu2* 、 完全沉淀(残余
离子浓度小于 ) ,应控制溶液的 pH 不小于_______ 。已知:①研究表明 ,该 “ 浸出液” 中
c(s") l gc(s')-PH-15.1 k,(cus)=1x10" K,(Fes)=1x10-""
与 pH 的关系为: ②
, 。
(4)“ 沉淀” 时生成四钼酸铵沉淀的离子方程式为_______。
第 16页/共 24页(5) 该流程中产生的工业废气可以回收利用, 实验原理如图 。装置b 中阴极的电极反应式为_______。
(6) 四钼酸铵“ 热分解” 可以制备 。某些层状结构的 , 其结构与S0; 相似 ,此时MO 原
子的杂化类型为_______杂化。
(7) 工业上, 还可以在碱性环境下用 Na cIO 溶液和MOS: 反应制备钼酸盐, 同时生成副产品硫酸盐 ,
补充该反应的离子方程式:_______。
_______ _______ _______ _______ _______ _______ _______
【答案】(1)
(2) ①. 蒸发浓缩 ②. 冷却结晶
(3)2 9 (4)
(5) CO,+2e+2H'=H COOH
(6) sp2
(7) MOS,+ 9CI0'+ 60H'= MOO+2SO+9CI+ 3HO
【解析】
【分析】 钼精矿( 主要含 MoS , 还有 Cu 、Fe 的化合物及 SiO 等) 通入氧气焙烧主要得到 MoO 和气体
2 2 3
SO 铁和铜的氧化物, SiO ;浸出时 MoO 转化为 Moof ,浸出液含 Moof 和少量 Cu2+ 、Fe2+ ,加
2, 2 3
(NH ) S 净化 ,Cu2+ 、Fe2+转化 CuS 、FeS 沉淀, 滤渣为 CuS 、FeS, 滤液主要含 Moof , 滤液中加
4 2
NH
4
NO
3
、HNO
3
进行沉淀得到(NH
4
)
2
Mo4O
13
•2H
2
O;浸渣中的铁的氧化物先转化为硫酸亚铁 ,最终制得硫酸
亚铁晶体 ,据此解答。
【小问 1 详解】
第 17页/共 24页焙烧产生的气体为二氧化硫 ,所以该步骤化学方程式为 ;
【小问 2 详解】
从 FeSO 溶液到 FeSO •7H O 晶体的“ 系列操作” 为蒸发浓缩 、冷却结晶 、过滤 、洗涤 、干
4 4 2
燥; 【小问 3 详解】
K
sp
越小的越先沉淀 ,则 Cu2+先生成沉淀;要使 Cu2+浓度小于 1.0×10-5mol/L ,则 S2-浓度大于
, 要使 Fe2+浓度小于 1.0×10-5mol/L ,则 S2-浓度大于
, 综述 :c(S2-) 10-12.2 mol/L, 当 c(S2-)=10-12.2 mol/L 时 ,lg
(10-12.2)=pH 15.1 ,pH=15.1-12.2=2.9, 综上所述, 为了使溶液中的杂质离子浓度小于 1.0×10-5mol/L ,应
控制溶液的 pH 不小于2.9;
【小问 4 详解】
沉淀步骤中, 向含滤液中加 NH
4
NO
3
、HNO
3
“ 沉淀” 时生成(NH
4
)
2
Mo4O
13
•2H
2
O 的离子方程式为
;
【小问 5 详解】
NaHCO 溶液能和 SO 反应, 而不与 CO 反应, 故装置 a 中溶液的作用是吸收废气中的 SO , 并且转化
3 2 2 2
为Na2SO
3
进入电解池, 装置b 电解过程的阴极的 CO
2
得到电子生成 HCOOH, 电极反应式为
CO,+2e+2H'=H COOH ;
【小问 6 详解】
某些层状结构的 MoO 其结构与S0; 相似, SO 中 S 的杂化方式为 sp2 杂化, 故 MO 原子的杂化类型为
3 3
sp2杂化;
【小问 7 详解】
根据得失电子守恒元素守恒及电荷守恒可确定离子方程式为
。
【点睛】
cr cr
18. 三价铬 (Ⅲ)是人体必需微量元素, 六价铬 (Ⅵ)则是—类强致癌
cr cr
物。 (1) 纳米铁可将废水中的 (Ⅵ)还原为 (Ⅲ)。
cr
①含 (Ⅵ)物种的浓度随 pH 的变化如图所示。
第 18页/共 24页H;cro
的两级电离常数 的比值为_______(用含 M 、N 的式子表示, 下同); 当
时, 溶液PH= _______。
②已知: 的 k,=6.3x10-" , PH=8 的废水中,纳米铁除去 cr (Ⅵ)的离子方程式为_______ 。
cr
实验发现 ,在纳米铁中添加少量铜粉, 去除水体中 (Ⅵ)的效率比纯纳米铁更高, 其原因是_______。
(2) 溶液中存在多个平衡, 以下问题仅考虑如下平衡:
cr,0;(aq)+H,0(1)=2H cro;(aq)
( ⅰ ) (25℃)
H cro;(aq)=cro(aq)+H'(aq) K,=3.3x10-'
(ⅱ) (25℃)
K=
①25℃ , 反应 的平衡常数 _______(结果保留 2 位
有效数字)。
②取适量k2cr zo, 固体溶于水, 配成0.10mol/LK2cr zo,溶液(25℃), 下列有关说法正确的有
_______。
A. 加入少量0.10mo lIL 硫酸, 溶液的 pH 减小
B. 加入少量水稀释, 溶液中离子总数不变
C. 加入少量NaoH 溶液, 反应( ⅰ )的平衡逆向移动
k:;c: o, c'(H cro;) c(cr,0;
D 加入少量 固体 25℃重新平衡时 与 比值保持不变
. , ,
③25℃时, 0.10mol/LK2cr zo,溶液中 随 pH 的变化关系如图。
第 19页/共 24页当溶液PH =9.0 时 设cro H cro7 与 的平衡浓度分别为 x mo lIL zmol
, 、 、 、
lL 则 x 、y 、z 之间的关系式为_______=0.10 ; PH=9,0 时溶液中H cro7 的平衡浓度为_______
,
mol/L (结果保留 2 位有效数字)。
【答案】(1) ① . ② . ③ . cro +(cid:1)Fe+4H, O-cr(OH),+Fe(OH),+2OH
④ .加入铜粉形成了原电池 ,加快了反应速率
ssr o"
(2) ①. ②. AD ③. ④.
【解析】
【小问 1 详解】
①根据图示 ,pH = N 时 ,c(H CrO ) = c(H cro7 ) 。根据 H CrO 的 K 的表达式:
2 4 2 4 a1
H cro7 cro t.
, pH = M 时,c( ) = c( ),根据 H CrO 的 的
2 4
s.
表达式: , 因此, ;根据 和 的关
系:
cro
, 当 c(H 2 CrO 4 ) = c( )时:
, 因此:
;
cro
②在 pH = 8 时 ,c(OH-)= ,溶液中主要存在 ,Fe 作为还原剂 ,将
cro
还原为 Cr3+, 自身最终被氧化为 Fe3+, 由图可知 ,c(Cr3+)>0.15mol/L ,则
Q
c
=c(Cr3+)c3(OH-)>cr10H), 的
K,=6.3X10-" Cr3+和 Fe3+会分别转化为cr(OH);沉淀和Fe(OH)S沉淀 该反应中Fe 元素由 0 价上
, ,
·
升 第 20页/共 24页到+3 价 ,Cr 元素由+6 价下降到+3 价 ,根据得失电子守恒和原子守恒配平离子方程式为:
cro +(cid:1)Fe+4H, O-cr(OH),+Fe(OH),+2OH 在纳米铁中加入少量铜粉后 Fe 和 Cu 可以形成原电
, ,
池 原电池效应会显著加快电子转移速率 ,从而提高了去除水体中 Cr(VI)的效率。
,
【小问 2 详解】
①由盖斯定律可知, 反应(i) + 2 反应(ii)得到 ,则该
反应的平衡常数
k=k, x(k,)= 3.0x10"x(3.3x10-")'x3.3x10-8
;
②A .加入硫酸后, c(H") 增大 ,根据勒夏特列原理 ,反应(i)和 (ii)均会左移,但 增加的量远大
于平衡移动减少的量, 因此 c(H") 仍然增大, 溶液的PH 会减小 ,A 正确;
B.稀释溶液,根据勒夏特列原理 ,平衡会向粒子数增多 方向移动 ,反应(i)和(ii)均会右移 ,溶液中离子
总数增大 ,B 错误;
C. 加入 后, 溶液中 减小, 反应 (ii) 右移, 减小, 导致反应 (i) 右移 ,C
错误;
D. 只与温度有关 ,加入 后, 不变 ,D 正
确;故选AD;
③根据 Cr 元素守恒有 , 即 。由图可知, 当 PH=9,0
时, , 则c(cr zo$)即 z 可忽略不计 ,物料守恒可近似为 。根据
, 可得 。联立 和 ,解得
。
19. 六氯化钨(WCl )可用作有机合成催化剂,易潮解和升华。实验室中,先将三氧化钨(WO )用 H 还原为金
6 3 2
属钨(W), 再制备 WCl , 装置如图所示(夹持装置略)。
6
第 21页/共 24页回答下列问题:
(1) 将 WO 用 H 还原为 W ,该金属冶炼方法属于_______法。
3 2
(2) 实验操作如下, 选填操作序号:_______。
检查装置气密性→加入 WO →通 N —段时间→加热管式电炉, 改通 H —段时间
3 2 2
→_______→_______→ _______→再次通 N —段时间→_______(不可重复选择)。
2
①以 E 替换D;②停止通 H ;③冷却;④加热管式电炉至 1000℃ , 通 Cl , 同时将电热丝温度保持在
2 2
350℃
(3) 实验室用 MnO 制备 Cl 化学方程式为_______ 。A 中盛放的试剂的名称为_______ ,C 中冷却水
2 2
从_______(选填“ a” 或 “ b” )口通入 ,E 中 U 形管中碱石灰的作用是_______ 、_______。
(4) 测定 WCl 产品纯度的实验如下:
6
①称量 ag 样品(不考虑空气中水蒸气的干扰) ,将 WCl
6
转化为可溶的 Na2WO
4
, 通过离子交换柱发生反应:
。
②交换结束后, 向所得含IO;的溶液中加入适量酸化的 KI 溶液 ,发生反应: IO;+5I'+6H'=3I,+3H,O
。
③充分反应后, 取 体积的溶液 ,用 c mol∙L-1 的 Na2S
2
O
3
标准溶液滴定至溶液呈浅黄色 ,加几滴淀粉溶
液后继续滴定 ,发生反应: , 滴定达终点时消耗 Na2S
2
O
3
标准溶液bmL。
滴定实验达终点的现象是_______;样品中 WCl
6
(摩尔质量为 397g∙mol-1)的质量分数为_______%;已知:当
I
2
浓度很高时 ,与淀粉形成的蓝色复合物非常稳定 ,难以分解。若先加淀粉溶液 ,再用 Na2S
2
O
3
标准溶液
滴定至终点 ,则样品中 WCl 质量分数的测定值将_______(填“ 偏高” “ 偏低” 或 “ 不变” )。
6
【答案】(1)热还原 (2)③②①④
(3) ①. Mno2+4Hcl(浓) ②. 浓硫酸 ③. b ④. 吸收多余氯气,
防止污染空气 ⑤. 防止空气中的水蒸气进入 F
(4) ①. 滴入最后半滴Na2S
2
O
3
标准溶液,溶液由蓝色变无色,且半分钟内不恢复 ②.
·
③. 第 22页/共 24页偏高
【解析】
【分析】将三氧化钨(WO )用 H 还原为金属钨(W),为防止空气与 H 混合时发生爆炸,需先通 N 排尽装
3 2 2 2
置内的空气 ,然后用管式炉加热, 通 H 将 WO 还原为W 后, 改用 Cl 与 W 反应 ,此时需将 D 装置换
2 3 2
成 E装置,但在这个操作前,需将装置冷却,并先通 N 排尽装置内的 H ,然后再通入 Cl 。加热管式电炉至
2 2 2
1000 ℃ , 通 Cl , 同时将电热丝温度保持在 350℃ , 从而制得 WCl 。
2 6
【小问 1 详解】
将 WO 用 H 还原为 W ,是在加热条件下 ,用还原剂(H )将 WO 还原为 W ,该金属冶炼方法属于热还原
3 2 2 3
法。 【小问 2 详解】
由分析可知, 通入 H 前, 需使用 H 排尽装置内的空气, 防止 H 、空气混合发生爆炸;通入 Cl 前, 需
2 2 2 2
使用 N 排尽装置内的 H , 防止 Cl 、H 混合发生爆炸 。所以实验操作顺序为:检查装置气密性→加入
2 2 2 2
WO →通 N —段时间→加热管式电炉, 改通 H —段时间→③冷却→②停止通 H →①以 E 替换 D→再次
3 2 2 2
通 N —段时间→④加热管式电炉至 1000℃ , 通 Cl , 同时将电热丝温度保持在350℃ 。故选③②①④。
2 2
【小问 3 详解】
实验室用 MnO 与浓盐酸反应制备 Cl , 同时生成 MnCl 和水 ,依据得失电子守恒 、原子守恒 ,可得出发生
2 2 2
反应的化学方程式为Mno2+4Hcl(浓) 。A 装置用于干燥 Cl ,盛放的试剂的名
2
称为:浓硫酸 ,C 中冷却水流向下进上出 ,即从 b 口通入 ,E 中 U 形管中碱石灰既处理 Cl 又防止空气中
2
水蒸气的进入 ,则作用是: 吸收多余氯气, 防止污染空气 、防止空气中的水蒸气进入 F。
【小问 4 详解】
(4) 测定 WCl 产品纯度的实验如下:
6
滴定前,I
2
使淀粉溶液变蓝色,则滴定实验达终点的现象是:滴入最后半滴 Na2S
2
O
3
标准溶液 ,溶液由蓝
色变无色, 且半分钟内不恢复 。由反应可建立关系式:
WCl
6
——Na2WO
4
——2NaIO
3
——6I
2
——12Na2S
2
O
3
,ag 样品配成的溶液, 共需要消耗 Na2S
2
O
3
的物质的
量为 b×10-3L×c mol∙L-1 ×5=5bc×10-3mol ,n mol,
样品中 WCl
6
(摩尔质量为 397g∙mol-1)的质量分数为 = %。已
知: 当 I
2
浓度很高时, 与淀粉形成的蓝色复合物非常稳定 ,难以分解 。若先加淀粉溶液, 再用 Na2S
2
O
3
标
准溶液滴定至终点 ,则消耗 Na2S
2
O
3
标准溶液的体积偏大 ,计算所得样品中 WCl
6
质量分数的测定值将偏
高。
第 23页/共 24页【点睛】 当 I 浓度很高时 ,与淀粉形成的蓝色复合物非常稳定 ,难以分解 ,当加入刚好完全反应的
2
Na2S
2
O
3
标准溶液时,溶液的蓝色可能并未褪去,于是继续滴加 Na2S
2
O
3
标准溶液,从而使所用 Na2S
2
O
3
标
准溶液体积偏大。
第 24页/共 24页