文档内容
哈尔滨市第九中学校 2024-2025 学年度上学期
12 月考试高二学年化学学科试卷
(考试时间:75分钟 满分:100分)
可能用到的相对原子质量:H-1,C-12,N-14,O-16,Na-23,P-31,Cl-35.5
第I卷(共45分)
一、选择题:(每小题仅有一个选项符合题意)
1. 化学与生活密切相关。下列有关题干说法错误的是
A. 将 与 混合加热制得无水
B. 与 两种盐溶液可用作泡沫灭火剂的主要原料
C. 用 溶液处理锅炉水垢,使 转化为溶解度更小且疏松、易溶于酸的
D. 除废水中 、 时,常用 等,是因为生成的 、 极难溶,使废水中 、
浓度降的很低
2. 下列电离或离子方程式书写正确的是
A. 溶液与 溶液混合:
B. 熔融 的电离:
C. 的水解:
D. 工业废水中的 用 去除:
3. 室温下,在实验室中用0.1mol/LHCl滴定0.1mol/LNaOH溶液,中和后加水至20mL。若滴定终点判断有
误差:①多加半滴HCl;②少加了半滴HCl(已知1mL为25滴),则①和②c水(H+)之比为:
A. B. 4 C. 1 D. 10
4. 在实验室中可以利用 的水解反应制取 ,下列措施不能获得更多 的是
A. 开始时要将 缓慢加入大量水中 B. 反应后期可以加入少量氨水
C. 适当加热 D. 延长达平衡后的反应时间
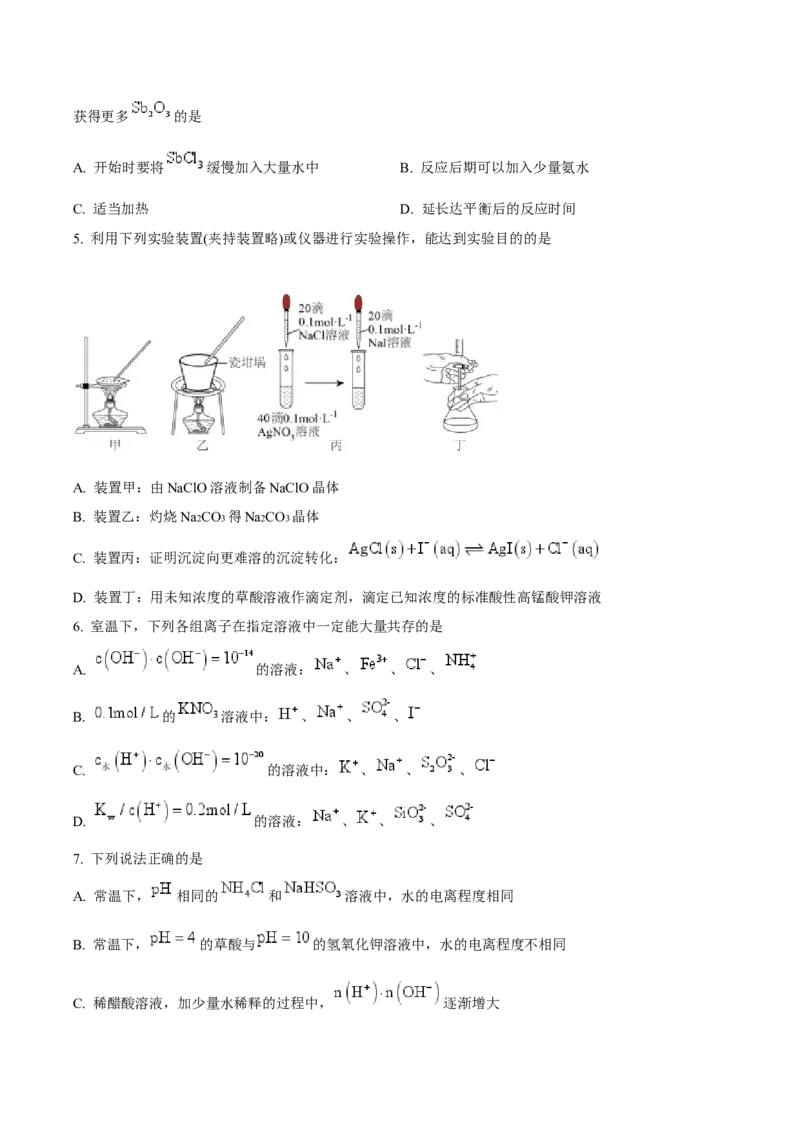
5. 利用下列实验装置(夹持装置略)或仪器进行实验操作,能达到实验目的的是
A. 装置甲:由NaClO溶液制备NaClO晶体
B. 装置乙:灼烧Na2CO3 得Na2CO3 晶体
C. 装置丙:证明沉淀向更难溶的沉淀转化:
D. 装置丁:用未知浓度的草酸溶液作滴定剂,滴定已知浓度的标准酸性高锰酸钾溶液
6. 室温下,下列各组离子在指定溶液中一定能大量共存的是
A. 的溶液: 、 、 、
B. 的 溶液中: 、 、 、
C. 的溶液中: 、 、 、
D. 的溶液: 、 、 、
7. 下列说法正确的是
A. 常温下, 相同的 和 溶液中,水的电离程度相同
B. 常温下, 的草酸与 的氢氧化钾溶液中,水的电离程度不相同
C. 稀醋酸溶液,加少量水稀释的过程中, 逐渐增大D. 醋酸钠溶液中加少量氟化钠, 减小
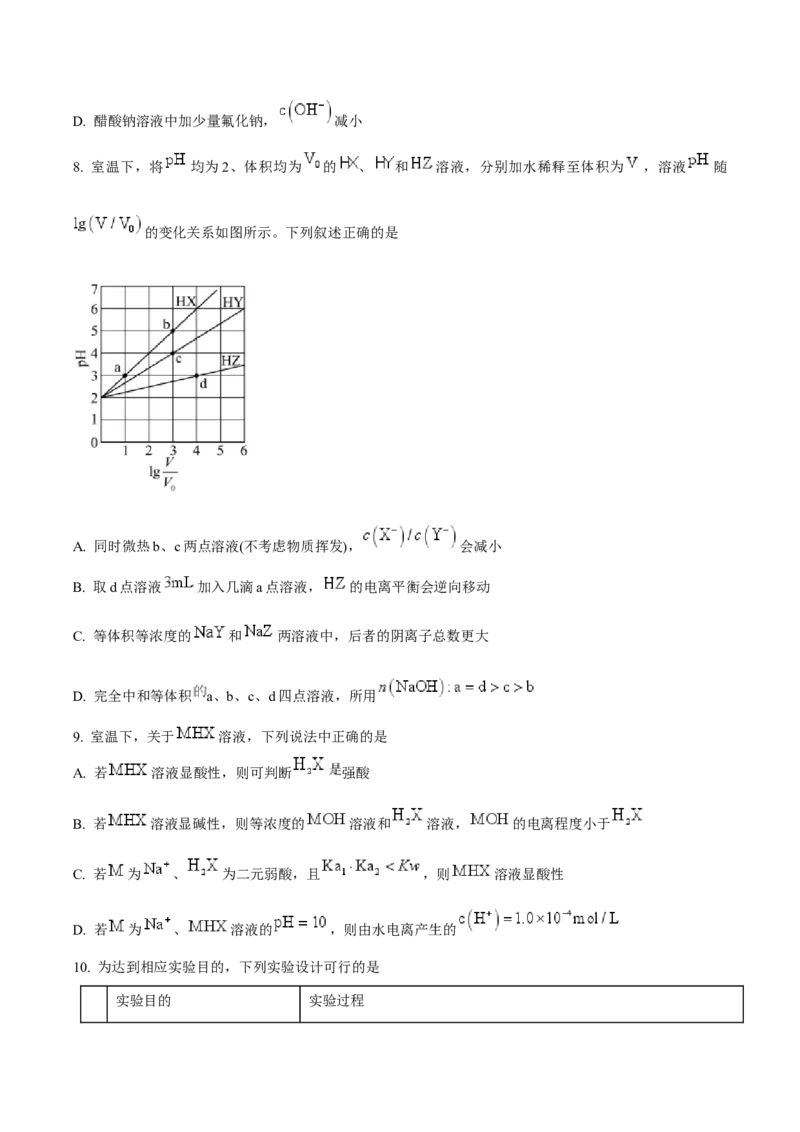
8. 室温下,将 均为2、体积均为 的 、 和 溶液,分别加水稀释至体积为 ,溶液 随
的变化关系如图所示。下列叙述正确的是
A. 同时微热b、c两点溶液(不考虑物质挥发), 会减小
B. 取d点溶液 加入几滴a点溶液, 的电离平衡会逆向移动
C. 等体积等浓度的 和 两溶液中,后者的阴离子总数更大
D. 完全中和等体积 a、b、c、d四点溶液,所用
9. 室温下,关于 溶液,下列说法中正确的是
A. 若 溶液显酸性,则可判断 强酸
B. 若 溶液显碱性,则等浓度的 溶液和 溶液, 的电离程度小于
C. 若 为 、 为二元弱酸,且 ,则 溶液显酸性
D. 若 为 、 溶液的 ,则由水电离产生的
10. 为达到相应实验目的,下列实验设计可行的是
实验目的 实验过程A 证明碳酸的酸性强于次氯酸 向碳酸钠溶液中滴入少量次氯酸溶液
验证镁离子与碳酸根可形成 已 知 MgCO3 的 Ksp=6.8×10-6 , 向 1L0.01mol/LMgCl2 溶 液 中 加
B
沉淀 1mL0.01mol/LNa2CO3 溶液,有沉淀析出
C
验证Na2HPO4 发生了水解反
向Na2HPO4 溶液中滴加AgNO3 溶液,出现黄色沉淀Ag3PO4
应
D
证明 Na2CO3 溶液中存在
向滴有酚酞的Na2CO3 溶液中加入少量BaCl2 固体,溶液红色变浅并
有白色沉淀生成
的水解平衡
A. A B. B C. C D. D
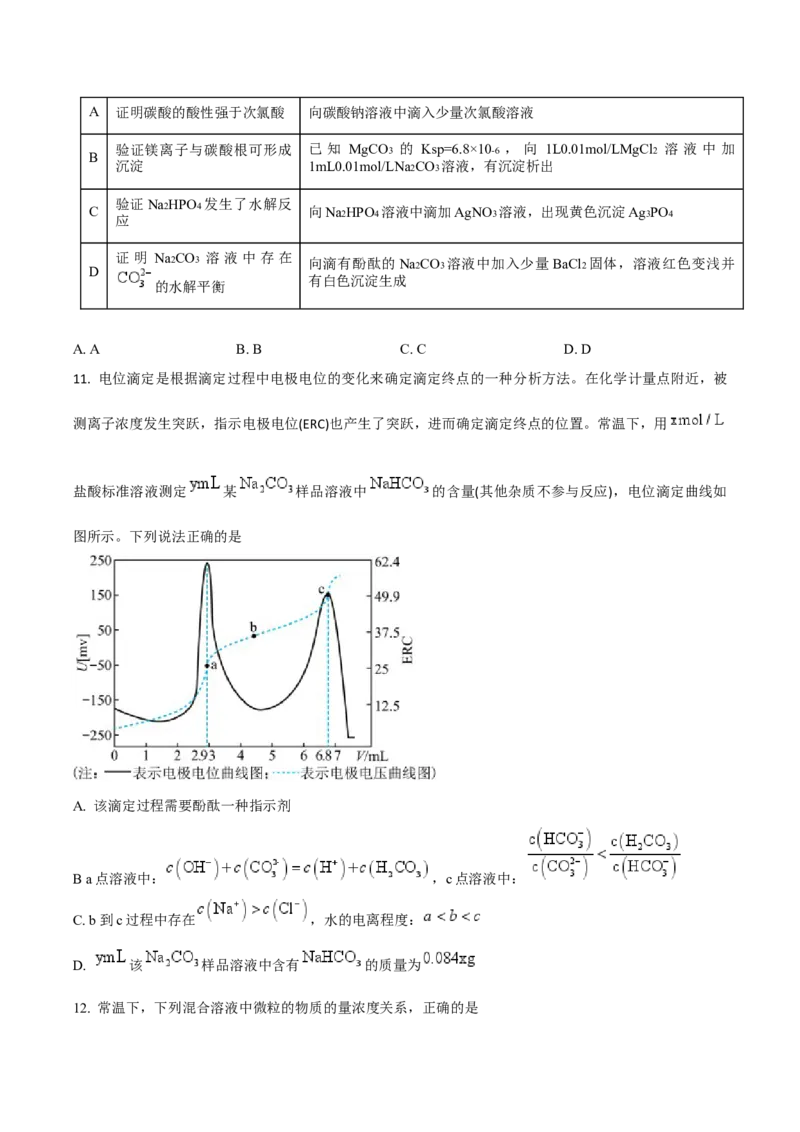
11. 电位滴定是根据滴定过程中电极电位的变化来确定滴定终点的一种分析方法。在化学计量点附近,被
测离子浓度发生突跃,指示电极电位(ERC)也产生了突跃,进而确定滴定终点的位置。常温下,用
盐酸标准溶液测定 某 样品溶液中 的含量(其他杂质不参与反应),电位滴定曲线如
图所示。下列说法正确的是
A. 该滴定过程需要酚酞一种指示剂
B a点溶液中: ,c点溶液中:
C. b到c过程中存在 ,水的电离程度:
D. 该 样品溶液中含有 的质量为
12. 常温下,下列混合溶液中微粒的物质的量浓度关系,正确的是A. 将pH=9的氨水溶液与pH=5的盐酸等体积混合:
B. 溶液与 溶液等体积混合:
C. 与 等体积混合呈碱性:
D. 向含有 的 溶液中,通入 气体,所得溶液中:
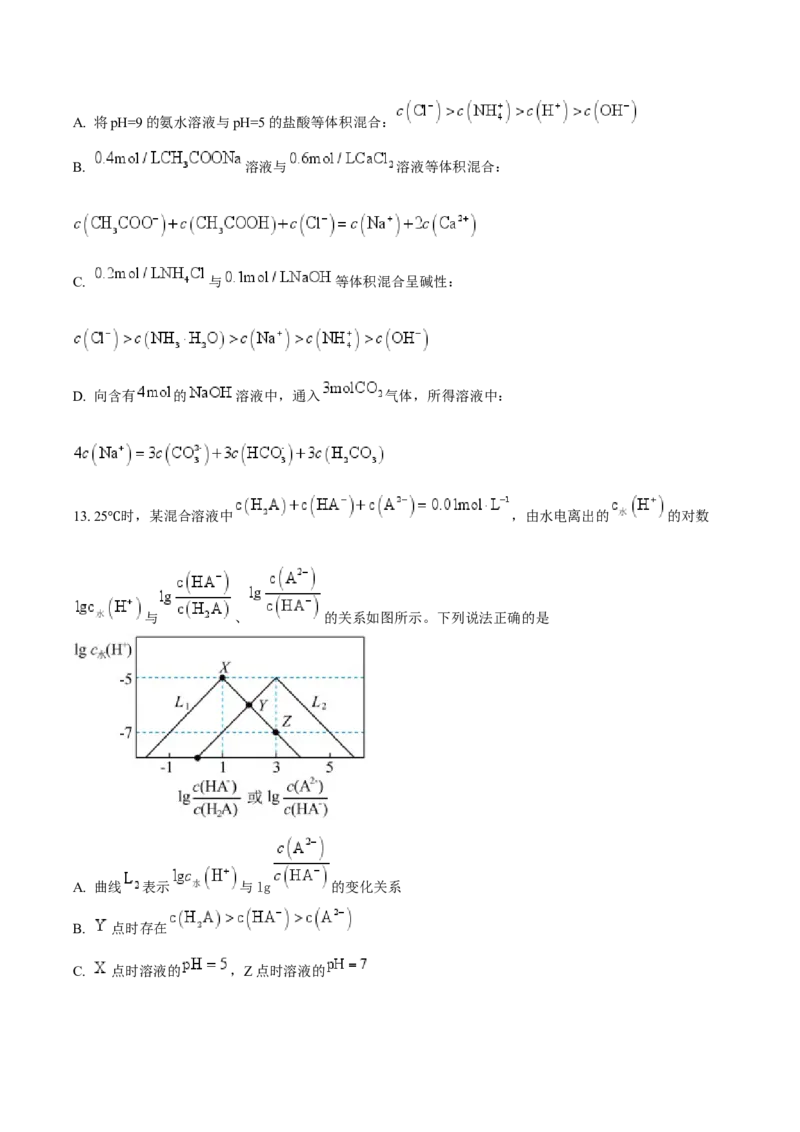
13. 25 时,某混合溶液中 ,由水电离出的 的对数
℃
与 、 的关系如图所示。下列说法正确的是
A. 曲线 表示 与lg 的变化关系
B. 点时存在
C. 点时溶液的 ,Z点时溶液的D. ,
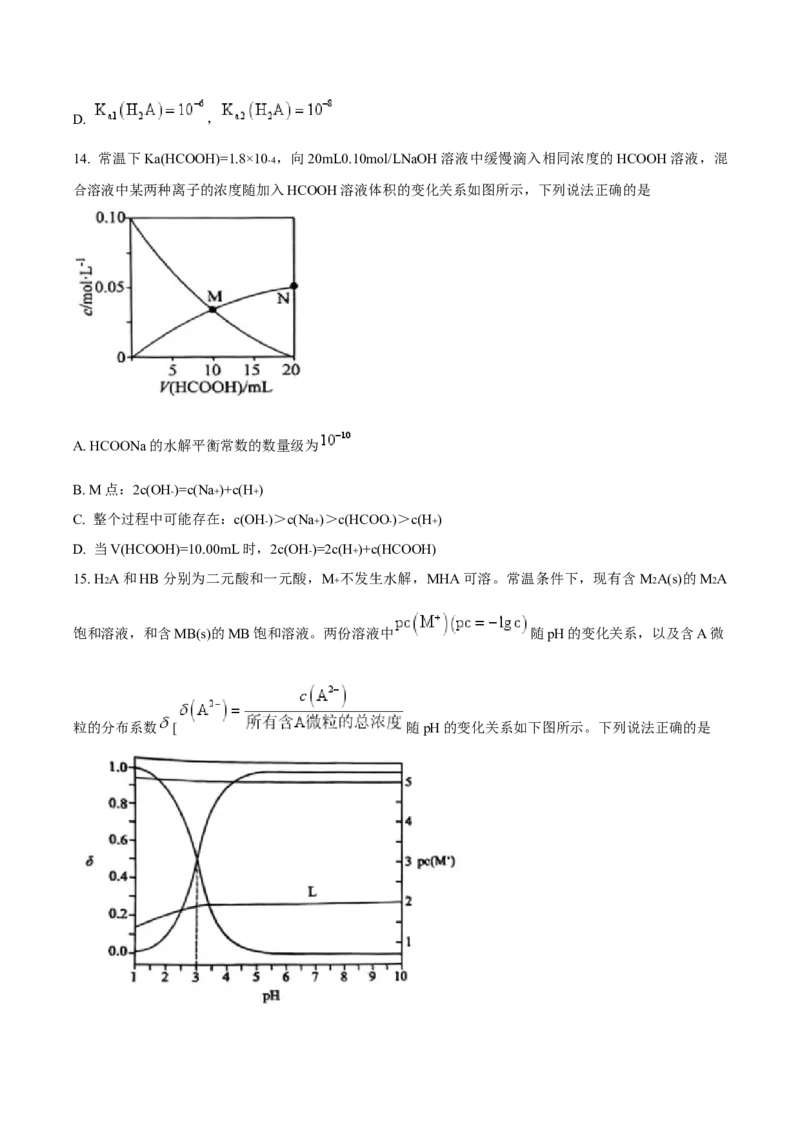
14. 常温下Ka(HCOOH)=1.8×10-4 ,向20mL0.10mol/LNaOH溶液中缓慢滴入相同浓度的HCOOH溶液,混
合溶液中某两种离子的浓度随加入HCOOH溶液体积的变化关系如图所示,下列说法正确的是
A. HCOONa的水解平衡常数的数量级为
B. M点:2c(OH-)=c(Na+)+c(H+)
C. 整个过程中可能存在:c(OH-)>c(Na+)>c(HCOO-)>c(H+)
D. 当V(HCOOH)=10.00mL时,2c(OH-)=2c(H+)+c(HCOOH)
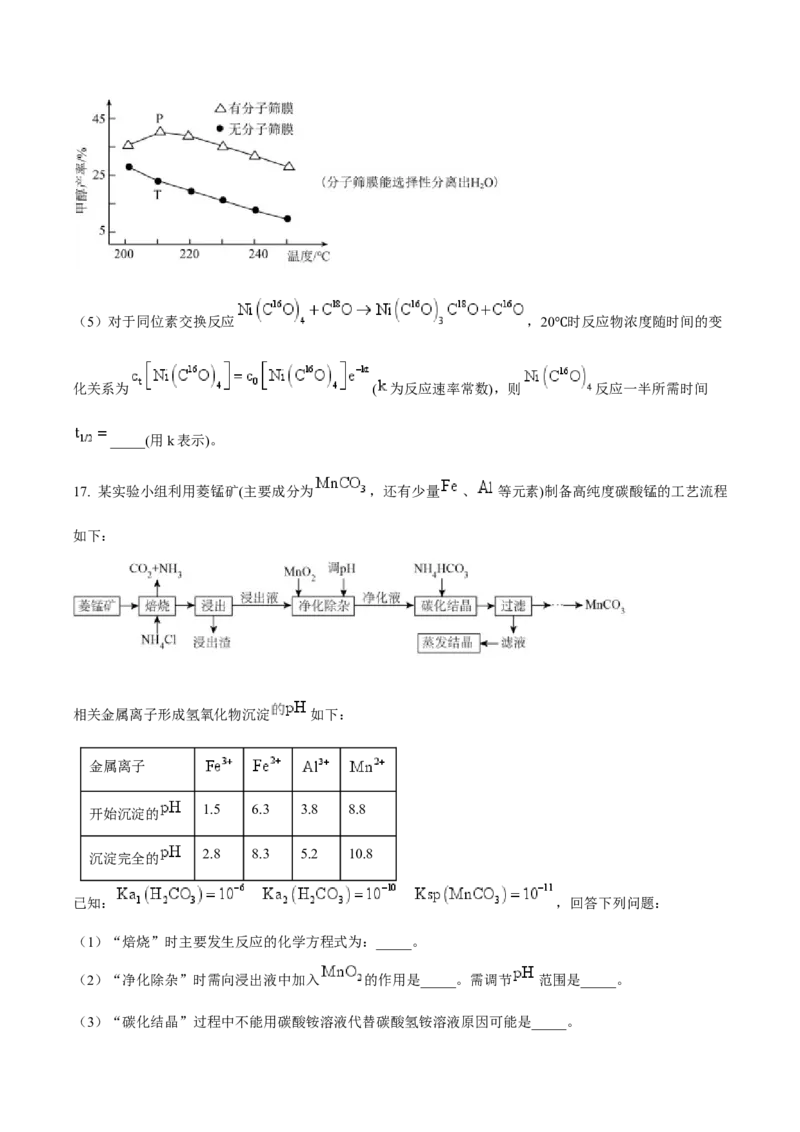
15. H2A和HB分别为二元酸和一元酸,M+ 不发生水解,MHA可溶。常温条件下,现有含M2A(s)的M2A
饱和溶液,和含MB(s)的MB饱和溶液。两份溶液中 随pH的变化关系,以及含A微
粒的分布系数 [ 随pH的变化关系如下图所示。下列说法正确的是A. L表示含MB(s)的MB饱和溶液中pc(M+)随pH变化的图像
B. MHA与少量HB反应的离子方程式为:HA-+H+=H2A
C. 反应 M2A(s)+2B-+H+ 2MB(s)+HA- 的平衡常数约为5×1016
D. pH=3时,M2A的饱和溶液中,存在c(H+)+c(M+)-3c(HA-)-c(OH-)>0
第II卷(共55分)
二、非选择题:
16. 工业上,以煤炭为原料,通入一定比例的空气和水蒸气,经过系列反应可以得到满足不同需求的原料
气。请回答:
(1)在101kPa时,1g氢气燃烧完全燃烧生成液态水时,放出热142.9kJ的热量,则表示H2 燃烧热的热化
学方程式为_____。
(2)水煤气反应: 。工业生产水煤气时,通常交
替通入合适量的空气和水蒸气与煤炭反应,其理由是_____。
(3)一氧化碳变换反应: 。
①一定温度下,反应后测得各组分的平衡压强(即组分的物质的量分数 总压): 、
、 和 ,则反应的平衡常数 的数值为_____。
②维持与题①相同的温度和总压,提高水蒸气的比例,使 的平衡转化率提高到90%,则原料气中水蒸
气和 的物质的量之比为_____。
③生产过程中,为了提高变换反应的速率,下列措施中合适的是_____。
A.通入一定量的氮气 B.选择合适的催化剂 C.适当提高反应物压强 D.反应温度愈高愈好
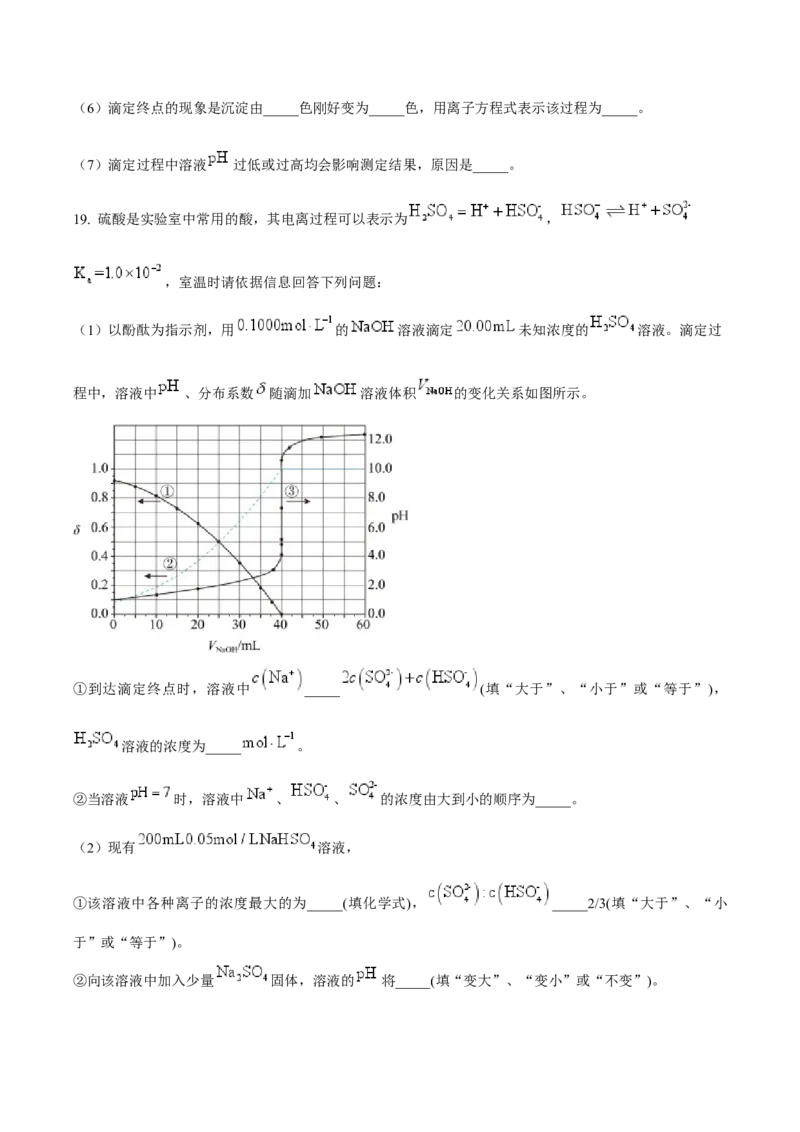
(4)用氢气和二氧化碳在催化剂作用下合成甲醇: 。恒压下,CO2和H2
的起始物质的量之比为1:3时,该反应甲醇的平衡产率随温度的变化如图,甲醇的产率P点高于T点的原
因为_____。(5)对于同位素交换反应 ,20 时反应物浓度随时间的变
℃
化关系为 ( 为反应速率常数),则 反应一半所需时间
_____(用k表示)。
17. 某实验小组利用菱锰矿(主要成分为 ,还有少量 、 等元素)制备高纯度碳酸锰的工艺流程
如下:
相关金属离子形成氢氧化物沉淀 如下:
金属离子
1.5 6.3 3.8 8.8
开始沉淀的
2.8 8.3 5.2 10.8
沉淀完全的
已知: ,回答下列问题:
(1)“焙烧”时主要发生反应的化学方程式为:_____。
(2)“净化除杂”时需向浸出液中加入 的作用是_____。需调节 范围是_____。
(3)“碳化结晶”过程中不能用碳酸铵溶液代替碳酸氢铵溶液原因可能是_____。结合所给数据计算说明该过程能够发生的可能性_____。
(4)“过滤”后,洗涤碳酸锰操作中需要用到的仪器有_____(填字母序号)。
A. 烧杯 B. 酒精灯 C. 玻璃棒 D. 分液漏斗E.漏斗
(5)整个流程中能够循环利用的固体物质是_____。
18. 已知:
难溶电解质 (白色) (白色) (红色)
溶度积常数
(一)通过佛尔哈德法可测定经过提纯后的产品中 的含量:
准确称取1.9100g样品在水解瓶中摇动至完全水解,将水解液配成 ,取 于锥形瓶中,加
的 溶液 ,再加少许硝基苯,用力振荡,使沉淀
被有机物覆盖。加入 作指示剂,用 标准溶液滴定过量的 至
终点 ,做平行实验,平均消耗 标准溶液 。
(1) 的水解方程式为_____。
(2)滴定终点的现象是溶液恰好变为_____色。
(3) 的纯度为_____%(保留到小数点后一位)。
(4)实验中,若不加硝基苯,测定 的纯度将_____(填“偏大”“偏小”或“无影响”)。
(二)现用标准 溶液滴定含 水样:
移取 含 水样于锥形瓶中,调 ,滴加指示剂 溶液。在不断摇动下,
用 的 标准溶液进行滴定。
(5)滴定时,理论上混合液中指示剂浓度不宜超过_____ 。(6)滴定终点的现象是沉淀由_____色刚好变为_____色,用离子方程式表示该过程为_____。
(7)滴定过程中溶液 过低或过高均会影响测定结果,原因是_____。
19. 硫酸是实验室中常用的酸,其电离过程可以表示为 ,
,室温时请依据信息回答下列问题:
(1)以酚酞为指示剂,用 的 溶液滴定 未知浓度的 溶液。滴定过
程中,溶液中 、分布系数 随滴加 溶液体积 的变化关系如图所示。
①到达滴定终点时,溶液中 _____ (填“大于”、“小于”或“等于”),
溶液的浓度为_____ 。
②当溶液 时,溶液中 、 、 的浓度由大到小的顺序为_____。
(2)现有 溶液,
①该溶液中各种离子的浓度最大的为_____(填化学式), _____2/3(填“大于”、“小
于”或“等于”)。
②向该溶液中加入少量 固体,溶液的 将_____(填“变大”、“变小”或“不变”)。③向该溶液中加入一定量 固体,使溶液的 , 的电离度为_____ (以分数表示)。
(3)已知 ,将足量 固体溶于水形成悬浊液,向体系中通入 气体调节
,该过程中可能发生 。
①计算过程的平衡常数 _____
②当体系的 时, _____ 。哈尔滨市第九中学校 2024-2025 学年度上学期
12 月考试高二学年化学学科试卷
(考试时间:75分钟 满分:100分)
可能用到的相对原子质量:H-1,C-12,N-14,O-16,Na-23,P-31,Cl-35.5
第I卷(共45分)
一、选择题:(每小题仅有一个选项符合题意)
1题答案
答案:B
2题答案
答案:C
3题答案
答案:C
4题答案
答案:D
5题答案
答案:D
6题答案
答案:D
7题答案答案:C
8题答案
答案:A
9题答案
答案:D
10题答案
答案:D
11题答案
答案:D
12题答案
答案:B
13题答案
答案:D
14题答案
答案:B
15题答案
答案:C
第II卷(共55分)
二、非选择题:
16题答案
答案:(1)H2(g)+ O2(g)=H2O(l) =-285.8kJ/mol
(2)维持体系在足够高的温度条件下能保持较快的速率反应,并提高煤炭的利用率
(3) . 9 . 9:5 . BC
(4)P点有①分子筛,②分离出水有③利于平衡正向移动,从而提高甲醇的产率
(5)
17题答案
答案:(1)
(2) . 将浸出液中Fe2+ 氧化成Fe3+ . 1.5≤pH<8.8
(3) ① . 碳酸铵溶液中氢氧根离子浓度②大于碳酸氢铵,易形成氢氧化锰沉淀 . 当溶液中
① ②pH≥8.8时,Mn2+ 开始生成沉淀 (4)ACE
(5)NH4Cl
18题答案
答案:(1)
(2)红 (3)80.4%
(4)偏小 (5)10-2mol/L
(6) . 白 . 红 .
① ② ③
(7)滴定过程中溶液 过低,指示剂会与氢离子反应生成重铬酸根,氧化氯离子,导致消耗的硝酸银偏
少, 过高氢氧根会与银离子反应,导致消耗的硝酸银偏多
19题答案
答案:(1) . 大于 . .
① ② ③
(2) . . 大于 . 增大 .
① ② ③ ④
(3) . .
① ②