文档内容
大庆实验中学
大庆实验中学实验一部 2023 级高二上学期 浓硫
B Fe片 浓硫酸 制取干燥的SO
酸 2
开学考试质量检测
浓盐
C MnO 饱和NaCl溶液 制取Cl 并除去HCl
化学学科试题 酸 2 2
稀硝
D Cu片 HO 制取NO并除去NO
2024.08.21—2024.08.22 酸 2 2
说明:1.请将答案填涂在答题卡的指定区域内。
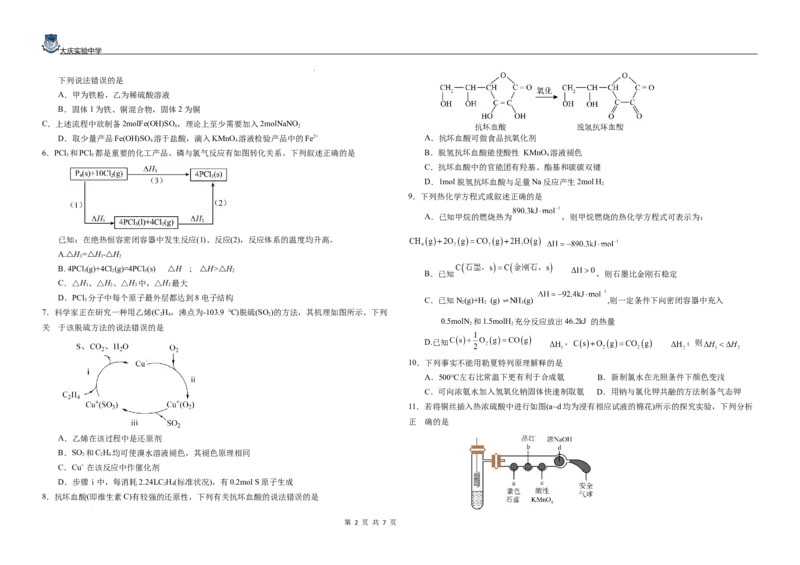
4.下列装置和操作不能达到实验目的的是
2. 满分100分,考试时间90分钟。
可能用到的相对原子质量 H:1 C:12 O:16 Na:23 Mn:55 I:127
一.选择题(本大题共20小题,1-15题每小题2分,16-20题每小题3分。共45分)
1.化学创造美好生活,下列说法正确的是
A.苯甲酸及其钠盐常用作食品防腐剂
B.天宫一号使用的太阳能电池板主要成分为二氧化硅
C.淀粉、纤维素和油脂均是天然有机高分子
D.氧化亚铁常用作油漆的红色颜料
2.设N 为阿伏加德罗常数的值。下列叙述正确的是
A
A.常温常压下,15g甲基(-CH )含有电子数为10N
3 A
B.标准状况下,11.2L氯仿(CHCl )中含有C-Cl键的数目为1.5N
3 A
C.常温常压下,28g乙烯和丙烯(C H)的混合气体中含有原子总数目为6N
3 6 A
D.1molCH 3 CH 2 OH分子中含有的共价键数目为7N A A.用图①装置检验纯碱中是否含有钾元素
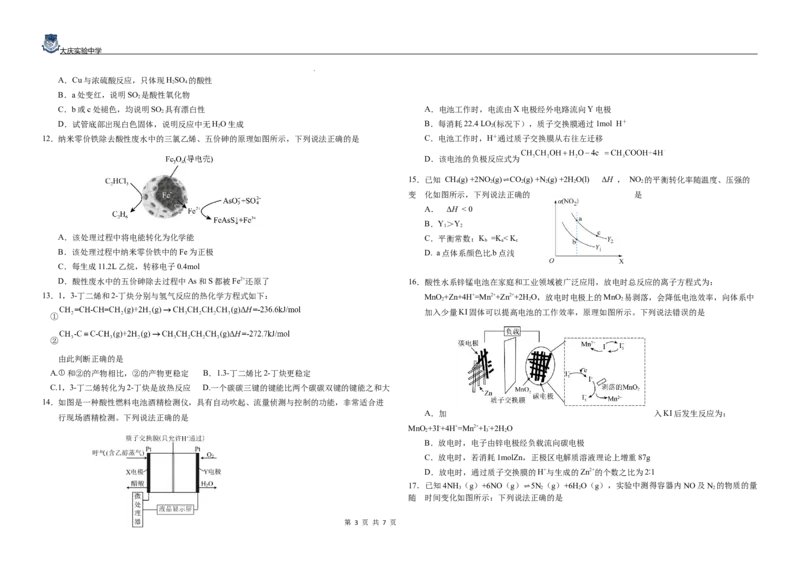
3.用如图所示装置完成相应实验(a、b、c中分别盛有试剂1、2、3),能达到实验目的的是 B.用图②装置测定锌和一定浓度稀硫酸的反应速率
C.用图③装置分离I 和NH Cl固体
2 4
D.用图④装置检验石蜡油分解产生的不饱和烃
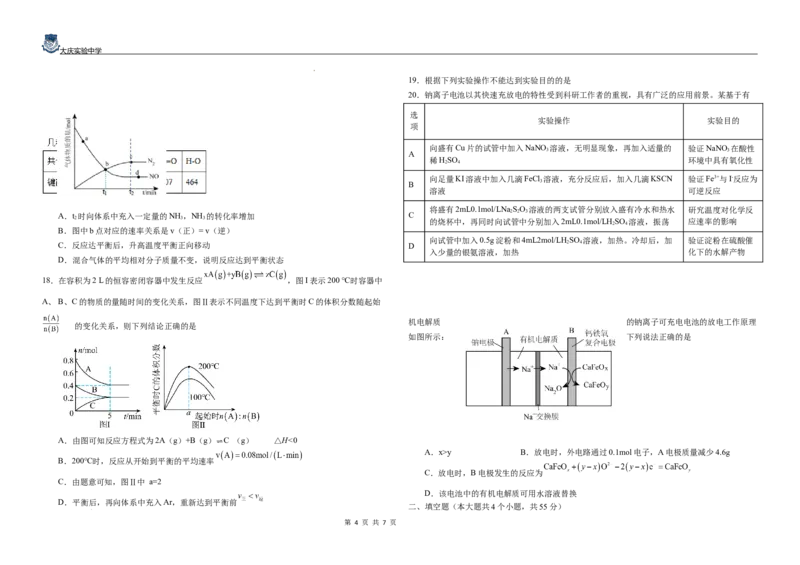
5.某工业废水中含有大量的Fe2+、SO 2-、Cu2+。兴趣小组模拟工业从该废水中回收金属铜,并制
4
备Fe(OH)SO ,流程如下:
4
选项 试剂1 试剂2 试剂3 实验目的
浓氨
A CaO 浓硫酸 制取干燥的NH
水 3
已知:该流程中NaNO 的还原产物为NO
2
第 1 页 共 7 页
学科网(北京)股份有限公司大庆实验中学
下列说法错误的是
A.甲为铁粉,乙为稀硫酸溶液
B.固体1为铁、铜混合物,固体2为铜
C.上述流程中欲制备2molFe(OH)SO ,理论上至少需要加入2molNaNO
4 2
D.取少量产品Fe(OH)SO 溶于盐酸,滴入KMnO 溶液检验产品中的Fe2+ A.抗坏血酸可做食品抗氧化剂
4 4
6.PCl 和PCl 都是重要的化工产品。磷与氯气反应有如图转化关系。下列叙述正确的是 B.脱氢抗坏血酸能使酸性 KMnO 溶液褪色
3 5 4
C.抗坏血酸中的官能团有羟基、酯基和碳碳双键
D.1mol脱氢抗坏血酸与足量Na反应产生2mol H
2
9.下列热化学方程式或叙述正确的是
A.已知甲烷的燃烧热为 ,则甲烷燃烧的热化学方程式可表示为:
已知:在绝热恒容密闭容器中发生反应(1)、反应(2),反应体系的温度均升高。
A.△H=△H-△H
3 1 2
B. 4PCl (g)+4Cl (g)=4PCl (s) △H ; △H>△H
3 2 5 2 B.已知 ,则石墨比金刚石稳定
C.△H、△H、△H 中,△H 最大
1 2 3 3
D.PCl 分子中每个原子最外层都达到8电子结构
3 C.已知N
2
(g)+H
2
(g) ⇌NH
3
(g) ,则一定条件下向密闭容器中充入
7.科学家正在研究一种用乙烯(C H,沸点为-103.9 ℃)脱硫(SO )的方法,其机理如图所示。下列
2 4 2
0.5molN 和1.5molH 充分反应放出46.2kJ 的热量
2 2
关 于该脱硫方法的说法错误的是
D.已知 , ;则
10.下列事实不能用勒夏特列原理解释的是
A.500℃左右比常温下更有利于合成氨 B.新制氯水在光照条件下颜色变浅
C.可向浓氨水加入氢氧化钠固体快速制取氨 D.用钠与氯化钾共融的方法制备气态钾
11.若将铜丝插入热浓硫酸中进行如图(a~d均为浸有相应试液的棉花)所示的探究实验,下列分析
正 确的是
A.乙烯在该过程中是还原剂
B.SO 和C H 均可使溴水溶液褪色,其褪色原理相同
2 2 4
C.Cu+ 在该反应中作催化剂
D.步骤ⅰ中,每消耗2.24LCH(标准状况),有0.2mol S原子生成
2 4
8.抗坏血酸(即维生素C)有较强的还原性,下列有关抗坏血酸的说法错误的是
第 2 页 共 7 页
学科网(北京)股份有限公司大庆实验中学
A.Cu与浓硫酸反应,只体现HSO 的酸性
2 4
B.a处变红,说明SO 是酸性氧化物
2
C.b或c处褪色,均说明SO 具有漂白性 A.电池工作时,电流由X电极经外电路流向Y电极
2
D.试管底部出现白色固体,说明反应中无HO生成 B.每消耗22.4 LO(标况下),质子交换膜通过1mol H+
2 2
12.纳米零价铁除去酸性废水中的三氯乙烯、五价砷的原理如图所示,下列说法正确的是 C.电池工作时,H+通过质子交换膜从右往左迁移
D.该电池的负极反应式为
15.已知 CH
4
(g) +2NO
2
(g)⇌CO
2
(g) +N
2
(g) +2H
2
O(l) ΔH , NO
2
的平衡转化率随温度、压强的
变 化如图所示,下列说法正确的 是
A. ΔH < 0
B.Y>Y
1 2
A.该处理过程中将电能转化为化学能 C.平衡常数:K =K< K
b a c
B.该处理过程中纳米零价铁中的Fe为正极 D. a点体系颜色比.b点浅
C.每生成11.2L乙烷,转移电子0.4mol
D.酸性废水中的五价砷除去过程中As和S都被Fe2+还原了 16.酸性水系锌锰电池在家庭和工业领域被广泛应用,放电时总反应的离子方程式为:
13.1,3-丁二烯和2-丁炔分别与氢气反应的热化学方程式如下: MnO +Zn+4H+=Mn2++Zn2++2H O,放电时电极上的MnO 易剥落,会降低电池效率,向体系中
2 2 2
加入少量KI固体可以提高电池的工作效率,原理如图所示。下列说法错误的是
①
②
由此判断正确的是
A.①和②的产物相比,②的产物更稳定 B.1.3-丁二烯比2-丁炔更稳定
C.1,3-丁二烯转化为2-丁炔是放热反应 D.一个碳碳三键的键能比两个碳碳双键的键能之和大
14.如图是一种酸性燃料电池酒精检测仪,具有自动吹起、流量侦测与控制的功能,非常适合进
A.加 入KI后发生反应为:
行现场酒精检测。下列说法正确的是
MnO +3I-+4H+=Mn2++I -+2H O
2 3 2
B.放电时,电子由锌电极经负载流向碳电极
C.放电时,若消耗1molZn,正极区电解质溶液理论上增重87g
D.放电时,通过质子交换膜的H+与生成的Zn2+的个数之比为2∶1
17.已知4NH
3
(g)+6NO(g) ⇌5N
2
(g)+6H
2
O(g),实验中测得容器内NO及N
2
的物质的量
随 时间变化如图所示:下列说法正确的是
第 3 页 共 7 页
学科网(北京)股份有限公司大庆实验中学
19.根据下列实验操作不能达到实验目的的是
20.钠离子电池以其快速充放电的特性受到科研工作者的重视,具有广泛的应用前景。某基于有
选
实验操作 实验目的
项
向盛有Cu片的试管中加入NaNO 溶液,无明显现象,再加入适量的 验证NaNO 在酸性
3 3
A
稀HSO 环境中具有氧化性
2 4
向足量KI溶液中加入几滴FeCl 溶液,充分反应后,加入几滴KSCN 验证Fe3+与I-反应为
3
B
溶液 可逆反应
将盛有2mL0.1mol/LNa SO 溶液的两支试管分别放入盛有冷水和热水 研究温度对化学反
2 2 3
A.t 时向体系中充入一定量的NH ,NH 的转化率增加 C
2 3 3 的烧杯中,再同时向试管中分别加入2mL0.1mol/LH SO 溶液,振荡 应速率的影响
2 4
B.图中b点对应的速率关系是v(正)= v(逆)
向试管中加入0.5g淀粉和4mL2mol/LHSO 溶液,加热。冷却后,加 验证淀粉在硫酸催
C.反应达平衡后,升高温度平衡正向移动 D 2 4
入少量的银氨溶液,加热 化下的水解产物
D.混合气体的平均相对分子质量不变,说明反应达到平衡状态
18.在容积为2 L的恒容密闭容器中发生反应 ,图I表示200 ℃时容器中
A、B、C的物质的量随时间的变化关系,图Ⅱ表示不同温度下达到平衡时C的体积分数随起始
机电解质 的钠离子可充电电池的放电工作原理
的变化关系,则下列结论正确的是
如图所示: 下列说法正确的是
A.由图可知反应方程式为2A(g)+B(g) C (g) △H<0
⇌
A.x>y B.放电时,外电路通过0.1mol电子,A电极质量减少4.6g
B.200℃时,反应从开始到平衡的平均速率
C.放电时,B电极发生的反应为
C.由题意可知,图Ⅱ中 a=2
D.该电池中的有机电解质可用水溶液替换
D.平衡后,再向体系中充入Ar,重新达到平衡前
二、填空题(本大题共4个小题,共55分)
第 4 页 共 7 页
学科网(北京)股份有限公司大庆实验中学
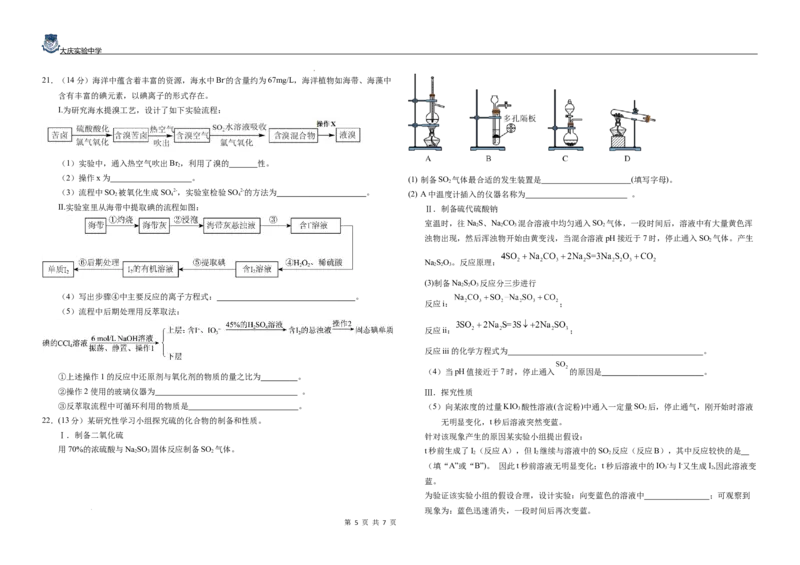
21.(14分)海洋中蕴含着丰富的资源,海水中Br-的含量约为67mg/L,海洋植物如海带、海藻中
含有丰富的碘元素,以碘离子的形式存在。
Ⅰ.为研究海水提溴工艺,设计了如下实验流程:
(1)实验中,通入热空气吹出Br ,利用了溴的 性。
2
(2)操作x为 。 (1) 制备SO 气体最合适的发生装置是 (填写字母)。
2
(3)流程中SO 2 被氧化生成SO 4 2-,实验室检验SO 4 2-的方法为 。 (2) A中温度计插入的仪器名称为 。
Ⅱ.实验室里从海带中提取碘的流程如图: Ⅱ.制备硫代硫酸钠
室温时,往NaS、NaCO 混合溶液中均匀通入SO 气体,一段时间后,溶液中有大量黄色浑
2 2 3 2
浊物出现,然后浑浊物开始由黄变浅,当混合溶液pH接近于7时,停止通入SO 气体。产生
2
NaSO。反应原理:
2 2 3
(3)制备NaSO 反应分三步进行
2 2 3
(4)写出步骤④中主要反应的离子方程式: 。
反应i: ;
(5)流程中后期处理用反萃取法:
反应ii: ;
反应iii的化学方程式为 。
(4)当pH值接近于7时,停止通入 的原因是 。
①上述操作1的反应中还原剂与氧化剂的物质的量之比为 。
②操作2使用的玻璃仪器为 。 Ⅲ.探究性质
③反萃取流程中可循环利用的物质是 。 (5)向某浓度的过量KIO 酸性溶液(含淀粉)中通入一定量SO 后,停止通气,刚开始时溶液
3 2
22.(13分)某研究性学习小组探究硫的化合物的制备和性质。 无明显变化,t秒后溶液突然变蓝。
Ⅰ.制备二氧化硫 针对该现象产生的原因某实验小组提出假设:
用70%的浓硫酸与Na 2 SO 3 固体反应制备SO 2 气体。 t秒前生成了I 2 (反应A),但I 2 继续与溶液中的SO 2 反应(反应B),其中反应较快的是
(填“A”或“B”)。 因此t秒前溶液无明显变化;t秒后溶液中的IO -与I-又生成I,因此溶液变
3 2
蓝。
为验证该实验小组的假设合理,设计实验:向变蓝色的溶液中 ;可观察到
现象为:蓝色迅速消失,一段时间后再次变蓝。
第 5 页 共 7 页
学科网(北京)股份有限公司大庆实验中学
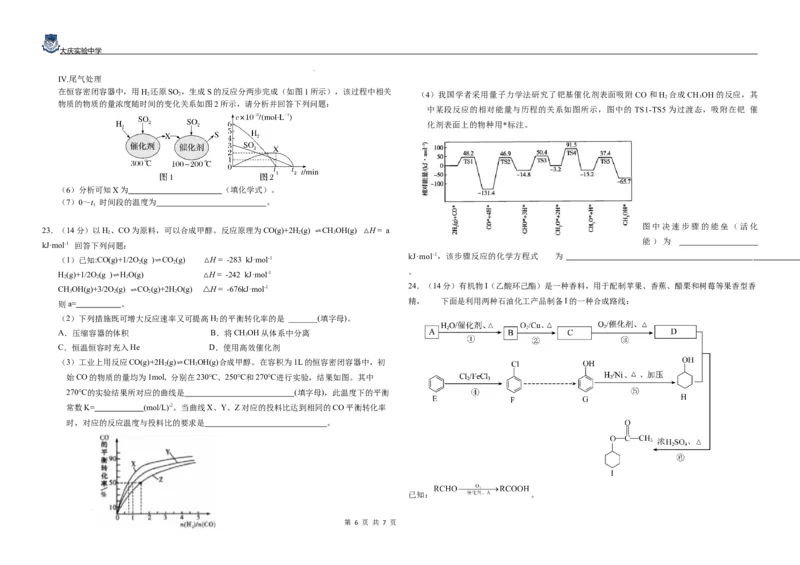
Ⅳ.尾气处理
在恒容密闭容器中,用H 还原SO ,生成S的反应分两步完成(如图1所示),该过程中相关
2 2 (4)我国学者采用量子力学法研究了钯基催化剂表面吸附CO和H 合成CH OH的反应,其
2 3
物质的物质的量浓度随时间的变化关系如图2所示,请分析并回答下列问题:
中某段反应的相对能量与历程的关系如图所示,图中的 TS1-TS5为过渡态,吸附在钯 催
化剂表面上的物种用*标注。
(6)分析可知X为 (填化学式)。
(7)0~t 时间段的温度为 。
1
图中决速步骤的能垒(活化
23.(14分)以H
2
、CO为原料,可以合成甲醇。反应原理为CO(g)+2H
2
(g) ⇌CH
3
OH(g) △H = a
能)为
kJ·mol-1 回答下列问题:
kJ·mol-1,该步骤反应的化学方程式 为
(1)已知:CO(g)+1/2O
2
(g )⇌CO
2
(g) △H = -283 kJ·mol-1
。
H
2
(g)+1/2O
2
(g )⇌H
2
O(g) △H = -242 kJ·mol-1
24.(14分)有机物I(乙酸环己酯)是一种香料,用于配制苹果、香蕉、醋栗和树莓等果香型香
CH
3
OH(g)+3/2O
2
(g)
⇌
CO
2
(g)+2H
2
O(g) △H = -676kJ·mol-1
精, 下面是利用两种石油化工产品制备I的一种合成路线:
则a= 。
(2)下列措施既可增大反应速率又可提高H 的平衡转化率的是 _______(填字母)。
2
A.压缩容器的体积 B.将CHOH从体系中分离
3
C.恒温恒容时充入He D.使用高效催化剂
(3)工业上用反应CO(g)+2H
2
(g)⇌CH
3
OH(g)合成甲醇。在容积为1L的恒容密闭容器中,初
始CO的物质的量均为1mol, 分别在230℃、250℃和270℃进行实验,结果如图。其中
270℃的实验结果所对应的曲线是 (填字母),此温度下的平衡
常数K= (mol/L)-2。当曲线X、Y、Z对应的投料比达到相同的CO平衡转化率
时,对应的反应温度与投料比的要求是 。
已知: 。
第 6 页 共 7 页
学科网(北京)股份有限公司大庆实验中学
(1)由石油生产A的工艺名称为 。I的分子式为 。 (4)二氧化硫继续通入会反应生成亚硫酸,而硫代硫酸钠易与酸反应,故减少硫代硫酸钠的损失
(5)B 通入少量SO
(2)C中官能团的名称为 。 2
(6)HS(1分) (7)300℃(1分)
(3)反应①~ ⑥中属于加成反应的是 (填序号)。 2
23.(14分)
(4)反应⑥的化学方程式为 。
答案:(每空2分,共14分)
(5)H的同分异构体中,能够使新制的氢氧化铜产生砖红色沉淀的结构有 种。
(1)-91 (2)A
(6)下列关于合成路线中所涉及物质的说法正确的是 。
(3)Z 4 温度越高 投料比越大
A.B与 互为同系物
(4)178.3 CO*+4H* = CHO*+3H*
B. A、E分子中的原子均处于同一平面
24.(14分)
C.一定条件下,1molG可与3molH 反应生成H
2
答案:(每空2分,共14分)
D. 可用NaHCO 溶液鉴别B和D
3
(1)裂解 C8H14O2
大庆实验中学实验一部 2023 级高二上学期开学考试
(2)醛基
化学学科试题答案 (3)1 、 5
(4)略 (5)8 (6) BCD
一、 选择题(本大题共20小题,1-15题第小题2分,16-20题第小题3分,共45
分)
1 2 3 4 5 6 7 8 9 10
A C D C D D B D B A
11 12 13 14 15 16 17 18 19 20
B D B D A C D C D A
二、填空题(本大题共4个小题,共55分)
21.(14分)
答案:(每空2分,共14分)
(1)挥发性
(2)蒸馏
(3)取少量溶液于试管中,滴加几滴(盐酸酸化的)BaCl 溶液,若有白色沉淀产生,则说明有SO 2-
2 4
(4)HO+2I-+2H+=2H O+I
2 2 2 2
(5) ①1:5 ②烧杯、漏斗、玻璃棒 ③CCl
4
22. (13分)
答案:(除标注1分,其余每空2分,共13分)
(1)C(1分) (2)蒸馏烧瓶
(3)S+Na SO =Na SO
2 3 2 2 3
第 7 页 共 7 页
学科网(北京)股份有限公司