文档内容
大庆中学 2024----2025 学年度上学期期中考试
A. 0.50mol 分子中共价键的数目为2N
A
高三年级化学试题
B. 标准状况下,2.24LSO 中电子的数目为4.00N
3 A
考试时间:75分钟;试卷总分:100分
注意事项: C. pH=2的H SO 溶液中H+的数目为0.02N
2 4 A
1.答题前填写好自己的姓名、班级、考号等信息
D. 0.1mol基态硫原子核外含有的未成对电子数为0.2N
A
2.请将答案正确填写在答题卡上
可能用到的相对原子质量 H-1 Mg-24 O-16 N-14 C-12 S-32
5.关于Na CO 和NaHCO 的下列说法中,不正确的是( )
2 3 3
第Ⅰ卷(选择题 共45分)
A. 两种物质的溶液中,所含微粒的种类相同
B. 可用NaOH溶液使NaHCO 转化为Na CO
一、单选题(本题共15小题,每小题3分,每小题只有一个选项符合题意。) 3 2 3
C. 利用二者热稳定性差异,可从它们的固体混合物中除去NaHCO
1.下列化学用语或图示表达不正确的是( ) 3
D. 室温下,二者饱和溶液的pH差约为4,主要是由于它们的溶解度差异
A. NaCl的电子式: B. Fe2+的价层电子排布式:3d6
6.类比推理是重要的学科思想,下列“类比”合理的是( )
C. SO 分子的空间结构:直线形 D. H O 的结构式:H —O—O—H A. Fe与S反应生成FeS,则Cu与S反应生成Cu S
2 2 2 2
2.以下物质间的转化中,不能通过一步反应实现的是( ) B. CO (干冰)是分子晶体,则SiO (石英)也是分子晶体
2 2
A. B. C. Li在空气中燃烧生成Li O,则Na在空气中燃烧生成Na O
Fe→ FeCl →Fe(OH) →Fe(OH) Na→Na O →NaOH→NaAlO 2 2
2 2 3 2 2 2
D. CO 通入Ba(NO ) 溶液无沉淀生成,则SO 通入Ba(NO ) 溶液也无沉淀生成
2 3 2 2 3 2
C. S→SO →H SO →MgSO D. N →NO→NO →HNO
3 2 4 4 2 2 3 7.工业除去电石渣浆(含CaO)中的S2−并制取硫酸盐的一种常用流程如图。下列说法错误的是(
3.下列有关工业制法正确的是( )
)
A. 制铁:用铝还原氧化铁制备大量的铁
B. 制氯:用海水为原料制得饱和食盐水,再通电电解
C. 制钛:用金属钠置换氯化钛(TiCl )溶液中的钛
4
D. 炼铜:用黄铜矿经电解精炼得到纯度为99.95%的铜
4.N 为阿伏加德罗常数的值。下列叙述正确的是( )
A
A. 由上述过程 、 可知氧化性
I II O >MnO2−>S O2−
2 3 2 3
B. 过程II中,氧化剂和还原剂的物质的量之比为1:2C. 过程 中发生反应: C. 与铝粉反应放出 的透明溶液: 、 、 、
I 2Mn(OH) +O +4OH−=2MnO2−+4H O H Cu2+ Na+ SO2− Cl−
2 2 3 2 2 4
D. 将 渣浆中的 浓度为 转化为 ,理论上至少需要氧气
10L S2− ( 320mg/L) SO2− 0.2mol
4 D. c(OH− ) 的溶液中: 、 、 、
=10−12 K+ MnO− Na+ Cl−
c(H+
)
4
8.溴及其化合物广泛应用于医药、农药和阻燃剂等生产中。一种利用空气吹出法从海水中提取溴
的工艺流程如下。 10.将FeSO 溶液分别滴入Na CO 溶液和NaHCO 溶液中,如图所示, Ⅰ、Ⅱ中均有沉淀产生。
4 2 3 3
已知:FeCO 是白色难溶于水的固体。
3
已知: 与 反应时, 转化为 和 。 . 为强酸。
i. Na CO Br BrO− Br− ii HBrO
2 3 2 3 3
下列说法不正确的是( )
A. 酸化海水通入 提取溴的反应:
Cl Cl +2Br−=2Cl−+Br
2 2 2
B. 脱氯过程Fe2+和Br−均具有脱氯作用 下列说法不正确的是( )
A. Na CO 溶液和NaHCO 溶液中均存在:
2 3 3
C. 用 溶液吸收足量 蒸气后,所得产物中的含碳粒子主要是
Na CO Br HCO−
2 3 2 3
c(Na+)+c(H+)=c(HCO−)+2c(CO2−)+c(OH−)
3 3
D. 酸化后重新得到 的反应:
H SO Br 5Br−+BrO−+6H+=3Br +3H O B. Ⅰ中的沉淀可能有Fe(OH) 、Fe(OH) 和FeCO
2 4 2 3 2 2 2 3 3
C. Ⅰ和Ⅱ中加入FeSO 溶液后,pH均降低
9.常温下,在指定溶液中下列各组离子可能大量共存的是( ) 4
A. 滴加 显红色的溶液: 、 、 、
KSCN N H+
4
Cl− K+ HCO−
3
D. Ⅱ中生成 FeCO 的反应: HCO−+Fe2+=FeCO ↓+H+
3 3 3
B. 0.1mol⋅L−1KI 溶液:Na+、K+、ClO−、OH− 11.下列离子方程式书写正确的是( )
A. Mg(HCO ) 溶液与足量的NaOH溶液反应:
3 2
M g2++2HCO−+2OH−=MgCO ↓+CO2−+2H O
3 3 3 2B. 将 通入到含 的溶液中: C. 总反应的原子利用率达到100%
2molCl 1molFeBr 2Fe2++2Br−+2Cl =2Fe3++4Cl−+Br
2 2 2 2
C. 少量 通入到 溶液中:
SO NaClO SO +H O+ClO−=Cl−+SO2−+2H+ D. 若用苯乙炔代替上述过程中的同类物质与CH =CHI反应,可以合成
2 2 2 4 2
D. 工业上制漂白液: Cl +2OH−=ClO−+Cl−+H O 14.某科研小组用电化学方法将CO 2 转化为CO实现再利用,转化的基本原理如图所示。下列叙述
2 2
正确的是( )
12.一定温度下,1molX和nmolY在体积为2L的密闭容器中发生如下反应:
A. 光能全部转化成电能
X(g)+Y(g)⇌2Z(g)+M(s),5min后达到平衡,此时生成2amolZ。下列说法正确的是(
B. 上的电极反应方程式为
) M 2H O−4e−=O ↑+4H+
2 2
A. 用X表示此反应的反应速率是0.1amol·L−1·min−1
C. 该电池工作时溶液中 移向 极
B. 当混合气体的压强不再发生变化时,说明反应达到平衡状态 SO2− N
4
C. 向平衡后的体系中加入1molM,平衡向逆反应方向移动
D. 若消耗标况下22.4LCO ,溶液中转移的电子数目为2N
2 A
D. 向上述平衡体系中再充入1molX,v 增大,v 减小,平衡正向移动
正 逆
13.利用Sonogashira反应机理合成苯乙炔的基本过程如图,其中L 表示配体(PPh ) ,下列叙述
n 3 2 15.某农药杀虫剂中含有的成分如图。已知X、Y、Z、N、M为原子序数依次增大的短周期主族
正确的是( )
元素,Y、Z位于同一个周期,X、N位于同一主族。下列叙述正确的是( )
A. Z、M的最简单气态氢化物的键角:M>Z
B. X、Y形成的链状化合物Y X 中σ键数为:m+n−1
m n
C. 第一电离能比Z小且与Z同周期的元素有4种
D. Y、Z两种元素与X元素形成的最简单气态氢化物,均为非
极性分子
第Ⅱ卷(非选择题 共55分)
二、非选择题(本题共4小题,总共55分)
A. 步骤④过程中,Pd元素被还原 16.(共12分)溴酸镉[Cd(BrO ) ]常用作分析试剂、生产荧光粉等。以镉铁矿(主要成分为
3 2
CdO 、Fe O 、Fe及少量的Al O 和SiO )为原料制备[Cd(BrO ) ]的工艺流程如图所示。
2 2 3 2 3 2 3 2
B. L Pd和CuI是该反应过程的催化剂,可以提高 的平衡转化率
n已知:Cd(SO ) 可溶于水。请回答下列问题:
4 2
(1)滤渣1为______ (填化学式),为提高镉的浸取率,酸浸时可采取的措施为____________ (任写
(3)转化。向MgO中先加入稳定剂和30%H O 溶液,充分反应后,过滤、洗涤、干燥,可得
2 2
一种即可)。
粗品MgO 。
2
(2)还原镉时,产生能使澄清石灰水变浑浊的气体,则该反应的离子方程式为____________
①写出制备MgO 时发生反应的化学方程式:_______________________________________。
2
______________________________ 。 ②“转化”阶段有大量热量放出,为了提高MgO 的产率,添加30%H O 溶液时,比较理想的
2 2 2
(3)加入H 2 O 2 溶液的目的是 ________________________ (用离子方程式表示)。 操作方法为________________________________________________________________。
(4)已知几种金属离子的氢氧化物开始沉淀和完全沉淀的pH如表所示,调pH时,应调整pH的 (4)测定。某研究小组拟用下图装置测定样品(含MgO杂质)中MgO 的含量。
2
范围为 ________________________ ,滤渣2的主要成分为 __________________ (填化学式)。
金属离子 开始沉淀的pH 完全沉淀的pH
F e3 + 1 .5 2.8
A l3 + 3 .0 5.0
F e2 + 6 .3 8.3
C d2 + 7 .4 ① 实 验 时 在 稀 盐 酸9.4中加入FeCl 3 溶液的作用是
17.(共15分)MgO 可被用于治疗消化道疾病。某学习探究小组在实验室进行了制备 ____________________________________________________________(用化学方程式表示)。
2
②为了减小实验误差,在每次读数前需要进行的操作是_______________、_______________。
MgO 以及含量测定的实验。已知:常温下MgO 不溶于水,较稳定,与酸反应生成H O ;加
2 2 2 2
③该小组记录的实验数据如下:样品的质量为mg;反应开始前量气管的读数为amL;反应结束
热时会分解生成O 和MgO。请回答下列问题:
2
(1)镁元素属于元素周期表_______区。
冷却到室温后量气管的读数为 ,已知:室温条件下气体摩尔体积为 ,则样品中过
bmL V L·mol−1
0
(2)灼烧。灼烧Mg (OH) CO 制MgO时,可使用的实验装置有________(填字母)。
2 2 3
氧化镁的质量分数为________%(用含a、b、m、V 的代数式表示);若反应结束后读取量气管中
0
气体的体积时,液面左低右高,则测得MgO 的质量分数________(填“偏大”“偏小”或“无影
2
响”)。
18.
(共14分)[FeF ]
3−与许多金属离子或
N H+
形成的化合物有广泛的用途。
6 4(1)基态F原子的价层电子轨道表示式为__________________________________
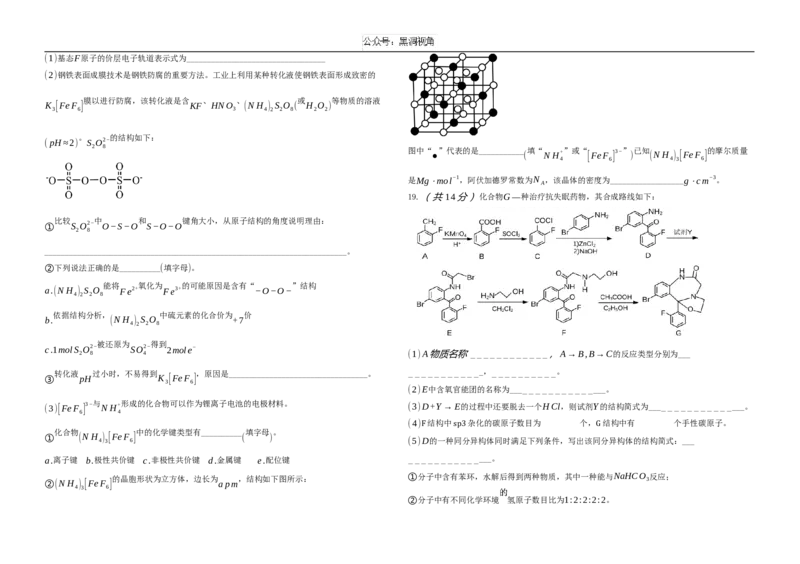
(2)钢铁表面成膜技术是钢铁防腐的重要方法。工业上利用某种转化液使钢铁表面形成致密的
膜以进行防腐,该转化液是含 、 、 或 等物质的溶液
K [FeF ] KF HNO (N H ) S O ( H O )
3 6 3 4 2 2 8 2 2
。 的结构如下:
(pH≈2) S O2−
2 8
图中“
●
”代表的是___________
(
填“
N
H+”或“
[FeF ]
3−”
)
已知
(N H ) [FeF ]
的摩尔质量
4 6 4 3 6
是Mg⋅mol−1,阿伏加德罗常数为N ,该晶体的密度为__________________g⋅cm−3。
A
19.(共14分)化合物G—种治疗抗失眠药物,其合成路线如下:
比较 中 和 键角大小,从原子结构的角度说明理由:
① S O2− O−S−O S−O−O
2 8
__________________________________________________________________________。
②下列说法正确的是__________(填字母)。
能将 氧化为 的可能原因是含有“ ”结构
a.(N H ) S O Fe2+ Fe3+ −O−O−
4 2 2 8
依据结构分析, 中硫元素的化合价为 价
b. (N H ) S O +7
4 2 2 8
被还原为 得到
c.1molS O2− SO2− 2mole−
2 8 4 (1)A物质名称____________,A→B,B→C的反应类型分别为___
转化液 过小时,不易得到 ,原因是__________________________________。 ____________,__________。
③ pH K [FeF ]
3 6
(2)E中含氧官能团的名称为_________________。
(3)[FeF ]
3−与
N
H+形成的化合物可以作为锂离子电池的电极材料。 (3)D+Y→E的过程中还要脱去一个HCl,则试剂Y的结构简式为_________________。
6 4
(4) 结构中 杂化的碳原子数目为______个, 结构中有______个手性碳原子。
化合物 中的化学键类型有__________ 填字母 。
① (N H ) [FeF ] ( )
4 3 6 (5)FD的一种s同p3分异构体同时满足下列条件,写出该同G分异构体的结构简式:___
a.离子键 b.极性共价键 c.非极性共价键 d.金属键 e.配位键 ______________。
的晶胞形状为立方体,边长为 ,结构如下图所示: ①分子中含有苯环,水解后得到两种物质,其中一种能与NaHCO 3 反应;
②(N H ) [FeF ] apm
4 3 6
②分子中有不同化学环境 氢原子数目比为1:2:2:2:2。