文档内容
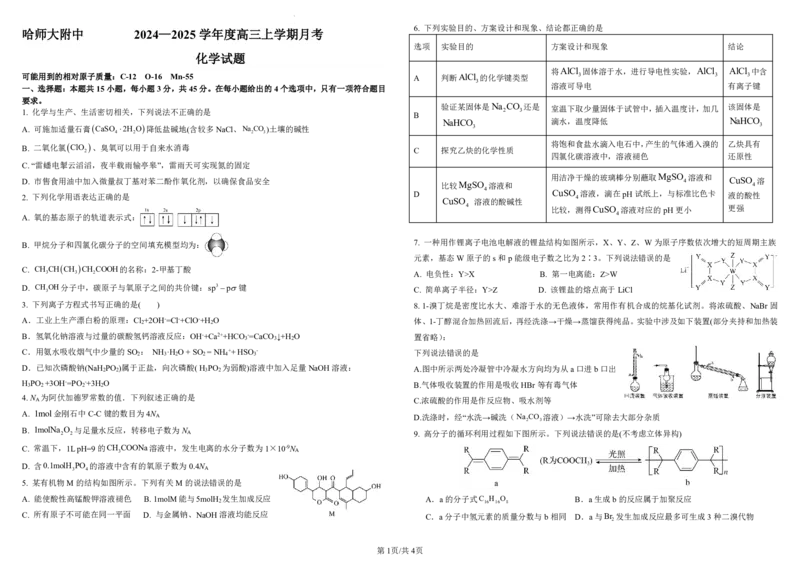
6. 下列实验目的、方案设计和现象、结论都正确的是
哈师大附中 2024—2025 学年度高三上学期月考
选项 实验目的 方案设计和现象 结论
化学试题
将AlCl 固体溶于水,进行导电性实验,AlCl AlCl 中含
可能用到的相对原子质量:C-12 O-16 Mn-55 A 判断AlCl 的化学键类型 3 3 3
3
溶液可导电 有离子键
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的4个选项中,只有一项符合题目
要求。
验证某固体是Na CO 还是 室温下取少量固体于试管中,插入温度计,加几 该固体是
1. 化学与生产、生活密切相关,下列说法不正确的是 2 3
B
NaHCO 滴水,温度降低 NaHCO
A. 可施加适量石膏CaSO 2H O降低盐碱地(含较多NaCl、Na CO )土壤的碱性 3 3
4 2 2 3
B.
二氧化氯ClO
2
、臭氧可以用于自来水消毒
C 探究乙炔的化学性质
将饱和食盐水滴入电石中,产生的气体通入溴的 乙炔具有
四氯化碳溶液中,溶液褪色 还原性
C.“雷蟠电掣云滔滔,夜半载雨输亭皋”,雷雨天可实现氮的固定
用洁净干燥的玻璃棒分别蘸取MgSO 溶液和
D. 市售食用油中加入微量叔丁基对苯二酚作氧化剂,以确保食品安全 4 CuSO 溶
比较MgSO 溶液和 4
4
2. 下列化学用语表达正确的是 D CuSO 4 溶液,滴在pH试纸上,与标准比色卡 液的酸性
CuSO 溶液的酸碱性
4 比较,测得CuSO 溶液对应的pH更小 更强
A. 氧的基态原子的轨道表示式: 4
B. 甲烷分子和四氯化碳分子的空间填充模型均为: 7. 一种用作锂离子电池电解液的锂盐结构如图所示,X、Y、Z、W为原子序数依次增大的短周期主族
元素,基态W原子的s和p能级电子数之比为2∶3。下列说法错误的是
C. CH CHCH CH COOH的名称:2-甲基丁酸
3 3 2 A. 电负性:Y>X B. 第一电离能:Z>W
D. CH 3 OH分子中,碳原子与氧原子之间的共价键:sp3p键 C. 简单离子半径:Y>Z D. 该锂盐的熔点高于LiCl
3. 下列离子方程式书写正确的是( ) 8.1-溴丁烷是密度比水大、难溶于水的无色液体,常用作有机合成的烷基化试剂。将浓硫酸、NaBr固
A.工业上生产漂白粉的原理:Cl
2
+2OH-=Cl-+ClO-+H
2
O 体、1-丁醇混合加热回流后,再经洗涤→干燥→蒸馏获得纯品。实验中涉及如下装置(部分夹持和加热装
B.氢氧化钠溶液与过量的碳酸氢钙溶液反应:OH-+Ca2++HCO -=CaCO ↓+H O 置省略):
3 3 2
C.用氨水吸收烟气中少量的SO : NH ·H O+SO =NH ++HSO - 下列说法错误的是
2 3 2 2 4 3
D.已知次磷酸钠(NaH
2
PO
2
)属于正盐,向次磷酸(H
3
PO
2
为弱酸)溶液中加入足量NaOH溶液: A.图中所示两处冷凝管中冷凝水方向均为从a口进b口出
H 3 PO 2 +3OH-=PO 2 -+3H 2 O B.气体吸收装置的作用是吸收HBr等有毒气体
4.N A 为阿伏加德罗常数的值.下列叙述正确的是 C.浓硫酸的作用是作反应物、吸水剂等
A. 1mol金刚石中C-C键的数目为4N A D.洗涤时,经“水洗→碱洗(Na CO 溶液)→水洗”可除去大部分杂质
2 3
B. 1molNa 2 O 2 与足量水反应,转移电子数为N A 9. 高分子的循环利用过程如下图所示。下列说法错误的是(不考虑立体异构)
C. 常温下,1LpH=9的CH COONa溶液中,发生电离的水分子数为1×10-9N
3 A
D. 含0.1molH PO 的溶液中含有的氧原子数为0.4N
3 4 A
5. 某有机物M的结构如图所示。下列有关M的说法错误的是
A. 能使酸性高锰酸钾溶液褪色 B.1molM能与5molH
2
发生加成反应 A.a的分子式C
16
H
16
O
8
B.a生成b的反应属于加聚反应
C. 所有原子不可能在同一平面 D. 与金属钠、NaOH溶液均能反应 C.a分子中氢元素的质量分数与b相同 D.a与Br 发生加成反应最多可生成3种二溴代物
2
第1页/共4页
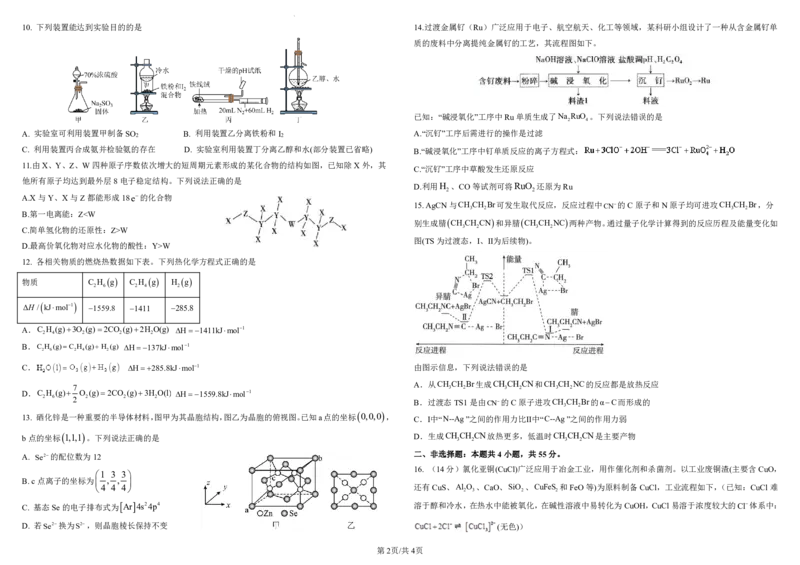
{#{QQABaQ6学科A网(北g京)股g份有限C公司gAIAAAAgCUwXqCgGQkBCACYgGRBAIsAAAyQFABCA=}#}10. 下列装置能达到实验目的的是 14.过渡金属钌(Ru)广泛应用于电子、航空航天、化工等领域,某科研小组设计了一种从含金属钌单
质的废料中分离提纯金属钌的工艺,其流程图如下。
已知:“碱浸氧化”工序中Ru单质生成了Na RuO 。下列说法错误的是
2 4
A. 实验室可利用装置甲制备SO B. 利用装置乙分离铁粉和I A.“沉钌”工序后需进行的操作是过滤
2 2
C. 利用装置丙合成氨并检验氨的存在 D. 实验室利用装置丁分离乙醇和水(部分装置已省略) B.“碱浸氧化”工序中钉单质反应的离子方程式:
11.由X、Y、Z、W四种原子序数依次增大的短周期元素形成的某化合物的结构如图,已知除X外,其
C.“沉钌”工序中草酸发生还原反应
他所有原子均达到最外层8电子稳定结构。下列说法正确的是
D.利用H 、CO等试剂可将RuO 还原为Ru
2 2
A.X与Y、X与Z都能形成18e的化合物
15.AgCN与CH CH Br可发生取代反应,反应过程中CN的C原子和N原子均可进攻CH CH Br,分
3 2 3 2
B.第一电离能:ZW 3 2 3 2
图(TS为过渡态,Ⅰ、Ⅱ为后续物)。
D.最高价氧化物对应水化物的酸性:Y>W
12. 各相关物质的燃烧热数据如下表。下列热化学方程式正确的是
物质 C H g C H g H g
2 6 2 4 2
ΔH /
kJmol1
1559.8 1411 285.8
A.C H (g)3O (g)2CO (g)2H O(g) H1411kJmol1
2 4 2 2 2
B.C H (g)C H (g)H (g) H137kJmol1
2 6 2 4 2
C. H285.8kJmol1 由图示信息,下列说法错误的是
A.从CH CH Br生成CH CH CN和CH CH NC的反应都是放热反应
7 3 2 3 2 3 2
D.C H (g) O (g) 2CO (g)3H O(l) H1559.8kJmol1
2 6 2 2 2 2 B.过渡态TS1是由CN的C原子进攻CH CH Br的αC而形成的
3 2
13. 硒化锌是一种重要的半导体材料,图甲为其晶胞结构,图乙为晶胞的俯视图。已知a点的坐标 0,0,0 , C.Ⅰ中“N--Ag”之间的作用力比Ⅱ中“C--Ag”之间的作用力弱
b点的坐标 1,1,1 。下列说法正确的是 D.生成CH
3
CH
2
CN放热更多,低温时CH
3
CH
2
CN是主要产物
A. Se2的配位数为12
二、非选择题:本题共4小题,共55分。
16. (14分)氯化亚铜(CuCl)广泛应用于冶金工业,用作催化剂和杀菌剂。以工业废铜渣(主要含CuO,
1 3 3
B.c点离子的坐标为 , ,
4 4 4 还有CuS、Al O 、CaO、SiO 、CuFeS 和FeO等)为原料制备CuCl,工业流程如下,(已知:CuCl难
2 3 2 2
C. 基态Se的电子排布式为 Ar 4s24p4 溶于醇和冷水,在热水中能被氧化,在碱性溶液中易转化为CuOH,CuCl易溶于浓度较大的Cl体系中:
D. 若Se2换为S2,则晶胞棱长保持不变 (无色))
第2页/共4页
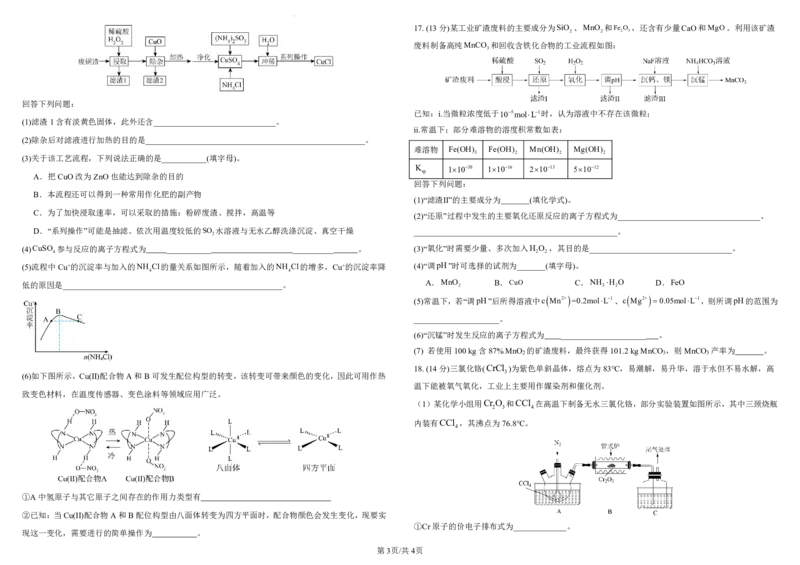
{#{QQABaQ6学科A网(北g京)股g份有限C公司gAIAAAAgCUwXqCgGQkBCACYgGRBAIsAAAyQFABCA=}#}17.(13分)某工业矿渣废料的主要成分为SiO 、MnO 和Fe O ,还含有少量CaO和MgO。利用该矿渣
2 2 2 3
废料制备高纯MnCO 和回收含铁化合物的工业流程如图:
3
回答下列问题:
已知:i.当微粒浓度低于105molL1时,认为溶液中不存在该微粒;
(1)滤渣1含有淡黄色固体,此外还含______________________________。
ii.常温下;部分难溶物的溶度积常数如表:
(2)除杂后对滤液进行加热的目的是______________________________________________________。
难溶物 Fe(OH) Fe(OH) Mn(OH) Mg(OH)
3 2 2 2
(3)关于该工艺流程,下列说法正确的是___________(填字母)。
K 11038 11016 21013 51012
sp
A.把CuO改为ZnO也能达到除杂的目的
回答下列问题:
B.本流程还可以得到一种常用作化肥的副产物
(1)“滤渣Ⅱ”的主要成分为 (填化学式)。
C.为了加快浸取速率,可以采取的措施:粉碎废渣、搅拌,高温等
(2)“还原”过程中发生的主要氧化还原反应的离子方程式为___________________________________、
D.“系列操作”可能是抽滤、依次用温度较低的SO 水溶液与无水乙醇洗涤沉淀、真空干燥 __________________________________________________。
2
(4)CuSO 参与反应的离子方程式为 ___________ __________ 。 (3)“氧化”时需要少量、多次加入H O ,其目的是___________________________________。
4 2 2
(5)流程中Cu+的沉淀率与加入的NH Cl的量关系如图所示,随着加入的NH Cl的增多,Cu+的沉淀率降 (4)“调pH”时可选择的试剂为_______(填字母)。
4 4
低的原因是______________________________________________________。 A.MnO 2 B.CuO C.NH 3 H 2 O D.FeO
(5)常温下,若“调pH”后所得溶液中c Mn2+ =0.2molL1、c Mg2+ 0.05molL1,则所调pH的范围为
_____________________。
(6)“沉锰”时发生反应的离子方程式为 _____________________ 。
(7) 若使用100kg含87%MnO 的矿渣废料,最终获得101.2kgMnCO ,则MnCO 产率为 。
2 3 3
18.(14分)三氯化铬(CrCl )为紫色单斜晶体,熔点为83℃,易潮解,易升华,溶于水但不易水解,高
3
(6)如下图所示,Cu(II)配合物A和B可发生配位构型的转变,该转变可带来颜色的变化,因此可用作热
温下能被氧气氧化,工业上主要用作媒染剂和催化剂。
致变色材料,在温度传感器、变色涂料等领域应用广泛。
(1)某化学小组用CrO 和CCl 在高温下制备无水三氯化铬,部分实验装置如图所示,其中三颈烧瓶
2 3 4
内装有CCl ,其沸点为76.8℃。
4
①A中氢原子与其它原子之间存在的作用力类型有
②已知:当Cu(II)配合物A和B配位构型由八面体转变为四方平面时,配合物颜色会发生变化,现要实
①Cr原子的价电子排布式为_____________。
现这一变化,需要进行的简单操作为 。
第3页/共4页
{#{QQABaQ6学科A网(北g京)股g份有限C公司gAIAAAAgCUwXqCgGQkBCACYgGRBAIsAAAyQFABCA=}#}②实验前先往装置A中通入N ,其目的是排尽装置中的空气,在实验过程中还需要持续通入N ,其 19.(14分)化合物F是合成盐酸多巴酚丁胺的中间体,其合成路线如下:
2 2
作用是_____________________。
③装置C的水槽中应盛有_______(填“冰水”或“沸水”)。
④装置B中还会生成光气(COCl ),B中反应的化学方程式为___________________________________。
2
(2)CrCl 的工业制法:先用40%的NaOH将红矾钠(Na Cr O )转化为铬酸钠(Na CrO ),加入过
3 2 2 7 2 4
量CH OH,再加入10%HCl溶液,可以看到有气泡产生。写出用CH OH将铬酸钠(Na CrO )还原
3 3 2 4
为CrCl 的离子方程式_____________________________________________________________。
3
(3)为进一步探究CrCl 的性质,某同学取试管若干支,分别加入10滴0.1mol/LCrCl 溶液,并用4
3 3
滴2mol/LH SO 酸化,再分别加入不同滴数的0.1mol/LKMnO 溶液,并在不同的温度下进行实验,
2 4 4
反应现象记录于表中。
已知:①
在不同温度下的反应现象
KMnO 的用量(滴
4
数)
25℃ 90-100℃
② (R 、R 、R 、R 均为烃基)
1 2 3 4
1 紫红色 蓝绿色溶液
回答下列问题:
2~9 紫红色 黄绿色溶液,且随KMnO 滴数增加,黄色成分增多 (1)A中C原子的杂化方式为___________。
4
(2)D中的官能团名称为___________,B→C的反应类型为___________。
10 紫红色 澄清的橙黄色溶液
(3)B的结构简式为___________。
11~23 紫红色 橙黄色溶液,有棕褐色沉淀,且随KMnO 滴数增加,沉淀增多 (4)C+D→E的化学方程式为________________________________。
4
(5)同时符合下列条件的D的同分异构体有___________种(不包括立体异构体),其中核磁共振氢谱的
24~25 紫红色 紫红色溶液,有较多的棕褐色沉淀
峰面积之比为9:2:2:2的结构简式为___________(任写一种)。
①温度对反应的影响。
①可以与氯化铁溶液发生显色反应; ②不含氮氧键; ③只有4种不同化学环境的氢原子。
CrCl
3
与KMnO
4
在常温下反应,观察不到Cr
2
O
7
2离子的橙色,甲同学认为其中一个原因是Cr
2
O
7
2离 (6)参照上述流程,设计以CH
3
CH
2
Br为原料合成CH
3
CHCHCHO的流程图:______(无机试剂、
子的橙色被MnO- 离子的紫红色掩盖,另一种可能的原因是___________________________,所以必须 有机溶剂任选)。
4
将反应液加热至沸腾4~5min后,才能观察到反应液由紫红色逐渐变为橙黄色的实验现象。
②CrCl 与KMnO 的用量对反应的影响。
3 4
对表中数据进行分析,在上述反应条件下,欲将Cr3氧化为Cr O 2-,CrCl 与KMnO 最佳用量比为
2 7 3 4
Δ
_______________。这与由反应10Cr3++6MnO-+11H O CrO2-+6Mn2++22H+ 所推断得到的用量比不符,
4 2 2 7
你推测的原因是______________________________。
第4页/共4页
{#{QQABaQ6学科A网(北g京)股g份有限C公司gAIAAAAgCUwXqCgGQkBCACYgGRBAIsAAAyQFABCA=}#}