文档内容
2019年湖南省株洲市中考化学试卷
一、选择题(每题2分,总共40分)
1.(2分)下列过程中一定发生了化学变化的是( )
A.干冰气化 B.塑料降解 C.铁水铸成锅 D.汽油除油污
2.(2分)下列与燃烧和爆炸有关的图标中不正确的是( )
A. 禁止吸烟 B. 禁止燃放鞭炮
C. 禁止放易燃物 D. 禁止烟火
3.(2分)下列物质中属于化合物的是( )
A.铝片 B.钢材 C.白酒 D.蔗糖
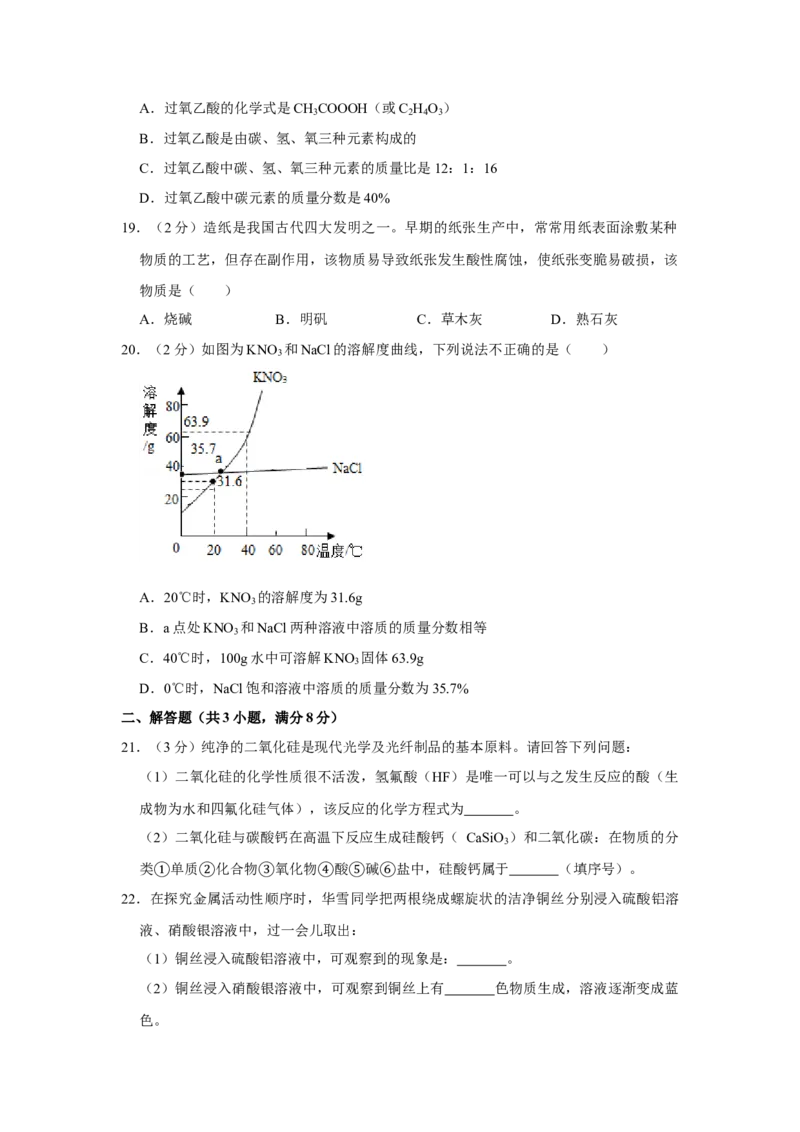
4 . ( 2 分 ) 下 列 有 关 化 学 实 验 操 作 的 图 示 中 正 确 的 是 ( )
A. B. C. D.
5.(2①分②)某小孩食欲不振、②生④长迟缓、发育不良,③下④列适合改善该小孩①症状的食品是(
)
A.高钙奶 B.补铁剂 C.补锌剂 D.海带汤
6.(2分)取用粉末状固体化学药品时,应使用的仪器是( )
A.滴管 B.研钵 C.药匙 D.镊子7.(2分)2019年是“国际化学元素周期表年”。制出第一张元素周期表的科学家的是(
)
A.舍勒 B.道尔顿 C.门捷列夫 D.阿伏伽德罗
8.(2分)下列说法中正确的是( )
A.凡是生成盐和水的反应都是中和反应
B.盐类物质中不一定含有金属元素
C.饱和溶液降温一定能析出晶体
D.碳酸饱和溶液的浓度比硼酸不饱和溶液的浓度大
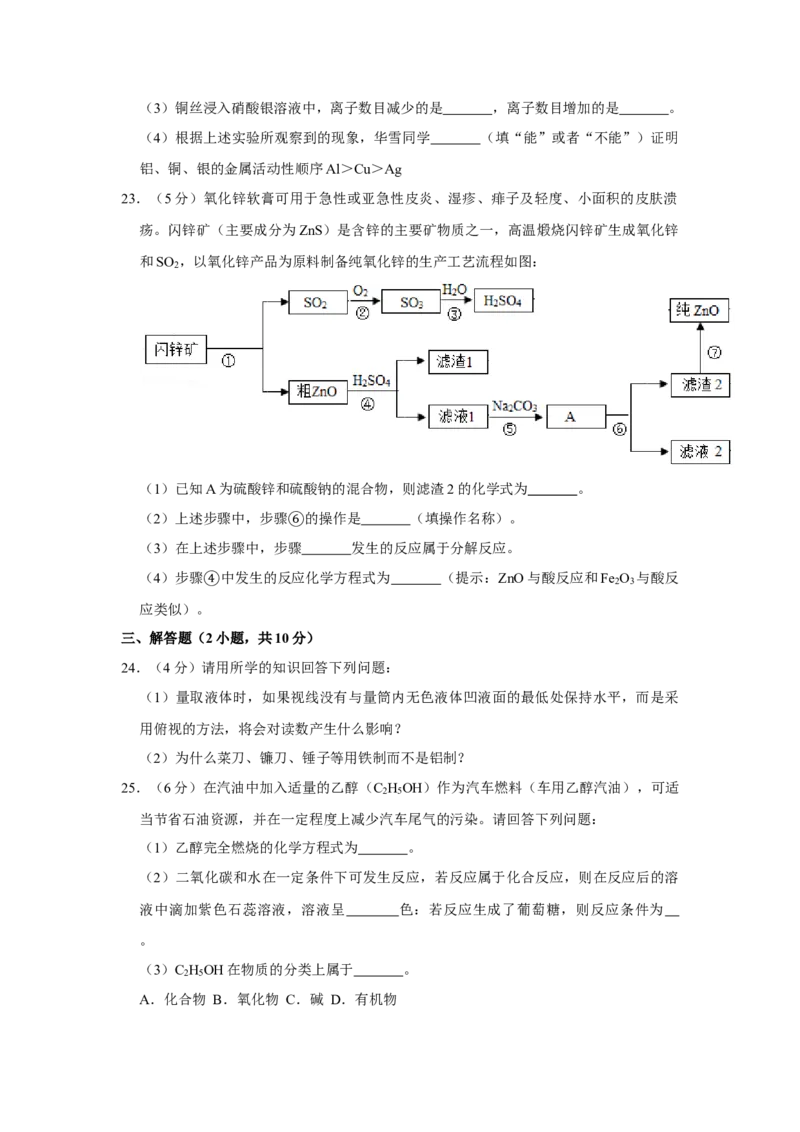
9.(2分)构建“单质及其化合物的价、类关系图”是学习化学的一种重要方法。如图是
华雪同学在化学学习中构建的“碳及其化合物的价、类关系图”。碳纳米管具有尺寸小、
机械强度高,导电性好等特点。在材料、催化、信息等诸多领域中具有重要的应用前景。
图中与碳纳米管对应的点是( )
A.A B.B C.C D.D
10.(2分)我国海水晒盐具有悠久的历史,所得“盐”的主要成分是( )
A.Na SO B.NaCl C.CaCl D.Na CO
2 4 2 2 3
11.(2分)将石油加热炼制,不可能得到的产品是( )
A.煤焦油 B.润滑油 C.柴油 D.煤油
12.(2分)一些重要作物最适宜生长的土壤的pH范围如下:
作物 水稻 马铃薯 草莓 薄荷
pH 6~7 4.8~5.5 5~7.5 7~8
下列说法中正确的是( )
A.水稻和薄荷生长都适宜酸性土壤
B.草莓生长只适宜酸性土壤
C.马铃薯生长不适宜碱性土壤
D.以上作物都不适宜碱性土壤13.(2分)下列选项中各种溶质的溶液混合,无明显现象的是( )
A.NaOH、NH Cl、Fe (SO ) B.KNO 、AgNO 、NaCl
4 2 4 3 3 3
C.KCl、CH COOH、Na CO D.H SO 、K SO 、HNO
3 2 3 2 4 2 4 3
14.(2分)如图为某元素原子的结构示意图。下列有关叙述不正确的是( )
A.该元素的原子序数为17
B.在该结构示意图中x=7
C.该元素的原子在化学反应中容易得到电子
D.该元素为硫,是一种非金属元素
15.(2分)下列化肥中,从外观即可与其他化肥区别的是( )
A.硝酸铵 B.磷矿粉 C.氯化钾 D.硫化钾
16.(2分)化学与生产、生活息息相关,下列说法中不正确的是( )
A.农药本身有毒,应该及早制订有关法律禁止施用农药
B.“中国居民平衡膳食宝塔”为我们提供了合理选择食物的指南
C.长期偏食和挑食不利于身体健康
D.运动员在剧烈运动、大量出汗后,常会饮用一些含无机盐的运动饮料
17.(2分)下列说法不正确的是( )
A.空气的成分按体积计算大约是:氮气78%,氧气21%,其他成分1%
B.地球上的水储量是丰富的,但可供利用的淡水资源是有限的
C.棉花、羊毛、蚕丝、涤纶、尼伦和腈纶等都是合成纤维
D.基本营养素包括蛋白质、糖类、油脂、维生素、无机盐和水六大类
18.(2分)过氧乙酸对细菌和病毒具有高效、快速杀灭作用,广泛应用于环境的消毒,
如图为过氧乙酸的分子结构图(其中 代表碳原子, 代表氢原子, 代表氧原子),
下列有关说法正确的是( )A.过氧乙酸的化学式是CH COOOH(或C H O )
3 2 4 3
B.过氧乙酸是由碳、氢、氧三种元素构成的
C.过氧乙酸中碳、氢、氧三种元素的质量比是12:1:16
D.过氧乙酸中碳元素的质量分数是40%
19.(2分)造纸是我国古代四大发明之一。早期的纸张生产中,常常用纸表面涂敷某种
物质的工艺,但存在副作用,该物质易导致纸张发生酸性腐蚀,使纸张变脆易破损,该
物质是( )
A.烧碱 B.明矾 C.草木灰 D.熟石灰
20.(2分)如图为KNO 和NaCl的溶解度曲线,下列说法不正确的是( )
3
A.20℃时,KNO 的溶解度为31.6g
3
B.a点处KNO 和NaCl两种溶液中溶质的质量分数相等
3
C.40℃时,100g水中可溶解KNO 固体63.9g
3
D.0℃时,NaCl饱和溶液中溶质的质量分数为35.7%
二、解答题(共3小题,满分8分)
21.(3分)纯净的二氧化硅是现代光学及光纤制品的基本原料。请回答下列问题:
(1)二氧化硅的化学性质很不活泼,氢氟酸(HF)是唯一可以与之发生反应的酸(生
成物为水和四氟化硅气体),该反应的化学方程式为 。
(2)二氧化硅与碳酸钙在高温下反应生成硅酸钙( CaSiO )和二氧化碳:在物质的分
3
类 单质 化合物 氧化物 酸 碱 盐中,硅酸钙属于 (填序号)。
22.在①探究金②属活动性③顺序时,④华雪⑤同学把⑥两根绕成螺旋状的洁净铜丝分别浸入硫酸铝溶
液、硝酸银溶液中,过一会儿取出:
(1)铜丝浸入硫酸铝溶液中,可观察到的现象是: 。
(2)铜丝浸入硝酸银溶液中,可观察到铜丝上有 色物质生成,溶液逐渐变成蓝
色。(3)铜丝浸入硝酸银溶液中,离子数目减少的是 ,离子数目增加的是 。
(4)根据上述实验所观察到的现象,华雪同学 (填“能”或者“不能”)证明
铝、铜、银的金属活动性顺序Al>Cu>Ag
23.(5分)氧化锌软膏可用于急性或亚急性皮炎、湿疹、痱子及轻度、小面积的皮肤溃
疡。闪锌矿(主要成分为ZnS)是含锌的主要矿物质之一,高温煅烧闪锌矿生成氧化锌
和SO ,以氧化锌产品为原料制备纯氧化锌的生产工艺流程如图:
2
(1)已知A为硫酸锌和硫酸钠的混合物,则滤渣2的化学式为 。
(2)上述步骤中,步骤 的操作是 (填操作名称)。
(3)在上述步骤中,步⑥骤 发生的反应属于分解反应。
(4)步骤 中发生的反应化学方程式为 (提示:ZnO与酸反应和Fe O 与酸反
2 3
应类似)。④
三、解答题(2小题,共10分)
24.(4分)请用所学的知识回答下列问题:
(1)量取液体时,如果视线没有与量筒内无色液体凹液面的最低处保持水平,而是采
用俯视的方法,将会对读数产生什么影响?
(2)为什么菜刀、镰刀、锤子等用铁制而不是铝制?
25.(6分)在汽油中加入适量的乙醇(C H OH)作为汽车燃料(车用乙醇汽油),可适
2 5
当节省石油资源,并在一定程度上减少汽车尾气的污染。请回答下列问题:
(1)乙醇完全燃烧的化学方程式为 。
(2)二氧化碳和水在一定条件下可发生反应,若反应属于化合反应,则在反应后的溶
液中滴加紫色石蕊溶液,溶液呈 色:若反应生成了葡萄糖,则反应条件为
。
(3)C H OH在物质的分类上属于 。
2 5
A.化合物 B.氧化物 C.碱 D.有机物(4)甲醇(CH OH)与乙醇 (填“属于”或“不属于”)同一种物质。
3
四、实验探究题(2小题,共18分)
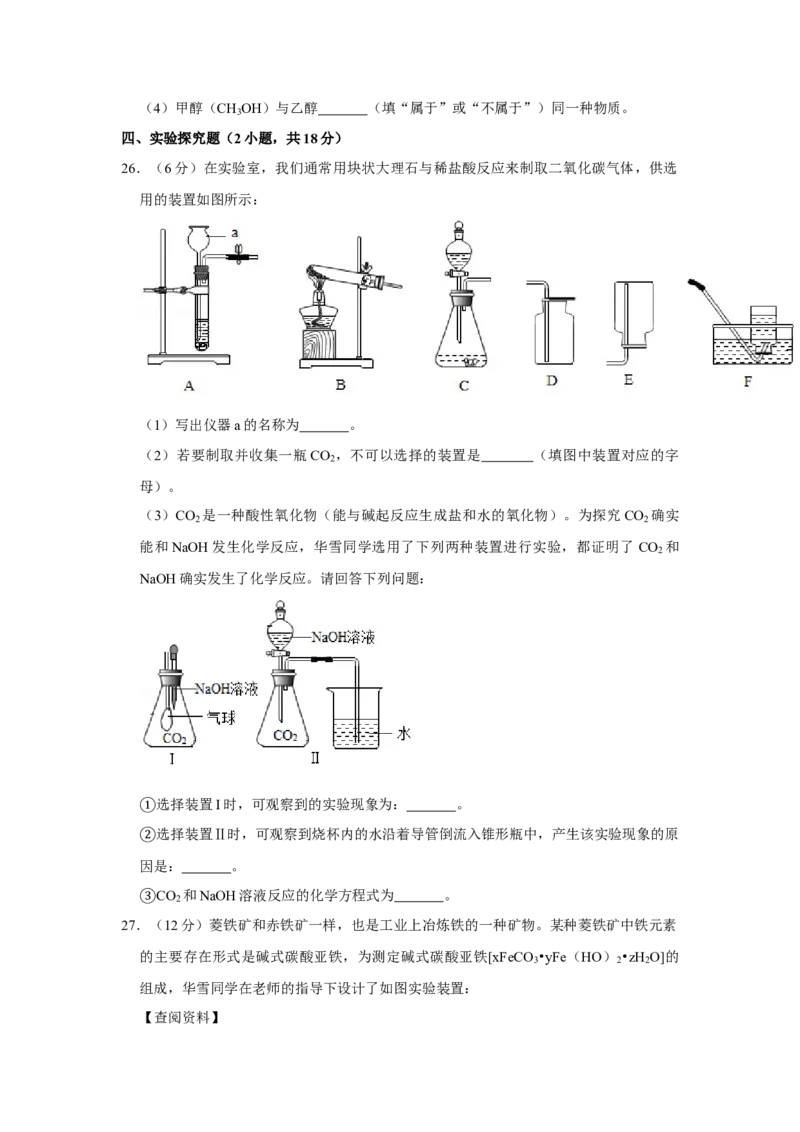
26.(6分)在实验室,我们通常用块状大理石与稀盐酸反应来制取二氧化碳气体,供选
用的装置如图所示:
(1)写出仪器a的名称为 。
(2)若要制取并收集一瓶CO ,不可以选择的装置是 (填图中装置对应的字
2
母)。
(3)CO 是一种酸性氧化物(能与碱起反应生成盐和水的氧化物)。为探究CO 确实
2 2
能和NaOH发生化学反应,华雪同学选用了下列两种装置进行实验,都证明了 CO 和
2
NaOH确实发生了化学反应。请回答下列问题:
选择装置I时,可观察到的实验现象为: 。
①选择装置Ⅱ时,可观察到烧杯内的水沿着导管倒流入锥形瓶中,产生该实验现象的原
②因是: 。
CO 和NaOH溶液反应的化学方程式为 。
2
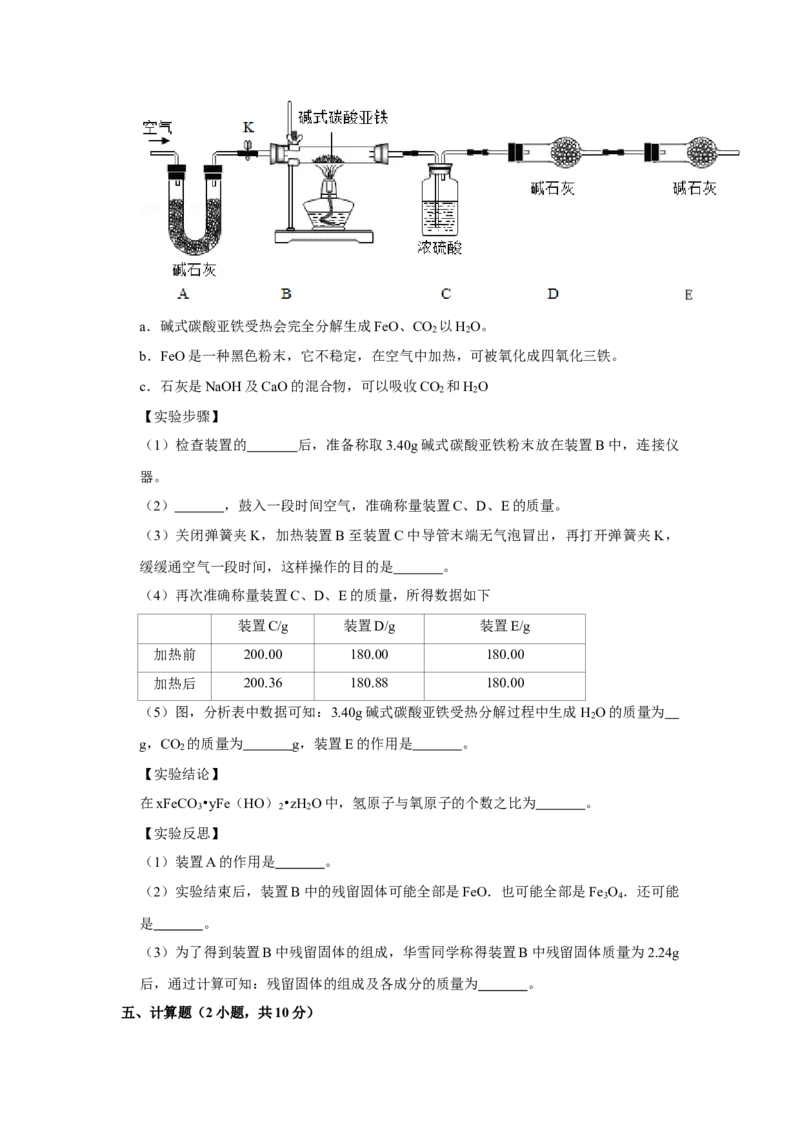
27.③(12分)菱铁矿和赤铁矿一样,也是工业上冶炼铁的一种矿物。某种菱铁矿中铁元素
的主要存在形式是碱式碳酸亚铁,为测定碱式碳酸亚铁[xFeCO •yFe(HO) •zH O]的
3 2 2
组成,华雪同学在老师的指导下设计了如图实验装置:
【查阅资料】a.碱式碳酸亚铁受热会完全分解生成FeO、CO 以H O。
2 2
b.FeO是一种黑色粉末,它不稳定,在空气中加热,可被氧化成四氧化三铁。
c.石灰是NaOH及CaO的混合物,可以吸收CO 和H O
2 2
【实验步骤】
(1)检查装置的 后,准备称取3.40g碱式碳酸亚铁粉末放在装置B中,连接仪
器。
(2) ,鼓入一段时间空气,准确称量装置C、D、E的质量。
(3)关闭弹簧夹K,加热装置B至装置C中导管末端无气泡冒出,再打开弹簧夹K,
缓缓通空气一段时间,这样操作的目的是 。
(4)再次准确称量装置C、D、E的质量,所得数据如下
装置C/g 装置D/g 装置E/g
加热前 200.00 180.00 180.00
加热后 200.36 180.88 180.00
(5)图,分析表中数据可知:3.40g碱式碳酸亚铁受热分解过程中生成H O的质量为
2
g,CO 的质量为 g,装置E的作用是 。
2
【实验结论】
在xFeCO •yFe(HO) •zH O中,氢原子与氧原子的个数之比为 。
3 2 2
【实验反思】
(1)装置A的作用是 。
(2)实验结束后,装置B中的残留固体可能全部是FeO.也可能全部是Fe O .还可能
3 4
是 。
(3)为了得到装置B中残留固体的组成,华雪同学称得装置B中残留固体质量为2.24g
后,通过计算可知:残留固体的组成及各成分的质量为 。
五、计算题(2小题,共10分)28.(4分)超市购物小票上含有BPA(双酚A),网上流传消费者接触小票会致癌。我
国规定:超市购物小票上双酚A的含量应不超过0.6mg/Kg.按照这个标准,收银员即
使每天接触小票10个小时,双酚A通过接触进入人体的量也不会比安全剂量低几十倍。
因此,普通消费者一天接触几张购物小票,致癌概率是完全可以忽略不计的。
(1)双酚A的化学式为C H O ,其相对分子质量为 。
15 16 2
(2)若每张超市购物小票的质量为 5g,则其中含有双酚 A 的质量应不能超过
mg才能符合国家标准。
29.(6分)在锥形瓶中加入80.0g质量分数为10%的硫酸铜溶液,塞好橡胶塞。将几根铁
钉用砂纸打磨干净后在天平上称得质量为 56.0g,再将盛有硫酸铜溶液的锥形瓶和铁钉
一起放在天平上称量,记录所称得质量m .将上述铁钉浸到硫酸铜溶液中,待反应一
1
段时间后溶液颜色改变时,将盛有硫酸铜溶液和锥形瓶放在天平上称量,记录所称的质
量为m 。
2
(1)m m (填“>”或“=”或“<”)。
1 2
(2)锥形瓶的质量为 (用含m 或m 的代数式表示)。
1 2
(3)若硫酸铜反应完全,求此时所得溶液的质量(写出计算结果)。