文档内容
广西桂林市2015年中考化学试卷
一、选择题(共20小题,每小题2分,满分40分)
1. 6月5日为“世界环境日”,今年我国的主题是“践行绿色生活”.下列做法符合这一主题的是( )
A.倡导使用节能灯 B.使用一次性筷子
C.随意排放生活污水 D.随便丢弃废电池
2.下列元素属于金属元素的是( )
A.氦 B.硫 C.锰 D.溴
3.潜水员长时间潜水,应携带的物质是( )
A.氮气 B.氧气 C.稀有气体 D.二氧化碳
4.下列变化中,发生了化学变化的是( )
A.玻璃破碎 B.饭菜变馊 C.酒精挥发 D.冰雪融化
5.(2分)(2015•桂林)下列食物中,富含蛋白质的是( )
A.果冻 B.玉米 C.桃子 D.鸡蛋
6.(2分)(2015•桂林)下列物品所含的主要材料,不属于合成材料的是( )
A.涤纶衣 B.塑料杯 C.铁桶 D.尼龙袜
7.(2分)(2015•桂林)在实验室用高锰酸钾制氧气的实验中,必需的仪器是( )
A. B. C. D.
蒸发皿
石棉网
烧杯
试管
8.(2分)(2015•桂林)下列物质可用作磷肥的是( )
A.尿素 B.硝酸钠 C.磷矿粉 D.硫酸钾
9.(2分)(2015•桂林)Cl的原子结构示意图为 ,下列关于Cl的说法错误的是( )
A.电子层数是3 B.核内质子数是17
C.最外层电子数是7 D.在化学反应中易失电子
10.(2分)(2015•桂林)SiO 中“Si”的化合价为( )
2
A.+4 B.+3 C.+2 D.+1
11.(2分)(2015•桂林)图中所示的实验操作中,正确的是( )
A. B.
给液体加热
放入铁钉C. D.
用灯帽熄灭酒精灯
测溶液的酸碱度
12.(2分)(2015•桂林)下列物质中能使紫色石蕊试液变红的是( )
A.二氧化碳 B.食盐水 C.烧碱 D.熟石灰
13.(2分)(2015•桂林)区分稀硫酸和稀盐酸,不能使用的试剂是( )
A.Ba(NO) B.BaCl C.Ba(OH) D.NaCl
3 2 2 2
14.(2分)(2015•桂林)要配制100g5%的蔗糖溶液,以下操作会导致所配溶液的浓度偏低的是( )
A.称取5g含杂质的蔗糖
B.用量筒量取90mL水
C.搅拌后玻璃棒上有液体残留
D.量筒中的水未完全倒入烧杯中
15.(2分)(2015•桂林)在试管中加入少量碘粒,再加入适量的汽油,振荡,静置,观察到的现象为( )
A. B. C. D.
16.(2分)(2015•桂林)关于反应2KClO 2KCl+3O↑的说法,错误的是( )
3 2
A.MnO 做该反应的催化剂 B.MnO 的质量随着反应减少
2 2
C.MnO 加快KClO 的分解速率 D.MnO 的化学性质没有改变
2 3 2
17.(2分)(2015•桂林)下列物质间的转化不能一步实现的是( )
A.Fe→FeO B.C→CO C.NaNO→NaCl D.Mg→MgO
3 4 2 3
18.(2分)(2015•桂林)下列所用试剂能达到实验目的是( )
实验目的 试剂
A 鉴别浓硫酸与稀硫酸 木条
B 鉴别氯化钡溶液与氯化钙溶液碳酸钾溶液
C 除去氮气中的氧气 水
D 除去二氧化碳中的一氧化碳 氢氧化钠溶液
A.A B.B C.C D.D
19.(2分)(2015•桂林)下列关于复分解反应的说法正确的是( )
A.中和反应不属于复分解反应 B.反应物必须都溶于水
C.反应物一定有酸 D.生成物一定有盐
20.(2分)(2015•桂林)a、b、c三种酸分别与足量的金属Mg充分反应,生成等质量的H,反应消耗a、b、c的
2
分子数目之比为3:6:2.下列关于a、b、c的推理合理的是(HX、HY、HZ分别表示三种酸)( )
2 3
A.a、b、c三种酸溶液中的H原子数目:c>a>b
B.a、b、c与金属Mg反应的速率:b>a>c
C.a、b、c的相对分子质量:b<a<cD.a、b、c可能分别为HY、HX、HZ
2 3
二、填空题(共5小题)
21.(4分)(2015•桂林)请用化学符号填空
(1)钾离子 ;(2)2个磷原子
(3)甲烷 ;(4)二氧化硫 .
22.(6分)(2015•桂林)现有①金刚石、②氯化钠、③酒精、④生石灰、⑤小苏打、⑥一氧化碳,从中选择恰当
的物质序号填空
(1) 用于治疗胃酸过多;(2) 用于配制生理盐水;(3) 用作食品干
燥剂;
(4) 用于刻画玻璃;(5) 用于冶炼金属;(6) 用作内燃机的燃料.
23.(4分)(2015•桂林)人类的生产和生活都离不开金属
(1)生铁和钢中最主要的元素是 ;用铝壶烧水主要利用铝具有良好的 性.
(2)铝制品有良好的抗腐蚀性,其原因是在空气中铝的表面易形成致密的 .
(3)验证Zn、Cu、Ag的金属活动性顺序,可选择的试剂是 (填字母序号)
A.Zn、Ag、CuCl 溶液 B.Cu、Ag、ZnSO 溶液
2 4
C.Zn、Cu、AgNO 溶液 D.Zn、Cu、Ag、稀硫酸.
3
24.(6分)(2015•桂林)A在B中充分燃烧生成C和D,A、B、C、D的微观示意图如下所示
物质 A B C D
分子示意图
看图回答:
(1)属于氧化物的是 (填字母序号)
(2)A中氮、氢原子数之比为 ,氮、氢元素质量之比为 .
(3)A在B中充分燃烧的化学方程式为 ,基本反应类型为 .
25.(6分)(2015•桂林)水是宝贵的自然资源
(1)下列常用净水方法,可以降低水的硬度的是 (填字母序号)
A.过滤 B.吸附 C.蒸馏
(2)图中表示NaCl、KNO、MgSO 三种物质的溶解度曲线.请回答:
3 4
①t℃时,饱和溶液的溶质质量分数相同的两种物质是 .
1
②t℃时,将40g KNO 放入60g水中,充分溶解后,所得溶液的质量为 g.
2 3
③t℃时,溶解度最大的是 .
3
④t℃时,其它条件不变,把MgSO 饱和溶液升温到t℃,观察到的现象是 .
4 4 5
⑤NaCl溶液中含有少量KNO 杂质,提纯的方法是 (填“蒸发溶剂”或“冷却热饱和溶液”)
3三、解答题(共5小题,满分34分)
26.(6分)(2015•桂林)淀粉是一种白色不溶于水的粉末.淀粉在人体内经酶的催化作用,与水发生一系列
反应,最终产物是葡萄糖.葡萄糖在酶的催化作用下缓慢氧化生成二氧化碳和水,并放出能量
(1)淀粉的组成元素是氧、 、 .
(2)列举淀粉的两个物理性质: 、 .
(3)写出葡糖糖在人体内缓慢氧化的化学方程式: .
27.(6分)(2015•桂林)甲、乙、丙、丁都是初中化学中最常见的物质,已知它们由H、O、C、Cl、Na、Ca 6种元
素中的2种或3种组成,丙与甲、乙、丁都能发生反应.将这四种物质的溶液按图所示相互滴加,现象为:①
产生白色沉淀;②有气泡冒出;③无明显现象
(1)甲、乙、丙、丁都属于 (填“单质”或“化合物”).
(2)试管②中产生的气体是 (填化学式).
(3)试管①中反应的化学方程式是 .
(4)向试管③滴加的溶液溶质可能是 (填化学式,下同)或 .
28.(6分)(2015•桂林)根据下列实验示意图,回答问题.
(1)图1铜片与黄铜片相互刻画,铜片表面留下明显划痕,说明铜片比黄铜片的硬度 (填
“大”或“小”)
(2)图2煤粉和木屑最先燃烧的是 ,燃烧的顺序说明燃烧的条件之一是 .
(3)在实验室中用图3装置制取CO,反应的化学方程式是 .
2
(4)图4、图5为两种验满CO 的方法,其中正确的操作是图 (填数字序号)
2
29.(9分)(2015•桂林)在一次化学实验中,同学们将饱和CuSO 溶液逐滴加到5mL饱和NaOH溶液中,观察
4
到以下异常实验现象:
实验序号 滴加CuSO 溶液的量 实验现象
4
① 第1﹣6滴 产生蓝色沉淀,但振荡后沉淀消失,形成亮蓝色溶液
② 第7﹣9滴 产生蓝色沉淀,且沉淀逐渐增多.振荡后沉淀不消失,很快沉淀逐渐变
黑色
在实验①中同学们根据所学初中化学知识判断蓝色沉淀是Cu(OH),请你写出生成蓝色沉淀的化学方程式
2
.
实验①中蓝色沉淀为什么消失?同学们继续进行如下探究.
【查阅资料】Ⅰ.Cu(OH) 在室温下稳定,70℃﹣80℃时可脱水分解生成CuO
2
Ⅱ.酮酸钠[NaCu(OH)]溶于水,溶液呈亮蓝色
2 4
【猜想与讨论】小陶认为蓝色沉淀消失可能是Cu(OH)发生了分解.其他同学一致否定了他的猜测,理由是
2
同学们交流讨论后,提出以下两种猜想.猜想一:少许Cu(OH) 可溶于足量水中.
2
猜想二:Cu(OH) 可在足量NaOH浓溶液中溶解,溶液呈亮蓝色
2
【实验探究】为验证猜想,同学们用Cu(OH)粉末(其它试剂可任选)设计如下实验.请你填写表中的空格.
2
实验序号 实验方法与操作 实验现象 结论
③ 将少许Cu(OH)粉末加到5mL蒸馏水中,充分振荡 猜想一错误
2
④ 猜想二正确
【结论与反思】(1)根据实验,并进一步查阅资料知道,Cu(OH)在NaOH溶液中溶解生成NaCu(OH),反应的
2 2 4
化学方程式是
(2)根据实验可知饱和CuSO 溶液与饱和NaOH溶液的反应是放热反应,依据的实验现象是 .
4
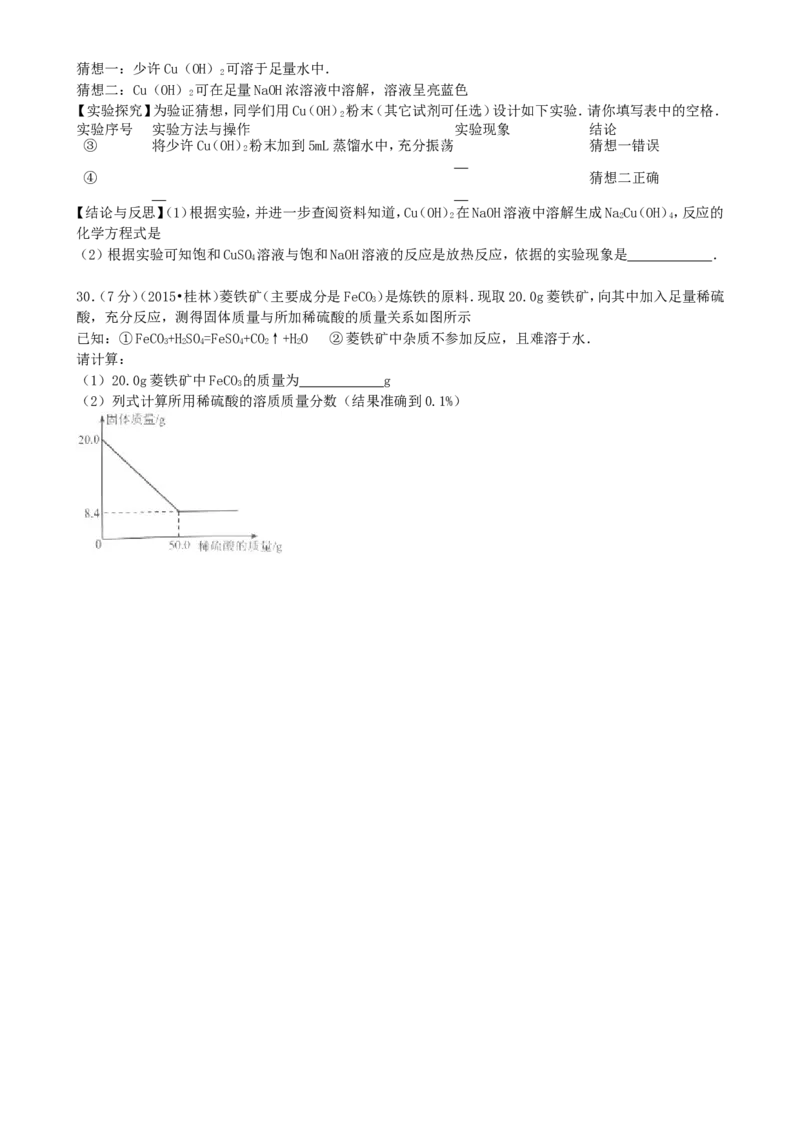
30.(7分)(2015•桂林)菱铁矿(主要成分是FeCO)是炼铁的原料.现取20.0g菱铁矿,向其中加入足量稀硫
3
酸,充分反应,测得固体质量与所加稀硫酸的质量关系如图所示
已知:①FeCO+HSO=FeSO+CO↑+HO ②菱铁矿中杂质不参加反应,且难溶于水.
3 2 4 4 2 2
请计算:
(1)20.0g菱铁矿中FeCO 的质量为 g
3
(2)列式计算所用稀硫酸的溶质质量分数(结果准确到0.1%)参考答案
1-10、ACBBD CDCDA 11-20、CADAB BCADD
21、(1)K+;(2)2P;(3)CH;(4)SO.
4 2
22、(1)⑤;(2)②;(3)④;(4)①;(5)⑥;(6)③
23、(1)铁元素 导热 (2)氧化铝保护膜 (3)A
24、(1)C;(2)1:3,14:3;(3)4NH+3O 2N+6HO,置换反应
3 2 2 2
25、①NaCl、KNO;②84;③KNO;④析出晶体;⑤蒸发溶剂
3 3
26、(1)碳;氢;(2)白色粉末;不溶于水;(3)CH O+6O 6CO+6HO
6 12 6 2 2 2
27、(1)化合物;(2)CO;(3)Ca(OH)+NaCO=CaCO↓+2NaOH;
2 2 2 3 3
(4)NaOH,Ca(OH).
2
28、1)小
(2)木屑 温度达到着火点
(3)CaCO+2HCl=CaCl+2HO+CO↑;
3 2 2 2
(4)4
29、CuSO+2NaOH=Cu(OH)↓+NaSO;
4 2 2 4
沉淀消失,形成亮蓝色溶液,而氢氧化铜分解产生的是黑色固体(合理即可);
实验序号 实验方法与操作 实验现象 结论
③ 将少许Cu(OH)粉末加到5mL蒸馏水中,充分振荡 猜想一错误
2
沉淀不消失
④ 猜想二正确
将少许Cu(OH) 粉末加到NaOH浓溶液中,充分振沉淀消失,溶液变成亮蓝
2
荡 色
Cu(OH)+2NaOH=NaCu(OH);
2 2 4
资料Ⅰ显示Cu(OH)在室温下稳定,70℃﹣80℃时可脱水分解生成CuO,而表格1可知随着氢氧化钠溶液的
2
滴加,观察到产生蓝色沉淀,且沉淀逐渐增多.振荡后沉淀不消失,很快沉淀逐渐变黑色(合理即可).
30、解:(1)20.0g菱铁矿中FeCO 的质量为:20.0g﹣8.4g=11.6g,
3
故填:11.6.
(2)设硫酸的质量为x,
FeCO+HSO=FeSO+CO↑+HO,
3 2 4 4 2 2
116 98
11.6g x
= ,
x=9.8g,
所用稀硫酸的溶质质量分数为: ×100%=19.6%,
答:所用稀硫酸的溶质质量分数为19.6%.