文档内容
五年(2021-2025)高考化学真题分类汇编
专题20 电解质溶液曲线分析
考向 五年考情(2021-2025) 命题趋势
水溶液中离子平衡是高考选择题必考内容,
2025·云南卷、2024·湖南卷、2023·湖南
考点一 滴定 可以分为两个大的方向,一是水溶液中的离
卷、2021·浙江
曲线分析 子平衡及其应用;二是电解质溶液曲线分
2021·湖南卷
析,该考查方向一直是高考的考查重点,也
是很多卷区选择题的必考题型,涉及电离平
2025·山东卷、2025·河南卷、2025·甘肃
衡常数、水解平衡常数、溶度积的计算,指
卷、2025·湖北卷、2024·浙江6月卷、
考点二 分布 示剂的选择,对水的电离平衡的影响,溶液
2024·山东卷、2024·新课标卷、2023·北京
曲线分析 中粒子浓度的大小关系,以及外界条件对电
卷、2023·湖北卷、2023·福建卷、2022·辽
离平衡、水解平衡、溶解平衡的影响等。此
宁卷、2021·山东卷
类题目考查的内容既与盐的水解有关,又与
弱电解质的电离平衡有关。题目不仅偏重考
2025·陕晋青宁卷、2025·黑吉辽蒙卷、
查粒子的浓度大小顺序,而且还侧重溶液中
考点三 对数 2025·河北卷、2025·安徽卷、2023·海南
的各种守恒(电荷守恒、物料守恒、质子守恒)
图像分析 卷、2023·山东卷、2022·山东卷、2021·全
关系的考查,从而使题目具有一定的综合
国乙卷
性、灵活性和技巧性。
考点 一 滴定曲线分析
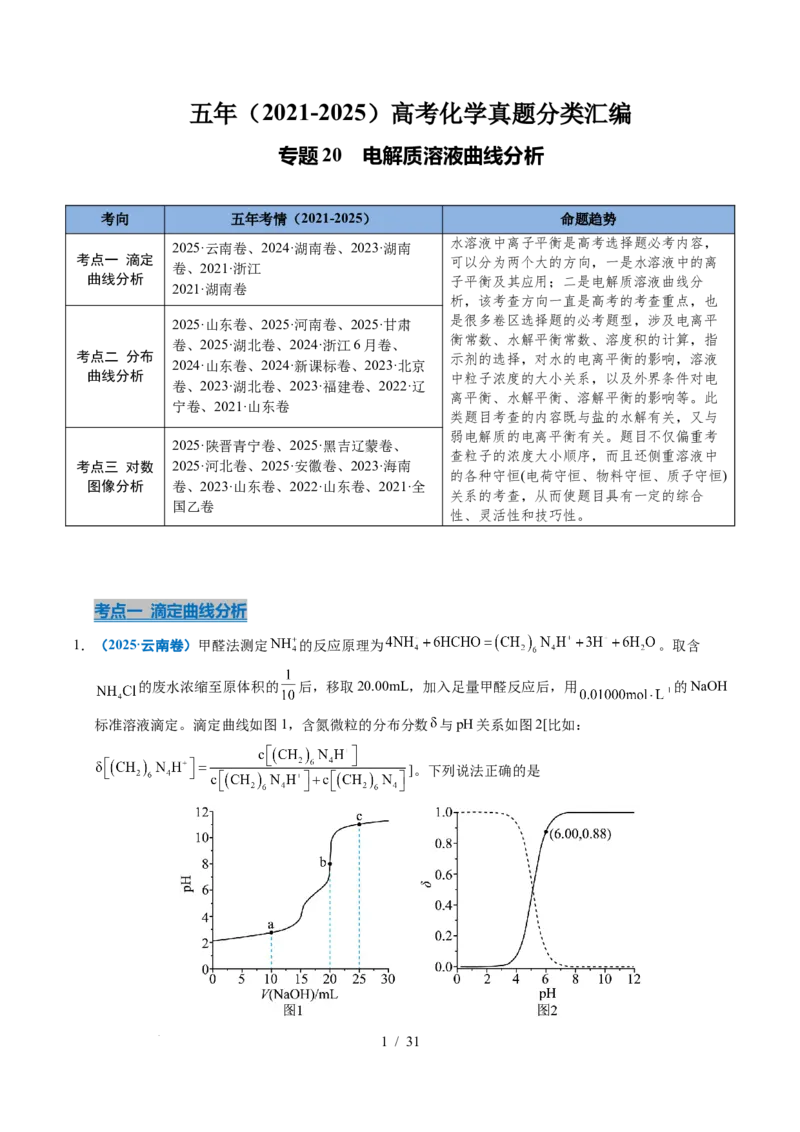
1.(2025·云南卷)甲醛法测定 的反应原理为 。取含
的废水浓缩至原体积的 后,移取20.00mL,加入足量甲醛反应后,用 的NaOH
标准溶液滴定。滴定曲线如图1,含氮微粒的分布分数 与pH关系如图2[比如:
]。下列说法正确的是
1 / 31
学科网(北京)股份有限公司A.废水中 的含量为
B.c点:
C.a点:
D. 的平衡常数
【答案】D
【详解】A.由图1中的信息可知,当加入NaOH标准溶液的体积为20.00mL时到达滴定终点,由关系
式 ~[ ]~4 可知,由于待测液的体积和标准溶液的体积相同,因此,浓缩后
的20.00mL溶液中 ,则原废水中
,因此,废水中 的含量为
,A错误;
B.c 点加入NaOH标准溶液的体积过量,且只过量了 ,由电荷守恒可知,
,浓缩后的废水中 的浓度是NaOH标准溶液
浓度的4倍, 和 均不参与离子反应,可以估算c点 ,
,B错误;
C. 在溶液中水解使溶液显酸性,类比 可知 在溶液中与水作用发生电离而
使溶液显碱性;a 点为半滴定点,由其纵坐标可知溶液显酸性,说明 的水解作用强于
的电离作用,可知溶液中相关粒子的浓度的大小关系为 ,
C错误;
D.由图1和图2可知,当 时, 占比较高, ,则由氮守恒可
知, ,两种粒子的浓度之比等于其分布分数之比,则
的平衡常数 ,D正
确;
综上所述,本题选D。
2.(2024·湖南卷)常温下 ,向 溶液中缓慢滴入相同浓度
的 溶液,混合溶液中某两种离子的浓度随加入 溶液体积的变化关系如图所示,下列说
法错误的是
2 / 31
学科网(北京)股份有限公司A.水的电离程度:
B.M点:
C.当 时,
D.N点:
【答案】D
【分析】结合起点和终点,向 溶液中滴入相同浓度的 溶液,发生浓度
改变的微粒是 和 ,当 ,溶液中存在的微粒是 ,可知随着甲酸的加
入, 被消耗,逐渐下降,即经过M点在下降的曲线表示的是 浓度的改变,经过M点、N点的
在上升的曲线表示的是 浓度的改变。
【解析】A.M点时, ,溶液中的溶质为 ,仍剩余有
未反应的甲酸,对水的电离是抑制的,N点HCOOH溶液与NaOH溶液恰好反应生成HCOONa,此时
仅存在HCOONa的水解,此时水的电离程度最大,故A正确;
B.M点时, ,溶液中的溶质为 ,根据电荷守恒有
,M点为交点可知 ,联合可得
,故B正确;
C.当 时,溶液中的溶质为 ,根据电荷守恒有
,根据物料守恒 ,联合可得
,故C正确;
D.N点HCOOH溶液与NaOH溶液恰好反应生成HCOONa,甲酸根发生水解,因此
及 观察图中N点可知, ,根据
,可知 ,故D错误;
故答案选D。
3 / 31
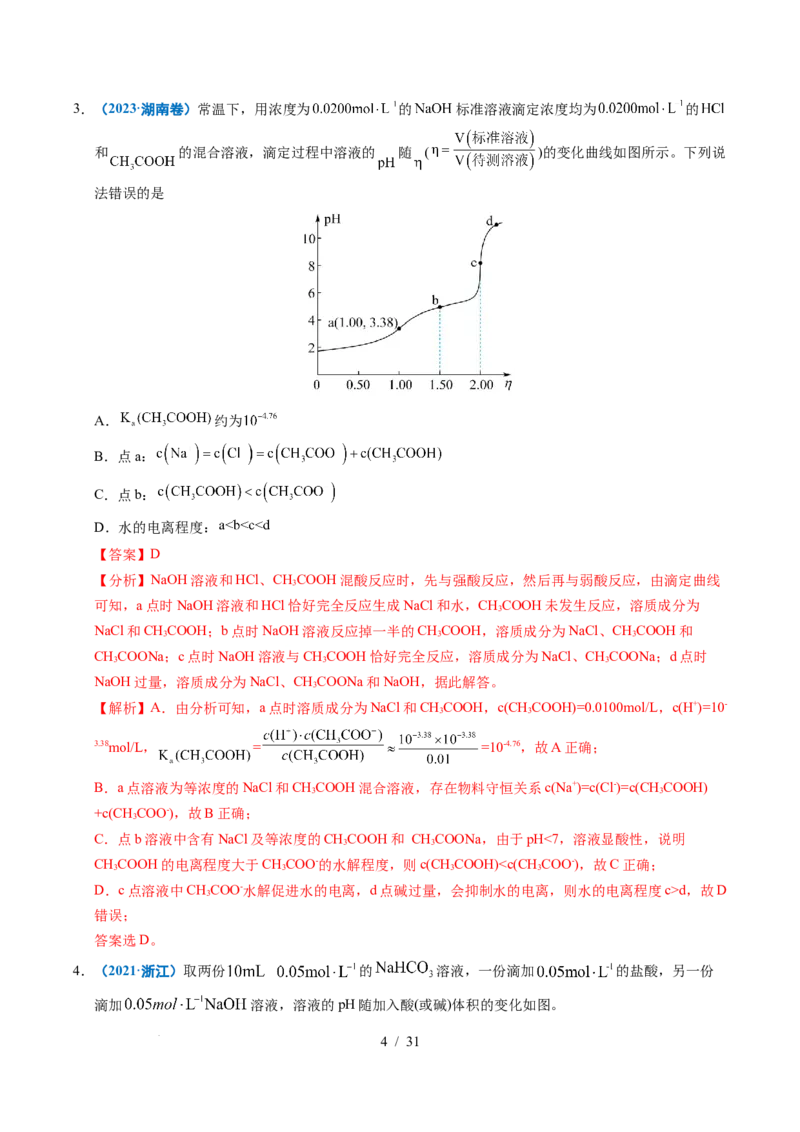
学科网(北京)股份有限公司3.(2023·湖南卷)常温下,用浓度为 的 标准溶液滴定浓度均为 的
和 的混合溶液,滴定过程中溶液的 随 ( )的变化曲线如图所示。下列说
法错误的是
A. 约为
B.点a:
C.点b:
D.水的电离程度:
【答案】D
【分析】NaOH溶液和HCl、CHCOOH混酸反应时,先与强酸反应,然后再与弱酸反应,由滴定曲线
3
可知,a点时NaOH溶液和HCl恰好完全反应生成NaCl和水,CHCOOH未发生反应,溶质成分为
3
NaCl和CHCOOH;b点时NaOH溶液反应掉一半的CHCOOH,溶质成分为NaCl、CHCOOH和
3 3 3
CHCOONa;c点时NaOH溶液与CHCOOH恰好完全反应,溶质成分为NaCl、CHCOONa;d点时
3 3 3
NaOH过量,溶质成分为NaCl、CHCOONa和NaOH,据此解答。
3
【解析】A.由分析可知,a点时溶质成分为NaCl和CHCOOH,c(CHCOOH)=0.0100mol/L,c(H+)=10-
3 3
3.38mol/L, = =10-4.76,故A正确;
B.a点溶液为等浓度的NaCl和CHCOOH混合溶液,存在物料守恒关系c(Na+)=c(Cl-)=c(CH COOH)
3 3
+c(CH COO-),故B正确;
3
C.点b溶液中含有NaCl及等浓度的CHCOOH和 CHCOONa,由于pH<7,溶液显酸性,说明
3 3
CHCOOH的电离程度大于CHCOO-的水解程度,则c(CHCOOH)d,故D
3
错误;
答案选D。
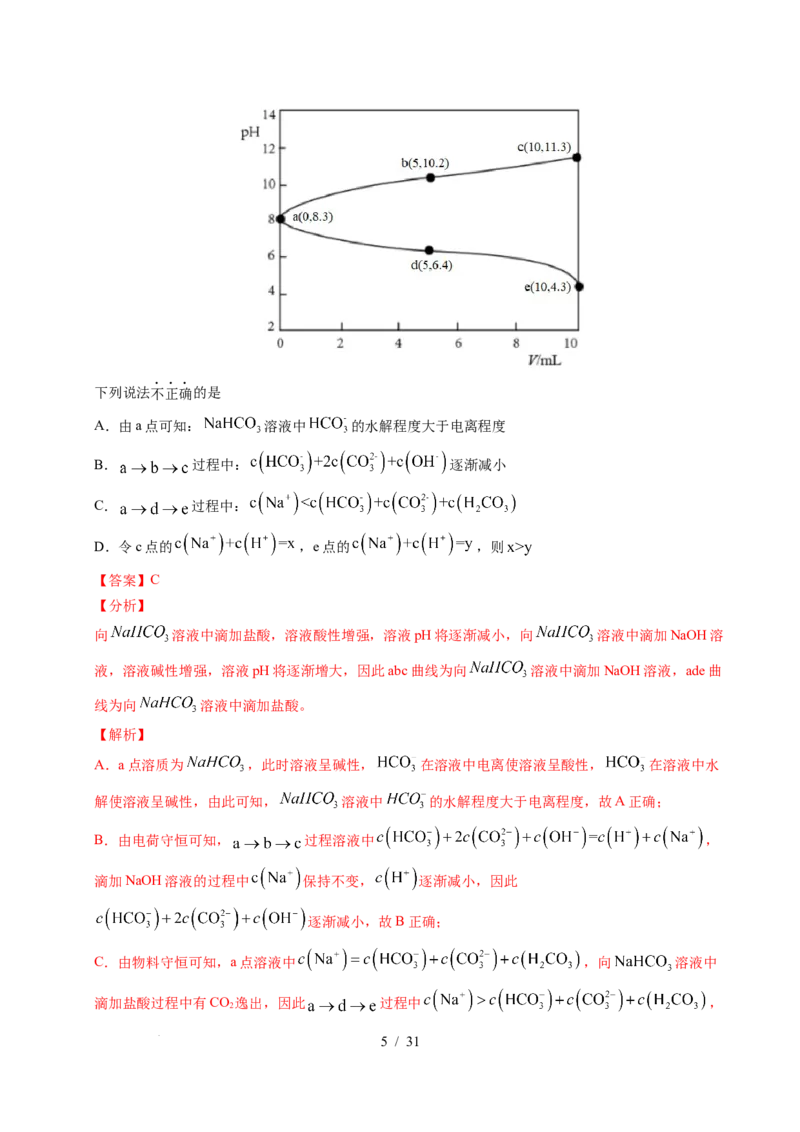
4.(2021·浙江)取两份 的 溶液,一份滴加 的盐酸,另一份
滴加 溶液,溶液的pH随加入酸(或碱)体积的变化如图。
4 / 31
学科网(北京)股份有限公司下列说法不正确的是
A.由a点可知: 溶液中 的水解程度大于电离程度
B. 过程中: 逐渐减小
C. 过程中:
D.令c点的 ,e点的 ,则
【答案】C
【分析】
向 溶液中滴加盐酸,溶液酸性增强,溶液pH将逐渐减小,向 溶液中滴加NaOH溶
液,溶液碱性增强,溶液pH将逐渐增大,因此abc曲线为向 溶液中滴加NaOH溶液,ade曲
线为向 溶液中滴加盐酸。
【解析】
A.a点溶质为 ,此时溶液呈碱性, 在溶液中电离使溶液呈酸性, 在溶液中水
解使溶液呈碱性,由此可知, 溶液中 的水解程度大于电离程度,故A正确;
B.由电荷守恒可知, 过程溶液中 ,
滴加NaOH溶液的过程中 保持不变, 逐渐减小,因此
逐渐减小,故B正确;
C.由物料守恒可知,a点溶液中 ,向 溶液中
滴加盐酸过程中有CO 逸出,因此 过程中 ,
2
5 / 31
学科网(北京)股份有限公司故C错误;
D.c点溶液中 =(0.05+10-11.3)mol/L,e点溶液体积增大1倍,此时溶液中
=(0.025+10-4)mol/L,因此x>y,故D正确;
综上所述,说法不正确的是C项,故答案为C。
5.(2021·湖南)常温下,用 的盐酸分别滴定20.00mL浓度均为 三种一元
弱酸的钠盐 溶液,滴定曲线如图所示。下列判断错误的是
A.该 溶液中:
B.三种一元弱酸的电离常数:
C.当 时,三种溶液中:
D.分别滴加20.00mL盐酸后,再将三种溶液混合:
【答案】C
【分析】
由图可知,没有加入盐酸时,NaX、NaY、NaZ溶液的pH依次增大,则HX、HY、HZ三种一元弱酸
的酸性依次减弱。
【解析】
A.NaX为强碱弱酸盐,在溶液中水解使溶液呈碱性,则溶液中离子浓度的大小顺序为c(Na+)>c(X-)>
c(OH-)>c(H+),故A正确;
B.弱酸的酸性越弱,电离常数越小,由分析可知,HX、HY、HZ三种一元弱酸的酸性依次减弱,则
三种一元弱酸的电离常数的大小顺序为K(HX)>K (HY)>K(HZ),故B正确;
a a a
C.当溶液pH为7时,酸越弱,向盐溶液中加入盐酸的体积越大,酸根离子的浓度越小,则三种盐溶
液中酸根的浓度大小顺序为c(X-)>c(Y-)>c(Z-),故C错误;
D.向三种盐溶液中分别滴加20.00mL盐酸,三种盐都完全反应,溶液中钠离子浓度等于氯离子浓度,
将三种溶液混合后溶液中存在电荷守恒关系c(Na+)+ c(H+)= c(X-)+c(Y-)+c(Z-)+ c(Cl-)+ c(OH-),由
c(Na+)= c(Cl-)可得:c(X-)+c(Y-)+c(Z-)= c(H+)—c(OH-),故D正确;
故选C。
6 / 31
学科网(北京)股份有限公司考点 二 分布曲线分析
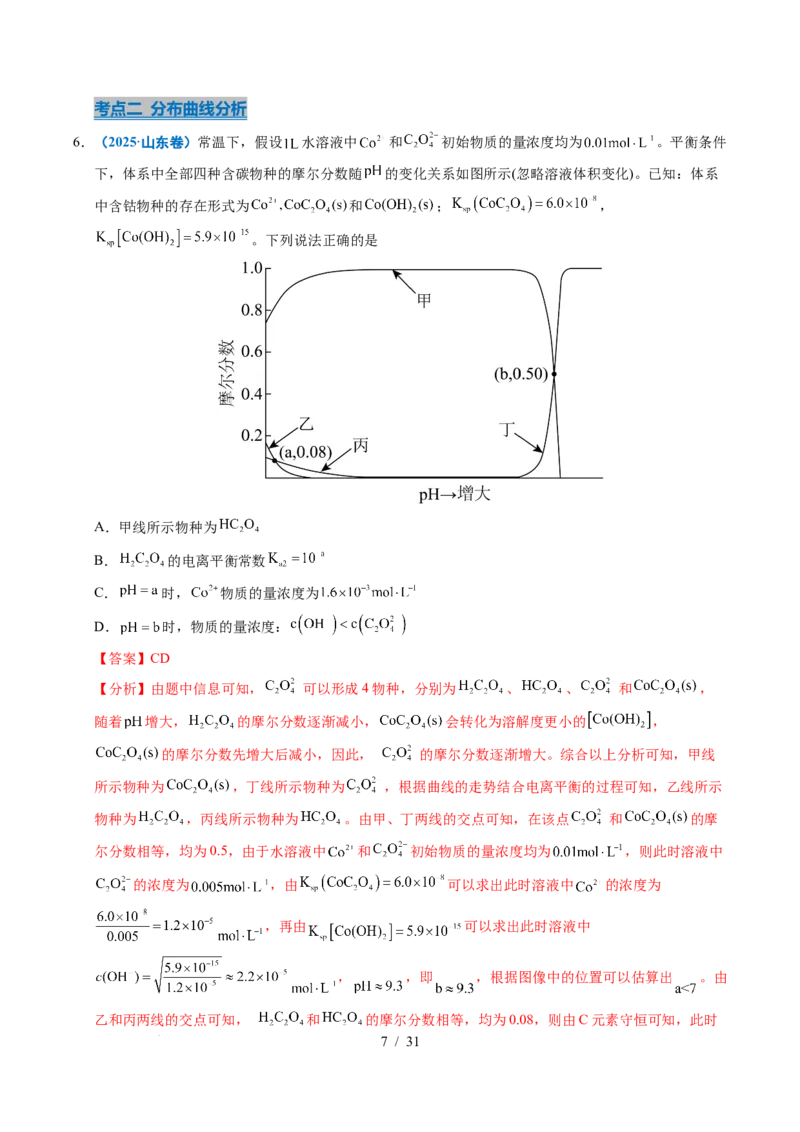
6.(2025·山东卷)常温下,假设 水溶液中 和 初始物质的量浓度均为 。平衡条件
下,体系中全部四种含碳物种的摩尔分数随 的变化关系如图所示(忽略溶液体积变化)。已知:体系
中含钴物种的存在形式为 和 ; ,
。下列说法正确的是
A.甲线所示物种为
B. 的电离平衡常数
C. 时, 物质的量浓度为
D. 时,物质的量浓度:
【答案】CD
【分析】由题中信息可知, 可以形成4物种,分别为 、 、 和 ,
随着 增大, 的摩尔分数逐渐减小, 会转化为溶解度更小的 ,
的摩尔分数先增大后减小,因此, 的摩尔分数逐渐增大。综合以上分析可知,甲线
所示物种为 ,丁线所示物种为 ,根据曲线的走势结合电离平衡的过程可知,乙线所示
物种为 ,丙线所示物种为 。由甲、丁两线的交点可知,在该点 和 的摩
尔分数相等,均为0.5,由于水溶液中 和 初始物质的量浓度均为 ,则此时溶液中
的浓度为 ,由 可以求出此时溶液中 的浓度为
,再由 可以求出此时溶液中
, ,即 ,根据图像中的位置可以估算出 。由
乙和丙两线的交点可知, 和 的摩尔分数相等,均为0.08,则由C元素守恒可知,此时
7 / 31
学科网(北京)股份有限公司的摩尔分数为0.84。
【详解】A.由分析可知,甲线所示物种为 ,A不正确;
B.已知 二元中强酸,其酸式盐的水溶液显酸性, 的电离程度大于其水解程度;当溶液
中 与 浓度相等时,溶液显酸性, ,则
,故B不正确;
C. 时, 的摩尔分数为0.84, 的物质的量为
,由水于溶液中 初始物质的量浓度为 ,以Co2+极限
最大浓度估算形成Co(OH) 时所要最小c(OH-)= ,此时溶液呈碱
2
性,应有较多草酸跟,则a点无Co(OH) ,此时Co元素只有两种存在形式:Co2+和CoC O,由Co元素
2 2 4
守恒可得, 的物质的量浓度=0.01mol/L-0.01mol/L×84%= ,C正确;
D.由分析可知 时, 的浓度为 , ,
,D正确;
综上所述,本题选CD。
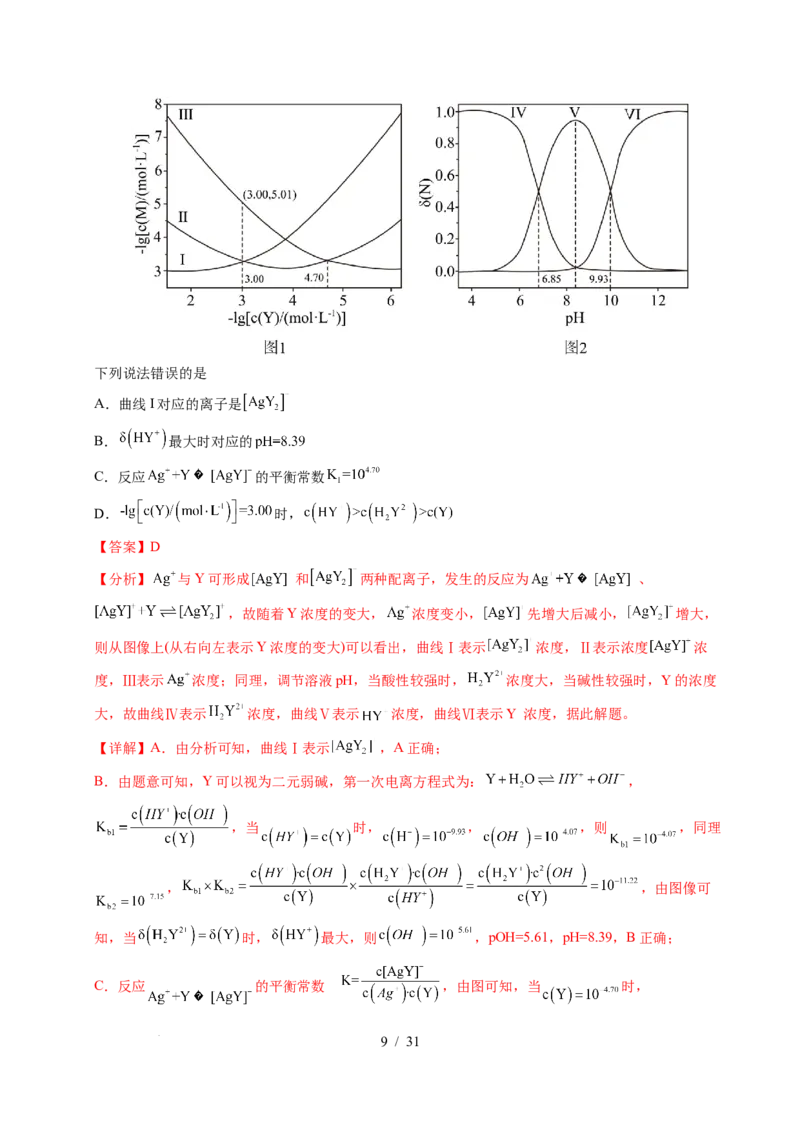
7.(2025·河南卷)乙二胺( ,简写为Y)可结合 转化为 (简写为
) (简写为 )。 与Y可形成 和 两种配离子。室温下向
溶液中加入Y,通过调节混合溶液的 改变Y的浓度,从而调控不同配离子的浓度(忽略体积
变化)。混合溶液中 和Y的初始浓度分别为 和 。
与 的变化关系如图1所示(其中M代表 、 或
),分布系数 与 的变化关系如图2所示(其中N代表Y、 或 )。比如
。
8 / 31
学科网(北京)股份有限公司下列说法错误的是
A.曲线I对应的离子是
B. 最大时对应的
C.反应 的平衡常数
D. 时,
【答案】D
【分析】 与Y可形成 和 两种配离子,发生的反应为 、
,故随着Y浓度的变大, 浓度变小, 先增大后减小, 增大,
则从图像上(从右向左表示Y浓度的变大)可以看出,曲线Ⅰ表示 浓度,Ⅱ表示浓度 浓
度,Ⅲ表示 浓度;同理,调节溶液pH,当酸性较强时, 浓度大,当碱性较强时,Y的浓度
大,故曲线Ⅳ表示 浓度,曲线Ⅴ表示 浓度,曲线Ⅵ表示Y 浓度,据此解题。
【详解】A.由分析可知,曲线Ⅰ表示 ,A正确;
B.由题意可知,Y可以视为二元弱碱,第一次电离方程式为: ,
,当 时, , ,则 ,同理
, ,由图像可
知,当 时, 最大,则 ,pOH=5.61,pH=8.39,B正确;
C.反应 的平衡常数 ,由图可知,当 时,
9 / 31
学科网(北京)股份有限公司,则 ,C正确;
D. 时, , , ,由物料守
恒可知, ,则 ,Y的初
始浓度为 ,由物料守恒得
,代入数据,
,则 ,由图像可知,pH
在8.39-9.93之间,此时 ,D错误;
故选D。
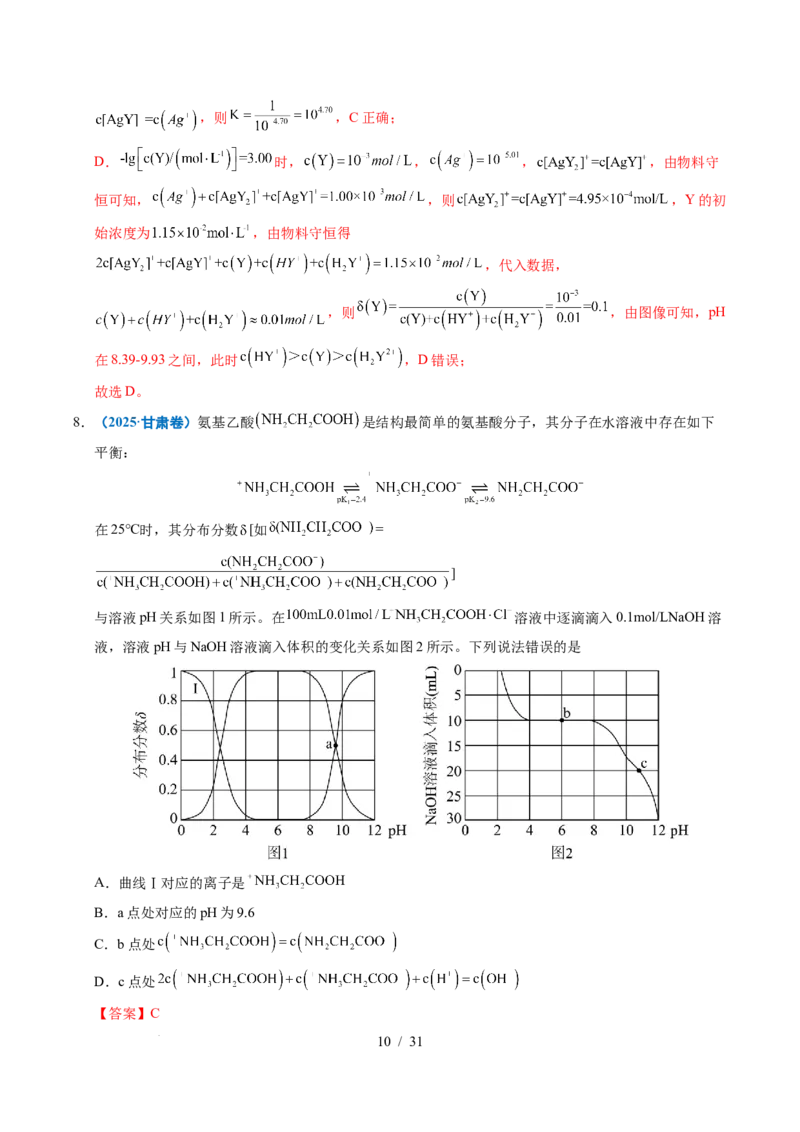
8.(2025·甘肃卷)氨基乙酸 是结构最简单的氨基酸分子,其分子在水溶液中存在如下
平衡:
在25℃时,其分布分数 [如 =
]
与溶液pH关系如图1所示。在 溶液中逐滴滴入0.1mol/LNaOH溶
液,溶液pH与NaOH溶液滴入体积的变化关系如图2所示。下列说法错误的是
A.曲线Ⅰ对应的离子是
B.a点处对应的pH为9.6
C.b点处
D.c点处
【答案】C
10 / 31
学科网(北京)股份有限公司【分析】图1可知,随着pH增大,平衡 右
移,+NH CHCOOH的分布分数减少,+NH CHCOO-先增加后减少,NH CHCOO-最后增加,a点代表
3 2 3 2 2 2
+NH CHCOO-和NH CHCOO-分布分数相等的点;图2中b点滴入NaOH为10mL,
3 2 2 2
和NaOH的物质的量相等,得到+NH CHCOO-,c点 和NaOH
3 2
的物质的量之比为1:2,得到主要粒子为NH CHCOO-。
2 2
【详解】A.根据分析可知,随着pH值增大,+NH CHCOOH的分布分数减少,曲线I代表
3 2
+NH CHCOOH的分布分数,A正确;
3 2
B.a点代表+NH CHCOO-和NH CHCOO-分布分数相等的点,二者浓度相等,Pk =9.6,K =
3 2 2 2 a2 a2
,pH=9.6,B正确;
C.图2中b点滴入NaOH为10mL, 和NaOH的物质的量相等,得到主要离子为
+NH CHCOO-,+NH CHCOO-存在电离和水解,K =10-9.6,K= = ,电离大于水解,则
3 2 3 2 a2 h
,C错误;
D.c点 和NaOH的物质的量之比为1:2,得到主要粒子为NH CHCOO-,根据质子
2 2
守恒,有 ,D正确;
答案选C。
9.(2025·湖北卷)铜(I)、乙腈(简写为L)的某水溶液体系中含铜物种的分布曲线如图。纵坐标(δ)为含铜
物种占总铜的物质的量分数,总铜浓度为 。下列描述正确的是
A. 的
B.当 时,
C.n从0增加到2, 结合L的能力随之减小
D.若 ,则
11 / 31
学科网(北京)股份有限公司【答案】C
【详解】A. 的 ,当图中 时, ,
,由图像可知,此时 ,则 ≠0.27,A错误;
B.当 时,由图像可知, , 可忽略不计,
则, , ,B错误;
C. 结合L的离子方程式为 ,当 时,
,由图像交点可知,随着n变大, 逐渐变大,则K值变小,说明 结合L的能力
随之减小,C正确;
D.若 ,由图像交点可知, , ,
则 ,故 ,D错误;
故选C。
10.(2024·浙江6月卷)室温下, 水溶液中各含硫微粒物质的量分数 随 变化关系如下图[例如
]。已知: 。
下列说法正确的是
A.溶解度: 大于
B.以酚酞为指示剂(变色的 范围8.2~10.0),用 标准溶液可滴定 水溶液的浓度
C.忽略 的第二步水解, 的 溶液中 水解率约为
D. 的 溶液中加入等体积 的 溶液,反应初始生成的沉淀是
【答案】C
【解析】在HS溶液中存在电离平衡:HS H++HS-、HS- H++S2-,随着pH的增大,HS的物质的
2 2 2
量分数逐渐减小,HS-的物质的量分数先增大后减小,S2-的物质的量分数逐渐增大,图
12 / 31
学科网(北京)股份有限公司中线①、②、③依次代表HS、HS-、S2-的物质的量分数随pH
2
的变化,由①和②交点的pH=7可知K (H S)=1×10-7,由②和③交点的pH=13.0可知K (H S)=1×10-
a1 2 a2 2
13。A.FeS的溶解平衡为FeS(s) Fe2+(aq)+S2-(aq),饱和FeS溶液物质的量浓度为 =
mol/L= ×10-9mol/L,Fe(OH) 的溶解平衡为Fe(OH) Fe2+(aq)+2OH-(aq),饱和
2 2
Fe(OH) 溶液物质的量浓度为 = mol/L= ×10-6mol/L> ×10-9mol/L,
2
故溶解度:FeS小于Fe(OH) ,A项错误;
2
B.酚酞的变色范围为8.2~10,若以酚酞为指示剂,用NaOH标准溶液滴定HS水溶液,由图可知当
2
酚酞发生明显颜色变化时,反应没有完全,即不能用酚酞作指示剂判断滴定终点,B项错误;
C.NaS溶液中存在水解平衡S2-+H O HS-+OH-、HS-+H O HS+OH-(忽略第二步水解),第一
2 2 2 2
步水解平衡常数K (S2-)= = = = =0.1,设水解的S2-的
h
浓度为x mol/L,则 =0.1,解得x≈0.062,S2-的水解率约为 ×100%=62%,C项正确;
D.0.01mol/L FeCl 溶液中加入等体积0.2mol/L Na S溶液,瞬间得到0.005mol/L FeCl 和0.1mol/L
2 2 2
NaS的混合液,结合C项,瞬时c(Fe2+)c(S2-)=0.005mol/L×(0.1mol/L-0.062mol/L)=1.9×10-4>K (FeS),
2 sp
c(Fe2+)c2(OH-)=0.005mol/L×(0.062mol/L)2=1.922×10-5>K [Fe(OH) ],故反应初始生成的沉淀是FeS和
sp 2
Fe(OH) ,D项错误;
2
答案选C。
11.(2024·山东卷)常温下 水溶液体系中存在反应:
,平衡常数为K。已初始浓度 ,所有含碳物种的摩尔分数与
变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
A.线Ⅱ表示 的变化情况
13 / 31
学科网(北京)股份有限公司B. 的电离平衡常数
C. 时,
D. 时,
【答案】C
【分析】在溶液中存在平衡:CHCOOH CHCOO-+H+(①)、Ag++CH COO- CHCOOAg(aq)
3 3 3 3
(②),Ag+的水解平衡Ag++H O AgOH+H+(③),随着pH的增大,c(H+)减小,平衡①③正向移
2
动,c(CHCOOH)、c(Ag+)减小,pH较小时(约小于7.8)CHCOO-浓度增大的影响大于Ag+浓度减小
3 3
的影响,CHCOOAg浓度增大,pH较大时(约大于7.8)CHCOO-浓度增大的影响小于Ag+浓度减小
3 3
的影响,CHCOOAg浓度减小,故线Ⅰ表示CHCOOH的摩尔分数随pH变化的关系,线Ⅱ表示
3 3
CHCOO-的摩尔分数随pH变化的关系,线Ⅲ表示CHCOOAg随pH变化的关系。
3 3
【解析】A.根据分析,线Ⅱ表示CHCOO-的变化情况,A项错误;
3
B.由图可知,当c(CHCOOH)=c(CHCOO-)相等时(即线Ⅰ和线Ⅱ的交点),溶液的pH=m,则
3 3
CHCOOH的电离平衡常数K = =10-m,B项错误;
3 a
C.pH=n时 =10-m,c(CHCOO-)= =10n-mc(CHCOOH),Ag+
3 3
+CH COO- CHCOOAg(aq)的K= ,c(Ag+)= ,由图可知pH=n时,
3 3
c(CHCOOH)=c(CHCOOAg),代入整理得c(Ag+)= mol/L,C项正确;
3 3
D.根据物料守恒,pH=10时溶液中c(Ag+)+c(CHCOOAg)+c(AgOH)=0.08mol/L,D项错误;
3
答案选C。
12.(2024·新课标卷)常温下 和 的两种溶液中,分布系数δ与pH的变化关系
如图所示。[比如: ]
14 / 31
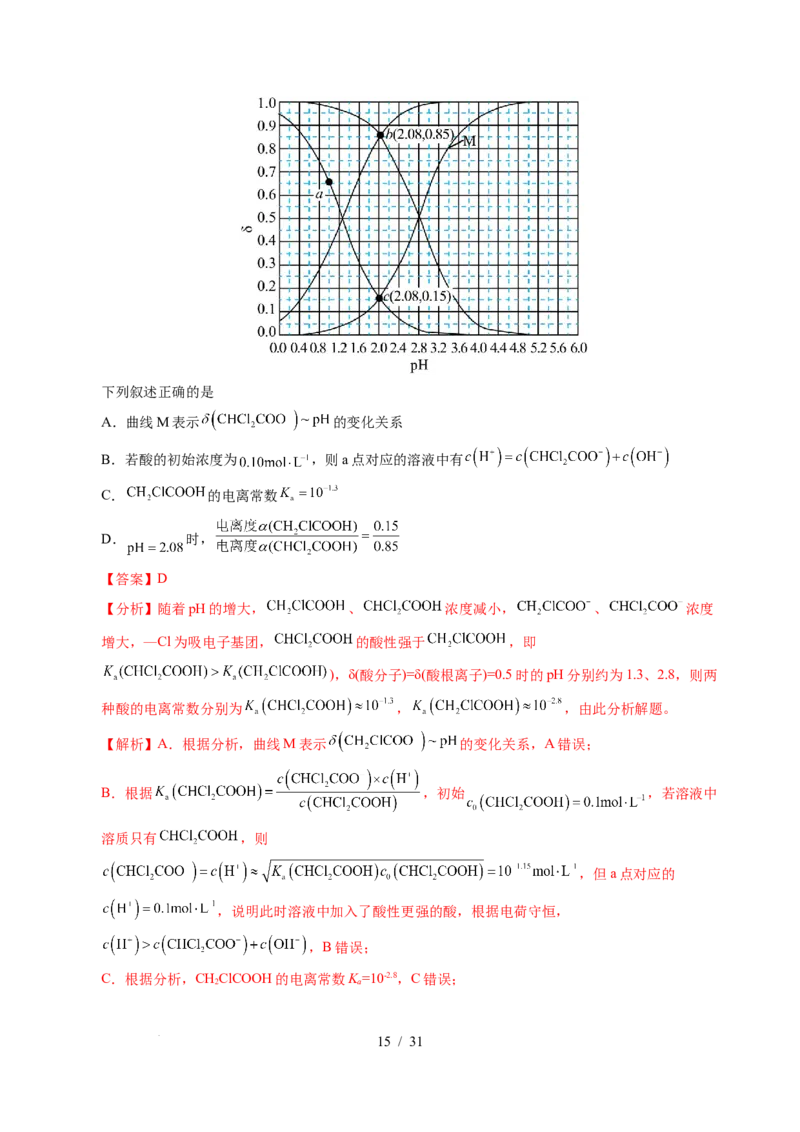
学科网(北京)股份有限公司下列叙述正确的是
A.曲线M表示 的变化关系
B.若酸的初始浓度为 ,则a点对应的溶液中有
C. 的电离常数
D. 时,
【答案】D
【分析】随着pH的增大, 、 浓度减小, 、 浓度
增大,—Cl为吸电子基团, 的酸性强于 ,即
),δ(酸分子)=δ(酸根离子)=0.5时的pH分别约为1.3、2.8,则两
种酸的电离常数分别为 , ,由此分析解题。
【解析】A.根据分析,曲线M表示 的变化关系,A错误;
B.根据 ,初始 ,若溶液中
溶质只有 ,则
,但a点对应的
,说明此时溶液中加入了酸性更强的酸,根据电荷守恒,
,B错误;
C.根据分析,CHClCOOH的电离常数K =10-2.8,C错误;
2 a
15 / 31
学科网(北京)股份有限公司D.电离度 , ,则 = ,
, 时, , ,
D正确;
故答案选D。
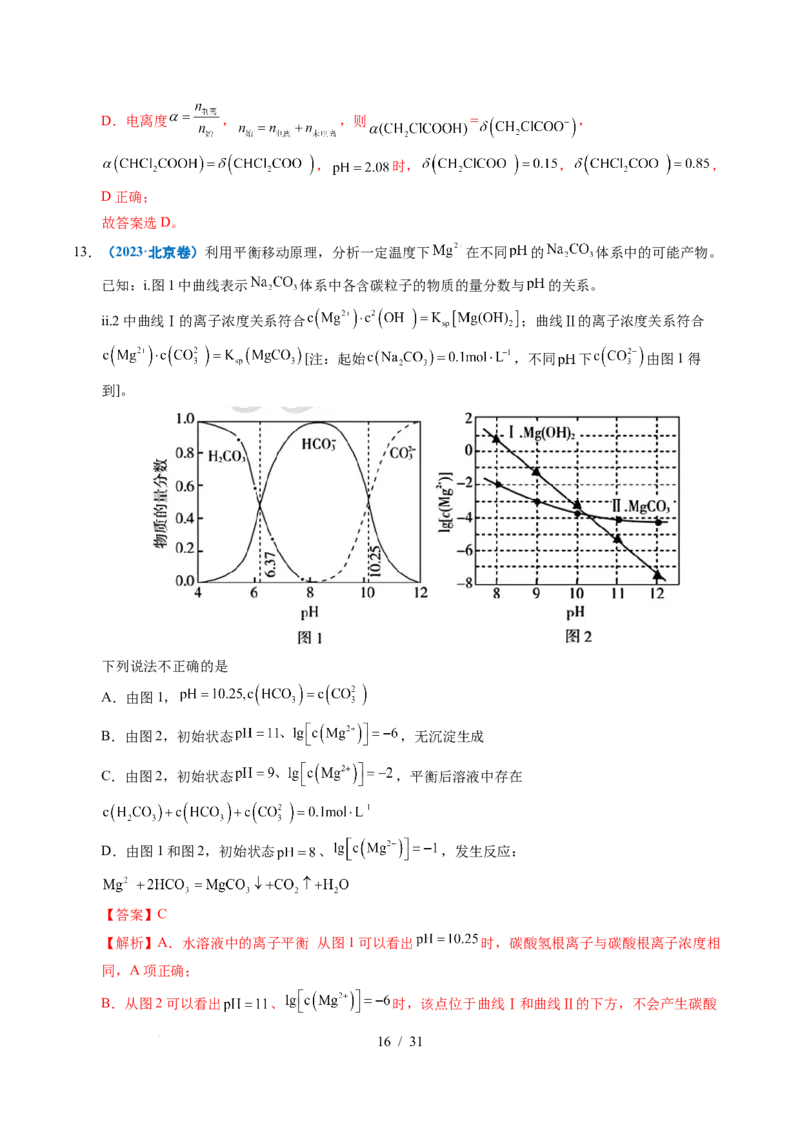
13.(2023·北京卷)利用平衡移动原理,分析一定温度下 在不同 的 体系中的可能产物。
已知:i.图1中曲线表示 体系中各含碳粒子的物质的量分数与 的关系。
ii.2中曲线Ⅰ的离子浓度关系符合 ;曲线Ⅱ的离子浓度关系符合
[注:起始 ,不同 下 由图1得
到]。
下列说法不正确的是
A.由图1,
B.由图2,初始状态 ,无沉淀生成
C.由图2,初始状态 ,平衡后溶液中存在
D.由图1和图2,初始状态 、 ,发生反应:
【答案】C
【解析】A.水溶液中的离子平衡 从图1可以看出 时,碳酸氢根离子与碳酸根离子浓度相
同,A项正确;
B.从图2可以看出 、 时,该点位于曲线Ⅰ和曲线Ⅱ的下方,不会产生碳酸
16 / 31
学科网(北京)股份有限公司镁沉淀或氢氧化镁沉淀,B项正确;
C.从图2可以看出 、 时,该点位于曲线Ⅱ的上方,会生成碳酸镁沉淀,根据
物料守恒,溶液中 ,C项错误;D. 时,溶液中主
要含碳微粒是 , , 时,该点位于曲线Ⅱ的上方,会生成碳酸镁沉淀,因
此反应的离子方程式为 ,D项正确;
故选C。
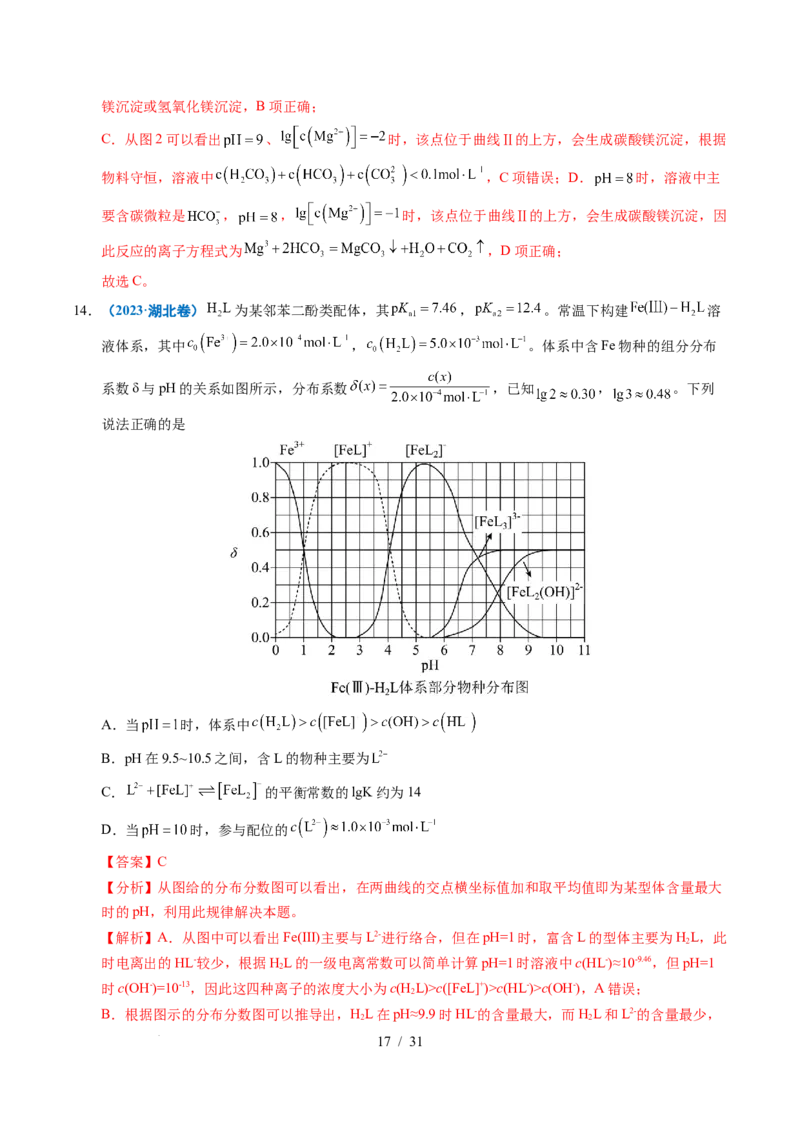
14.(2023·湖北卷) 为某邻苯二酚类配体,其 , 。常温下构建 溶
液体系,其中 , 。体系中含Fe物种的组分分布
系数δ与pH的关系如图所示,分布系数 ,已知 , 。下列
说法正确的是
A.当 时,体系中
B.pH在9.5~10.5之间,含L的物种主要为
C. 的平衡常数的lgK约为14
D.当 时,参与配位的
【答案】C
【分析】从图给的分布分数图可以看出,在两曲线的交点横坐标值加和取平均值即为某型体含量最大
时的pH,利用此规律解决本题。
【解析】A.从图中可以看出Fe(Ⅲ)主要与L2-进行络合,但在pH=1时,富含L的型体主要为HL,此
2
时电离出的HL-较少,根据HL的一级电离常数可以简单计算pH=1时溶液中c(HL-)≈10-9.46,但pH=1
2
时c(OH-)=10-13,因此这四种离子的浓度大小为c(H L)>c([FeL]+)>c(HL-)>c(OH-),A错误;
2
B.根据图示的分布分数图可以推导出,HL在pH≈9.9时HL-的含量最大,而HL和L2-的含量最少,
2 2
17 / 31
学科网(北京)股份有限公司因此当pH在9.5~10.5之间时,含L的物种主要为HL-,B错误;
C.该反应的平衡常数K= ,当[FeL ]-与[FeL]+分布分数相等时,可以将K简化为K=
2
,此时体系的pH=4,在pH=4时可以计算溶液中c(L2-)=5.0×10-14.86,则该络合反应的平衡常数
K≈10-14.16,即lg K≈14,C正确;
D.根据图像,pH=10时溶液中主要的型体为[FeL ]3-和[FeL (OH)]2-,其分布分数均为0.5,因此可以得
3 2
到c([FeL ]3-)=c([FeL (OH)]2-)=1×10-4mol·L-1,此时形成[FeL ]3-消耗了3×10-4mol·L-1的L2-,形成
3 2 3
[FeL (OH)]2-消耗了2×10-4mol·L-1的L2-,共消耗了5×10-4mol·L-1的L2-,即参与配位的c(L2-)≈5×10-4,D
2
错误;
故答案选C。
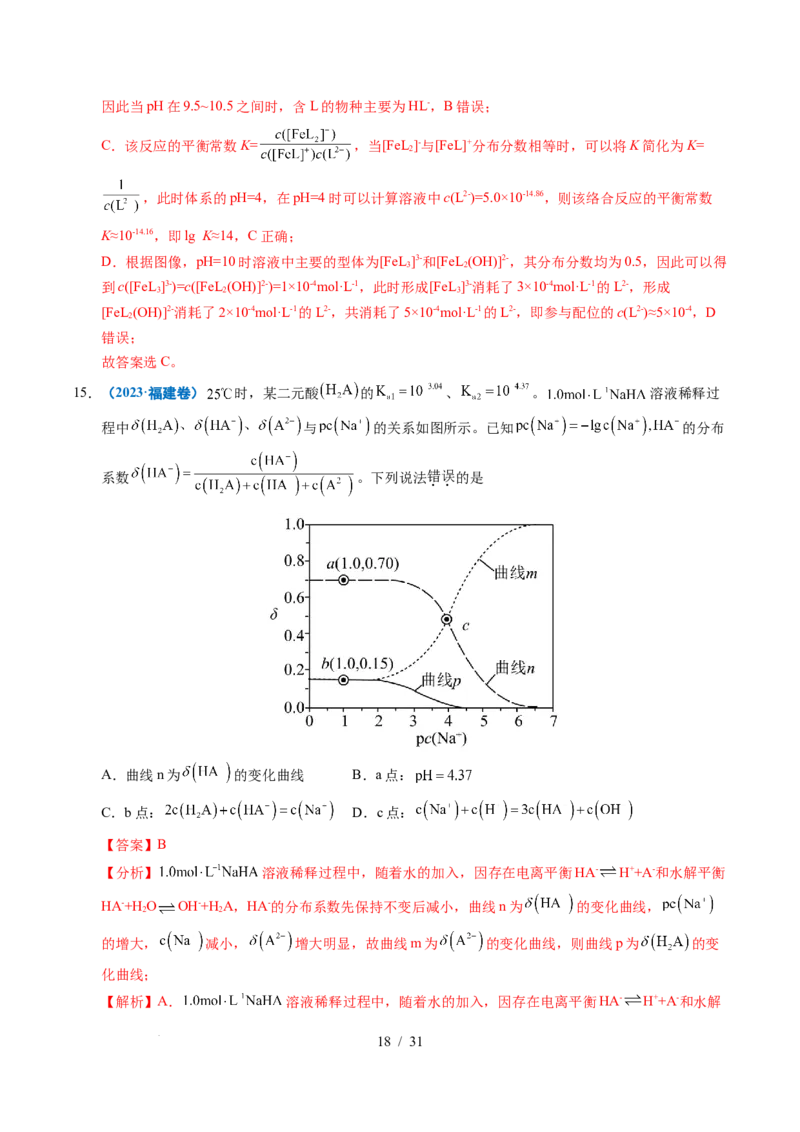
15.(2023·福建卷) 时,某二元酸 的 、 。 溶液稀释过
程中 与 的关系如图所示。已知 的分布
系数 。下列说法错误的是
A.曲线n为 的变化曲线 B.a点:
C.b点: D.c点:
【答案】B
【分析】 溶液稀释过程中,随着水的加入,因存在电离平衡HA- H++A-和水解平衡
HA-+H O OH-+H A,HA-的分布系数先保持不变后减小,曲线n为 的变化曲线,
2 2
的增大, 减小, 增大明显,故曲线m为 的变化曲线,则曲线p为 的变
化曲线;
【解析】A. 溶液稀释过程中,随着水的加入,因存在电离平衡HA- H++A-和水解
18 / 31
学科网(北京)股份有限公司平衡HA-+H O OH-+H A,HA-的分布系数开始时变化不大且保持较大,故曲线n为 的变化
2 2
曲线,选项A正确;
B.a点, =1.0,则 =0.1mol/L, =0.70, = =0.15,
, , ,选项B错误;
C.b点, =0.70, = =0.15,即 = ,根据物料守恒有,
,故 ,选项C正确;
D.c点: = ,故 根据电荷守恒有
,故 ,选项D正确;
答案选B。
16.(2022·辽宁卷)甘氨酸 是人体必需氨基酸之一、在 时, 、
和 的分布分数【如 】与溶液 关系如
图。下列说法错误的是
A.甘氨酸具有两性
B.曲线c代表
C. 的平衡常数
D.
【答案】D
【解析】A. 中存在 和-COOH,所以溶液既有酸性又有碱性,故A正确;
B.氨基具有碱性,在酸性较强时会结合氢离子,羧基具有酸性,在碱性较强时与氢氧根离子反应,
故曲线a表示 的分布分数随溶液pH的变化,曲b表示
的分布分数随溶液pH的变化,曲线c表示 的分布分数随溶液pH的变
19 / 31
学科网(北京)股份有限公司化,故B正确;
C. 的平衡常数 ,
时,根据a,b曲线交点坐标 可知, 时, ,则
,故C正确;
D.由C项分析可知, ,根据b,c曲线交点坐标坐标 分析可
得电离平衡 的电离常数为K= ,
1
,则 ,
即 ,故D错误;
故答案选D。
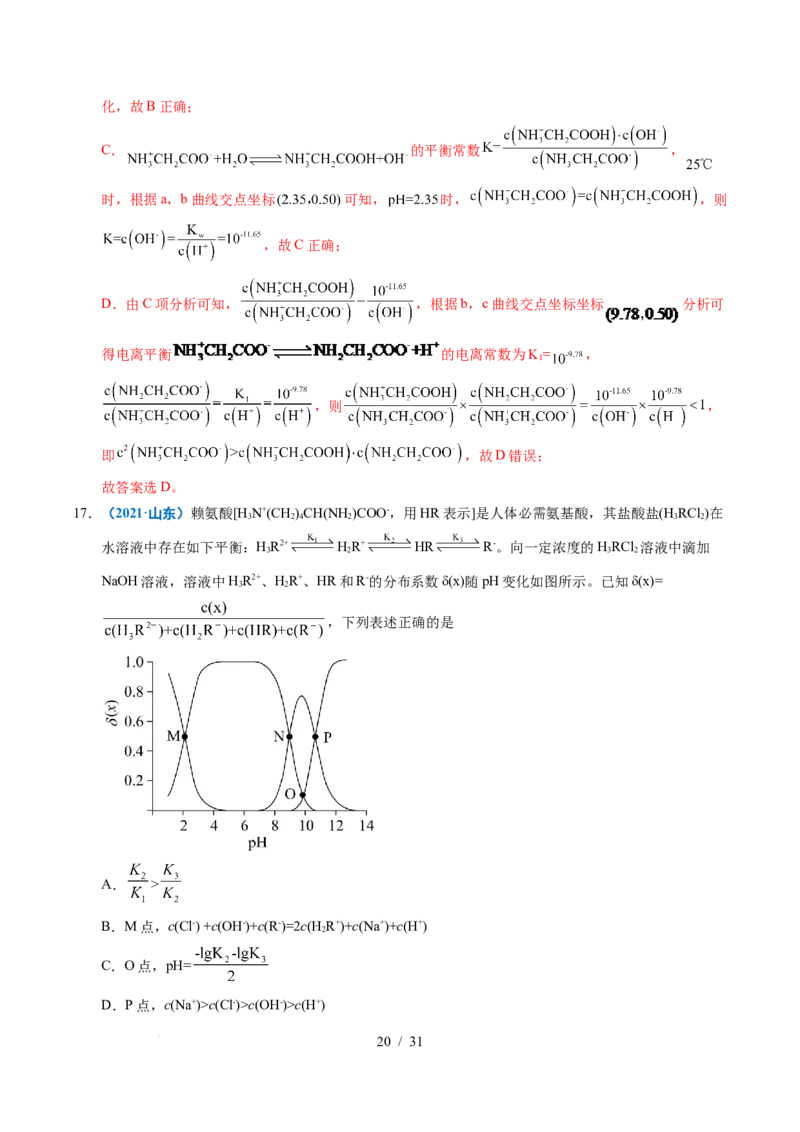
17.(2021·山东)赖氨酸[H N+(CH)CH(NH)COO-,用HR表示]是人体必需氨基酸,其盐酸盐(H RCl )在
3 2 4 2 3 2
水溶液中存在如下平衡:HR2+ HR+ HR R-。向一定浓度的HRCl 溶液中滴加
3 2 3 2
NaOH溶液,溶液中HR2+、HR+、HR和R-的分布系数δ(x)随pH变化如图所示。已知δ(x)=
3 2
,下列表述正确的是
A. >
B.M点,c(Cl-) +c(OH-)+c(R-)=2c(H R+)+c(Na+)+c(H+)
2
C.O点,pH=
D.P点,c(Na+)>c(Cl-)>c(OH-)>c(H+)
20 / 31
学科网(北京)股份有限公司【答案】CD
【分析】
向HRCl 溶液中滴加NaOH溶液,依次发生离子反应: 、
3 2
、 ,溶液中 逐渐减小, 和 先增
大后减小, 逐渐增大。 , , ,
M点 ,由此可知 ,N点 ,则 ,P点
,则 。
【解析】
A. , ,因此 ,故A错误;
B.M点存在电荷守恒: ,
此时 ,因此 ,故B
错误;
C.O点 ,因此 ,即
,因此 ,溶液
,故C正确;
D.P点溶质为NaCl、HR、NaR,此时溶液呈碱性,因此 ,溶质浓度大于水解和电
离所产生微粒浓度,因此 ,故D正确;
综上所述,正确的是CD,故答案为CD。
考点 三 对数图像分析
18.(2025·陕晋青宁卷)常温下,溶液中 以氢氧化物形式沉淀时,
与 的关系如图[其中X代表 或 ]。
已知: , 比 更易与碱反应,形成 ;溶液中
时,X可忽略不计。
21 / 31
学科网(北京)股份有限公司下列说法错误的是
A.L为 与 的关系曲线
B. 的平衡常数为
C.调节 溶液浓度,通过碱浸可完全分离 和
D.调节溶液 为 ,可将浓度均为 的 和 完全分离
【答案】B
【分析】 和 沉淀形成 和 , 沉淀形成 ,则 和 的曲线
平行,根据 , 比 更易与碱反应,因此 生成的
pH低于 ,故从左到右曲线依次为: 或 。如图
可知: 的平衡常数为
, 的平衡常数为
, 的平衡常数为
, 的平衡常
数为 , 的平衡常数为
, 的平衡常数为 。据此分析:
【详解】A.据分析,L为 与 的关系曲线,故A正确;
B.如图可知, 的平衡常数为
,则 的平衡常数
22 / 31
学科网(北京)股份有限公司为 ,故B错误;
C.如图可知,pH=14时 开始溶解,pH=8.4时 开始溶解,且pH=14时
,即可认为 完全溶解,并转化为 ,因此调节 溶液浓度,通
过碱浸可完全分离 和 ,故C正确;
D. 的 开始沉淀pH为 , 的 完全沉淀pH为
,因此调节溶液 为 ,可将浓度均为 的 和 完全分
离,故D正确;
故答案为B。
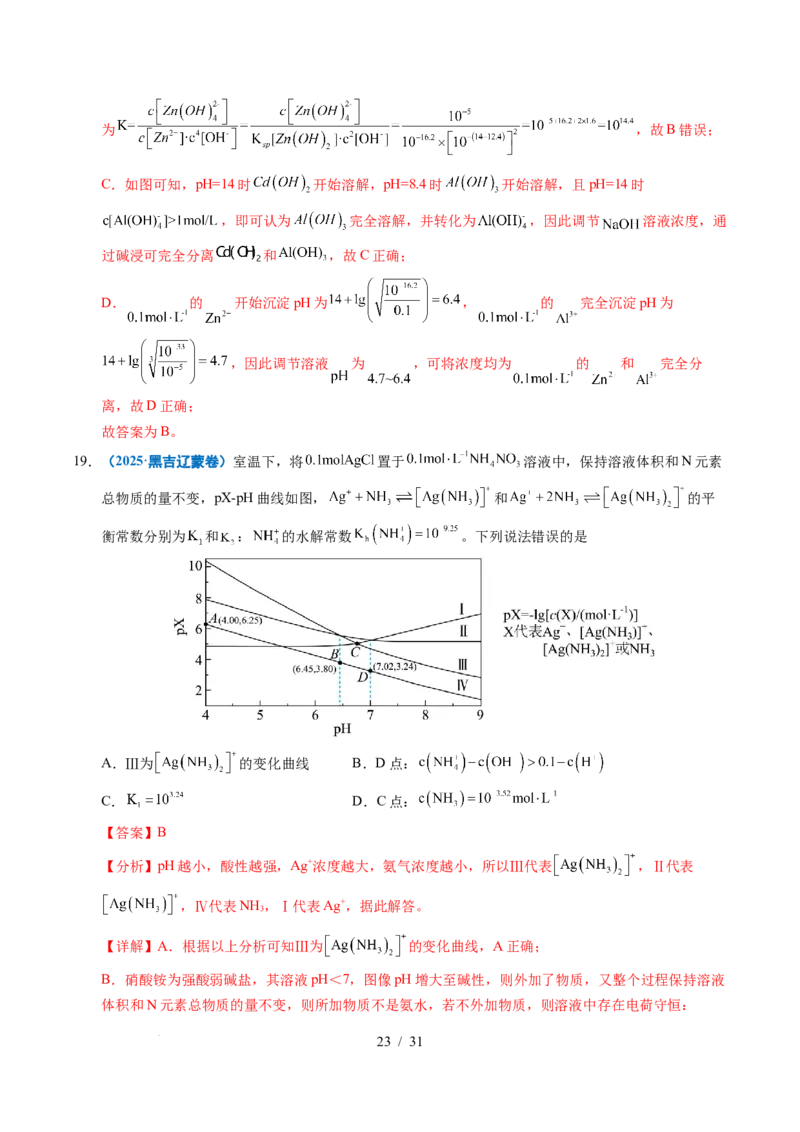
19.(2025·黑吉辽蒙卷)室温下,将 置于 溶液中,保持溶液体积和N元素
总物质的量不变,pX-pH曲线如图, 和 的平
衡常数分别为 和 : 的水解常数 。下列说法错误的是
A.Ⅲ为 的变化曲线 B.D点:
C. D.C点:
【答案】B
【分析】pH越小,酸性越强,Ag+浓度越大,氨气浓度越小,所以Ⅲ代表 ,Ⅱ代表
,Ⅳ代表NH ,Ⅰ代表Ag+,据此解答。
3
【详解】A.根据以上分析可知Ⅲ为 的变化曲线,A正确;
B.硝酸铵为强酸弱碱盐,其溶液pH<7,图像pH增大至碱性,则外加了物质,又整个过程保持溶液
体积和N元素总物质的量不变,则所加物质不是氨水,若不外加物质,则溶液中存在电荷守恒:
23 / 31
学科网(北京)股份有限公司,物料守恒:
, ,
,但外加了碱,设为NaOH,则c(Na+)+
, ,B错误;
C.根据图像可知D点时 和Ag+浓度相等,此时氨气浓度是10-3.24,根据
可知 ,C正确;
D.C点时 和Ag+浓度相等,B点时 和 浓度相等,所以反应的
的平衡常数为103.8,因此K= ,C点时
2
和Ag+浓度相等,所以 ,D正确;
答案选B。
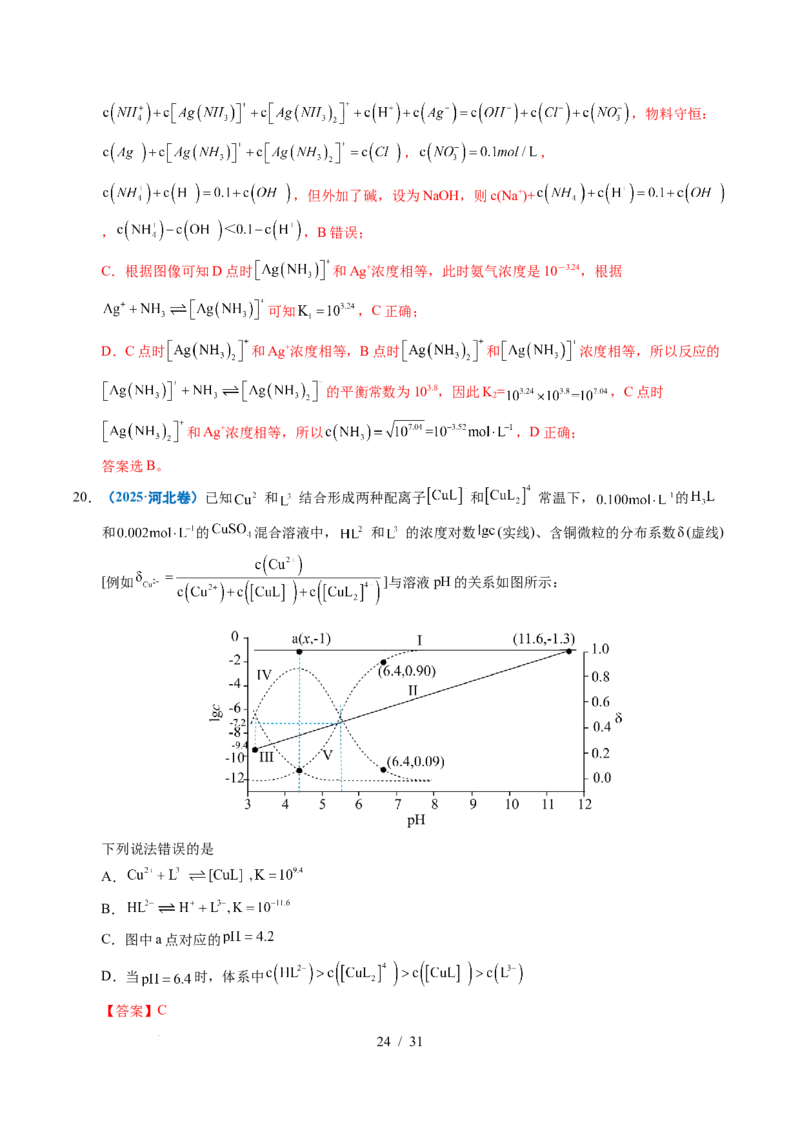
20.(2025·河北卷)已知 和 结合形成两种配离子 和 常温下, 的
和 的 混合溶液中, 和 的浓度对数 (实线)、含铜微粒的分布系数 (虚线)
[例如 ]与溶液pH的关系如图所示:
下列说法错误的是
A.
B.
C.图中a点对应的
D.当 时,体系中
【答案】C
24 / 31
学科网(北京)股份有限公司【分析】 和 之间存在 转化关系,则pH较小时,平衡逆向移动,以 为
主,则 , ,则曲线I代表 ,曲线II代表 ,随着
pH增大, 正向移动, 增大, 和 结合形成配离子的反应依次为
、 ,因此随pH增大, 持续减小,为曲线
III, ,先增大后减小,为曲线IV, 一直增大,为曲线V,据此回答。
【详解】A.曲线III和曲线IV的交点代表 ,即 ,由图可知,此时
,带入平衡表达式得 ,A正确;
B.曲线I和曲线II的交点代表 ,即 ,此时pH=11.6,带入平衡常
数表达式得 ,B正确;
C.曲线IV和曲线V得交点代表, ,即 ,此时 ,
可得 的平衡常数 ,a点时,
,带入 ,解得
,且a点对应 ,带入 的平衡常数
,计算得 ,故pH=4.3,C错误;
D.当pH=6.4时, 最大,接近 ,结合B项中平衡常数可计算得 ,
, 结合Cu 元素守恒知, ,
,因此体系中
,D正确;
故选C。
21.(2025·安徽卷) 是二元弱酸, 不发生水解。 时,向足量的难溶盐 粉末中加入稀盐
酸,平衡时溶液中 与 的关系如下图所示。
25 / 31
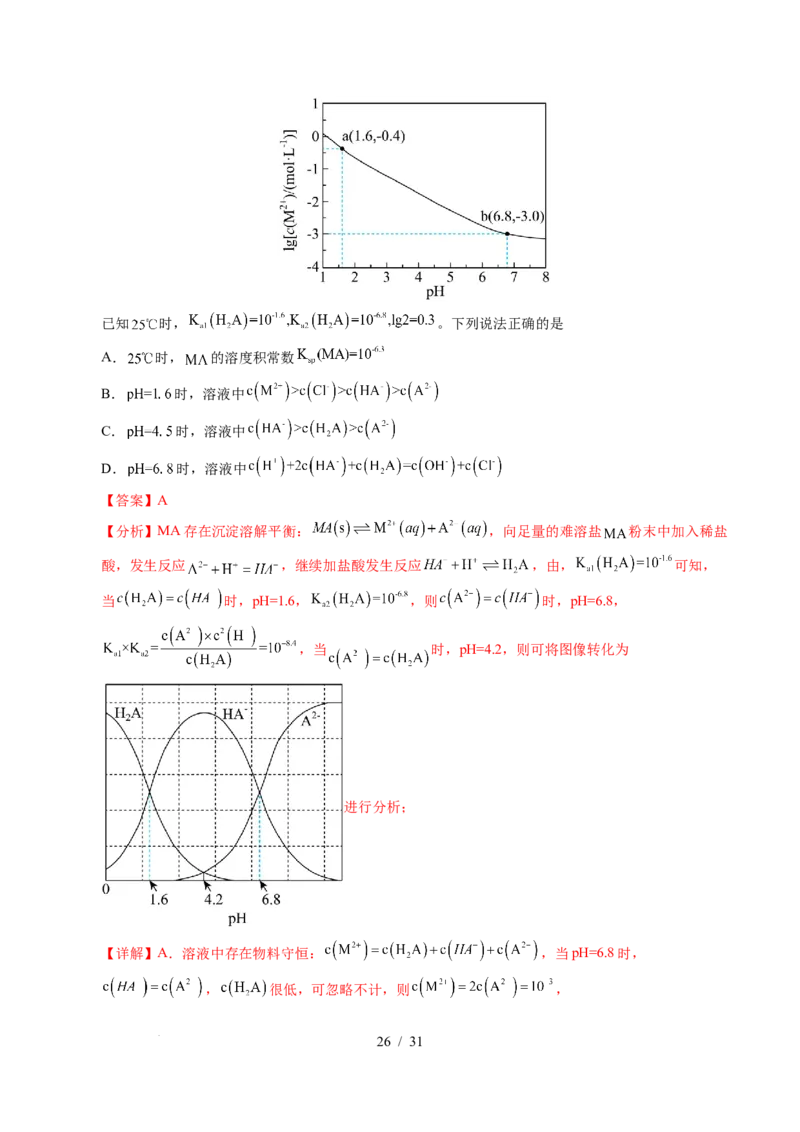
学科网(北京)股份有限公司已知 时, 。下列说法正确的是
A. 时, 的溶度积常数
B. 时,溶液中
C. 时,溶液中
D. 时,溶液中
【答案】A
【分析】MA存在沉淀溶解平衡: ,向足量的难溶盐 粉末中加入稀盐
酸,发生反应 ,继续加盐酸发生反应 ,由, 可知,
当 时,pH=1.6, ,则 时,pH=6.8,
,当 时,pH=4.2,则可将图像转化为
进行分析;
【详解】A.溶液中存在物料守恒: ,当pH=6.8时,
, 很低,可忽略不计,则 ,
26 / 31
学科网(北京)股份有限公司, ,则 ,A正
确;
B.根据物料守恒: , ,由图像可知,pH=1.6
时, 成立,由电荷守恒: ,结
合物料守恒,约掉 得到 ,由图像可知,
且 ,则 ,故离子浓度顺序:
,B错误;
C.由图像可知, 时,溶液中 ,C错误;
D. 时, ,根据电荷守恒关系:
,将物料守恒代入,约掉 得到
,化简得到
,D错误;
故选A。
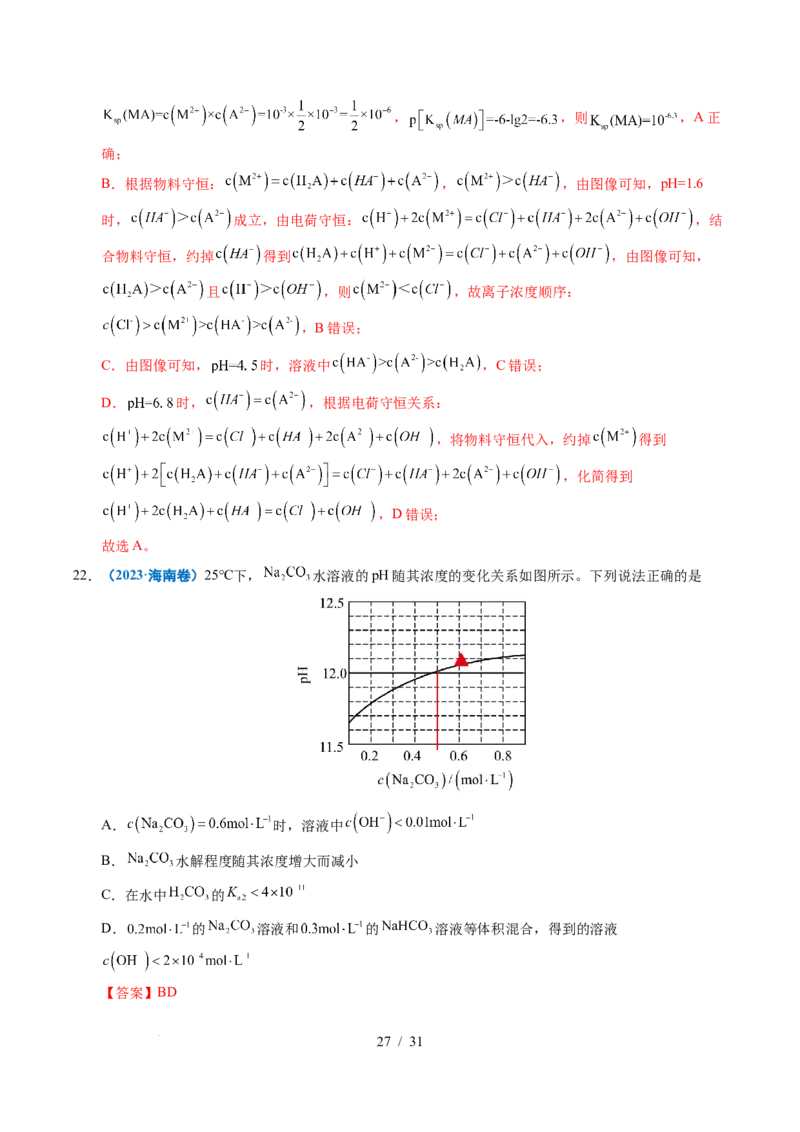
22.(2023·海南卷)25℃下, 水溶液的pH随其浓度的变化关系如图所示。下列说法正确的是
A. 时,溶液中
B. 水解程度随其浓度增大而减小
C.在水中 的
D. 的 溶液和 的 溶液等体积混合,得到的溶液
【答案】BD
27 / 31
学科网(北京)股份有限公司【解析】A.由图像可以, 时,pH>12.0,溶液中 ,故A
错误;
B.盐溶液越稀越水解, 水解程度随其浓度增大而减小,故B正确;
C.结合图像可知,当 ,pH=12,碳酸根水解程度大于碳酸氢根,则K=
h
,则K < ,故C错误;
a2
D.混合后 溶液浓度变为0.1mol/L, 溶液浓度变为0.15mol/L,由
, ,故D正确。
答案为:BD。
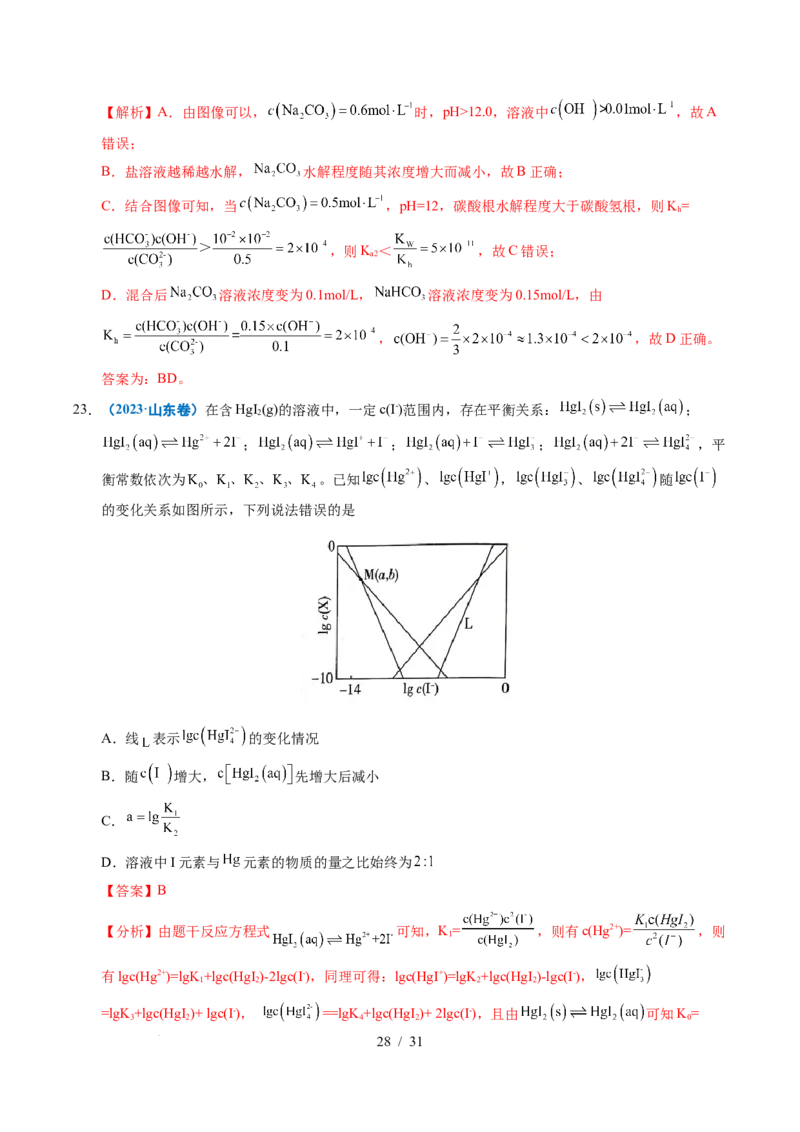
23.(2023·山东卷)在含HgI (g)的溶液中,一定c(I-)范围内,存在平衡关系: ;
2
; ; ; ,平
衡常数依次为 。已知 、 , 、 随
的变化关系如图所示,下列说法错误的是
A.线 表示 的变化情况
B.随 增大, 先增大后减小
C.
D.溶液中I元素与 元素的物质的量之比始终为
【答案】B
【分析】由题干反应方程式 可知,K= ,则有c(Hg2+)= ,则
1
有lgc(Hg2+)=lgK +lgc(HgI )-2lgc(I-),同理可得:lgc(HgI+)=lgK +lgc(HgI )-lgc(I-),
1 2 2 2
=lgK +lgc(HgI )+ lgc(I-), ==lgK+lgc(HgI )+ 2lgc(I-),且由 可知K=
3 2 4 2 0
28 / 31
学科网(北京)股份有限公司为一定值,故可知图示中 曲线1、2、3、4即L分别代
表 、 、 、 ,据此分析解题。
【解析】A.由分析可知,线 表示 的变化情况,A正确;
B.已知 的化学平衡常数K= ,温度不变平衡常数不变,故随
0
增大, 始终保持不变,B错误;
C.由分析可知,曲线1方程为:lgc(Hg2+)=lgK +lgc(HgI )-2lgc(I-),曲线2方程为:
1 2
lgc(HgI+)=lgK +lgc(HgI )-lgc(I-)即有①b= lgK+lgc(HgI )-2a,②b= lgK+lgc(HgI )-a,联合①②可知得:
2 2 1 2 2 2
,C正确;
D.溶液中的初始溶质为HgI ,根据原子守恒可知,该溶液中I元素与 元素的物质的量之比始终为
2
,D正确;
故答案为:B。
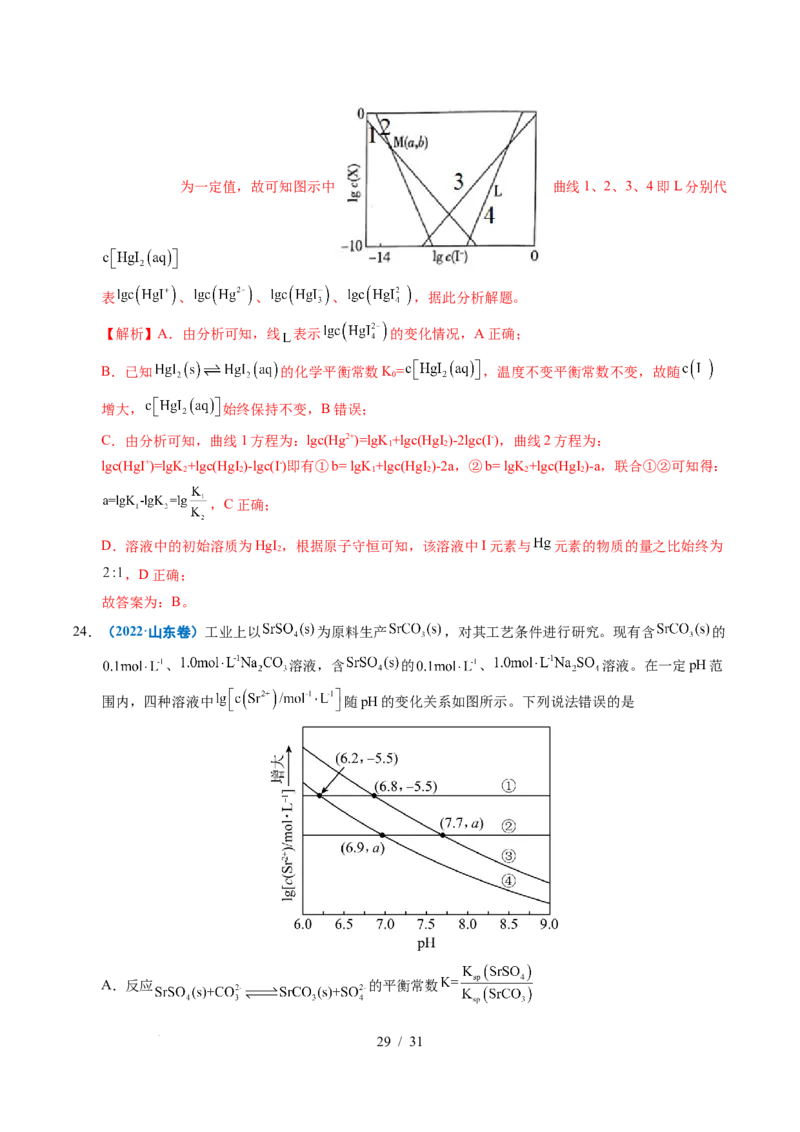
24.(2022·山东卷)工业上以 为原料生产 ,对其工艺条件进行研究。现有含 的
、 溶液,含 的 、 溶液。在一定pH范
围内,四种溶液中 随pH的变化关系如图所示。下列说法错误的是
A.反应 的平衡常数
29 / 31
学科网(北京)股份有限公司B.
C.曲线④代表含 的 溶液的变化曲线
D.对含 且 和 初始浓度均为 的混合溶液, 时才发生沉淀转
化
【答案】D
【解析】硫酸是强酸,溶液pH变化,溶液中硫酸根离子浓度几乎不变,则含硫酸锶固体的硫酸钠溶
液中锶离子的浓度几乎不变,pH相同时,溶液中硫酸根离子越大,锶离子浓度越小,所以曲线①代
表含硫酸锶固体的0.1mol/L硫酸钠溶液的变化曲线,曲线②代表含硫酸锶固体的1mol/L硫酸钠溶液
的变化曲线;碳酸是弱酸,溶液pH减小,溶液中碳酸根离子离子浓度越小,锶离子浓度越大,pH相
同时,1mol/L碳酸钠溶液中碳酸根离子浓度大于0.1mol/L碳酸钠溶液,则曲线③表示含碳酸锶固体的
0.1mol/L碳酸钠溶液的变化曲线,曲线④表示含碳酸锶固体的1mol/L碳酸钠溶液的变化曲线。
A.反应SrSO (s)+CO SrCO (s)+SO 的平衡常数K= = = ,故A
4 3
正确;
B.由分析可知,曲线①代表含硫酸锶固体的0.1mol/L硫酸钠溶液的变化曲线,则硫酸锶的溶度积
K (SrSO )=10—5.5×0.1=10—6.5,温度不变,溶度积不变,则溶液pH为7.7时,锶离子的浓度为
sp 4
=10—6.5,则a为6.5;
C.由分析可知,曲线④表示含碳酸锶固体的1mol/L碳酸钠溶液的变化曲线,故C正确;
D.由分析可知,硫酸是强酸,溶液pH变化,溶液中硫酸根离子浓度几乎不变,则含硫酸锶固体的硫
酸钠溶液中锶离子的浓度几乎不变,所以硫酸锶的生成与溶液pH无关,故D错误;
故选D。
25.(2021·全国乙)HA是一元弱酸,难溶盐MA的饱和溶液中 随c(H+)而变化, 不发生水
解。实验发现, 时 为线性关系,如下图中实线所示。
下列叙述错误的是
30 / 31
学科网(北京)股份有限公司A.溶液 时,
B.MA的溶度积度积
C.溶液 时,
D.HA的电离常数
【答案】C
【分析】
本题考查水溶液中离子浓度的关系,在解题过程中要注意电荷守恒和物料守恒的应用,具体见详解。
【解析】
A.由图可知pH=4,即c(H+)=10×10-5mol/L时,c2(M+)=7.5×10-8mol2/L2,c(M+)=
mol/L<3.0×10-4mol/L,A正确;
B.由图可知,c(H+)=0时,可看作溶液中有较大浓度的OH-,此时A-的水解极大地被抑制,溶液中
c(M+)=c(A-),则 ,B正确;
C.设调pH所用的酸为HX,则结合电荷守恒可知
n
,题给等式右边缺阴离子部分nc(Xn-),C错误;
D. 当 时,由物料守恒知 ,则
, ,则 ,对应图得此
时溶液中 , ,D正确;
故选C。
31 / 31
学科网(北京)股份有限公司