文档内容
2024 年江苏省镇江市中考化学试卷
一、单项选择题:共20题,每题2分,共40分。每题只有一个选项最符合题意。
1. 下列属于纯净物的是
A. 矿泉水 B. 液态氮 C. 加碘盐 D. 不锈钢
2. 下列现象主要由化学变化引起的是
A. 海水晒盐 B. 汽油挥发 C. 红磷燃烧 D. 瓜果飘香
3. 下列物质的用途主要与化学性质有关的是
A. 用镁粉制作照明弹 B. 用活性炭除冰箱异味
C. 用铜制作电线电缆 D. 用干冰进行人工降雨
4. 反应2CaO+2H O=2Ca(OH)+O ↑可用于鱼塘供氧。其中属于碱的是
2 2 2 2
.
A CaO B. HO C. Ca(OH) D. O
2 2 2 2
5. 下列归类正确的是
选
归类 内容
项
A 常见合金 青铜、硬铝、玻璃钢
B 营养物质 糖类、油脂、蛋白质
C 常见氮肥 碳铵、尿素、氯化钾
D 清洁能源 石油、风能、太阳能
A. A B. B C. C D. D
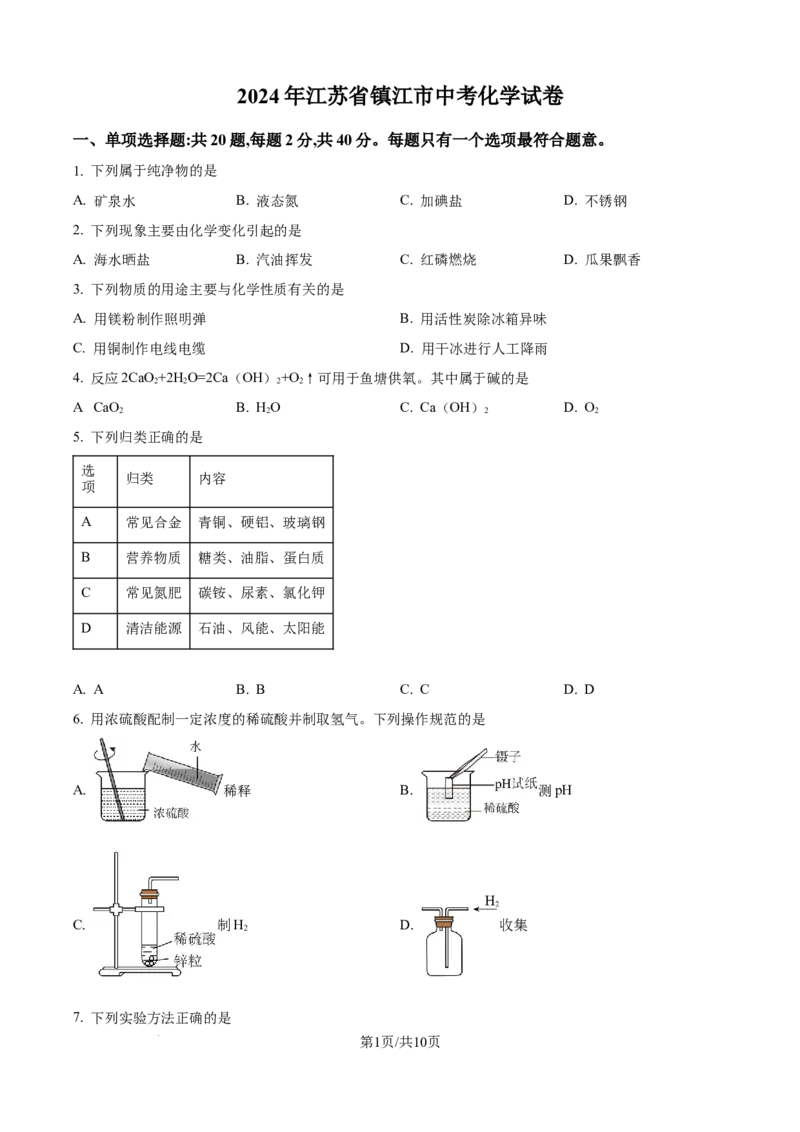
6. 用浓硫酸配制一定浓度的稀硫酸并制取氢气。下列操作规范的是
A. 稀释 B. 测pH
C. 制H D. 收集
2
7. 下列实验方法正确的是
第1页/共10页
学科网(北京)股份有限公司A. 用托盘天平称取5.85g氯化钠 B. 用肥皂水区分硬水和软水
C. 用明矾对自来水进行杀菌消毒 D. 用点燃的方法除去CO 中的CO
2
8. 下列排序正确的是
A. 利用金属的年代: B. 溶液的pH:
C. 地壳中元素含量: D. 硫元素的化合价:
9. 下列指定反应的化学方程式正确的是
A. 甲烷完全燃烧:CH+O CO+H O
4 2 2 2
B. 湿法炼铜:2Fe+3CuSO═Fe (SO )+3Cu
4 2 4 3
C. 小苏打治疗胃酸过多:NaCO+2HCl═2NaCl+CO ↑+H O
2 3 2 2
D. 汽车尾气中CO和NO催化转化为无毒气体:2NO+2CO N+2CO
2 2
10. 配制波尔多液的反应为CuSO +Ca(OH)=X↓+CaSO 。下列说法不正确的是
4 2 4
A. CuSO 可用于游泳池消毒 B. Ca(OH) 可用于改良酸性土壤
4 2
C. X为Cu(OH) D. 反应前后溶液的质量保持不变
2
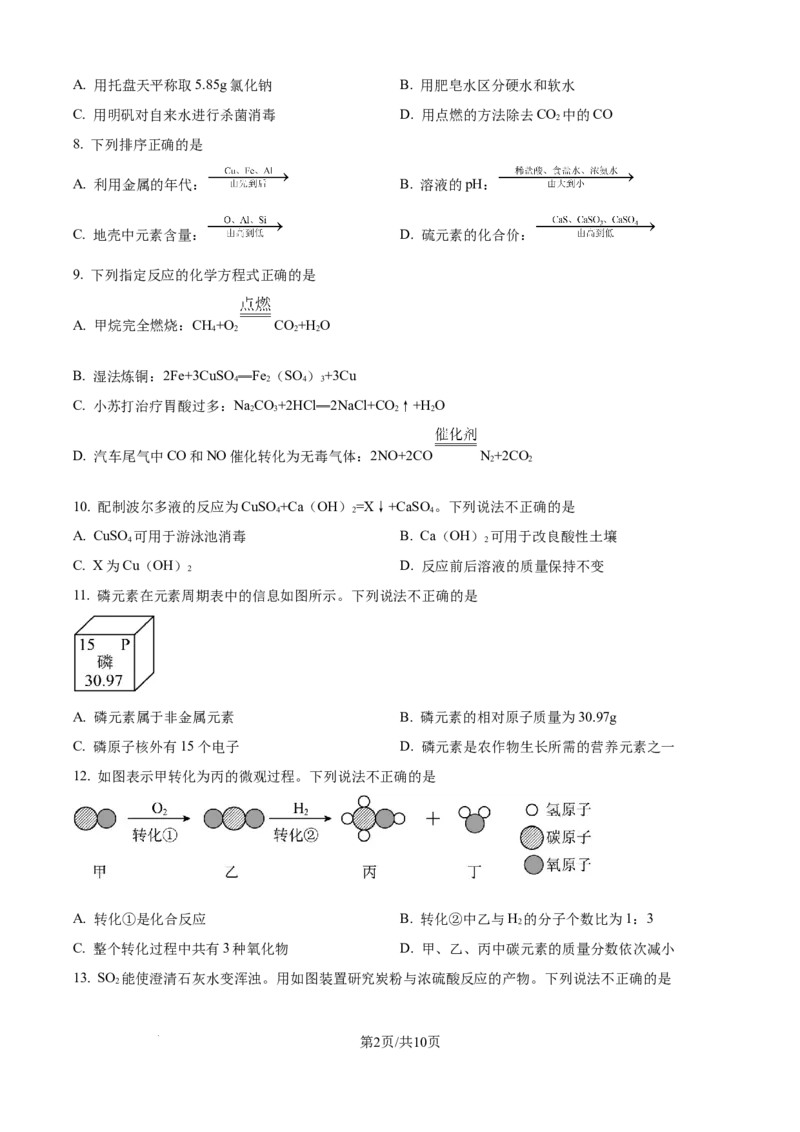
11. 磷元素在元素周期表中的信息如图所示。下列说法不正确的是
A. 磷元素属于非金属元素 B. 磷元素的相对原子质量为30.97g
C. 磷原子核外有15个电子 D. 磷元素是农作物生长所需的营养元素之一
12. 如图表示甲转化为丙的微观过程。下列说法不正确的是
A. 转化①是化合反应 B. 转化②中乙与H 的分子个数比为1:3
2
C. 整个转化过程中共有3种氧化物 D. 甲、乙、丙中碳元素的质量分数依次减小
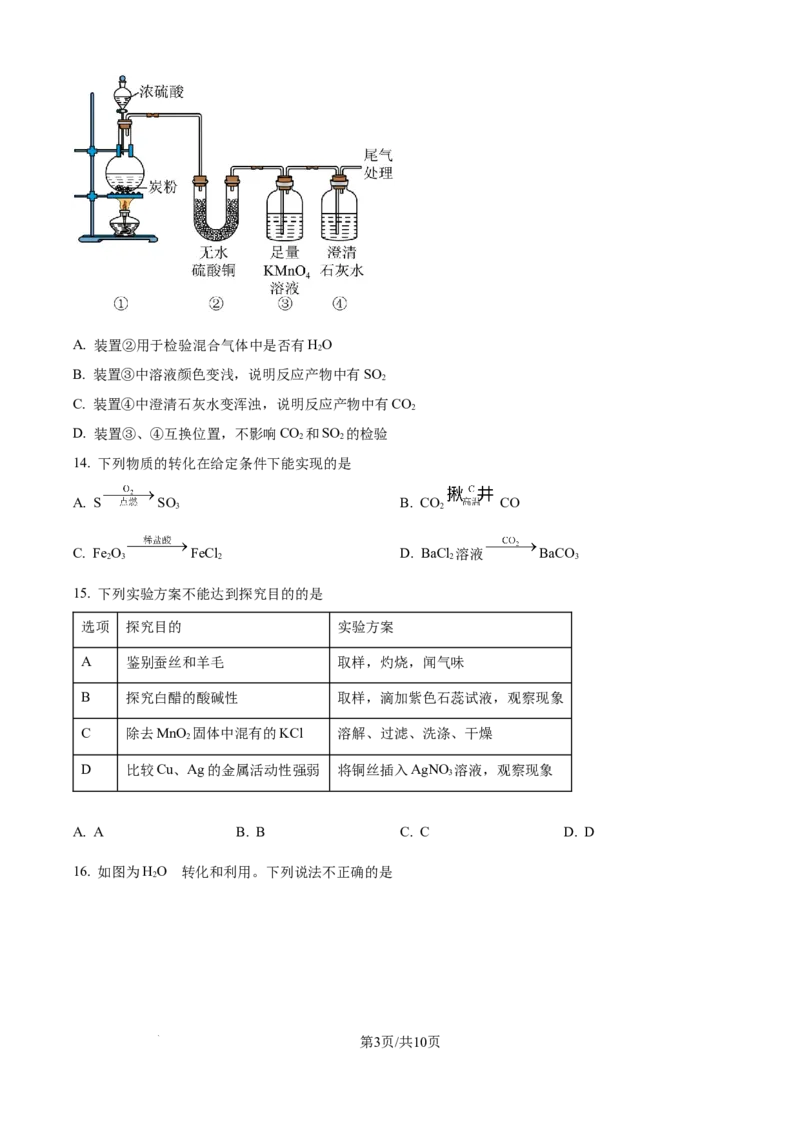
13. SO 能使澄清石灰水变浑浊。用如图装置研究炭粉与浓硫酸反应的产物。下列说法不正确的是
2
第2页/共10页
学科网(北京)股份有限公司A. 装置②用于检验混合气体中是否有HO
2
B. 装置③中溶液颜色变浅,说明反应产物中有SO
2
C. 装置④中澄清石灰水变浑浊,说明反应产物中有CO
2
D. 装置③、④互换位置,不影响CO 和SO 的检验
2 2
14. 下列物质的转化在给定条件下能实现的是
A. S SO B. CO CO
3 2
C. Fe O FeCl D. BaCl 溶液 BaCO
2 3 2 2 3
15. 下列实验方案不能达到探究目的的是
选项 探究目的 实验方案
A 鉴别蚕丝和羊毛 取样,灼烧,闻气味
B 探究白醋的酸碱性 取样,滴加紫色石蕊试液,观察现象
C 除去MnO 固体中混有的KCl 溶解、过滤、洗涤、干燥
2
D 比较Cu、Ag的金属活动性强弱 将铜丝插入AgNO 溶液,观察现象
3
A. A B. B C. C D. D
的
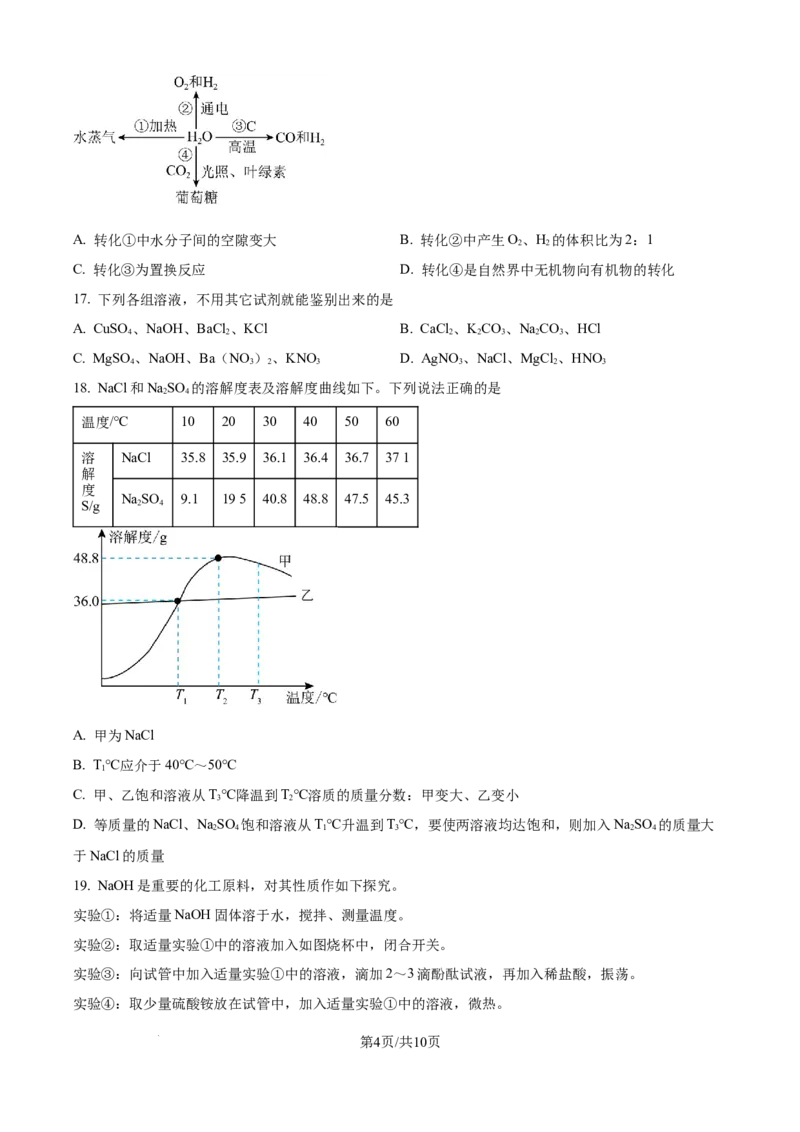
16. 如图为HO 转化和利用。下列说法不正确的是
2
第3页/共10页
学科网(北京)股份有限公司A. 转化①中水分子间的空隙变大 B. 转化②中产生O、H 的体积比为2:1
2 2
C. 转化③为置换反应 D. 转化④是自然界中无机物向有机物的转化
17. 下列各组溶液,不用其它试剂就能鉴别出来的是
A. CuSO 、NaOH、BaCl 、KCl B. CaCl 、KCO、NaCO、HCl
4 2 2 2 3 2 3
C. MgSO 、NaOH、Ba(NO )、KNO D. AgNO、NaCl、MgCl 、HNO
4 3 2 3 3 2 3
18. NaCl和NaSO 的溶解度表及溶解度曲线如下。下列说法正确的是
2 4
温度/℃ 10 20 30 40 50 60
.
溶 NaCl 35.8 35.9 36.1 36.4 36.7 371
解
.
度
NaSO 9.1 195 40.8 48.8 47.5 45.3
S/g 2 4
A. 甲为NaCl
B. T℃应介于40℃~50℃
1
C. 甲、乙饱和溶液从T℃降温到T℃溶质的质量分数:甲变大、乙变小
3 2
D. 等质量的NaCl、NaSO 饱和溶液从T℃升温到T℃,要使两溶液均达饱和,则加入NaSO 的质量大
2 4 1 3 2 4
于NaCl的质量
19. NaOH是重要的化工原料,对其性质作如下探究。
实验①:将适量NaOH固体溶于水,搅拌、测量温度。
实验②:取适量实验①中的溶液加入如图烧杯中,闭合开关。
实验③:向试管中加入适量实验①中的溶液,滴加2~3滴酚酞试液,再加入稀盐酸,振荡。
实验④:取少量硫酸铵放在试管中,加入适量实验①中的溶液,微热。
第4页/共10页
学科网(北京)股份有限公司下列说法不正确的是
A. 实验①中温度升高,说明NaOH固体溶解放热
B. 实验②中小灯泡发光,说明NaOH溶解时生成自由移动的离子
C. 实验③中溶液由红色变成无色,说明溶液恰好呈中性
D. 实验④中产生氨臭气味,该反应为2NaOH+(NH )SO NaSO +2NH↑+2H O
4 2 4 2 4 3 2
20. 已知:2NaHCO NaCO+CO ↑+H O,将16.8gNaHCO 固体加热一段时间后,剩余固体质量为
3 2 3 2 2 3
13.7g。下列说法正确的是
A. 原固体加热生成3.1gCO
2
B. 加热后,固体中钠元素的质量分数减小
C. 剩余固体中NaHCO 和NaCO 的质量比为42:53
3 2 3
D. 将13.7g剩余固体溶于足量盐酸后,蒸发结晶,得11.7gNaCl
二、非选择题共60分
21. 用化学符号表示:
(1)金刚石_____;
(2)最常见的溶剂________;
(3)2个铁离子__________;
(4)人体缺少_______元素会骨骼疏松。
22. 选择下列适当的物质填空(选填序号):
A.食盐 B.硫酸 C.维生素 D.聚氯乙烯 E.石墨 F.烧碱 G.聚乙烯 H.武德合金
(1)可用作电池电极的是_____;
(2)可用于制保险丝的是_____;
(3)可用于食品包装的是_____;
(4)厨房中作调味品的是_____;
第5页/共10页
学科网(北京)股份有限公司的
(5)作铅蓄电池中 酸是_____;
(6)蔬菜、水果中富含有_____。
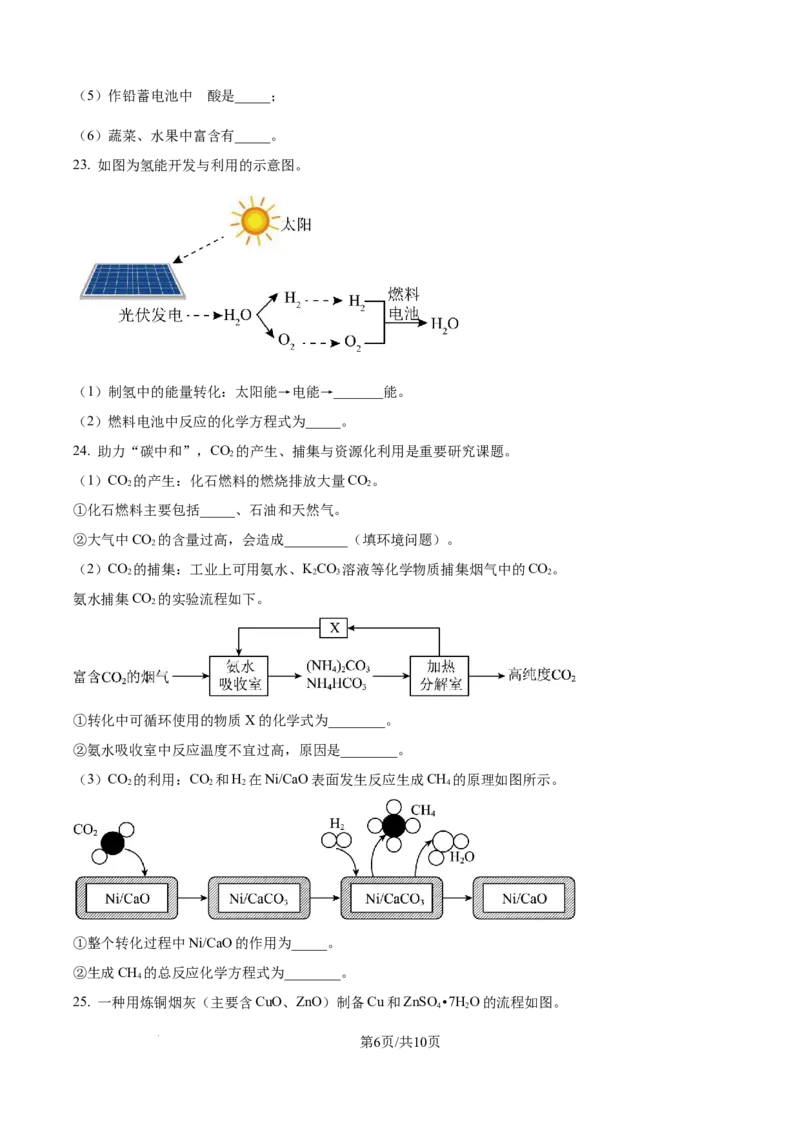
23. 如图为氢能开发与利用的示意图。
(1)制氢中的能量转化:太阳能→电能→_______能。
(2)燃料电池中反应的化学方程式为_____。
24. 助力“碳中和”,CO 的产生、捕集与资源化利用是重要研究课题。
2
(1)CO 的产生:化石燃料的燃烧排放大量CO。
2 2
①化石燃料主要包括_____、石油和天然气。
②大气中CO 的含量过高,会造成_________(填环境问题)。
2
(2)CO 的捕集:工业上可用氨水、KCO 溶液等化学物质捕集烟气中的CO。
2 2 3 2
氨水捕集CO 的实验流程如下。
2
①转化中可循环使用的物质X的化学式为________。
②氨水吸收室中反应温度不宜过高,原因是________。
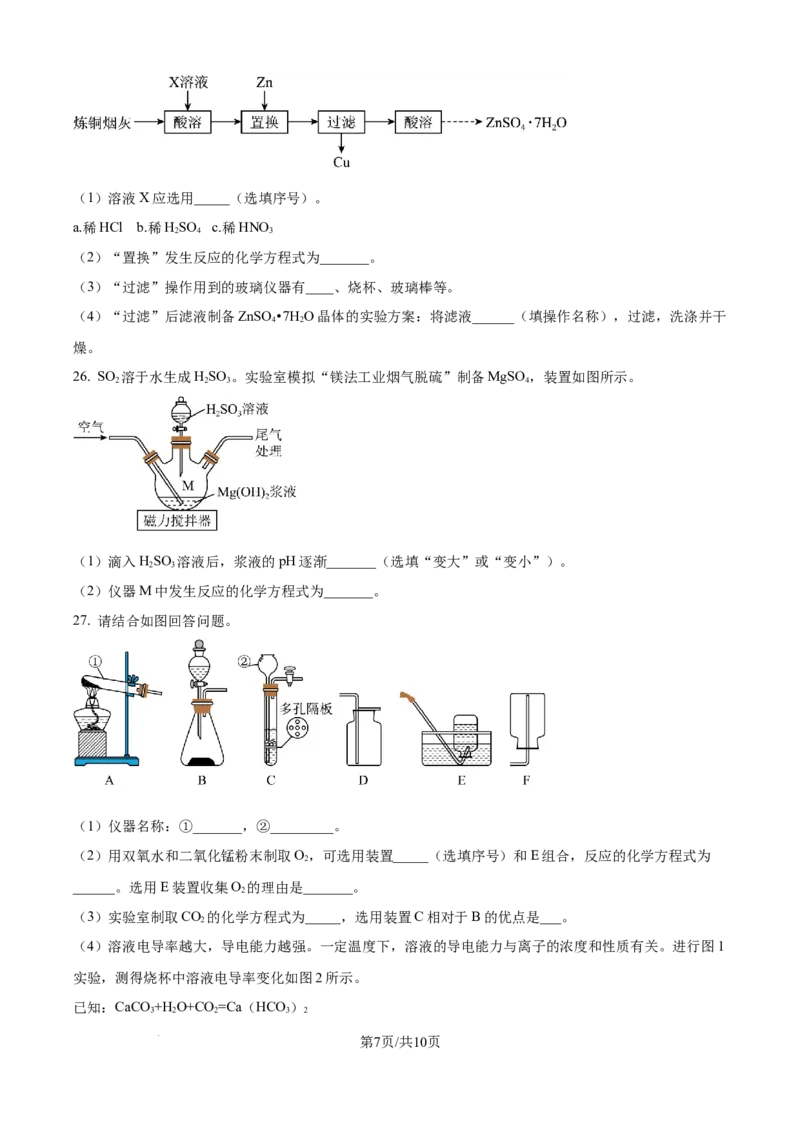
(3)CO 的利用:CO 和H 在Ni/CaO表面发生反应生成CH 的原理如图所示。
2 2 2 4
①整个转化过程中Ni/CaO的作用为_____。
②生成CH 的总反应化学方程式为________。
4
25. 一种用炼铜烟灰(主要含CuO、ZnO)制备Cu和ZnSO•7HO的流程如图。
4 2
第6页/共10页
学科网(北京)股份有限公司(1)溶液X应选用_____(选填序号)。
a.稀HCl b.稀HSO c.稀HNO
2 4 3
(2)“置换”发生反应的化学方程式为_______。
(3)“过滤”操作用到的玻璃仪器有____、烧杯、玻璃棒等。
(4)“过滤”后滤液制备ZnSO•7HO晶体的实验方案:将滤液______(填操作名称),过滤,洗涤并干
4 2
燥。
26. SO 溶于水生成HSO 。实验室模拟“镁法工业烟气脱硫”制备MgSO ,装置如图所示。
2 2 3 4
(1)滴入HSO 溶液后,浆液的pH逐渐_______(选填“变大”或“变小”)。
2 3
(2)仪器M中发生反应的化学方程式为_______。
27. 请结合如图回答问题。
(1)仪器名称:①_______,②_________。
(2)用双氧水和二氧化锰粉末制取O,可选用装置_____(选填序号)和E组合,反应的化学方程式为
2
______。选用E装置收集O 的理由是_______。
2
(3)实验室制取CO 的化学方程式为_____,选用装置C相对于B的优点是___。
2
(4)溶液电导率越大,导电能力越强。一定温度下,溶液的导电能力与离子的浓度和性质有关。进行图1
实验,测得烧杯中溶液电导率变化如图2所示。
已知:CaCO +H O+CO=Ca(HCO )
3 2 2 3 2
第7页/共10页
学科网(北京)股份有限公司①饱和NaHCO 溶液的作用为___________。
3
②用化学方程式解释AB段电导率下降的原因_____________。
③从微粒的角度解释BC段电导率上升的原因___________。
28. 以废铜屑制备碱式碳酸铜的实验步骤如下。
步骤一:以废铜屑制备硫酸铜,途径有两种。
途径Ⅰ:Cu+2H SO (浓) CuSO +SO↑+2H O
2 4 4 2 2
途径Ⅱ:Cu CuO CuSO
4
(1)转化③的化学方程式为_____________。
(2)转化①、②、③中铜元素的化合价升高的为___(选填序号)。
(3)实际生产选择途径Ⅱ制备硫酸铜,途径Ⅱ优于途径Ⅰ的原因是______,_______(从绿色化学和原料
利用率两个角度解释)。
步骤二:以硫酸铜为原料制备碱式碳酸铜 。实验过程如下。
(4)“沉淀”时应将NaCO 溶液滴入CuSO 溶液中,其原因是_________。
2 3 4
(5)检验产品已洗净的方法是:取最后一次洗涤后的滤液,先滴加过量稀盐酸,再滴加___(填化学式)
溶液,无现象,则产品已洗净。
(6)碱式碳酸铜加热到220℃会分解为三种常见的氧化物。取碱式碳酸铜固体充分加热,将生成气体依次
用足量的浓硫酸和碱石灰充分吸收。实验测得浓硫酸增重0.36g,碱石灰增重0.88g。则碱式碳酸铜的化学
式为________________。
29. 以海水为原料生产的NaOH固体,可能含有NaCl、NaCO、NaSO ,CaCl 、MgSO 中的一种或几种。
2 3 2 4 2 4
第8页/共10页
学科网(北京)股份有限公司进行如下实验。
(1)取适量固体加水溶解,得无色澄清溶液A,则原固体中一定不含_______。
(2)取适量A溶液,加入过量BaCl 溶液,过滤得白色固体B。取固体B,加入过量稀盐酸,固体全部溶
2
解,产生气泡,则原固体中一定不含______。生成固体B反应的化学方程式为___。
(3)另取适量A溶液,先加入过量的稀_____酸化,再滴加AgNO 溶液,产生白色沉淀,则原固体中一定
3
含____。
30. 铁及其化合物在生产生活中有广泛应用。
一、铁的有关知识
(1)北固山铁塔由生铁铸成,展现了我国古代精湛的冶铁、铸造技术。因年代久远,塔身锈蚀严重。
①生铁的熔点比纯铁_____(选填“高”或“低”)。
②铁锈主要成分是Fe O•nH O,铁生锈主要与空气中的_______有关。
2 3 2
(2)工业上冶炼钢铁的主要工艺流程如图。
①以赤铁矿为原料炼铁反应的化学方程式为_______。
②炼钢炉中存在转化:Fe FeO Fe+CO,目的为降低____元素含量。
(3)铁及其化合物在现代多种领域发挥着重要作用。
①纳米零价铁(Fe)用于废水处理,可用H 和Fe(OH) 在高温下反应获得,反应的化学方程式为
2 3
____________________。
②Fe O 是合成氨催化剂铁触媒的主要成分,可用CH 和Fe O 在高温下反应获得,同时生成CO 和HO的
3 4 4 2 3 2 2
质量比为_____。
二、制备硫酸亚铁铵晶体
用废铁屑制备硫酸亚铁铵晶体[(NH )Fe(SO )•6H O]的实验流程如下。
4 2 4 2 2
第9页/共10页
学科网(北京)股份有限公司(4)“洗涤”是用蒸馏水洗去铁屑表面残留的NaCO 等杂质,判断铁屑已洗净的方法是:取最后一次洗
2 3
涤后的滤液,测定其pH=_____,则已洗净。
(5)“酸溶”时控温75℃加热至不再产生气泡。
①加热的目的是___________。
②产生的气体为H,用点燃法检验H 前必须______。
2 2
(6)“反应”后冷却至20℃过滤。
①“反应”的化学方程式为_________。
表:“反应”中相关物质的溶解度
温度/℃ 20℃
FeSO •7H O 48.0
4 2
溶解
(NH )SO 75.4
4 2 4
度S/g
(NH )Fe(SO )•6H O 21.2
4 2 4 2 2
②“反应”过程中析出硫酸亚铁铵晶体,参考表中数据分析其原因________。
三、测定硫酸亚铁铵晶体样品纯度
准确称取19.00g硫酸亚铁铵晶体(相对分子质量为392)样品溶于水,与硫酸酸化的KMnO 溶液完全反应,
4
消耗KMnO 的质量为1.58g。
4
已知:10(NH )Fe(SO )·6H O+2KMnO +8H SO =10(NH )SO +5Fe (SO )+K SO +2MnSO +14H O
4 2 4 2 2 4 2 4 4 2 4 2 4 3 2 4 4 2
(7)该样品的纯度为_________%(精确到0.1%)。
(8)判断该计算结果是否合理并分析其原因__________。
第10页/共10页
学科网(北京)股份有限公司