文档内容
绝密★启用前
2009 年普通高等学校招生全国统一考试试题卷(全国 2)
理科综合(化学部分)
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。第Ⅰ卷 1至5页,第Ⅱ卷6至14
页。考试结束后,将本试卷和答题卡一并交回。
注意事项:
1. 答卷前,考生务必将自己的姓名,准考证号填写在试题卷和答题卡上,并将准考证号条
形码粘贴在答题卡上指定位置。
2. 选择题每小题选出答案后,用2B铅笔将答题卡上,对应题目的答案标号涂写,如需改动,
用橡皮擦干净后,再选涂其它答案标号,答在试题卷上无效。
3. 非选择题用0.5毫米的黑色墨水签字笔答在答题卡上每题对应的答题区域内,答在试题卷
上无效。
4. 考试结束,请将本试题卷和答题卡一并上交。
第Ⅰ卷
(选择题)
本卷共21小题,每小题6分,共126分。
以下数据可供解题时参考:
相对原子质量(原子量):H – 1 C – 12 N – 14 O - 16
一、 选择题(本题共13小题。在每小题给出的四个选项中,只有一项是符合题目要求
的。)
6. 物质的量之比为2:5的锌与稀硝酸反应,若硝酸被还原的产物为NO,反应结束后锌没有
2
剩余,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是
A. 1:4 B.1:5 C. 2:3 D.2:5
7. 下列关于溶液和胶体的叙述,正确的是
A. 溶液是电中性的,胶体是带电的
B. 通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动
C. 溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动
D. 一束光线分别通过溶液和胶体时,后者会出现明显的光带,前者则没有
8. 下列徐树中正确的是
A. 向含有CaCO 沉淀的水中通入CO 至沉淀恰好溶解,再向溶液中加入NaHCO 饱
3 2 3
和溶液,又有CaCO 沉淀生成
3
B. 向Na CO 溶液中逐滴加入等物质的量的稀盐酸,生成的CO 与原Na CO 的物质的
2 3 2 2 3
量之比为1:2.
C. 等质量的NaHCO 和Na CO 分别与足量盐酸反应,在同温同压下,生成的CO 体积
3 2 3 2
相同
D. 向Na CO 饱和溶液中通入CO,有NaHCO 结晶析出
2 3 2 3
9. 某元素只存在两种天然同位素,且在自然界它们的含量相近,其相对原子质量为152.0,原子核外的电子数为63。下列叙述中错误的是
A. 它是副族元素 B. 它是第六周期元素
C. 它的原子核内有63个质子 D. 它的一种同位素的核内有89个中子
10. 现有等浓度的下列溶液:①醋酸,②苯酚,③苯酚钠,④碳酸,⑤碳酸钠,⑥碳酸氢钠。
按溶液pH由小到大排列正确的是
A. ④①②⑤⑥③ B. ④①②⑥⑤③
C. ①④②⑥③⑤ D. ①④②③⑥⑤
11. 已知:2H(g)+ O (g)=2HO(l) ΔH= -571.6KJ· mol-1
2 2 2
CH (g)+ 2O (g)=CO(g)+2HO(l) ΔH= -890KJ· mol-1
4 2 2 2
现有H 与CH 的混合气体112L(标准状况),使其完全燃烧生成CO 和HO(l),若实验
2 4 2 2
测得反应放热3695KJ,则原混合气体中H 与CH 的物质的量之比是
2 4
A.1∶1 B.1∶3
C.1∶4 D.2∶3
O O
12、1 mol HO —OC— —OCCH 3 与足量的NaOH
溶液充分反应,消耗的NaOH的物质的量为
A.5 mol B.4 mol C.3 mol D.2 mol
13. 含有a mol FeBr 的溶液中,通入x mol Cl 。下列各项为通Cl 过程中,溶液内发生反应的
2 2 2
离子方程式,其中不正确的是
A.x=0.4a,2Fe2++Cl=2Fe3++2Cl-
2
B.x=0.6a,2Br-+ Cl =Br +2Cl-
2 2
C.x=a,2Fe2++2Br-+2Cl=Br +2Fe3++4Cl-
2 2
D.x=1.5a,2Fe2++4Br-+3Cl=2Br +2Fe3++6Cl-
2 2
第Ⅱ卷 非选择题
27. (15分)
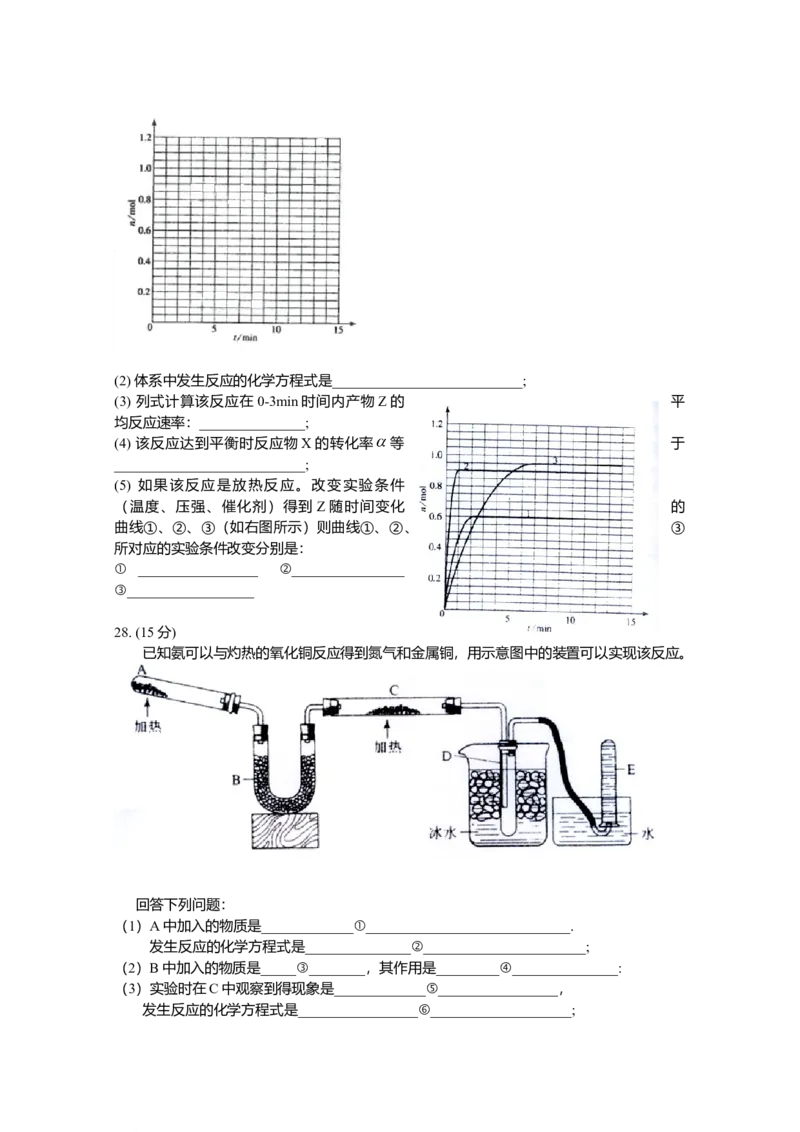
某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随
时间的变化如表所示。
(1)根据左表中数据,在右图中画出X、Y、Z的物质的量(n)随时间(t)变化的曲线:
t/min X/mol Y/mol Z/mol
0 1.00 1.00 0.00
1 0.90 0.80 0.20
3 0.75 0.50 0.50
5 0.65 0.30 0.70
9 0.55 0.10 0.90
10 0.55 0.10 0.90
14 0.55 0.10 0.90(2) 体系中发生反应的化学方程式是___________________________;
(3) 列式计算该反应在0-3min时间内产物Z的 平
均反应速率:_______________;
(4) 该反应达到平衡时反应物X的转化率 等 于
___________________________;
(5) 如果该反应是放热反应。改变实验条件
(温度、压强、催化剂)得到 Z随时间变化 的
曲线①、②、③(如右图所示)则曲线①、②、 ③
所对应的实验条件改变分别是:
① _________________ ②________________
③__________________
28. (15分)
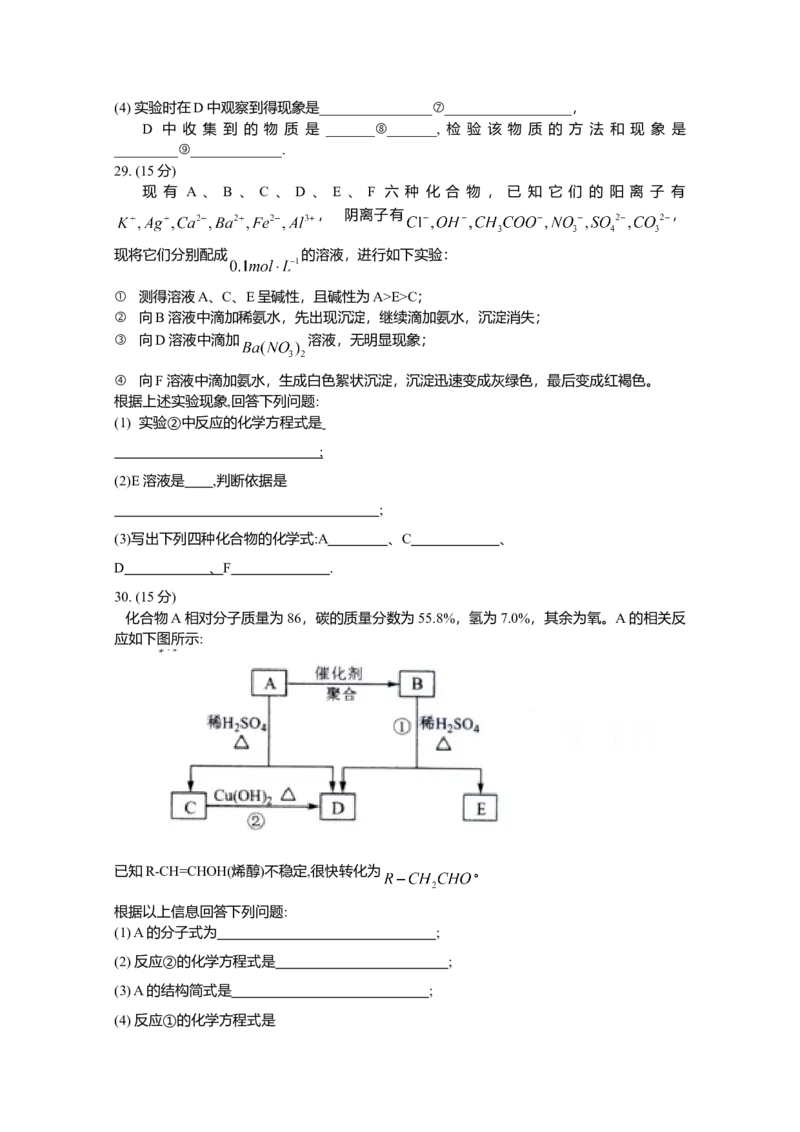
已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。
回答下列问题:
(1)A中加入的物质是_____________①_____________________________.
发生反应的化学方程式是_______________②_______________________;
(2)B中加入的物质是_____③________,其作用是_________④_______________:
(3)实验时在C中观察到得现象是_____________⑤_________________,
发生反应的化学方程式是_________________⑥____________________;(4) 实验时在D中观察到得现象是________________⑦__________________,
D 中 收 集 到 的 物 质 是 _______⑧_______, 检 验 该 物 质 的 方 法 和 现 象 是
_________⑨_____________.
29. (15分)
现 有 A 、 B 、 C 、 D 、 E 、 F 六 种 化 合 物 , 已 知 它 们 的 阳 离 子 有
, 阴离子有 ,
现将它们分别配成 的溶液,进行如下实验:
① 测得溶液A、C、E呈碱性,且碱性为A>E>C;
② 向B溶液中滴加稀氨水,先出现沉淀,继续滴加氨水,沉淀消失;
③ 向D溶液中滴加 溶液,无明显现象;
④ 向F溶液中滴加氨水,生成白色絮状沉淀,沉淀迅速变成灰绿色,最后变成红褐色。
根据上述实验现象,回答下列问题:
(1) 实验②中反应的化学方程式是
;
(2)E溶液是 ,判断依据是
;
(3)写出下列四种化合物的化学式:A 、C 、
D 、 F .
30. (15分)w.w.w.k.s.5.u.c.o.m
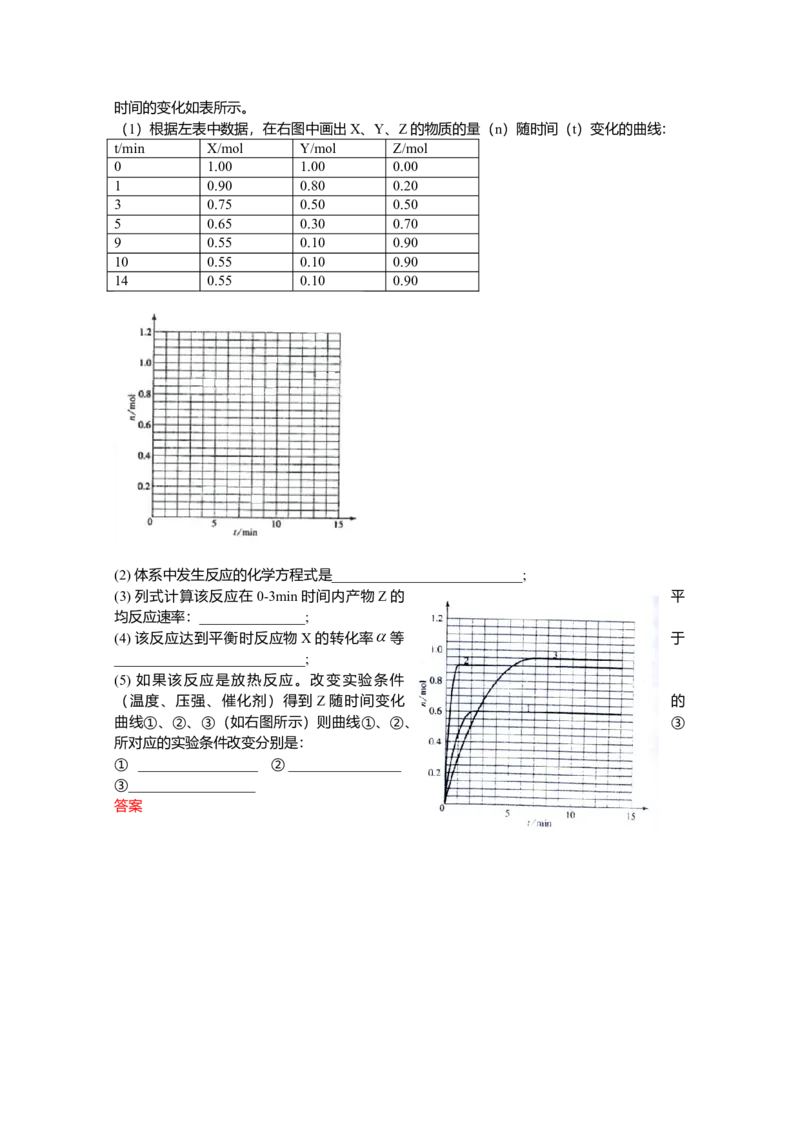
化合物A相对分子质量为86,碳的质量分数为55.8%,氢为7.0%,其余为氧。A的相关反
应如下图所示:
已知R-CH=CHOH(烯醇)不稳定,很快转化为 。
根据以上信息回答下列问题:
(1) A的分子式为 ;
(2) 反应②的化学方程式是 ;
(3) A的结构简式是 ;
(4) 反应①的化学方程式是;
(5) A有多种同分异构体,写出四个同时满足(i)能发生水解反应(ii)能使溴的四氯化碳溶液褪色
两个条件的同分异构体的结构简式: 、 、 、
;
(6)A的另一种同分异构体,其分子中所有碳原子在一条直线上,它的结构简式为
。
第Ⅰ卷
(选择题)
本卷共21小题,每小题6分,共126分。
以下数据可供解题时参考:
相对原子质量(原子量):H – 1 C – 12 N – 14 O - 16一、 选择题(本题共13小题。在每小题给出的四个选项中,只有一项是符合题目要求
的。)
6. 物质的量之比为2:5的锌与稀硝酸反应,若硝酸被还原的产物为NO,反应结束后锌没有
2
剩余,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是
A. 1:4 B.1:5 C. 2:3 D.2:5
答案A
【解析】设2molZn参与反应,因Zn无剩余,则最终生成了2molZn(NO),显然含有4molNO
3 2 3
- ,这部分是没有参与氧化还原反应的HNO,根据得失电子守恒有:2×n(Zn)=n(HNO)×4,
3 3
则n(HNO)=1mol,即有1molHNO 被还原。
3 3
7. 下列关于溶液和胶体的叙述,正确的是
A. 溶液是电中性的,胶体是带电的
B. 通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动
C. 溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动
D. 一束光线分别通过溶液和胶体时,后者会出现明显的光带,前者则没有
答案D
【解析】胶体本身是不带电,只是其表面积较大,吸附了溶液中的离子而带了电荷,故A项
错;溶液中的溶质,要看能否电离,若是非电解质,则不导电,也即不会移动,B项错;溶
液中溶质粒子没有规律,C项错;丁达尔效应可以用来区分溶液和胶体,D项正确。
8. 下列叙述中正确的是
A. 向含有CaCO 沉淀的水中通入CO 至沉淀恰好溶解,再向溶液中加入NaHCO 饱
3 2 3
和溶液,又有CaCO 沉淀生成
3
B. 向Na CO 溶液中逐滴加入等物质的量的稀盐酸,生成的 CO 与原Na CO 的物质的
2 3 2 2 3
量之比为1:2.
C. 等质量的NaHCO 和Na CO 分别与足量盐酸反应,在同温同压下,生成的CO 体积
3 2 3 2
相同
D. 向Na CO 饱和溶液中通入CO,有NaHCO 结晶析出
2 3 2 3
答案D
【解析】CaCO 与CO 反应生成Ca(HCO),再加入NaHCO 是没有现象的,A项错;向NaCO 溶液
3 2 3 2 3 2 3
中逐滴加入等物质的量的稀盐酸,仅生成NaHCO,无CO 气体放出,B项错;等质量的NaHCO
3 2 3
和NaCO,其中NaHCO 的物质的量多,与足量HCl反应时,放出的CO 多,C项错;D项,发
2 3 3 2
生的反应为:NaCO + CO + HO =2NaHCO↓,由于NaHCO 的溶解性较小,故有结晶析出,正确。
2 3 2 2 3 3
9. 某元素只存在两种天然同位素,且在自然界它们的含量相近,其相对原子质量为152.0,原
子核外的电子数为63。下列叙述中错误的是
A. 它是副族元素 B. 它是第六周期元素
C. 它的原子核内有63个质子 D. 它的一种同位素的核内有89个中子
答案D
【解析】核外电子数等于其质子数,C项正确;用质子数分别减去各周期所含有的元素种类,
63-2-8-8-18-18=9,显然其属于第六周期,从左到右的第9种,而第六周期中包含镧系,所
以它应属于副族,A项、B项均正确;由于存在同位素,所以相对原子质量应是同位素的平均
值,而不代表其中一种元素的质量数,故中子数不能用152-63=89来计算,D项错。
10. 现有等浓度的下列溶液:①醋酸,②苯酚,③苯酚钠,④碳酸,⑤碳酸钠,⑥碳酸氢钠。按溶液pH由小到大排列正确的是
A. ④①②⑤⑥③ B. ④①②⑥⑤③
C. ①④②⑥③⑤ D. ①④②③⑥⑤
答案C
【解析】①②④均属于酸,其中醋酸最强,碳酸次之,苯酚最弱。③⑤⑥均属于强碱弱酸盐,
根据越弱越水解的原理知,因HCO>苯酚>HCO- ,所以对应的盐,其碱性为:碳酸钠>苯酚钠
2 3 3
>碳酸氢钠,pH顺序相反,故C项正确。
11. 已知:2H(g)+ O(g)=2HO(l) ΔH= -571.6KJ· mol-1
2 2 2
CH(g)+ 2O(g)=CO(g)+2HO(l) ΔH= -890KJ· mol-1
4 2 2 2
现有H 与CH 的混合气体112L(标准状况),使其完全燃烧生成CO 和HO(l),若实验
2 4 2 2
测得反应放热3695KJ,则原混合气体中H 与CH 的物质的量之比是
2 4
A.1∶1 B.1∶3
C.1∶4 D.2∶3
答案B
【解析】设H、CH 的物质的量分别为x、ymol。则x + y =5,571.6x/2 + 890y = 3695,解得
2 4
x=1.25mol; y=3.75mol,两者比为1:3,故选B项。
O O
12、1 mol HO 与足量的NaOH
—OC— —OCCH
3
溶液充分反应,消耗的NaOH的物质的量为
A.5 mol B.4 mol C.3 mol D.2 mol
答案A
【解析】该有机物含有酚,还有两个酯基,要注意该有机物的酯基与NaOH水解时,生成羧酸
钠,此外生成的酚还要继续消耗NaOH,故需要5molNaOH,A项正确。
13. 含有a mol FeBr 的溶液中,通入x mol Cl 。下列各项为通Cl 过程中,溶液内发生反应的
2 2 2
离子方程式,其中不正确的是
A.x=0.4a,2Fe2++Cl=2Fe3++2Cl-
2
B.x=0.6a,2Br-+ Cl=Br +2Cl-
2 2
C.x=a,2Fe2++2Br-+2Cl=Br +2Fe3++4Cl-
2 2
D.x=1.5a,2Fe2++4Br-+3Cl=2Br +2Fe3++6Cl-
2 2
答案B
【解析】由于Fe2+的还原性强于Br-,故根据氧化还原反应的先后顺序知,Cl 先氧化Fe2+,
2
然后再氧化Br-。2Fe2+ + Cl 2Fe3+ + 2Cl-,2Br-+ Cl Br + 2Cl-,2FeBr + 3Cl
2 2 2 2 2
2FeCl + 2Br 。当x/a ≤0.5时,Cl 仅氧化Fe2+,故A项正确。当x/a ≥1.5时,Fe2+和
3 2 2
Br-合部被氧化,D项正确;当介于两者之间时,则要分步书写方程式,然后进行叠加得总反
应。如B项,当x=0.5a时,Cl 刚好把Fe2+全部氧化,而当x=0.6a,显然Cl 还要氧化Br-,
2 2
而选项中没有表示,故错。
第Ⅱ卷 非选择题
27. (15分)
某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示。
(1)根据左表中数据,在右图中画出X、Y、Z的物质的量(n)随时间(t)变化的曲线:
t/min X/mol Y/mol Z/mol
0 1.00 1.00 0.00
1 0.90 0.80 0.20
3 0.75 0.50 0.50
5 0.65 0.30 0.70
9 0.55 0.10 0.90
10 0.55 0.10 0.90
14 0.55 0.10 0.90
(2) 体系中发生反应的化学方程式是___________________________;
(3) 列式计算该反应在0-3min时间内产物Z的 平
均反应速率:_______________;
(4) 该反应达到平衡时反应物X的转化率 等 于
___________________________;
(5) 如果该反应是放热反应。改变实验条件
(温度、压强、催化剂)得到 Z随时间变化 的
曲线①、②、③(如右图所示)则曲线①、②、 ③
所对应的实验条件改变分别是:
① _________________ ②________________
③__________________
答案【解析】本题考查化学反应速率和化学平衡的综合运用,注意图像和有关计算。
(1)根据题目中表格给出的数据,在坐标系中找出相应的点,然后用光滑的曲线描点即可。
(2)根据题意,可以利用“三步法”求解
aX + bY cZ
开始 1.00 1.00 0
转化 0.45 0.9 0.9
平衡 0.55 0.1 0.9
根据各物质的量之比可得体系中发生反应的化学方程式是: X+2Y 2Z。
(3)根据图像可知在 3min 时,生成物 Z 的物质的量为 0.5mol, 其平均速率
为0.083mol/L·min。
(4)X的转化率等于0.45。
(5)由题目所给图象可知,在1中,平衡时Z的物质的量小于原平衡的物质的量,说明平衡
逆向移动,条件为升高温度。在2中,平衡时Z的物质的量与原平衡相同,且速率加快,条
件为加入催化剂;在3中,平衡正向移动,且速率加快,条件为加压。
28. (15分)
已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。
回答下列问题:(1)A中加入的物质是_____________①_____________________________.
发生反应的化学方程式是_______________②_______________________;
(2)B中加入的物质是_____③________,其作用是_________④_______________:
(3)实验时在C中观察到得现象是_____________⑤_________________,
发生反应的化学方程式是_________________⑥____________________;
(4) 实验时在D中观察到得现象是________________⑦__________________,
D 中 收 集 到 的 物 质 是 _______⑧ _______, 检 验 该 物 质 的 方 法 和 现 象 是
_________⑨_____________.
答案
【解析】本题考查化学实验和有关化学方程式,注意化学实验现象的描述和试剂的选择。根
据反应原理,反应物为氨气和氧化铜,可以判断试管A为制取氨气的装置,因此装入的药品
应该为氯化铵和氢氧化钙,氨气要使用碱石灰。加热后,黑色氧化铜变为红色的铜,生成的
水和氨气生成氨水留在了D中,而氮气通过排水法进行收集。检验氨气可利用其碱性,检验
水可以用无水硫酸铜。
29. (15分)
现 有 A 、 B 、 C 、 D 、 E 、 F 六 种 化 合 物 , 已 知 它 们 的 阳 离 子 有
, 阴离子有 ,
现将它们分别配成 的溶液,进行如下实验:
① 测得溶液A、C、E呈碱性,且碱性为A>E>C;
② 向B溶液中滴加稀氨水,先出现沉淀,继续滴加氨水,沉淀消失;
③ 向D溶液中滴加 溶液,无明显现象;
④ 向F溶液中滴加氨水,生成白色絮状沉淀,沉淀迅速变成灰绿色,最后变成红褐色。
根据上述实验现象,回答下列问题:
(1) 实验②中反应的化学方程式是
;
(2)E溶液是 ,判断依据是
;
(3)写出下列四种化合物的化学式:A 、C 、
D 、F .
答案【解析】本题考查离子共存、盐类水解综合运用。根据溶液的性质,确定CO2—只能与K+形成
3
显碱性的溶液,另外可能形成的碱性溶液为碱Ba(OH) 。由于醋酸的酸性大于碳酸,所以醋
2
酸盐水解的碱性小于碳酸盐,因此A为Ba(OH) ,E为KCO ,C为醋酸盐,由②可得B中阳离
2 2 3
子为Ag+,则肯定为AgNO ,由③可得D中无SO2—,则F中的阴离子为SO2—,D中的阴离子为
3 4 4
Cl—。由④可得F中的阳离子为Fe2+,即F为FeSO ,而CHCOO—若与Al3+形成溶液时,Al3+也
4 3
发生水解,所以C为醋酸钙,而D为AlCl。
3
30. (15分)w.w.w.k.s.5.u.c.o.m
化合物A相对分子质量为86,碳的质量分数为55.8%,氢为7.0%,其余为氧。A的相关反
应如下图所示:
已知R-CH=CHOH(烯醇)不稳定,很快转化为 。
根据以上信息回答下列问题:
(1) A的分子式为 ;
(2) 反应②的化学方程式是 ;
(3) A的结构简式是 ;
(4) 反应①的化学方程式是
;
(5) A有多种同分异构体,写出四个同时满足(i)能发生水解反应(ii)能使溴的四氯化碳溶液褪色
两个条件的同分异构体的结构简式: 、 、 、
;
(6)A的另一种同分异构体,其分子中所有碳原子在一条直线上,它的结构简式为
。
答案【解析】本题考查有机物的结构推断和性质,注意结构简式、同分异构体、化学方程式的书
写。根据题意,A分子中碳的原子数为4个,氢原子的个数为6个,则氧原子的个数为2个,
即A的分子式为CHO。由于A可以发生聚合反应,说明含有碳碳双键,在硫酸存在条件下生
4 6 2
成两种有机物,则为酯的水解,即A中含有酯基。根据不饱和度,没有其他功能团。由 A的
水解产物 C 和 D 的关系可判断 C 与 D 中的碳原子数相等,均为两个。则 A 的结构为
CHCOOCH=CH ,因此A在酸性条件下水解后得到CHCOOH和CH=CHOH,碳碳双键的碳原子上接
3 2 3 2
羟基不稳定,转化为CHCHO。A聚合反应后得到的产物B为 ,在酸性条件下水
3
解,除了生成乙酸和 。
w.w.w.k.s.5.u.c.o.m