文档内容
2011 年全国统一高考化学试卷(新课标)
一、选择题
1.下列叙述正确的是( )
A.1.00molNaCl 中含有6.02×1023个NaCl 分子
B.1.00molNaCl 中,所有 Na+的最外层电子总数为8×6.02×1023
C.欲配置1.00L,1.00mol.L﹣1的NaCl 溶液,可将58.5gNaCl 溶于1.00L 水中
D.电解58.5g熔融的NaCl,能产生22.4L 氯气(标准状况)、23.0g金属钠
2.分子式为 C H Cl 的同分异构体共有(不考虑立体异构)( )
5 11
A.6种 B.7种 C.8种 D.9种
3.下列反应中,属于取代反应的是( )
①CH CH=CH +Br CH CHBrCH Br
3 2 2 3 2
②CH CH OH CH =CH +H O
3 2 2 2 2
③CH COOH+CH CH OH CH COOCH CH +H O
3 3 2 3 2 3 2
④C H +HNO C H NO +H O.
6 6 3 6 5 2 2
A.①② B.③④ C.①③ D.②④
4.将浓度为 0.1mol•L﹣1HF 溶液加水不断稀释,下列各量始终保持增大的是
( )
A.c(H+) B.K (HF) C. D.
a
5.铁镍蓄电池又称爱迪生电池,放电时的总反应为:Fe+Ni O +3H O=Fe(OH)
2 3 2
+2Ni(OH) 下列有关该电池的说法不正确的是( )
2 2
A.电池的电解液为碱性溶液,正极为Ni O 、负极为Fe
2 3
B.电池放电时,负极反应为Fe+2OH﹣﹣2e﹣=Fe(OH)
2
C.电池充电过程中,阴极附近溶液的碱性减弱
D.电池充电时,阳极反应为2Ni(OH) +2OH﹣﹣2e﹣=Ni O +3H O
2 2 3 2
6.能正确表示下列反应的离子方程式为( )
A.硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H S↑
2
B.NH HCO 溶于过量的NaOH溶液中:HCO ﹣+OH﹣=CO 2﹣+H O
4 3 3 3 2
第1页(共7页)C.少量SO 通入苯酚钠溶液中:C H O﹣+SO +H O=C H OH+HSO ﹣
2 6 5 2 2 6 5 3
D.大理石溶于醋酸中:CaCO +2CH COOH=Ca2++2CH COO﹣+CO ↑+H O
3 3 3 2 2
7.短周期元素 W、X、Y 和 Z 的原子序数依次增大.元素 W是制备一种高效电
池的重要材料,X 原子的最外层电子数是内层电子数的 2倍,元素 Y 是地壳
中含量最丰富的金属元素,Z 原子的最外层电子数是其电子层数的 2倍.下
列说法错误的是( )
A.元素 W、X 的氯化物中,各原子均满足 8电子的稳定结构
B.元素 X 与氢形成的原子比为1:1的化合物有很多种
C.元素Y 的单质与氢氧化钠溶液或盐酸反应均有氢气生成
D.元素Z 可与元素X 形成共价化合物XZ
2
二、解答题(共 3小题,满分 29分)
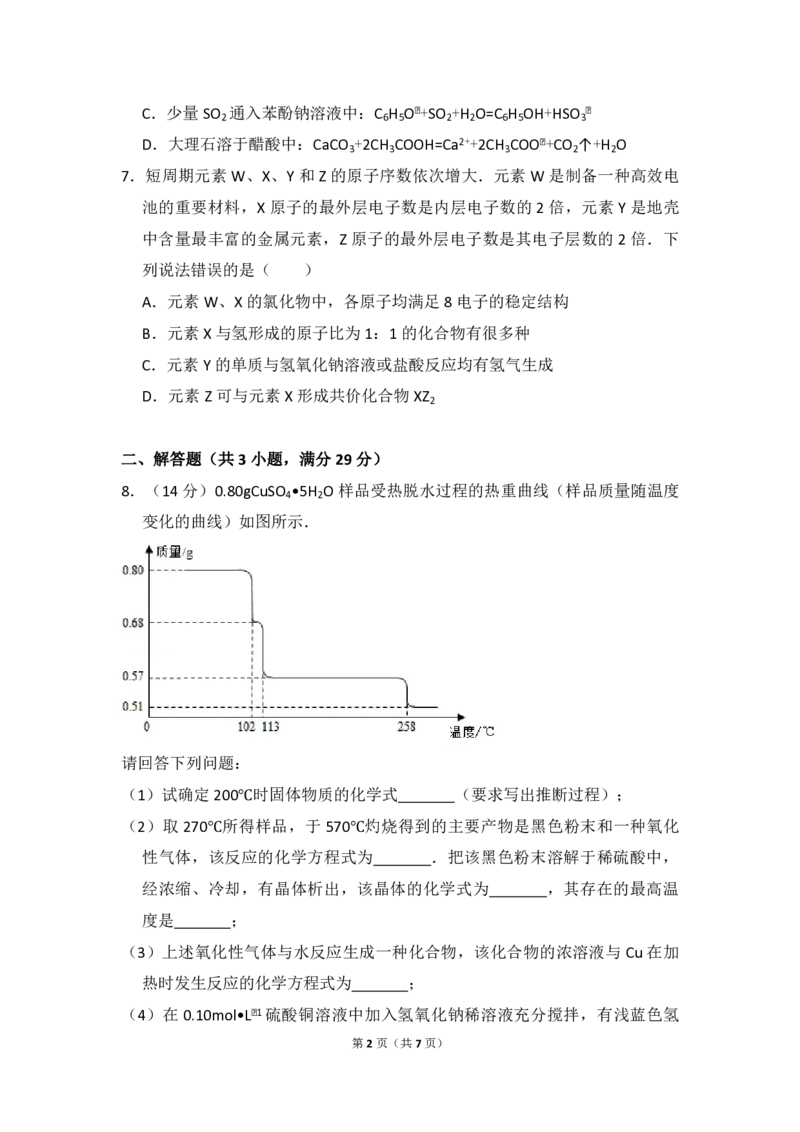
8.(14分)0.80gCuSO •5H O 样品受热脱水过程的热重曲线(样品质量随温度
4 2
变化的曲线)如图所示.
请回答下列问题:
(1)试确定200℃时固体物质的化学式 (要求写出推断过程);
(2)取 270℃所得样品,于 570℃灼烧得到的主要产物是黑色粉末和一种氧化
性气体,该反应的化学方程式为 .把该黑色粉末溶解于稀硫酸中,
经浓缩、冷却,有晶体析出,该晶体的化学式为 ,其存在的最高温
度是 ;
(3)上述氧化性气体与水反应生成一种化合物,该化合物的浓溶液与 Cu 在加
热时发生反应的化学方程式为 ;
(4)在 0.10mol•L﹣1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢
第2页(共7页)氧化铜沉淀生成,当溶液的 pH=8 时,c(Cu2+)= mol•L﹣1(K [Cu
sp
(OH) ]=2.2×10﹣20).若在 0.1mol•L﹣1硫酸铜溶液中通入过量 H S 气体,
2 2
使Cu2+完全沉淀为 CuS,此时溶液中的 H+浓度是 mol•L﹣1.
9.科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲
醇,并开发出直接以甲醇为燃料的燃料电池.已知 H (g)、CO(g)和
2
CH OH( l) 的 燃 烧 热 △ H 分 别 为 ﹣285.8kJ•mol﹣1、 ﹣283.0kJ•mol﹣1和
3
﹣726.5kJ•mol﹣1.请回答下列问题:
(1)用太阳能分解10mol 水消耗的能量是 kJ;
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为 ;
(3)在容积为 2L 的密闭容器中,由 CO 和 H 合成甲醇,在其他条件不变的情
2 2
况下,考察温度对反应的影响,实验结果如下图所示(注:T 、T 均大于
1 2
300℃);下列说法正确的是 (填序号)
①温度为 T 时,从反应开始到平衡,生成甲醇的平均速率为 v(CH OH)=
1 3
mol•L﹣1•min﹣1
②该反应在T 时的平衡常数比 T 时的小
1 2
③该反应为放热反应
④处于A点的反应体系从T 变到T ,达到平衡时 增大
1 2
(4)在 T 温度时,将 1molCO 和 3molH 充入一密闭恒容容器中,充分反应达
1 2 2
到平衡后,若CO 转化率为 a,则容器内的压强与起始压强之比为 ;
2
(5)在直接以甲醇为燃料的燃料电池中,电解质溶液为酸性,负极的反应式
为 ,正极的反应式为 .理想状态下,该燃料电池消耗 1mol
甲醇所能产生的最大电能为 702.1kJ,则该燃料电池的理论效率为
(燃料电池的理论效率是指电池所产生的最大电能与燃料电池反应所能释放
的全部能量之比).
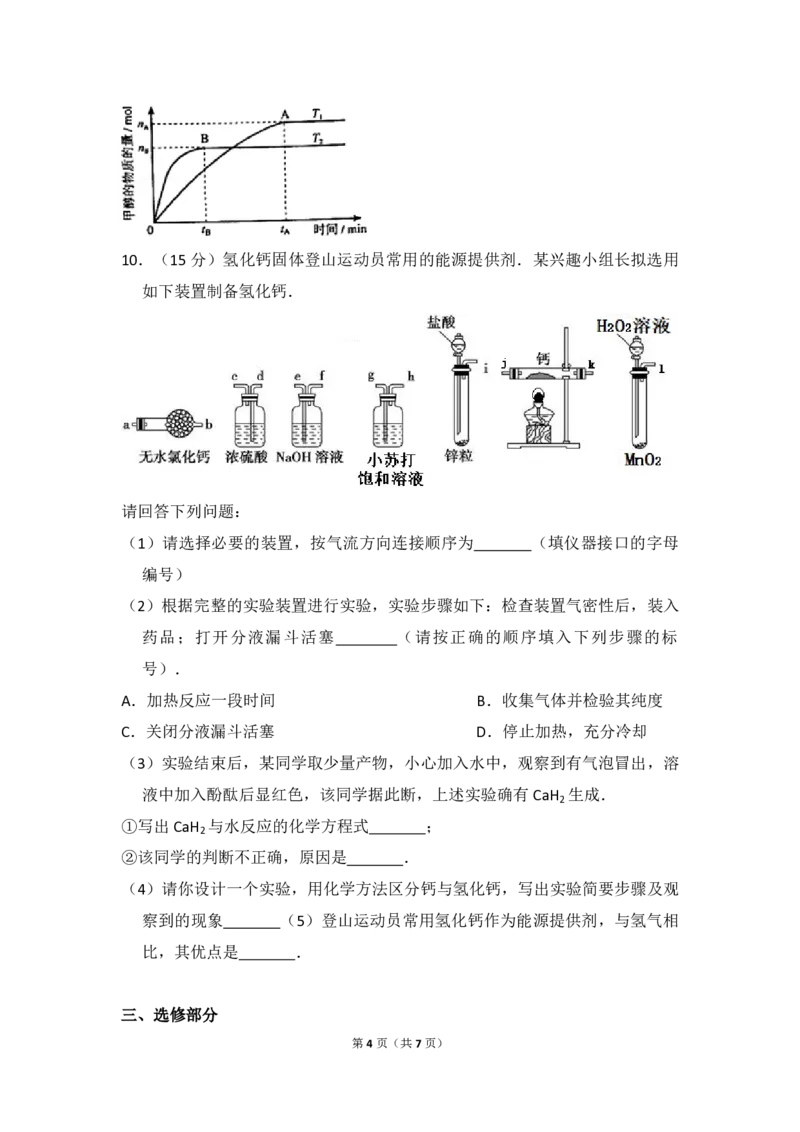
第3页(共7页)10.(15分)氢化钙固体登山运动员常用的能源提供剂.某兴趣小组长拟选用
如下装置制备氢化钙.
请回答下列问题:
(1)请选择必要的装置,按气流方向连接顺序为 (填仪器接口的字母
编号)
(2)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入
药品;打开分液漏斗活塞 (请按正确的顺序填入下列步骤的标
号).
A.加热反应一段时间 B.收集气体并检验其纯度
C.关闭分液漏斗活塞 D.停止加热,充分冷却
(3)实验结束后,某同学取少量产物,小心加入水中,观察到有气泡冒出,溶
液中加入酚酞后显红色,该同学据此断,上述实验确有 CaH 生成.
2
①写出CaH 与水反应的化学方程式 ;
2
②该同学的判断不正确,原因是 .
(4)请你设计一个实验,用化学方法区分钙与氢化钙,写出实验简要步骤及观
察到的现象 (5)登山运动员常用氢化钙作为能源提供剂,与氢气相
比,其优点是 .
三、选修部分
第4页(共7页)11.【化学﹣﹣选修2:化学与技术】
普通纸张的主要成分是纤维素,在早期的纸张生产中,常采用纸张表面涂敷明
矾的工艺,以填补其表面的微孔,防止墨迹扩散.请回答下列问题:
(1)人们发现纸张会发生酸性腐蚀而变脆、破损,严重威胁纸质文物的保
存.经分析检验,发现酸性腐蚀主要与造纸中涂敷明矾的工艺有关,其中的
化学原理是 ;为了防止纸张的酸性腐蚀,可在纸浆中加入碳酸钙等
添加剂,该工艺原理的化学(离子)方程式为 .
(2)为了保护这些纸质文物,有人建议采取下列措施:
①喷洒碱性溶液,如稀氢氧化钠溶液或氨水等.这样操作产生的主要问题
是 ;
②喷洒 Zn(C H ) .Zn(C H ) 可以与水反应生成氧化锌和乙烷.用化学
2 5 2 2 5 2
( 离 子 ) 方 程 式 表 示 该 方 法 生 成 氧 化 锌 及 防 止 酸 性 腐 蚀 的 原
理 、 .
(3)现代造纸工艺常用钛白粉(TiO )替代明矾.钛白粉的一种工业制法是以
2
钛铁矿(主要成分为 FeTiO )为原料按下列过程进行的,请完成下列化学方
3
程式:
① FeTiO + C+ Cl TiCl + FeCl +
3 2 4 3
CO
② TiCl + O TiO + Cl .
4 2 2 2
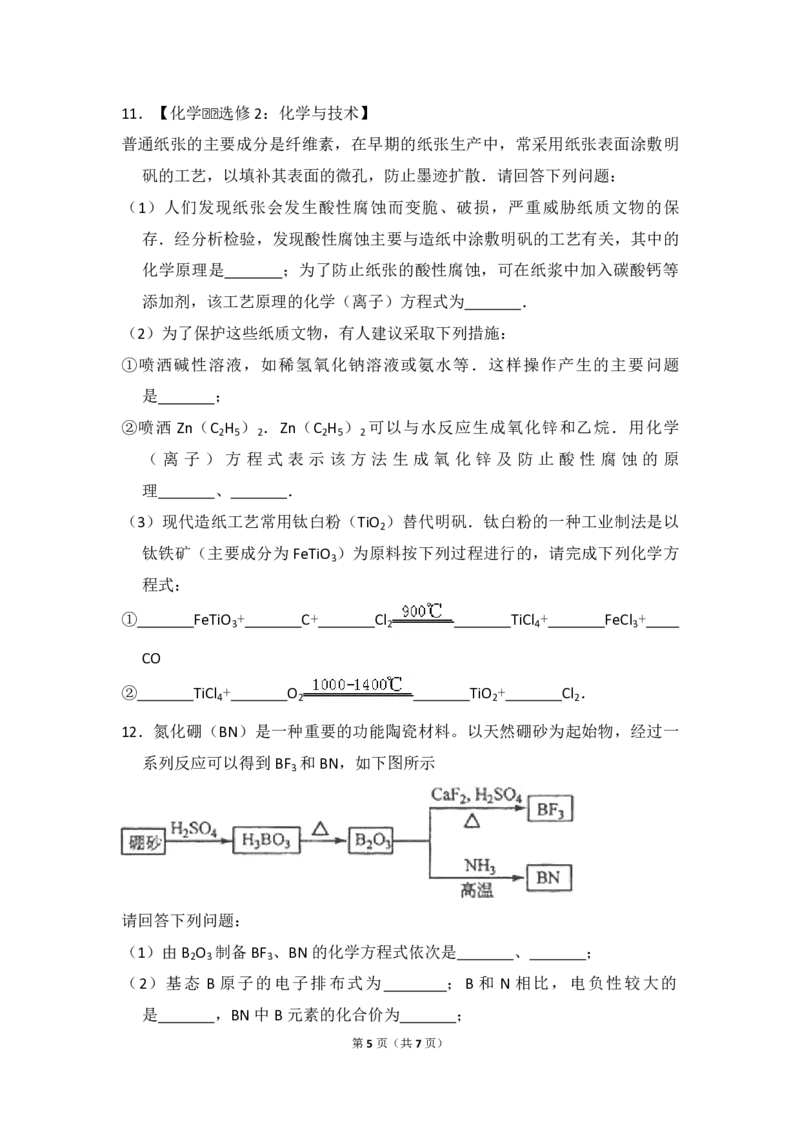
12.氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一
系列反应可以得到BF 和BN,如下图所示
3
请回答下列问题:
(1)由B O 制备BF 、BN的化学方程式依次是 、 ;
2 3 3
(2)基态 B原子的电子排布式为 ;B和 N相比,电负性较大的
是 ,BN中B元素的化合价为 ;
第5页(共7页)(3)在 BF 分子中,F﹣B﹣F 的键角是 ,B原子的杂化轨道类型
3
为 ,BF 和过量NaF 作用可生成NaBF ,BF ﹣的立体结构为 ;
3 4 4
(4)在与石墨结构相似的六方氮化硼晶体中,层内 B原子与 N原子之间的化
学键为 ,层间作用力为 ;
(5)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相
似,硬度与金刚石相当,晶胞边长为 361.5pm,立方氮化硼晶胞中含有
个氮原子、 个硼原子,立方氮化硼的密度是 g•pm﹣3(只要求
列算式,不必计算出数值,阿伏伽德罗常数为 N )。
A
13.香豆素是一种天然香料,存在于黑香豆、兰花等植物中.工业上常用水杨
醛 与 乙 酸 酐 在 催 化 剂 存 在 下 加 热 反 应 制 得 :
以下是由甲苯为原料生产香豆素的一种合成路线(部分反应条件及副产物已略
去 )
已知以下信息:
①A中有五种不同化学环境的氢
②B可与FeCl 溶液发生显色反应
3
③同一个碳原子上连有两个羟基通常不稳定,易脱水形成羰基.
请回答下列问题:
(1)香豆素的分子式为 ;
(2)由甲苯生成A的反应类型为 ;A的化学名称为
(3)由B生成C 的化学反应方程式为 ;
(4)B的同分异构体中含有苯环的还有 种,其中在核磁共振氢谱中只
出现四组峰的有 种;
(5)D 的同分异构体中含有苯环的还有 种,其中:
①既能发生银境反应,又能发生水解反应的是 (写结构简式)
第6页(共7页)②能够与饱和碳酸氢钠溶液反应放出CO 的是 (写结构简式)
2
第7页(共7页)