文档内容
2012 年天津市高考化学试卷
一、每题6分,共36分,只有一项是最符合题目要求的.
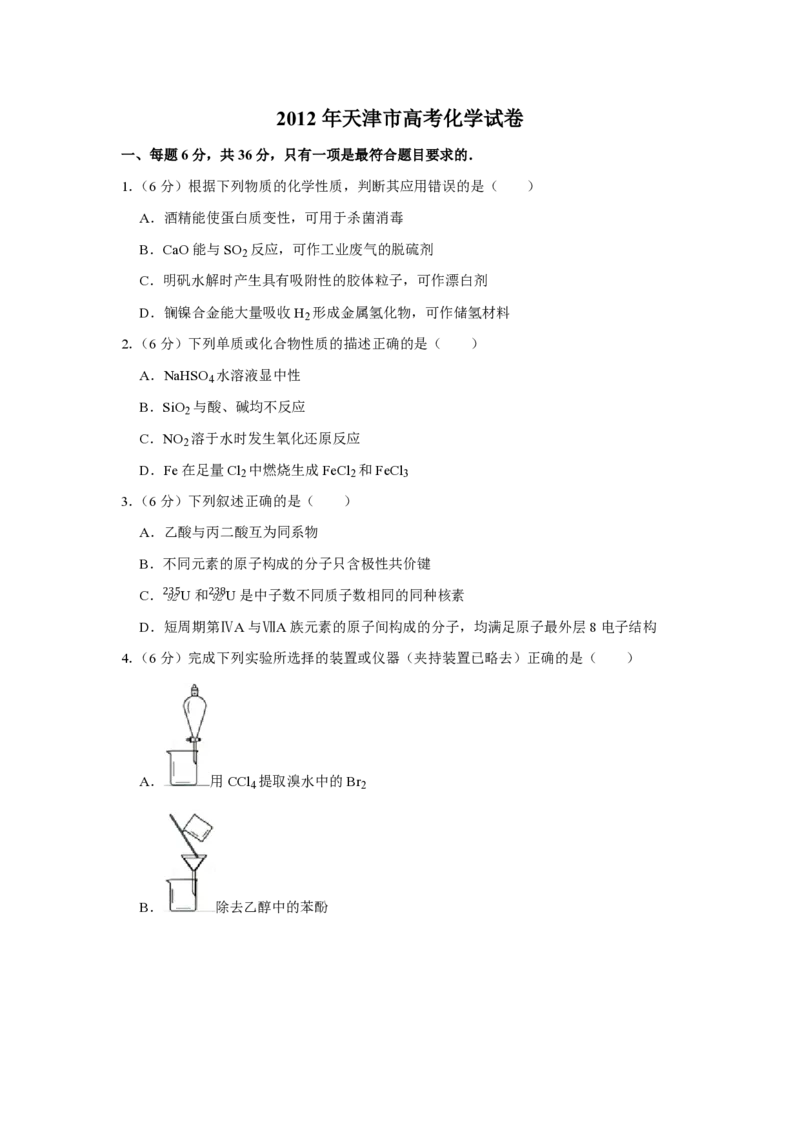
1.(6分)根据下列物质的化学性质,判断其应用错误的是( )
A.酒精能使蛋白质变性,可用于杀菌消毒
B.CaO能与SO 反应,可作工业废气的脱硫剂
2
C.明矾水解时产生具有吸附性的胶体粒子,可作漂白剂
D.镧镍合金能大量吸收H 形成金属氢化物,可作储氢材料
2
2.(6分)下列单质或化合物性质的描述正确的是( )
A.NaHSO 水溶液显中性
4
B.SiO 与酸、碱均不反应
2
C.NO 溶于水时发生氧化还原反应
2
D.Fe在足量Cl 中燃烧生成FeCl 和FeCl
2 2 3
3.(6分)下列叙述正确的是( )
A.乙酸与丙二酸互为同系物
B.不同元素的原子构成的分子只含极性共价键
C.2
9
3
2
5U和2
9
3
2
8U是中子数不同质子数相同的同种核素
D.短周期第ⅣA与ⅦA族元素的原子间构成的分子,均满足原子最外层8电子结构
4.(6分)完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是( )
A. 用CCl 提取溴水中的Br
4 2
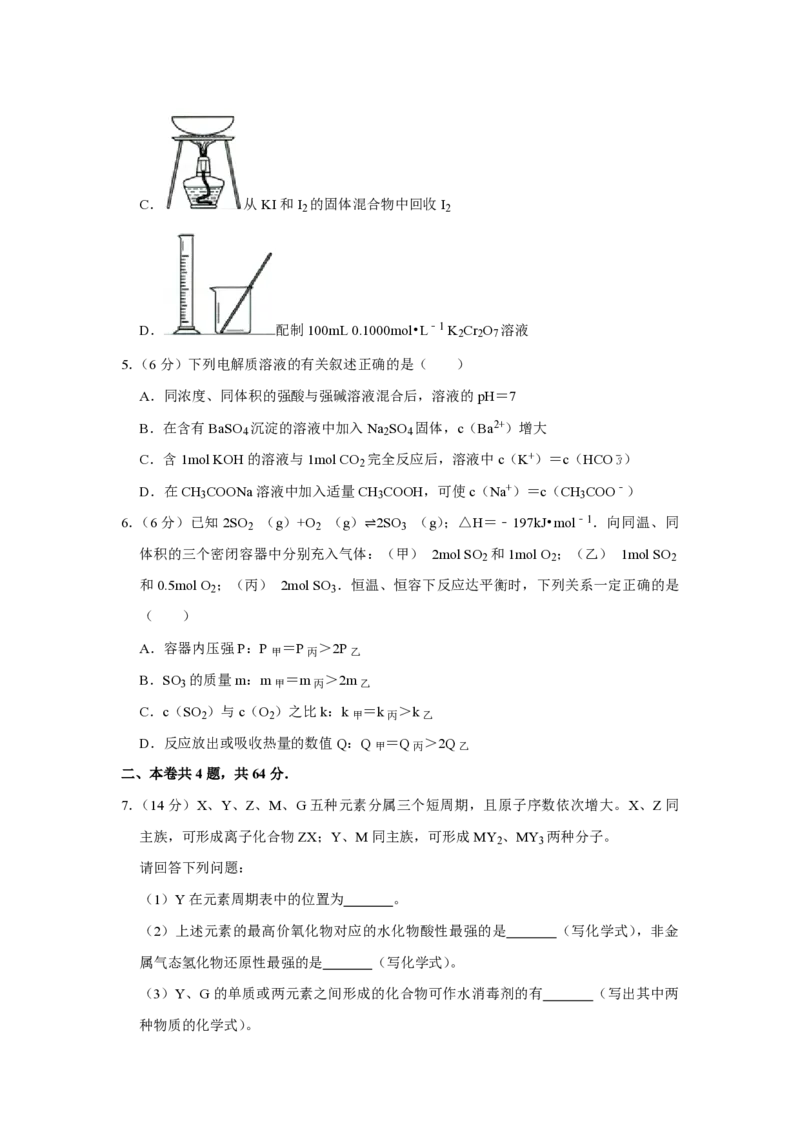
B. 除去乙醇中的苯酚C. 从KI和I 的固体混合物中回收I
2 2
D. 配制100mL 0.1000mol•L﹣1 K Cr O 溶液
2 2 7
5.(6分)下列电解质溶液的有关叙述正确的是( )
A.同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7
B.在含有BaSO 沉淀的溶液中加入Na SO 固体,c(Ba2+)增大
4 2 4
C.含1mol KOH的溶液与1mol CO
2
完全反应后,溶液中c(K+)=c(HCO3 ‒)
D.在CH COONa溶液中加入适量CH COOH,可使c(Na+)=c(CH COO﹣)
3 3 3
6.(6分)已知2SO (g)+O (g)⇌2SO (g);△H=﹣197kJ•mol﹣1.向同温、同
2 2 3
体积的三个密闭容器中分别充入气体:(甲) 2mol SO 和1mol O ;(乙) 1mol SO
2 2 2
和0.5mol O ;(丙) 2mol SO .恒温、恒容下反应达平衡时,下列关系一定正确的是
2 3
( )
A.容器内压强P:P
甲
=P
丙
>2P
乙
B.SO
3
的质量m:m
甲
=m
丙
>2m
乙
C.c(SO
2
)与c(O
2
)之比k:k
甲
=k
丙
>k
乙
D.反应放出或吸收热量的数值Q:Q
甲
=Q
丙
>2Q
乙
二、本卷共4题,共64分.
7.(14分)X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X、Z同
主族,可形成离子化合物ZX;Y、M同主族,可形成MY 、MY 两种分子。
2 3
请回答下列问题:
(1)Y在元素周期表中的位置为 。
(2)上述元素的最高价氧化物对应的水化物酸性最强的是 (写化学式),非金
属气态氢化物还原性最强的是 (写化学式)。
(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有 (写出其中两
种物质的化学式)。(4)X M的燃烧热△H=﹣a kJ•mol﹣1,写出 X M燃烧反应的热化学方程
2 2
式: 。
(5)ZX的电子式为 ;ZX与水反应放出气体的化学方程式为 。
(6)熔融状态下,Z的单质和FeG 能组成可充电电池(装置示意图如下),反应原理
2
放电
为:2Z+FeG2 ⇌Fe+2ZG. 放电时,电池的正极反应式为 ;充电时,
充电
(写物质名称)电极接电源的负极;该电池的电解质为 。
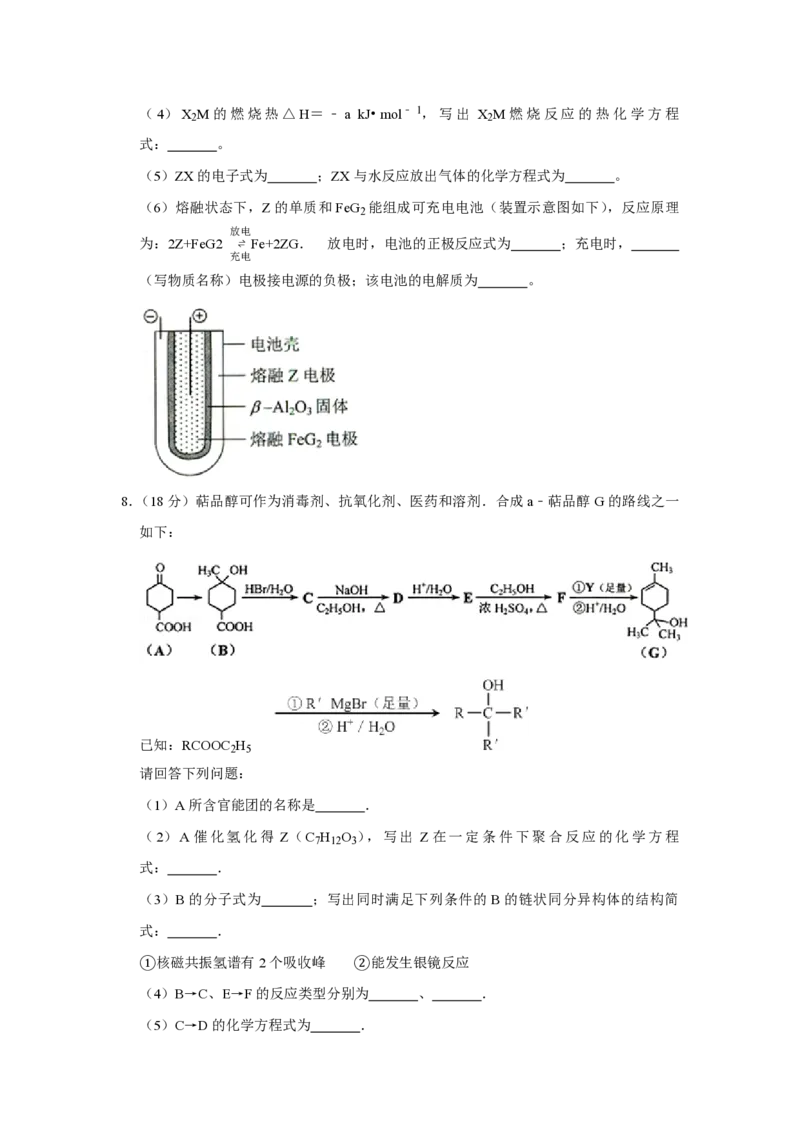
8.(18分)萜品醇可作为消毒剂、抗氧化剂、医药和溶剂.合成a﹣萜品醇G的路线之一
如下:
已知:RCOOC H
2 5
请回答下列问题:
(1)A所含官能团的名称是 .
(2)A催化氢化得 Z(C H O ),写出 Z在一定条件下聚合反应的化学方程
7 12 3
式: .
(3)B的分子式为 ;写出同时满足下列条件的B的链状同分异构体的结构简
式: .
①核磁共振氢谱有2个吸收峰 ②能发生银镜反应
(4)B→C、E→F的反应类型分别为 、 .
(5)C→D的化学方程式为 .(6)试剂Y的结构简式为 .
(7)通过常温下的反应,区别E、F和G的试剂是 和 .
(8)G与H O催化加成得不含手性碳原子(连有4个不同原子或原子团的碳原子叫手
2
性碳原子)的化合物H,写出H的结构简式: .
9.(18分)信息时代产生的大量电子垃圾对环境构成了极大的威胁.某“变废为宝”学生
探究小组将一批废弃的线路板简单处理后,得到含70%Cu、25%Al、4%Fe及少量Au、
Pt等金属的混合物,并设计出如图1制备硫酸铜和硫酸铝晶体的路线:
请回答下列问题:
(1)第①步Cu与酸反应的离子方程式为 ;
得到滤渣1的主要成分为 .
(2)第②步加H O 的作用是 ,使用H O 的优点是 ;调溶液pH的目
2 2 2 2
的是使 生成沉淀.
(3)用第③步所得CuSO •5H O制备无水CuSO 的方法是 .
4 2 4
( 4) 由 滤 渣 2制 取 Al ( SO ) • 18H O, 探 究 小 组 设 计 了 三 种 方 案 :
2 4 3 2
上述三种方案中, 方案不可行,原因是 :从原子利用率角度考虑,
方案更合理.
(5)探究小组用滴定法测定CuSO •5H O (M=250)含量.取a g试样配成100mL
4 2 r
溶液,每次取20.00mL,消除干扰离子后,用c mol•L﹣1 EDTA(H Y2﹣)标准溶液滴
2
定至终点,平均消耗EDTA溶液b mL.滴定反应如下:Cu2++H2Y2﹣=CuY2﹣+2H+
写出计算CuSO •5H O质量分数的表达式ω= ;
4 2
下列操作会导致CuSO •5H O含量的测定结果偏高的是 .
4 2
a.未干燥锥形瓶 b.滴定终点时滴定管尖嘴中产生气泡 c.未除净可与EDTA反应的干扰离子.
10.(14分)金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝。高
温下,在密闭容器中用H 还原WO 可得到金属钨,其总反应为:WO (s)+3H (g)
2 3 3 2
高温
⇌ W(s)+3H O(g)
2
请回答下列问题:
(1)上述反应的化学平衡常数表达式为 。
(2)某温度下反应达平衡时,H 与水蒸气的体积比为 2:3,则 H 的平衡转化率
2 2
为 ;随温度的升高,H 与水蒸气的体积比减小,则该反应为反应 (填
2
“吸热”或“放热”)。
(3)上述总反应过程大致分为三个阶段,各阶段主要成分与温度的关系如下表所示:
温度 25℃~550℃~600℃~700℃
主要成份 WO W O WO W
3 2 5 2
第一阶段反应的化学方程式为 ;580℃时,固体物质的主要成分为 ;假
设WO 完全转化为W,则三个阶段消耗H 物质的量之比为 。
3 2
(4)已知:温度过高时,WO (s)转变为WO (g);
2 2
WO (s)+2H (g)⇌W(s)+2H O(g);△H=+66.0kJ•mol﹣1
2 2 2
WO (g)+2H ⇌W(s)+2H O(g);△H=﹣137.9kJ•mol﹣1
2 2 2
则WO (s)⇌WO (g)的△H= 。
2 2
(5)钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I 可延长灯管的使用
2
寿命,其工作原理为:
1400℃
W(s)+2I (g) ⇌ WI (g)。
2 4
约3000℃
下列说法正确的有 。
a.灯管内的I 可循环使用
2
b.WI 在灯丝上分解,产生的W又沉积在灯丝上
4
c.WI 在灯管壁上分解,使灯管的寿命延长
4
d.温度升高时,WI 的分解速率加快,W和I 的化合速率减慢。
4 2