文档内容
2013年高考全国理综化学II卷
可能用到的相对原子质量:H 1 C 12 N 14 O 16 F 19 Na 23 Al 27 S 32 Cl 35.5 K 39 Ca 40 Cr
52 Fe 56 Ni 59 Cu 64 Zn 65
一、选择题:本题共7小题,每小题6分。在每小题给出的四个选项中,只有一项是符合题目要求的。
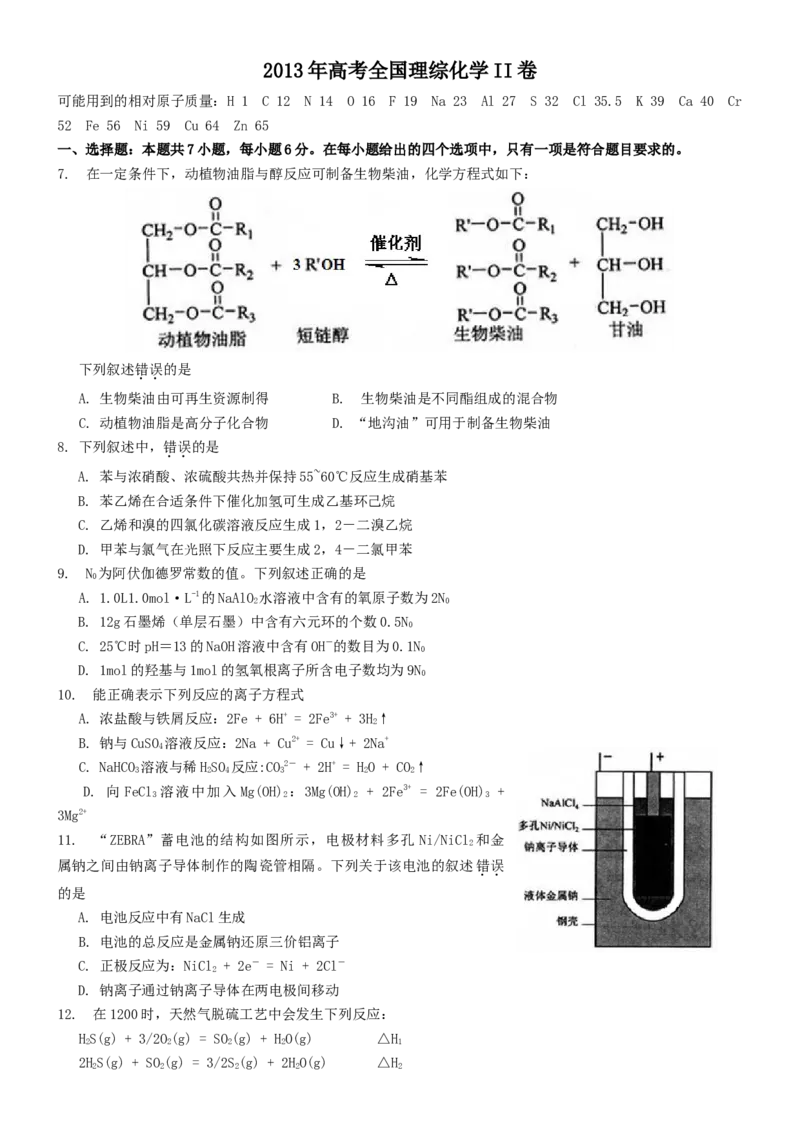
7. 在一定条件下,动植物油脂与醇反应可制备生物柴油,化学方程式如下:
下列叙述错误的是
A. 生物柴油由可再生资源制得 B. 生物柴油是不同酯组成的混合物
C. 动植物油脂是高分子化合物 D. “地沟油”可用于制备生物柴油
8. 下列叙述中,错误的是
A. 苯与浓硝酸、浓硫酸共热并保持55~60℃反应生成硝基苯
B. 苯乙烯在合适条件下催化加氢可生成乙基环己烷
C. 乙烯和溴的四氯化碳溶液反应生成1,2-二溴乙烷
D. 甲苯与氯气在光照下反应主要生成2,4-二氯甲苯
9. N 为阿伏伽德罗常数的值。下列叙述正确的是
0
A. 1.0L1.0mol·L-1的NaAlO 水溶液中含有的氧原子数为2N
2 0
B. 12g石墨烯(单层石墨)中含有六元环的个数0.5N
0
C. 25℃时pH=13的NaOH溶液中含有OH-的数目为0.1N
0
D. 1mol的羟基与1mol的氢氧根离子所含电子数均为9N
0
10. 能正确表示下列反应的离子方程式
A. 浓盐酸与铁屑反应:2Fe + 6H+ = 2Fe3+ + 3H↑
2
B. 钠与CuSO 溶液反应:2Na + Cu2+ = Cu↓+ 2Na+
4
C. NaHCO 溶液与稀HSO 反应:CO2- + 2H+ = HO + CO↑
3 2 4 3 2 2
D. 向 FeCl 溶液中加入 Mg(OH) :3Mg(OH) + 2Fe3+ = 2Fe(OH) +
3 2 2 3
3Mg2+
11. “ZEBRA”蓄电池的结构如图所示,电极材料多孔 Ni/NiCl 和金
2
属钠之间由钠离子导体制作的陶瓷管相隔。下列关于该电池的叙述错误
的是
A. 电池反应中有NaCl生成
B. 电池的总反应是金属钠还原三价铝离子
C. 正极反应为:NiCl + 2e- = Ni + 2Cl-
2
D. 钠离子通过钠离子导体在两电极间移动
12. 在1200时,天然气脱硫工艺中会发生下列反应:
HS(g) + 3/2O(g) = SO(g) + HO(g) △H
2 2 2 2 1
2HS(g) + SO(g) = 3/2S(g) + 2HO(g) △H
2 2 2 2 2HS(g) +1/2O(g) = S(g) + HO(g) △H
2 2 2 3
2S(g) = S(g) △H
2 4
则△H 的正确表达式为
4
A. △H = 2/3(△H + △H - 3△H) B. △H = 2/3(3△H - △H - △H)
4 1 2 3 4 3 1 2
C. △H = 3/2(△H + △H - 3△H) D. △H = 3/2(△H - △H - 3△H)
4 1 2 3 4 1 2 3
13. 室温时,M(OH)(s) M2+(aq) + 2OH-(aq) K = a。C(M2+) = b mol·L-1时,溶液的pH等于
2 sp
A. B.
C. D.
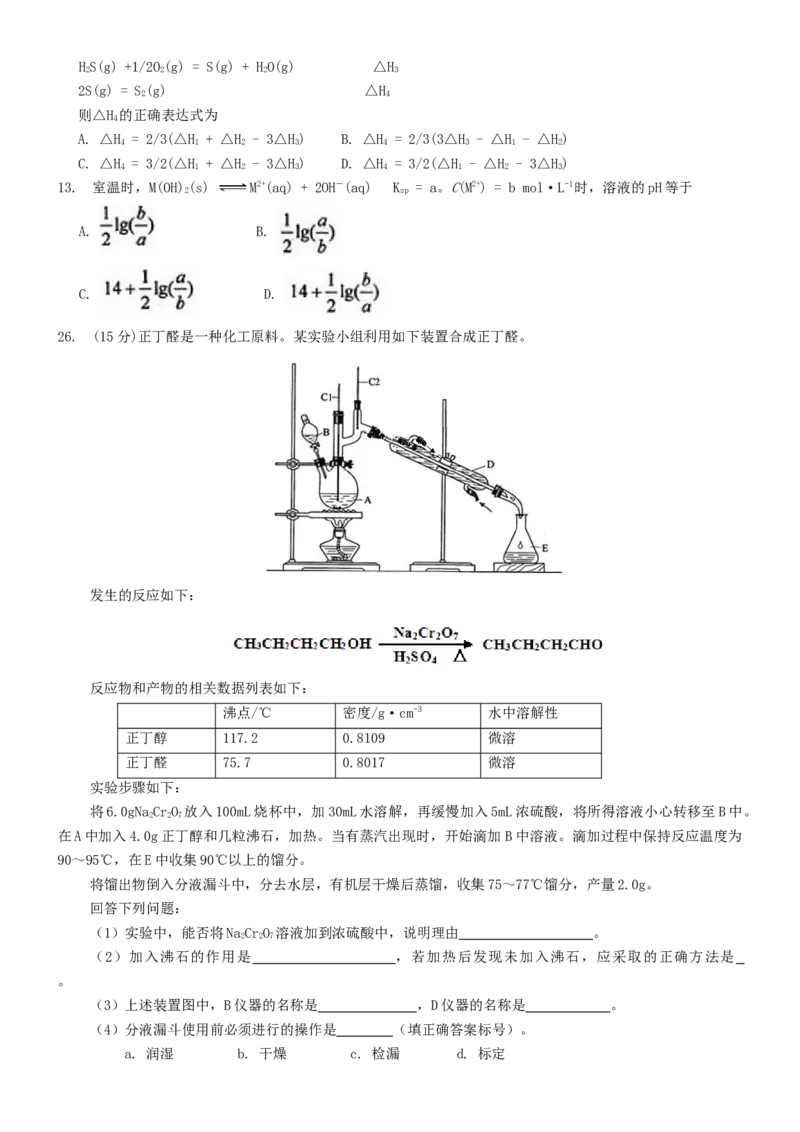
26. (15分)正丁醛是一种化工原料。某实验小组利用如下装置合成正丁醛。
发生的反应如下:
反应物和产物的相关数据列表如下:
沸点/℃ 密度/g·cm-3 水中溶解性
正丁醇 117.2 0.8109 微溶
正丁醛 75.7 0.8017 微溶
实验步骤如下:
将6.0gNaCrO 放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中。
2 2 7
在A中加入4.0g正丁醇和几粒沸石,加热。当有蒸汽出现时,开始滴加 B中溶液。滴加过程中保持反应温度为
90~95℃,在E中收集90℃以上的馏分。
将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77℃馏分,产量2.0g。
回答下列问题:
(1)实验中,能否将NaCrO 溶液加到浓硫酸中,说明理由 。
2 2 7
(2)加入沸石的作用是 ,若加热后发现未加入沸石,应采取的正确方法是
。
(3)上述装置图中,B仪器的名称是 ,D仪器的名称是 。
(4)分液漏斗使用前必须进行的操作是 (填正确答案标号)。
a. 润湿 b. 干燥 c. 检漏 d. 标定(5)将正丁醛粗产品置于分液漏斗中分水时,水在 层(填“上”或“下”)。
(6)反应温度应保持在90~95℃,其原因是 。
(7)本实验中,正丁醛的产率为 %。
27. (14分) 氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。纯化工业级氧化锌(含有 Fe(II)、
Mn(II)、Ni(II)等杂质)的流程如下:
提示:在本实验条件下,Ni(II)不能被氧化;高锰酸钾的还原产物是MnO。
2
回答下列问题:
(1)反应②中除掉的杂质离子是 ,发生反应的离子方程式为
;在加高锰酸钾溶液前,若pH较低,对除杂的影响是 。
(2)反应③的反应类型为 ,过滤得到的滤渣中,除了过量的锌外还有 。
(3)反应④形成的沉淀要用水洗,检查沉淀是否洗涤干净的方法是 。
(4)反应④中产物的成分可能是ZnCO·xZn(OH) 。取干燥后的滤饼11.2g,锻烧后可得到产品8.1g,则
3 2
x等于 。
28. (14分)在1.0L密闭容器中放入0.10molA(g),在一定温度进行如下反应:
A(g) B(g) + C(g ) △H =+85.1kJ·mol-1
反应时间(t)与容器内气体总压强(p)的数据见下表:
时间t/h 0 1 2 4 8 16 20 25 30
总压强p/100kPa 4.91 5.58 6.32 7.31 8.54 9.50 9.52 9.53 9.53
回答下列问题:
(1)欲提高A的平衡转化率,应采取的措施为 。
(2)由总压强p和起始压强p计算反应物A的转化率α(A)的表达式为 ,
0
平衡时A的转化率为 ,列式并计算反应的平衡常数K 。
(3)①由总压强p和起始压强p表示反应体系的总物质的量n 和反应物A的物质的量n(A), n =
0 总 总
mol,n(A)= mol。
②下表为反应物A浓度与反应时间的数据,计算:α= 。
反应时间t/h 0 4 8 16
c(A)/(mol·L-1) 0.10 a 0.026 0.0065
分析该反应中反应物的浓度c(A)变化与时间间隔(△t)的规律,得出的结论是 ,
由此规律推出反应在12h时反应物的浓度c(A)为 mol·L-1。
36. 〔化学——选修2:化学与技术〕(15分)
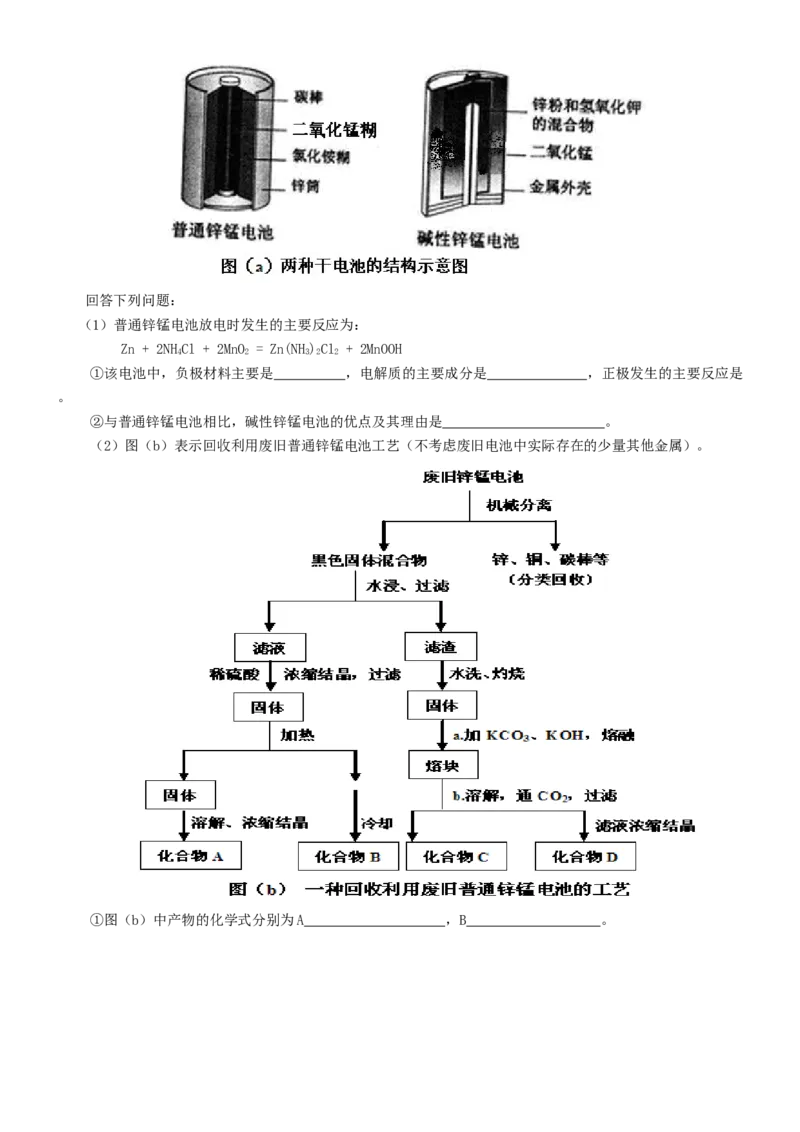
锌锰电池(俗称干电池)在生活中的用量很大。两种锌锰电池的构造如图(a)所示。回答下列问题:
(1)普通锌锰电池放电时发生的主要反应为:
Zn + 2NHCl + 2MnO = Zn(NH)Cl + 2MnOOH
4 2 3 2 2
①该电池中,负极材料主要是 ,电解质的主要成分是 ,正极发生的主要反应是
。
②与普通锌锰电池相比,碱性锌锰电池的优点及其理由是 。
(2)图(b)表示回收利用废旧普通锌锰电池工艺(不考虑废旧电池中实际存在的少量其他金属)。
①图(b)中产物的化学式分别为A ,B 。②操作a中得到熔块的主要成分是KMnO 。操作b中,绿色的KMnO 溶液反应生成紫色溶液和一种黑褐色
2 4 2 4
固体,该反应的离子方程式为 。
③采用惰性电极电解KMnO 溶液也能得到化合物D,则阴极处
2 4
得到的主要物质是
(填化学式)。
37. 〔化学——选修3:物质结构与性质〕(15分)
前四周期原子序数依次增大的元素A、B、C、D中,A和B的
价电子层中未成对电子均只有一个,并且A-和B+的电子数相差为
8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分
别为4和2,且原子序数相差为2.
回答下列问题:
(1)D2+的价层电子排布图为 。
(2)四种元素中第一电离能最小的是 ,
电负性最大的是 。(填元素符号)
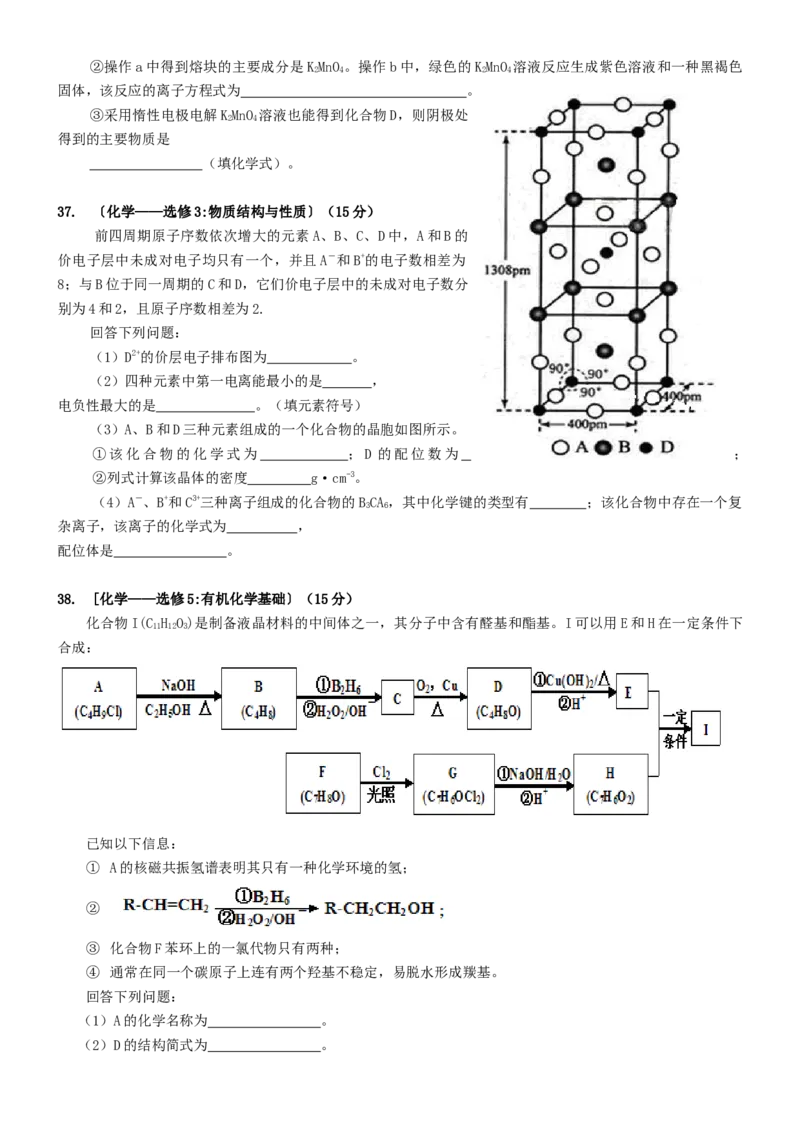
(3)A、B和D三种元素组成的一个化合物的晶胞如图所示。
①该化合物的化学式为 ;D 的配位数为 ;
②列式计算该晶体的密度 g·cm-3。
(4)A-、B+和C3+三种离子组成的化合物的BCA,其中化学键的类型有 ;该化合物中存在一个复
3 6
杂离子,该离子的化学式为 ,
配位体是 。
38. [化学——选修5:有机化学基础〕(15分)
化合物I(C H O)是制备液晶材料的中间体之一,其分子中含有醛基和酯基。I可以用E和H在一定条件下
11 12 3
合成:
已知以下信息:
① A的核磁共振氢谱表明其只有一种化学环境的氢;
②
③ 化合物F苯环上的一氯代物只有两种;
④ 通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
回答下列问题:
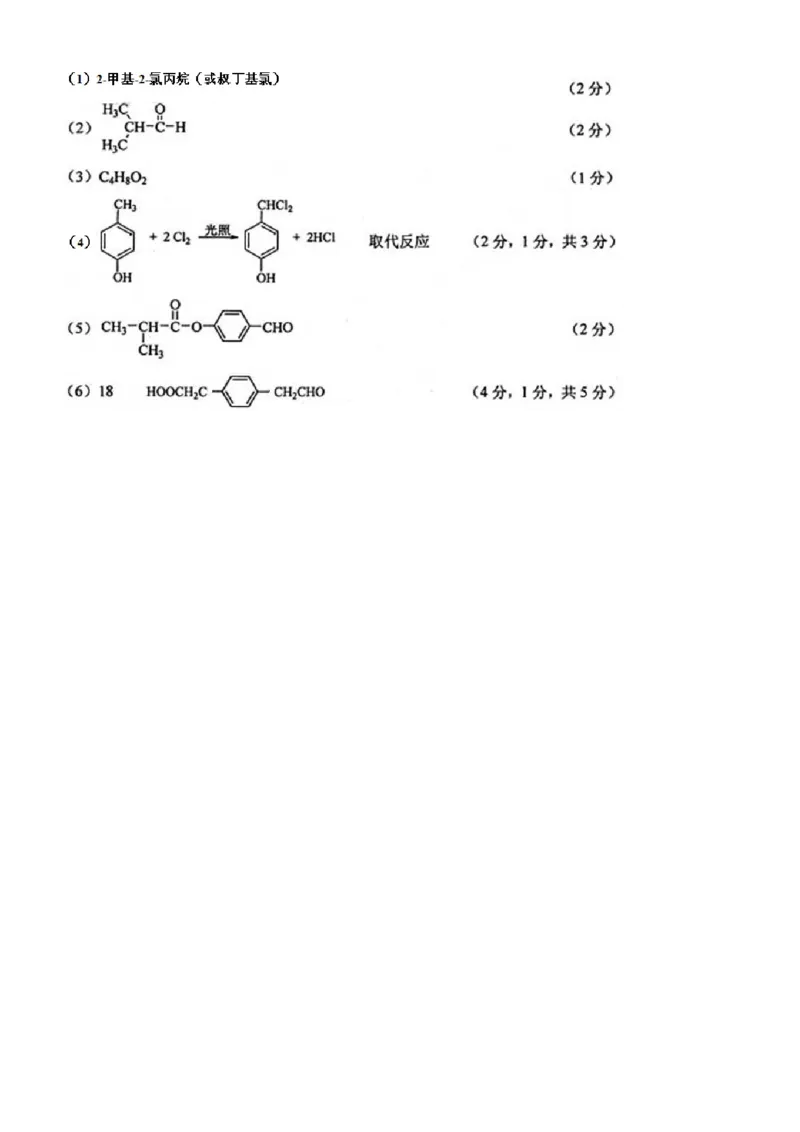
(1)A的化学名称为 。
(2)D的结构简式为 。(3)E的分子式为 。
(4)F生成G的化学方程式为 ,该反应类型为 。
(5)I的结构简式为 。
(6)I的同系物J比I相对分子质量小14,J的同分异构体中能同时满足如下条件:
①苯环上只有两个取代基,②既能发生银镜反应,又能与饱和NaHCO 溶液反应放出CO,共有 种(不
3 2
考虑立体异构)。J的一个同分异构体发生银镜反应并酸化后核磁共振氢谱为三组峰,且峰面积比为 2∶2∶1,
写出J的这种同分异构体的结构简式 。
2013年高考全国理综化学II卷
参考答案
第I卷
一、选择题
7.C 8.D 9.B 10.D 11.B 12.A 13.C
第II卷
26. (15分)
(1)不能,易迸溅 (2分)
(2)防止暴沸 冷却后补加 (每空1分,共2分)
(3)分液漏斗 直形冷凝管 (每空1分,共2分)
(4) C (2分)
(5)下 (2分)
(6)既可保证正丁醛及时蒸出,又可尽量避免其被进一步氧化 (2分)
(7)51 (2分)
27. (14分)
(1)Fe2+和Mn2+ (2分)
MnO- + 3Fe2+ + 7HO = 3Fe(OH)↓+ MnO↓ + 5H+ (2分)
4 2 3 2
2 MnO- + 3Mn2+ + 2HO = 5MnO↓ + 4H+ (2分)
4 2 2
铁离子和锰离子不能生成沉淀,从而无法除去铁和锰杂质 (2分)
(2)置换反应 镍 (每空1分,共2分)
(3)取少量水洗夜于试管中,滴入1~2滴稀硝酸,再滴入硝酸钡溶液,若无白色沉淀生成,则说明沉淀已经
洗涤干净 (2分)
(4)1 (2分)
28. (14分)
(1)升高温度、降低压强 (2分)(2)
(3)
②0.051 (2分)
达到平衡前每间隔4h,c(A)减少约一半 (2分)
0.013 (1分)
36. 〔化学——选修2:化学与技术〕(15分)
37. 〔化学——选修3:物质结构与性质〕(15分)
38. [化学——选修5:有机化学基础〕(15分)