文档内容
2014 年广东省高考化学试卷
一、选择题:每小题4份,在给出的四个选项中,只有一个符合题目要求选对得四分,选错或不答的得0分
7.(4分)(2014•广东)生活处处有化学.下列说法正确的是( )
A. 制饭勺、饭盒、高压锅等的不锈钢是合金
B. 做衣服的棉和麻均与淀粉互为同分异构体
C. 煎炸食物的花生油和牛油都是可皂化的饱和酯类
D. 磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸
8.(4分)(2014•广东)水溶液中能大量共存的一组离子是( )
A. Na+、Ca2+、Cl﹣、SO 2﹣ B. Fe2+、H+、SO 2﹣、ClO﹣
4 3
C. Mg2+、NH +、Cl﹣、SO 2﹣ D. K+、Fe3+、NO ﹣、SCN﹣
4 4 3
9.(4分)(2014•广东)下列叙述Ⅰ和Ⅱ均正确并有因果关系的是( )
选项 叙述Ⅰ 叙述Ⅱ
A KNO 的溶解度大 用重结晶法除去KNO 中混有的NaCl
3 3
B BaSO 难溶于酸 用盐酸和BaCl 溶液检验SO 2﹣
4 2 4
C NH 能使酚酞溶液变红 NH 可用于设计喷泉实验
3 3
D Ca(OH) 能制成澄清石灰水 可配制2.0mol•L﹣1的Ca(OH) 溶液
2 2
A A B B C C D D
. . . .
10.(4分)(2014•广东)设N 为阿伏加德罗常数的数值.下列说法正确的是( )
A
A. 1mol甲苯含有6N 个C﹣H键
A
B. 18g H O含有10N 个质子
2 A
C. 标准状况下,22.4L氨水含有N 个NH 分子
A 3
D. 56g铁片投入足量浓H SO 中生成N 个SO 分子
2 4 A 2
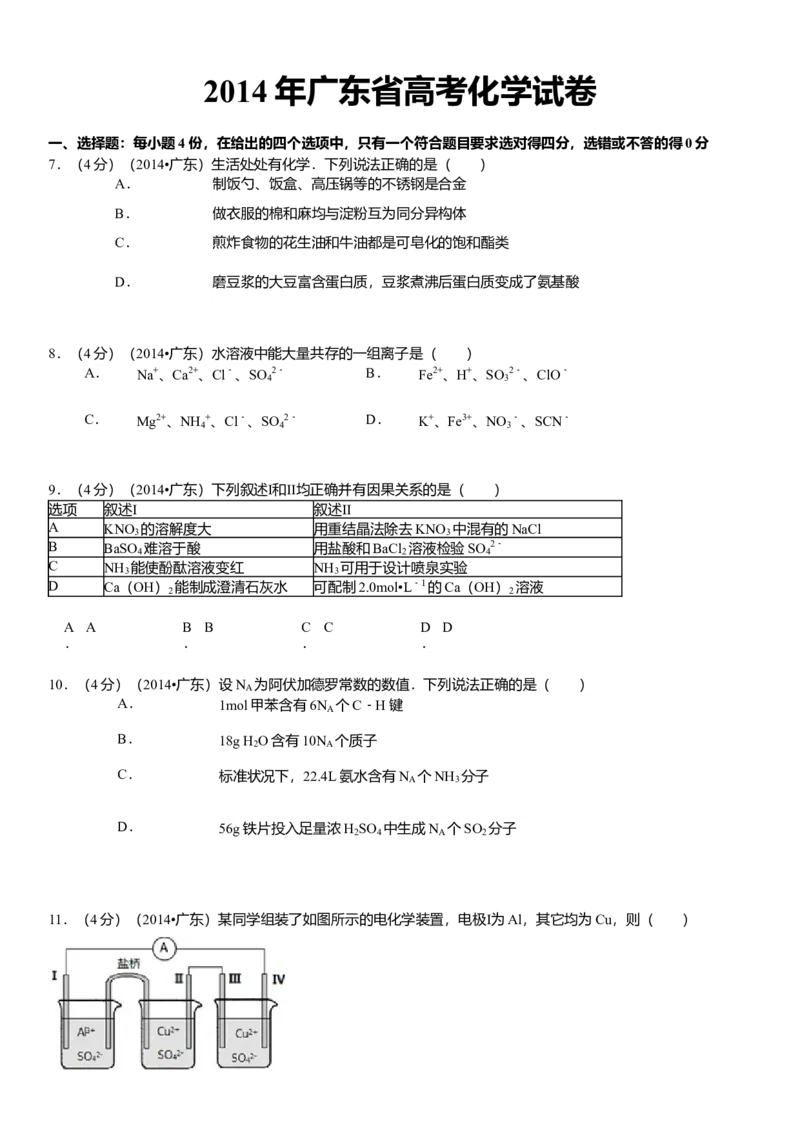
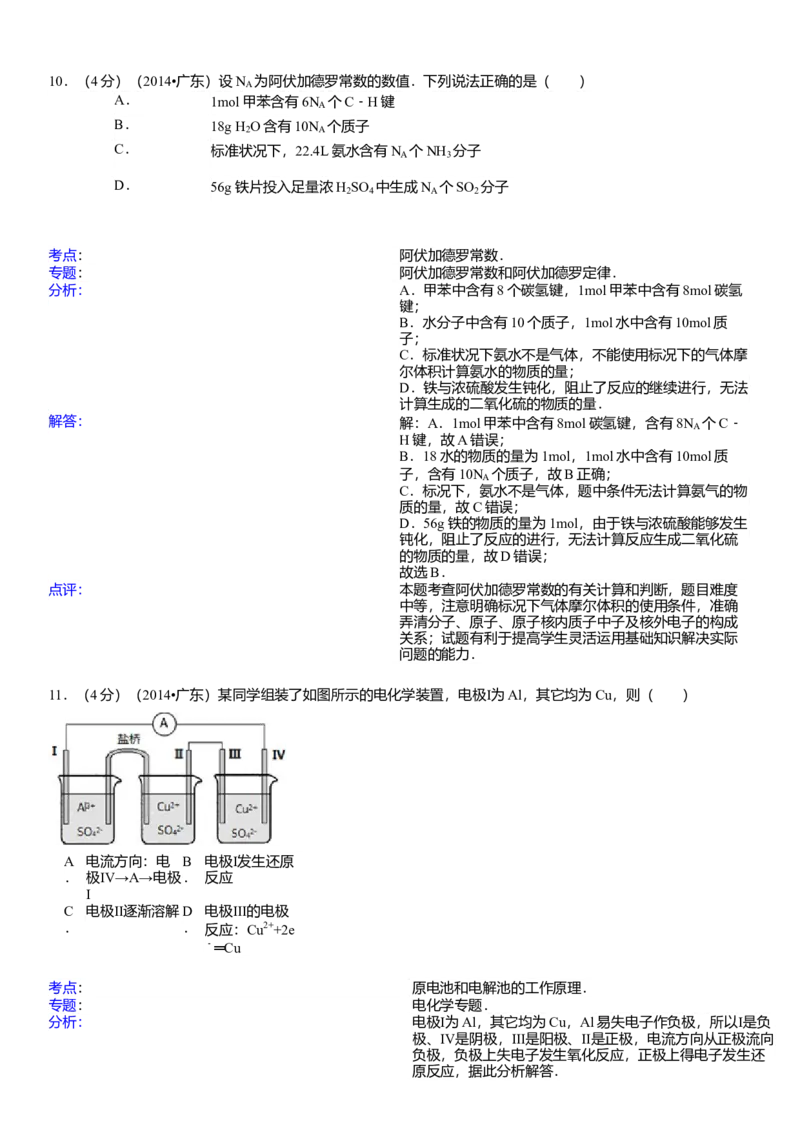
11.(4分)(2014•广东)某同学组装了如图所示的电化学装置,电极Ⅰ为Al,其它均为Cu,则( )A. 电流方向:电极Ⅳ→A→电极Ⅰ B. 电极Ⅰ发生还原反应
C. 电极Ⅱ逐渐溶解 D. 电极Ⅲ的电极反应:Cu2++2e﹣═Cu
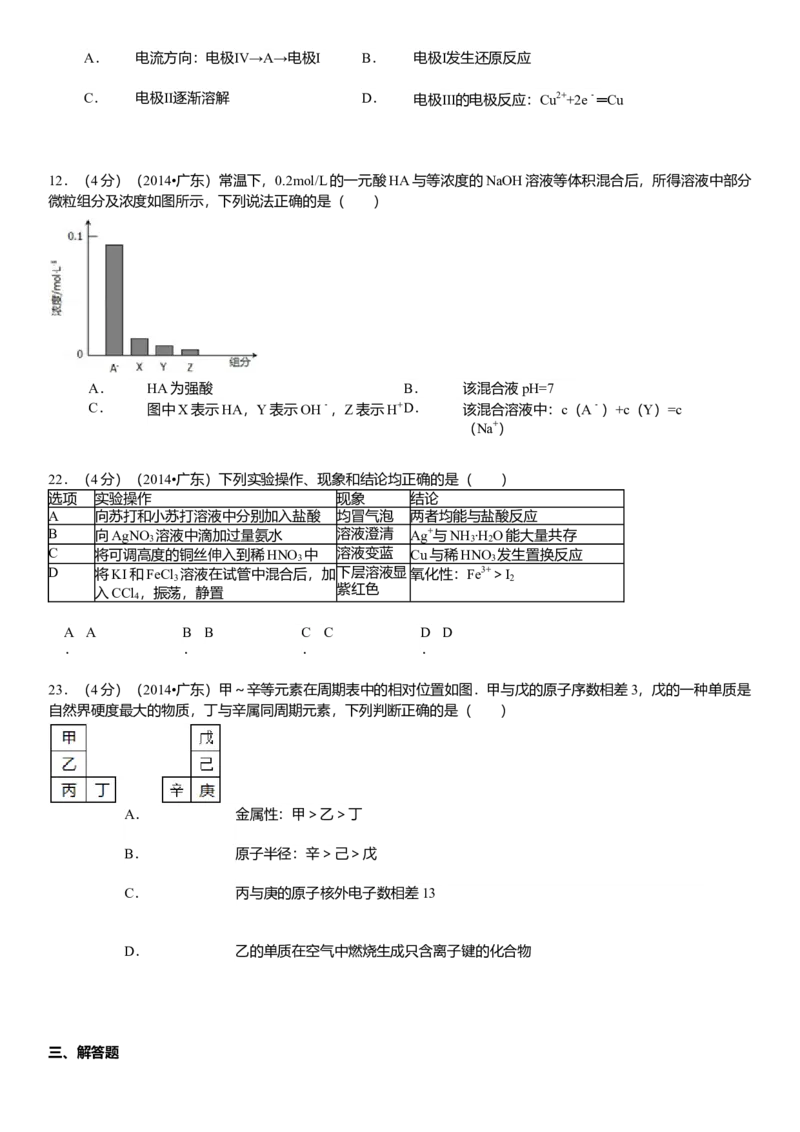
12.(4分)(2014•广东)常温下,0.2mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分
微粒组分及浓度如图所示,下列说法正确的是( )
A. HA为强酸 B. 该混合液pH=7
C. 图中X表示HA,Y表示OH﹣,Z表示H+D. 该混合溶液中:c(A﹣)+c(Y)=c
(Na+)
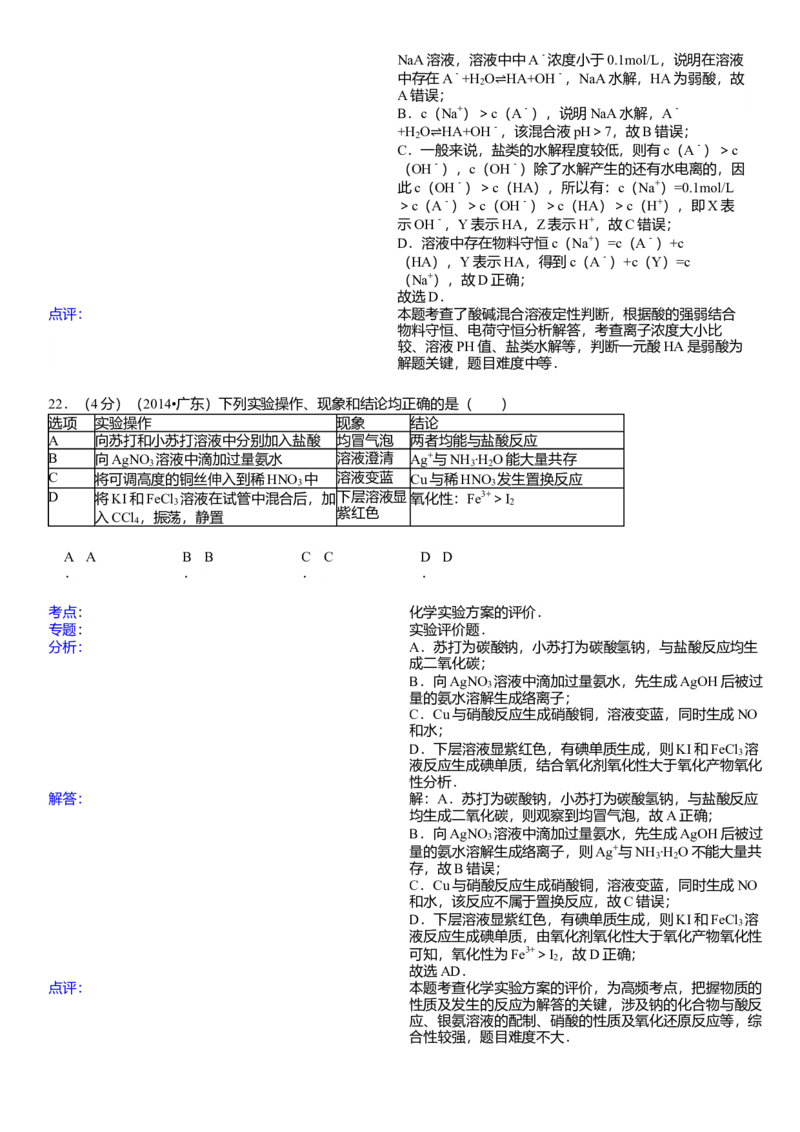
22.(4分)(2014•广东)下列实验操作、现象和结论均正确的是( )
选项 实验操作 现象 结论
A 向苏打和小苏打溶液中分别加入盐酸 均冒气泡 两者均能与盐酸反应
B 向AgNO 溶液中滴加过量氨水 溶液澄清 Ag+与NH ∙H O能大量共存
3 3 2
C 将可调高度的铜丝伸入到稀HNO 中 溶液变蓝 Cu与稀HNO 发生置换反应
3 3
D 将KI和FeCl 溶液在试管中混合后,加下层溶液显氧化性:Fe3+>I
3 2
入CCl ,振荡,静置 紫红色
4
A A B B C C D D
. . . .
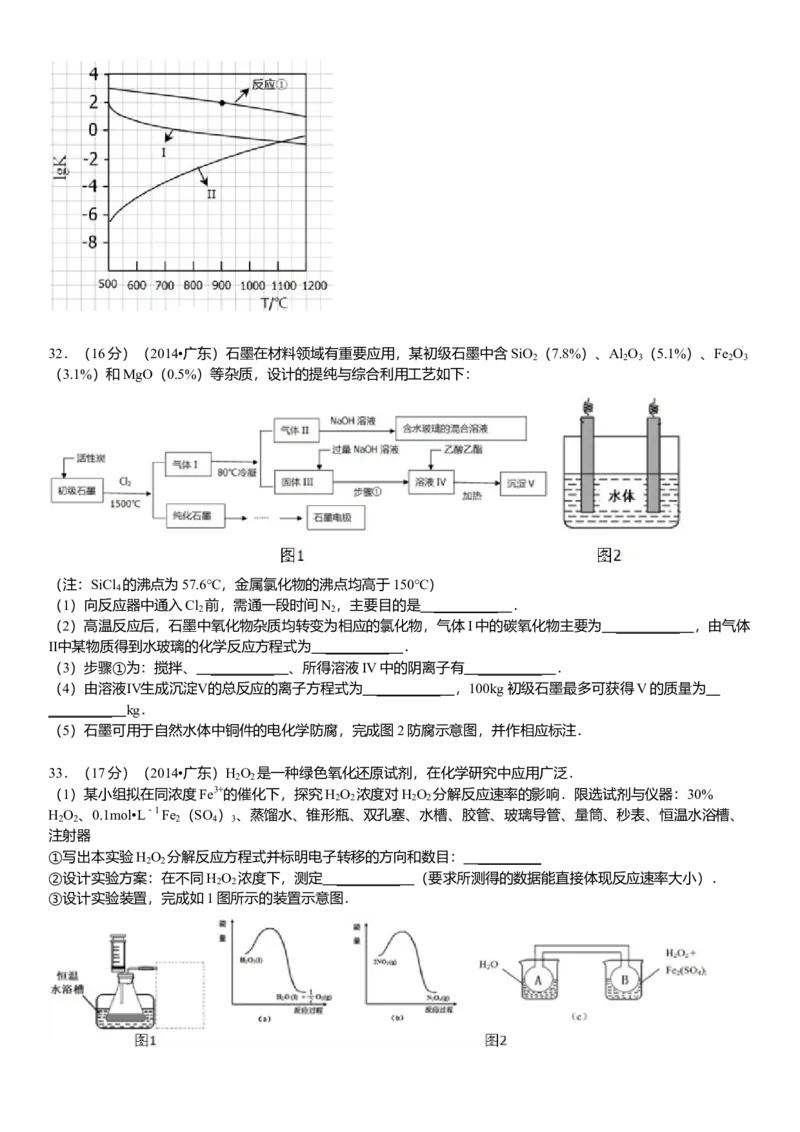
23.(4分)(2014•广东)甲~辛等元素在周期表中的相对位置如图.甲与戊的原子序数相差3,戊的一种单质是
自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是( )
A. 金属性:甲>乙>丁
B. 原子半径:辛>己>戊
C. 丙与庚的原子核外电子数相差13
D. 乙的单质在空气中燃烧生成只含离子键的化合物
三、解答题30.(15分)(2014•广东)不饱和酯类化合物在药物、涂料等应用广泛.
(1)下列化合物I的说法,正确的是 _________ .
A.遇FeCl 溶液可能显紫色
3
B.可发生酯化反应和银镜反应
C.能与溴发生取代和加成反应
D.1mol化合物I最多能与2mol NaOH反应
(2)反应①是一种由烯烃直接制备不饱和酯的新方法:
化合物Ⅱ的分子式为 _________ ,1mol化合物Ⅱ能与 _________ mol H 恰好完全反应生成饱和烃类化合物.
2
(3)化合物Ⅱ可由芳香族化合物Ⅲ或Ⅳ分别通过消去反应获得,但只有Ⅲ能与Na反应产生H ,Ⅲ的结构简式为
2
_________ (写1种);由Ⅳ生成Ⅱ的反应条件为 _________ .
(4)聚合物 可用于制备涂料,其单体结构简式为 _________ .利用类似反应①的方法,
仅以乙烯为有机物原料合成该单体,涉及的反应方程式为 _________ .
31.(16分)(2014•广东)用CaSO 代替O 与燃料CO反应,既可提高燃烧效率,又能得到高纯CO ,是一种高
4 2 2
效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应.
① CaSO 4 (s)+CO(g)⇋ CaS(s)+CO 2 (g)△H 1 =﹣47.3kJ•mol﹣1
②CaSO
4
(s)+CO(g)⇋CaO(s)+CO
2
(g)+SO
2
(g)△H
2
=+210.5kJ•mol﹣1
③CO(g)⇋ C(s)+ CO
2
(g)△H
3
=﹣86.2kJ•mol﹣1
(1)反应2CaSO
4
(s)+7CO(g)⇋CaS(s)+CaO(s)+6CO
2
(g)+C(s)+SO
2
(g)的△H= _________
(用△H 、△H 和△H 表示)
1 2 3
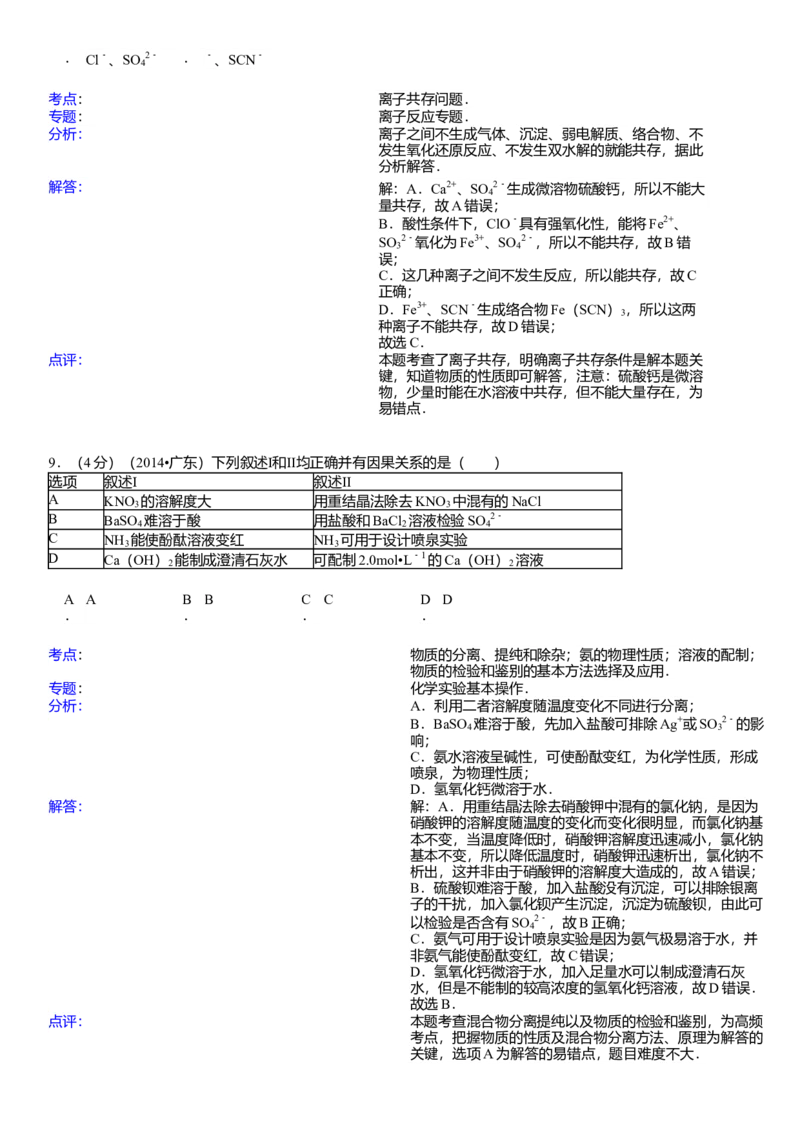
(2)反应①﹣③的平衡常数的对数lgK随反应温度T的变化曲线见图,结合各反应的△H,归纳lgK﹣T曲线变化
规律:
(a) _________ ;(b) _________ .
(3)向盛有CaSO 的真空恒容密闭容器中充入CO,反应①于900℃达到平衡,c (CO)=8.0×10﹣5 mol•L﹣1,
4 平衡
计算CO的转化率(忽略副反应,结果保留两位有效数字).
(4)为减少副产物,获得更纯净的CO ,可在初始燃料中适量加入 _________ .
2
(5)以反应①中生成的CaS为原料,在一定条件下经原子利用率100%的高温反应,可再生CaSO ,该反应的化
4
学方程式为 _________ ;在一定条件下,CO 可与对二甲苯反应,在其苯环上引入一个羧基,产物的结构简式
2
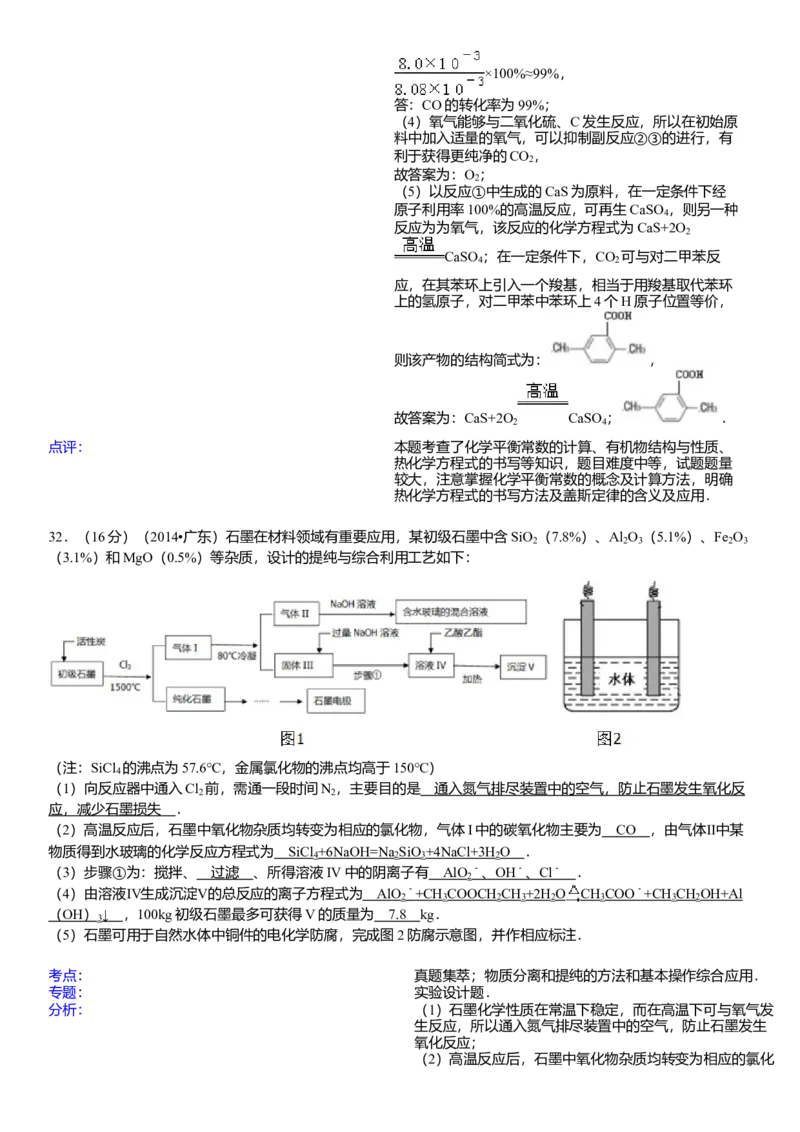
为 _________ .32.(16分)(2014•广东)石墨在材料领域有重要应用,某初级石墨中含SiO (7.8%)、Al O (5.1%)、Fe O
2 2 3 2 3
(3.1%)和MgO(0.5%)等杂质,设计的提纯与综合利用工艺如下:
(注:SiCl 的沸点为57.6℃,金属氯化物的沸点均高于150℃)
4
(1)向反应器中通入Cl 前,需通一段时间N ,主要目的是 _________ .
2 2
(2)高温反应后,石墨中氧化物杂质均转变为相应的氯化物,气体I中的碳氧化物主要为 _________ ,由气体
Ⅱ中某物质得到水玻璃的化学反应方程式为 _________ .
(3)步骤①为:搅拌、 _________ 、所得溶液IV中的阴离子有 _________ .
(4)由溶液Ⅳ生成沉淀Ⅴ的总反应的离子方程式为 _________ ,100kg初级石墨最多可获得V的质量为
_________ kg.
(5)石墨可用于自然水体中铜件的电化学防腐,完成图2防腐示意图,并作相应标注.
33.(17分)(2014•广东)H O 是一种绿色氧化还原试剂,在化学研究中应用广泛.
2 2
(1)某小组拟在同浓度Fe3+的催化下,探究H O 浓度对H O 分解反应速率的影响.限选试剂与仪器:30%
2 2 2 2
H O 、0.1mol•L﹣1 Fe (SO ) 、蒸馏水、锥形瓶、双孔塞、水槽、胶管、玻璃导管、量筒、秒表、恒温水浴槽、
2 2 2 4 3
注射器
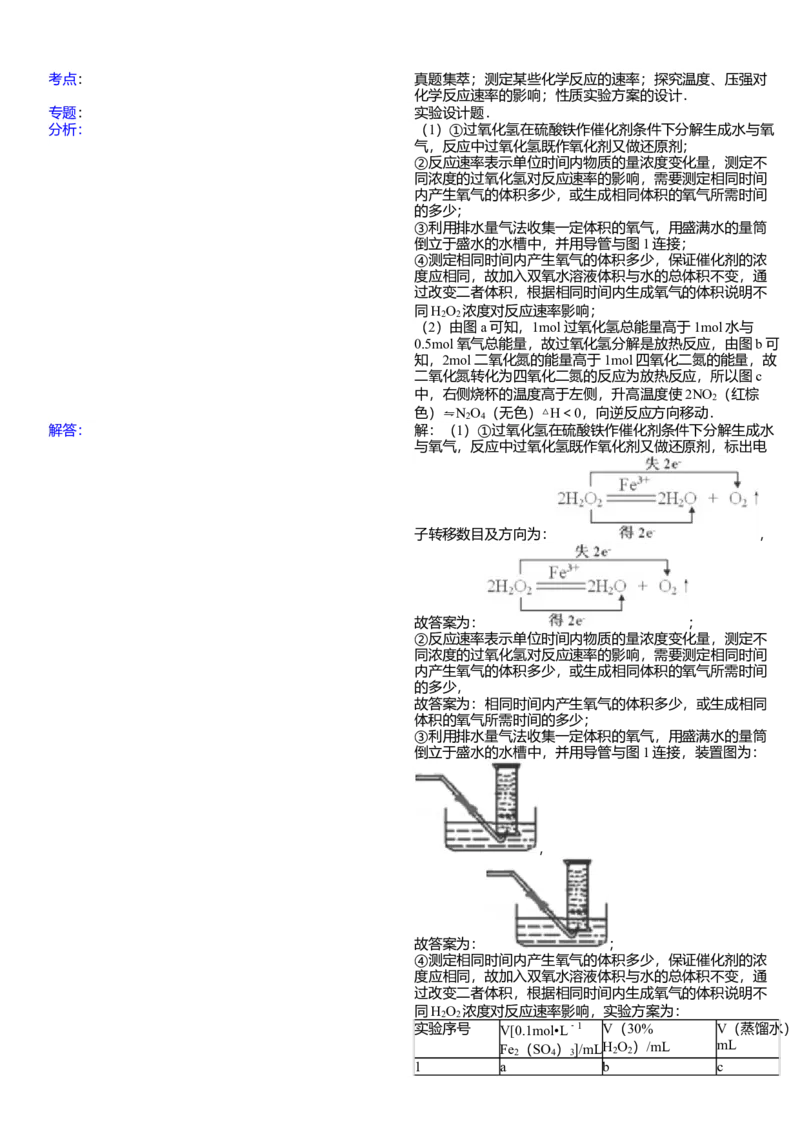
①写出本实验H O 分解反应方程式并标明电子转移的方向和数目: _________
2 2
②设计实验方案:在不同H O 浓度下,测定 _________ (要求所测得的数据能直接体现反应速率大小).
2 2
③设计实验装置,完成如1图所示的装置示意图.④参照下表格式,拟定实验表格,完整体现实验方案(列出所选试剂体积、需记录的待测物理量和所拟定的数据;
数据用字母表示).
实验序号 V[0.1mol•L﹣1 Fe (SO ) /mL …
2 4 3
物理量
]
1 a …
2 a …
(2)利用图2(a)和2(b)中的信息,按图2(c)装置(连能的A、B瓶中已充有NO 气体)进行实验.可观
2
察到B瓶中气体颜色比A瓶中的 _________ (填“深”或“浅”),其原因是 _________ .2014 年广东省高考化学试卷
参考答案与试题解析
一、选择题:每小题4份,在给出的四个选项中,只有一个符合题目要求选对得四分,选错或不答的得0分
7.(4分)(2014•广东)生活处处有化学.下列说法正确的是( )
A. 制饭勺、饭盒、高压锅等的不锈钢是合金
B. 做衣服的棉和麻均与淀粉互为同分异构体
C. 煎炸食物的花生油和牛油都是可皂化的饱和酯类
D. 磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸
考点: 金属与合金在性能上的主要差异;同分异构现象和同分
异构体;油脂的性质、组成与结构;氨基酸、蛋白质的
结构和性质特点.
菁优网版权所有
专题: 化学应用.
分析: A.合金就是某种金属与其他一种或几种金属或非金属
融合在一起形成的混合物;
B.棉和麻主要成分是纤维素;
C.花生油是植物油是不饱和酯类;
D.蛋白质要在催化剂作用下才能水解为氨基酸.
解答: 解:A.“不锈钢是合金”,不锈钢是铁、钴、镍的合
金,故A正确;
B.棉和麻主要成分是纤维素,与淀粉不属于同分异构
体,n值不同,故B错误;
C.花生油是不饱和酯类,牛油是饱和酯类,故C错
误;
D.豆浆煮沸是蛋白质发生了变性,故D错误.
故选A.
点评: 本题考查合金、同分异构体、油脂和蛋白质的性质,难
度较小,旨在考查学生对基础知识的识记,注意基础知
识的积累掌握.
8.(4分)(2014•广东)水溶液中能大量共存的一组离子是( )
A Na+、Ca2+、Cl B Fe2+、H+、SO 2
3
. ﹣、SO 2﹣ . ﹣、ClO﹣
4
C Mg2+、NH +、 D K+、Fe3+、NO
4 3. Cl﹣、SO 2﹣ . ﹣、SCN﹣
4
考点: 离子共存问题.
菁优网版权所有
专题: 离子反应专题.
分析: 离子之间不生成气体、沉淀、弱电解质、络合物、不
发生氧化还原反应、不发生双水解的就能共存,据此
分析解答.
解答: 解:A.Ca2+、SO 2﹣生成微溶物硫酸钙,所以不能大
4
量共存,故A错误;
B.酸性条件下,ClO﹣具有强氧化性,能将Fe2+、
SO 2﹣氧化为Fe3+、SO 2﹣,所以不能共存,故B错
3 4
误;
C.这几种离子之间不发生反应,所以能共存,故C
正确;
D.Fe3+、SCN﹣生成络合物Fe(SCN) ,所以这两
3
种离子不能共存,故D错误;
故选C.
点评: 本题考查了离子共存,明确离子共存条件是解本题关
键,知道物质的性质即可解答,注意:硫酸钙是微溶
物,少量时能在水溶液中共存,但不能大量存在,为
易错点.
9.(4分)(2014•广东)下列叙述Ⅰ和Ⅱ均正确并有因果关系的是( )
选项 叙述Ⅰ 叙述Ⅱ
A KNO 的溶解度大 用重结晶法除去KNO 中混有的NaCl
3 3
B BaSO 难溶于酸 用盐酸和BaCl 溶液检验SO 2﹣
4 2 4
C NH 能使酚酞溶液变红 NH 可用于设计喷泉实验
3 3
D Ca(OH) 能制成澄清石灰水 可配制2.0mol•L﹣1的Ca(OH) 溶液
2 2
A A B B C C D D
. . . .
考点: 物质的分离、提纯和除杂;氨的物理性质;溶液的配制;
物质的检验和鉴别的基本方法选择及应用.
菁优网版权所有
专题: 化学实验基本操作.
分析: A.利用二者溶解度随温度变化不同进行分离;
B.BaSO 难溶于酸,先加入盐酸可排除Ag+或SO 2﹣的影
4 3
响;
C.氨水溶液呈碱性,可使酚酞变红,为化学性质,形成
喷泉,为物理性质;
D.氢氧化钙微溶于水.
解答: 解:A.用重结晶法除去硝酸钾中混有的氯化钠,是因为
硝酸钾的溶解度随温度的变化而变化很明显,而氯化钠基
本不变,当温度降低时,硝酸钾溶解度迅速减小,氯化钠
基本不变,所以降低温度时,硝酸钾迅速析出,氯化钠不
析出,这并非由于硝酸钾的溶解度大造成的,故A错误;
B.硫酸钡难溶于酸,加入盐酸没有沉淀,可以排除银离
子的干扰,加入氯化钡产生沉淀,沉淀为硫酸钡,由此可
以检验是否含有SO 2﹣,故B正确;
4
C.氨气可用于设计喷泉实验是因为氨气极易溶于水,并
非氨气能使酚酞变红,故C错误;
D.氢氧化钙微溶于水,加入足量水可以制成澄清石灰
水,但是不能制的较高浓度的氢氧化钙溶液,故D错误.
故选B.
点评: 本题考查混合物分离提纯以及物质的检验和鉴别,为高频
考点,把握物质的性质及混合物分离方法、原理为解答的
关键,选项A为解答的易错点,题目难度不大.10.(4分)(2014•广东)设N 为阿伏加德罗常数的数值.下列说法正确的是( )
A
A. 1mol甲苯含有6N 个C﹣H键
A
B. 18g H O含有10N 个质子
2 A
C. 标准状况下,22.4L氨水含有N 个NH 分子
A 3
D. 56g铁片投入足量浓H SO 中生成N 个SO 分子
2 4 A 2
考点: 阿伏加德罗常数.
菁优网版权所有
专题: 阿伏加德罗常数和阿伏加德罗定律.
分析: A.甲苯中含有8个碳氢键,1mol甲苯中含有8mol碳氢
键;
B.水分子中含有10个质子,1mol水中含有10mol质
子;
C.标准状况下氨水不是气体,不能使用标况下的气体摩
尔体积计算氨水的物质的量;
D.铁与浓硫酸发生钝化,阻止了反应的继续进行,无法
计算生成的二氧化硫的物质的量.
解答: 解:A.1mol甲苯中含有8mol碳氢键,含有8N 个C﹣
A
H键,故A错误;
B.18水的物质的量为1mol,1mol水中含有10mol质
子,含有10N 个质子,故B正确;
A
C.标况下,氨水不是气体,题中条件无法计算氨气的物
质的量,故C错误;
D.56g铁的物质的量为1mol,由于铁与浓硫酸能够发生
钝化,阻止了反应的进行,无法计算反应生成二氧化硫
的物质的量,故D错误;
故选B.
点评: 本题考查阿伏加德罗常数的有关计算和判断,题目难度
中等,注意明确标况下气体摩尔体积的使用条件,准确
弄清分子、原子、原子核内质子中子及核外电子的构成
关系;试题有利于提高学生灵活运用基础知识解决实际
问题的能力.
11.(4分)(2014•广东)某同学组装了如图所示的电化学装置,电极Ⅰ为Al,其它均为Cu,则( )
A 电流方向:电 B 电极Ⅰ发生还原
. 极Ⅳ→A→电极. 反应
Ⅰ
C 电极Ⅱ逐渐溶解D 电极Ⅲ的电极
. . 反应:Cu2++2e
﹣═Cu
考点: 原电池和电解池的工作原理.
菁优网版权所有
专题: 电化学专题.
分析: 电极Ⅰ为Al,其它均为Cu,Al易失电子作负极,所以Ⅰ是负
极、Ⅳ是阴极,Ⅲ是阳极、Ⅱ是正极,电流方向从正极流向
负极,负极上失电子发生氧化反应,正极上得电子发生还
原反应,据此分析解答.解答: 解:电极Ⅰ为Al,其它均为Cu,Al易失电子作负极,所以Ⅰ
是负极、Ⅳ是阴极,Ⅲ是阳极、Ⅱ是正极,
A.电流从正极沿导线流向负极,即电极Ⅳ→A→电极Ⅰ,
故A正确;
B.电极Ⅰ上电极反应式为Al﹣3e﹣=Al3+,发生氧化反应,
故B错误;
C.电极Ⅱ是正极,正极上发生反应为Cu 2++2e﹣=Cu,所以
电极Ⅱ质量逐渐增大,故C错误;
D.电极Ⅲ为阳极,电极反应式为Cu﹣2e﹣═Cu 2+,故D错
误;
故选A.
点评: 本题考查了原电池原理,正确判断正负极是解本题关键,
再结合各个电极上发生的反应来分析解答,题目难度中
等.
12.(4分)(2014•广东)常温下,0.2mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分
微粒组分及浓度如图所示,下列说法正确的是( )
A. HA为强酸 B. 该混合液pH=7
C. 图中X表示HA,Y表示OH﹣,Z表示H+ D. 该混合溶液中:c(A﹣)+c(Y)=c
(Na+)
考点: 酸碱混合时的定性判断及有关ph的计算.
菁优网版权所有
专题: 电离平衡与溶液的pH专题.
分析: 一元酸HA和NaOH溶液等体积、等浓度0.2mol/L混
合,HA+NaOH=NaA+H O,所得溶液中A﹣浓度小于
2
0.1mol/L,说明在溶液中存在A﹣+H O HA+OH﹣,NaA
2
水解,HA为弱酸,NaA溶液呈碱性,则c(OH﹣)>c
(H+),一般来说,盐类的水解程度较 ⇌ 低,则有c(A
﹣)>c(OH﹣),所以有:c(Na+)=0.1mol/L>c(A
﹣)>c(OH﹣)>c(HA)>c(H+),即X表示OH
﹣,Y表示HA,Z表示H+,溶液中存在物料守恒为:c
(Na+)=c(A﹣)+c(HA).
A.HA为弱酸;B.该混合液pH>7;C.X表示OH
﹣,Y表示HA,Z表示H+;D.Y表示HA,溶液中存在
物料守恒得到c(A﹣)+c(Y)=c(Na+).
解答: 解:一元酸HA和NaOH溶液等体积、等浓度0.2mol/L
混合,HA+NaOH=NaA+H O,所得溶液中A﹣浓度小于
2
0.1mol/L,说明在溶液中存在A﹣+H O HA+OH﹣,NaA
2
水解,HA为弱酸,NaA溶液呈碱性,则c(OH﹣)>c
(H+),一般来说,盐类的水解程度较 ⇌ 低,则有c(A
﹣)>c(OH﹣),所以有:c(Na+)=0.1mol/L>c(A
﹣)>c(OH﹣)>c(HA)>c(H+),即X表示OH
﹣,Y表示HA,Z表示H+,溶液中存在物料守恒得到:
c(Na+)=c(A﹣)+c(HA).
A.一元酸HA和NaOH溶液等体积、等浓度0.2mol/L混
合,二者恰好反应:HA+NaOH=NaA+H O,所得溶液为
2NaA溶液,溶液中中A﹣浓度小于0.1mol/L,说明在溶液
中存在A﹣+H O HA+OH﹣,NaA水解,HA为弱酸,故
2
A错误;
B.c(Na+)>c⇌(A﹣),说明NaA水解,A﹣
+H O HA+OH﹣,该混合液pH>7,故B错误;
2
C.一般来说,盐类的水解程度较低,则有c(A﹣)>c
(OH
⇌﹣),c(OH﹣)除了水解产生的还有水电离的,因
此c(OH﹣)>c(HA),所以有:c(Na+)=0.1mol/L
>c(A﹣)>c(OH﹣)>c(HA)>c(H+),即X表
示OH﹣,Y表示HA,Z表示H+,故C错误;
D.溶液中存在物料守恒c(Na+)=c(A﹣)+c
(HA),Y表示HA,得到c(A﹣)+c(Y)=c
(Na+),故D正确;
故选D.
点评: 本题考查了酸碱混合溶液定性判断,根据酸的强弱结合
物料守恒、电荷守恒分析解答,考查离子浓度大小比
较、溶液PH值、盐类水解等,判断一元酸HA是弱酸为
解题关键,题目难度中等.
22.(4分)(2014•广东)下列实验操作、现象和结论均正确的是( )
选项 实验操作 现象 结论
A 向苏打和小苏打溶液中分别加入盐酸 均冒气泡 两者均能与盐酸反应
B 向AgNO 溶液中滴加过量氨水 溶液澄清 Ag+与NH ∙H O能大量共存
3 3 2
C 将可调高度的铜丝伸入到稀HNO 中 溶液变蓝 Cu与稀HNO 发生置换反应
3 3
D 将KI和FeCl 溶液在试管中混合后,加下层溶液显氧化性:Fe3+>I
3 2
入CCl ,振荡,静置 紫红色
4
A A B B C C D D
. . . .
考点: 化学实验方案的评价.
菁优网版权所有
专题: 实验评价题.
分析: A.苏打为碳酸钠,小苏打为碳酸氢钠,与盐酸反应均生
成二氧化碳;
B.向AgNO 溶液中滴加过量氨水,先生成AgOH后被过
3
量的氨水溶解生成络离子;
C.Cu与硝酸反应生成硝酸铜,溶液变蓝,同时生成NO
和水;
D.下层溶液显紫红色,有碘单质生成,则KI和FeCl 溶
3
液反应生成碘单质,结合氧化剂氧化性大于氧化产物氧化
性分析.
解答: 解:A.苏打为碳酸钠,小苏打为碳酸氢钠,与盐酸反应
均生成二氧化碳,则观察到均冒气泡,故A正确;
B.向AgNO 溶液中滴加过量氨水,先生成AgOH后被过
3
量的氨水溶解生成络离子,则Ag+与NH ∙H O不能大量共
3 2
存,故B错误;
C.Cu与硝酸反应生成硝酸铜,溶液变蓝,同时生成NO
和水,该反应不属于置换反应,故C错误;
D.下层溶液显紫红色,有碘单质生成,则KI和FeCl 溶
3
液反应生成碘单质,由氧化剂氧化性大于氧化产物氧化性
可知,氧化性为Fe3+>I ,故D正确;
2
故选AD.
点评: 本题考查化学实验方案的评价,为高频考点,把握物质的
性质及发生的反应为解答的关键,涉及钠的化合物与酸反
应、银氨溶液的配制、硝酸的性质及氧化还原反应等,综
合性较强,题目难度不大.23.(4分)(2014•广东)甲~辛等元素在周期表中的相对位置如图.甲与戊的原子序数相差3,戊的一种单质是
自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是( )
A. 金属性:甲>乙>丁
B. 原子半径:辛>己>戊
C. 丙与庚的原子核外电子数相差13
D. 乙的单质在空气中燃烧生成只含离子键的化合物
考点: 真题集萃;元素周期律和元素周期表的综合应用.
菁优网版权所有
专题: 元素周期律与元素周期表专题.
分析: 戊的一种单质(金刚石)是自然界硬度最大的物质,则戊
为C,甲与戊的原子序数相差3,则甲的原子序数为6﹣
3=3,即甲为Li,由元素在周期表中的相对位置图可知,
乙为Na,丙为K,丁为Ca;丁与辛属同周期元素,由第
ⅣA族元素可知,己为Si,庚为Ge,辛为Ga,然后结合
元素周期律及元素化合物知识来解答.
解答: 解:戊的一种单质(金刚石)是自然界硬度最大的物质,
则戊为C,甲与戊的原子序数相差3,则甲的原子序数为6
﹣3=3,即甲为Li,由元素在周期表中的相对位置图可
知,乙为Na,丙为K,丁为Ca;丁与辛属同周期元素,
由第ⅣA族元素可知,己为Si,庚为Ge,辛为Ga,
A.同主族,从上到下金属性增强;同周期,从左向右金
属性减弱,则金属性甲<乙<丁,故A错误;
B.电子层越多,半价越大;同主族从上到下原子半径增
大,则原子半径为辛>己>戊,故B正确;
C.原子序数等于核外电子数,丙(原子序数为19)与庚
(原子序数为32)的原子核外电子数相差32﹣19=13,故
C正确;
D.乙的单质在空气中燃烧生成Na O ,为含离子键和非极
2 2
性共价键的化合物,故D错误;
故选BC.
点评: 本题为2014年广东高考化学试题,侧重位置、结构、性质
的关系及元素周期律的考查,把握金刚石的硬度及甲与戊
的原子序数关系推断各元素为解答的关键,选项A中Ca
的金属性比Na强为解答的易错点,题目难度中等.
三、解答题
30.(15分)(2014•广东)不饱和酯类化合物在药物、涂料等应用广泛.
(1)下列化合物I的说法,正确的是 AC .
A.遇FeCl 溶液可能显紫色
3
B.可发生酯化反应和银镜反应
C.能与溴发生取代和加成反应
D.1mol化合物I最多能与2mol NaOH反应
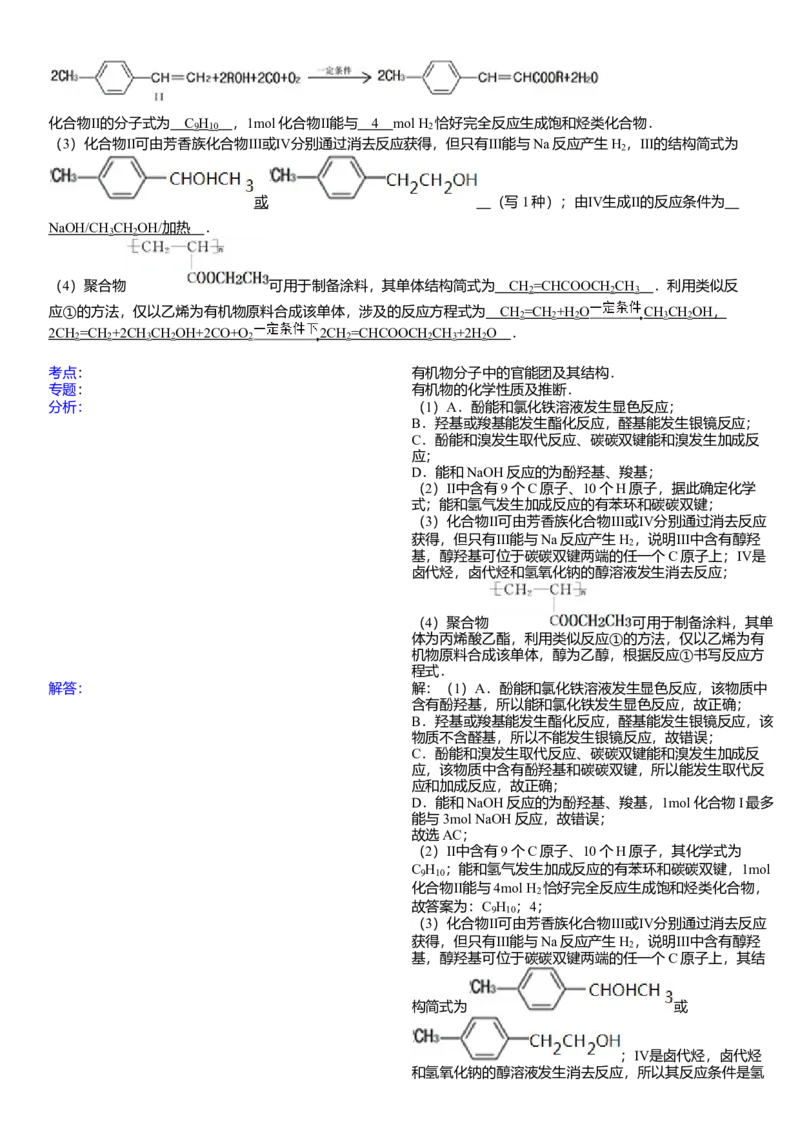
(2)反应①是一种由烯烃直接制备不饱和酯的新方法:化合物Ⅱ的分子式为 C H ,1mol化合物Ⅱ能与 4 mol H 恰好完全反应生成饱和烃类化合物.
9 10 2
(3)化合物Ⅱ可由芳香族化合物Ⅲ或Ⅳ分别通过消去反应获得,但只有Ⅲ能与Na反应产生H ,Ⅲ的结构简式为
2
或 (写1种);由Ⅳ生成Ⅱ的反应条件为
NaOH/CH CH OH/ 加热 .
3 2
(4)聚合物 可用于制备涂料,其单体结构简式为 CH =CHCOOCH CH .利用类似反
2 2 3
应①的方法,仅以乙烯为有机物原料合成该单体,涉及的反应方程式为 CH =CH +H O CH CH OH ,
2 2 2 3 2
2CH =CH +2CH CH OH+2CO+O 2CH =CHCOOCH CH +2H O .
2 2 3 2 2 2 2 3 2
考点: 有机物分子中的官能团及其结构.
菁优网版权所有
专题: 有机物的化学性质及推断.
分析: (1)A.酚能和氯化铁溶液发生显色反应;
B.羟基或羧基能发生酯化反应,醛基能发生银镜反应;
C.酚能和溴发生取代反应、碳碳双键能和溴发生加成反
应;
D.能和NaOH反应的为酚羟基、羧基;
(2)Ⅱ中含有9个C原子、10个H原子,据此确定化学
式;能和氢气发生加成反应的有苯环和碳碳双键;
(3)化合物Ⅱ可由芳香族化合物Ⅲ或Ⅳ分别通过消去反应
获得,但只有Ⅲ能与Na反应产生H ,说明Ⅲ中含有醇羟
2
基,醇羟基可位于碳碳双键两端的任一个C原子上;Ⅳ是
卤代烃,卤代烃和氢氧化钠的醇溶液发生消去反应;
(4)聚合物 可用于制备涂料,其单
体为丙烯酸乙酯,利用类似反应①的方法,仅以乙烯为有
机物原料合成该单体,醇为乙醇,根据反应①书写反应方
程式.
解答: 解:(1)A.酚能和氯化铁溶液发生显色反应,该物质中
含有酚羟基,所以能和氯化铁发生显色反应,故正确;
B.羟基或羧基能发生酯化反应,醛基能发生银镜反应,该
物质不含醛基,所以不能发生银镜反应,故错误;
C.酚能和溴发生取代反应、碳碳双键能和溴发生加成反
应,该物质中含有酚羟基和碳碳双键,所以能发生取代反
应和加成反应,故正确;
D.能和NaOH反应的为酚羟基、羧基,1mol化合物I最多
能与3mol NaOH反应,故错误;
故选AC;
(2)Ⅱ中含有9个C原子、10个H原子,其化学式为
C H ;能和氢气发生加成反应的有苯环和碳碳双键,1mol
9 10
化合物Ⅱ能与4mol H 恰好完全反应生成饱和烃类化合物,
2
故答案为:C H ;4;
9 10
(3)化合物Ⅱ可由芳香族化合物Ⅲ或Ⅳ分别通过消去反应
获得,但只有Ⅲ能与Na反应产生H ,说明Ⅲ中含有醇羟
2
基,醇羟基可位于碳碳双键两端的任一个C原子上,其结
构简式为 或
;Ⅳ是卤代烃,卤代烃
和氢氧化钠的醇溶液发生消去反应,所以其反应条件是氢氧化钠的醇溶液、加热;
故答案为: 或
;NaOH/CH CH OH/加
3 2
热;
(4)聚合物 可用于制备涂料,其单
体为丙烯酸乙酯,结构简式为CH =CHCOOCH CH ,利用
2 2 3
类似反应①的方法,仅以乙烯为有机物原料合成该单体,
醇为乙醇,根据反应①书写反应方程式,该反应方程式
为:CH =CH +H O CH CH OH,
2 2 2 3 2
2CH =CH +2CH CH OH+2CO+O 2CH =CHCOO
2 2 3 2 2 2
CH CH +2H O,
2 3 2
故答案为:CH =CHCOOCH CH ;CH =CH +H O
2 2 3 2 2 2
CH CH OH,2CH =CH +2CH CH OH+2CO+O
3 2 2 2 3 2 2
2CH =CHCOOCH CH +2H O
2 2 3 2
点评: 本题考查了有机物的官能团及其性质,知道常见有机物官
能团及其性质是解本题关键,知道有机反应中断键、成键
方式,并结合题给信息分析解答,题目难度中等.
31.(16分)(2014•广东)用CaSO 代替O 与燃料CO反应,既可提高燃烧效率,又能得到高纯CO ,是一种高
4 2 2
效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应.
① CaSO 4 (s)+CO(g)⇋ CaS(s)+CO 2 (g)△H 1 =﹣47.3kJ•mol﹣1
②CaSO
4
(s)+CO(g)⇋CaO(s)+CO
2
(g)+SO
2
(g)△H
2
=+210.5kJ•mol﹣1
③CO(g)⇋ C(s)+ CO
2
(g)△H
3
=﹣86.2kJ•mol﹣1
(1)反应2CaSO
4
(s)+7CO(g)⇋CaS(s)+CaO(s)+6CO
2
(g)+C(s)+SO
2
(g)的△H=
4△H
1
+△H
2
+2△H
3
(用△H
1
、△H
2
和△H
3
表示)
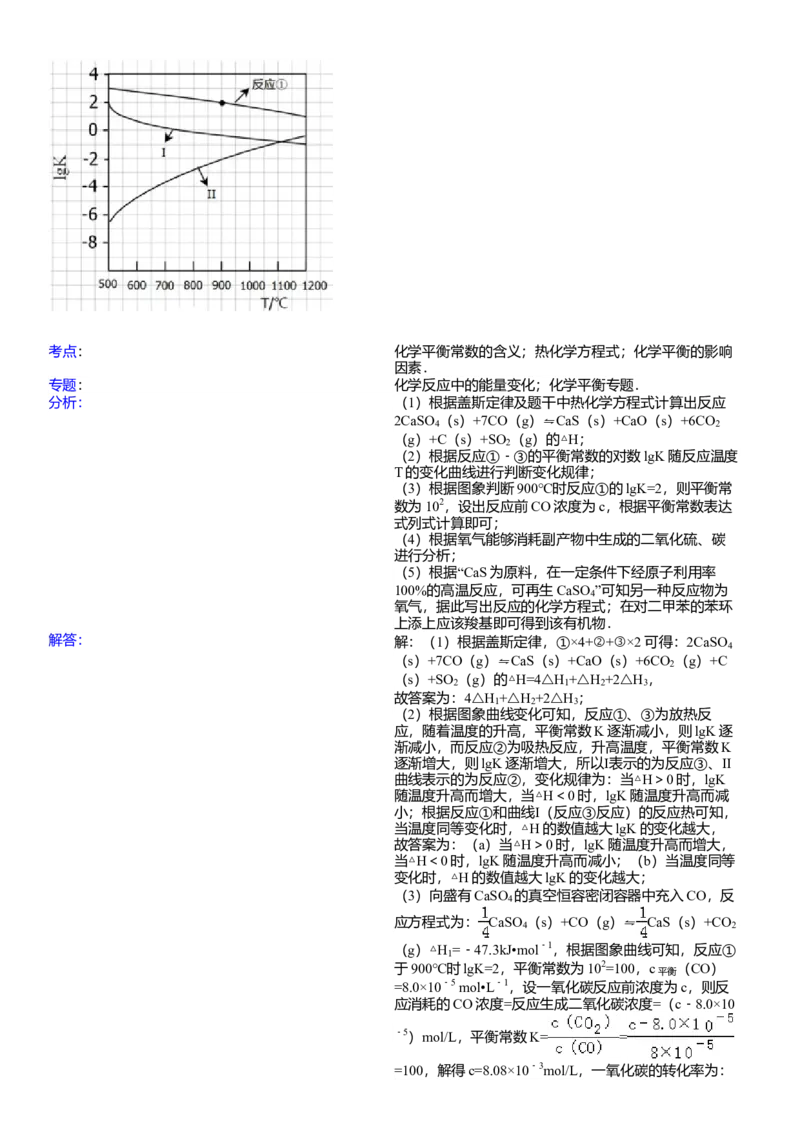
(2)反应①﹣③的平衡常数的对数lgK随反应温度T的变化曲线见图,结合各反应的△H,归纳lgK﹣T曲线变化
规律:
(a) 当△ H > 0 时, lgK 随温度升高而增大,当△ H < 0 时, lgK 随温度升高而减小 ;(b) 当温度同等变化时 ,
△ H 的数值越大 lgK 的变化越大 .
(3)向盛有CaSO 的真空恒容密闭容器中充入CO,反应①于900℃达到平衡,c (CO)=8.0×10﹣5 mol•L﹣1,
4 平衡
计算CO的转化率(忽略副反应,结果保留两位有效数字).
(4)为减少副产物,获得更纯净的CO ,可在初始燃料中适量加入 O .
2 2
(5)以反应①中生成的CaS为原料,在一定条件下经原子利用率100%的高温反应,可再生CaSO ,该反应的化
4
学方程式为 CaS+2O CaSO ;在一定条件下,CO 可与对二甲苯反应,在其苯环上引入一个羧基,产
2 4 2
物的结构简式为 .考点: 化学平衡常数的含义;热化学方程式;化学平衡的影响
因素.
菁优网版权所有
专题: 化学反应中的能量变化;化学平衡专题.
分析: (1)根据盖斯定律及题干中热化学方程式计算出反应
2CaSO
4
(s)+7CO(g)⇋CaS(s)+CaO(s)+6CO
2
(g)+C(s)+SO (g)的△H;
2
(2)根据反应①﹣③的平衡常数的对数lgK随反应温度
T的变化曲线进行判断变化规律;
(3)根据图象判断900℃时反应①的lgK=2,则平衡常
数为102,设出反应前CO浓度为c,根据平衡常数表达
式列式计算即可;
(4)根据氧气能够消耗副产物中生成的二氧化硫、碳
进行分析;
(5)根据“CaS为原料,在一定条件下经原子利用率
100%的高温反应,可再生CaSO ”可知另一种反应物为
4
氧气,据此写出反应的化学方程式;在对二甲苯的苯环
上添上应该羧基即可得到该有机物.
解答: 解:(1)根据盖斯定律,①×4+②+③×2可得:2CaSO
4
(s)+7CO(g)⇋CaS(s)+CaO(s)+6CO
2
(g)+C
(s)+SO
2
(g)的△H=4△H
1
+△H
2
+2△H
3
,
故答案为:4△H
1
+△H
2
+2△H
3
;
(2)根据图象曲线变化可知,反应①、③为放热反
应,随着温度的升高,平衡常数K逐渐减小,则lgK逐
渐减小,而反应②为吸热反应,升高温度,平衡常数K
逐渐增大,则lgK逐渐增大,所以Ⅰ表示的为反应③、Ⅱ
曲线表示的为反应②,变化规律为:当△H>0时,lgK
随温度升高而增大,当△H<0时,lgK随温度升高而减
小;根据反应①和曲线Ⅰ(反应③反应)的反应热可知,
当温度同等变化时,△H的数值越大lgK的变化越大,
故答案为:(a)当△H>0时,lgK随温度升高而增大,
当△H<0时,lgK随温度升高而减小;(b)当温度同等
变化时,△H的数值越大lgK的变化越大;
(3)向盛有CaSO 的真空恒容密闭容器中充入CO,反
4
应方程式为: CaSO
4
(s)+CO(g)⇋ CaS(s)+CO
2
(g)△H =﹣47.3kJ•mol﹣1,根据图象曲线可知,反应①
1
于900℃时lgK=2,平衡常数为102=100,c (CO)
平衡
=8.0×10﹣5 mol•L﹣1,设一氧化碳反应前浓度为c,则反
应消耗的CO浓度=反应生成二氧化碳浓度=(c﹣8.0×10
﹣5)mol/L,平衡常数K= =
=100,解得c=8.08×10﹣3mol/L,一氧化碳的转化率为:×100%≈99%,
答:CO的转化率为99%;
(4)氧气能够与二氧化硫、C发生反应,所以在初始原
料中加入适量的氧气,可以抑制副反应②③的进行,有
利于获得更纯净的CO ,
2
故答案为:O ;
2
(5)以反应①中生成的CaS为原料,在一定条件下经
原子利用率100%的高温反应,可再生CaSO ,则另一种
4
反应为为氧气,该反应的化学方程式为 CaS+2O
2
CaSO ;在一定条件下,CO 可与对二甲苯反
4 2
应,在其苯环上引入一个羧基,相当于用羧基取代苯环
上的氢原子,对二甲苯中苯环上4个H原子位置等价,
则该产物的结构简式为: ,
故答案为:CaS+2O CaSO ; .
2 4
点评: 本题考查了化学平衡常数的计算、有机物结构与性质、
热化学方程式的书写等知识,题目难度中等,试题题量
较大,注意掌握化学平衡常数的概念及计算方法,明确
热化学方程式的书写方法及盖斯定律的含义及应用.
32.(16分)(2014•广东)石墨在材料领域有重要应用,某初级石墨中含SiO (7.8%)、Al O (5.1%)、Fe O
2 2 3 2 3
(3.1%)和MgO(0.5%)等杂质,设计的提纯与综合利用工艺如下:
(注:SiCl 的沸点为57.6℃,金属氯化物的沸点均高于150℃)
4
(1)向反应器中通入Cl 前,需通一段时间N ,主要目的是 通入氮气排尽装置中的空气,防止石墨发生氧化反
2 2
应,减少石墨损失 .
(2)高温反应后,石墨中氧化物杂质均转变为相应的氯化物,气体I中的碳氧化物主要为 CO ,由气体Ⅱ中某
物质得到水玻璃的化学反应方程式为 SiCl +6NaOH=Na SiO +4NaCl+3H O .
4 2 3 2
(3)步骤①为:搅拌、 过滤 、所得溶液IV中的阴离子有 AlO ﹣ 、 OH ﹣ 、 Cl ﹣ .
2
(4)由溶液Ⅳ生成沉淀Ⅴ的总反应的离子方程式为 AlO ﹣ +CH COOCH CH +2H O CH COO ﹣ +CH CH OH+Al
2 3 2 3 2 3 3 2
( OH ) ↓ ,100kg初级石墨最多可获得V的质量为 7.8 kg.
3
(5)石墨可用于自然水体中铜件的电化学防腐,完成图2防腐示意图,并作相应标注.
考点: 真题集萃;物质分离和提纯的方法和基本操作综合应用.
菁优网版权所有
专题: 实验设计题.
分析: (1)石墨化学性质在常温下稳定,而在高温下可与氧气发
生反应,所以通入氮气排尽装置中的空气,防止石墨发生
氧化反应;
(2)高温反应后,石墨中氧化物杂质均转变为相应的氯化物,根据杂质的含量可知,气体I中氯化物主要为SiCl 、
4
AlCl 、FeCl 等,气体I中碳氧化物主要为CO,SiCl 的沸
3 3 4
点为57.6℃,金属氯化物的沸点均高于150℃,80℃冷却得
到的气体Ⅱ含有SiCl 及CO,SiCl 与氢氧化钠溶液反应得到
4 4
硅酸钠与氯化钠;
(3)金属氯化物的沸点均高于150℃,则固体Ⅲ中存在
AlCl 、FeCl 、MgCl ,其中FeCl 、MgCl 与过量的氢氧化
3 3 2 3 2
钠溶液反应得到沉淀,而氯化铝与过量的氢氧化钠溶液反
应生成偏铝酸钠,过滤得到的溶液中含有偏铝酸钠、过量
的氢氧化钠;
(4)偏铝酸钠发生水解,加入乙酸乙酯除去过量的氢氧化
钠,且加热条件下水解平衡一直正向移动,得到氢氧化铝
沉淀、醋酸钠、乙醇;
根据氧化铝的含量计算氧化铝质量,再根据Al元素守恒计
算氢氧化铝的质量;
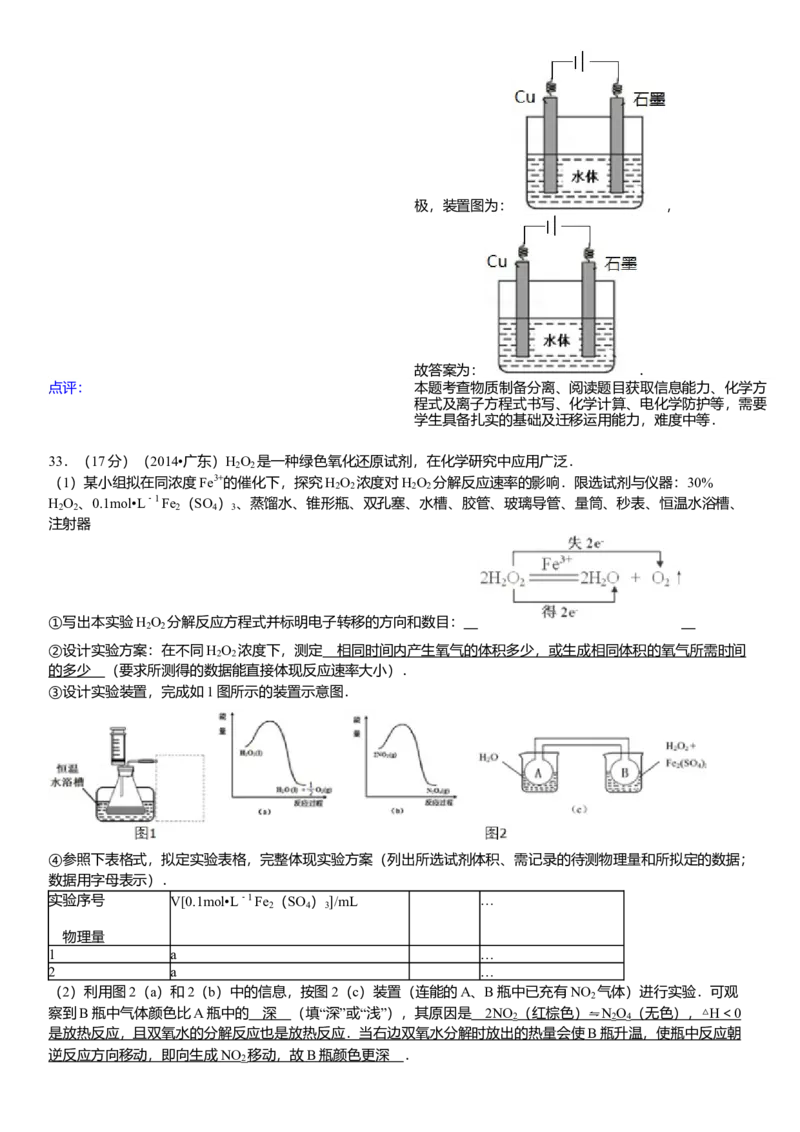
(5)Cu的化学性质比石墨活泼,所以应用外接电流的阴极
保护法保护Cu,故石墨作阳极,连接电源的正极,Cu作阴
极,连接电源的负极.
解答: 解:(1)石墨化学性质在常温下稳定,而在高温下可与氧
气发生反应,所以通入氮气排尽装置中的空气,防止石墨
发生氧化反应,减少石墨损失,
故答案为:通入氮气排尽装置中的空气,防止石墨发生氧
化反应,减少石墨损失;
(2)石墨过量高温反应后,石墨中氧化物杂质均转变为相
应的氯化物,根据杂质的含量可知,气体I中氯化物主要为
SiCl 、AlCl 、FeCl 等,气体I中碳氧化物主要为CO,
4 3 3
SiCl 的沸点为57.6℃,金属氯化物的沸点均高于150℃,
4
80℃冷却得到的气体Ⅱ含有SiCl 及CO,SiCl 与氢氧化钠
4 4
溶液反应得到硅酸钠与氯化钠,化学反应方程式为:
SiCl +6NaOH=Na SiO +4NaCl+3H O,
4 2 3 2
故答案为:CO;SiCl +6NaOH=Na SiO +4NaCl+3H O;
4 2 3 2
(3)金属氯化物的沸点均高于150℃,则固体Ⅲ中存在
AlCl 、FeCl 、MgCl ,其中FeCl 、MgCl 与过量的氢氧化
3 3 2 3 2
钠溶液反应得到沉淀,而氯化铝与过量的氢氧化钠溶液反
应生成偏铝酸钠,搅拌、过滤得到溶液IV,故溶液IV中的
阴离子有:AlO ﹣、OH﹣、Cl﹣,
2
故答案为:过滤;AlO ﹣、OH﹣、Cl﹣;
2
(4)偏铝酸钠发生水解,加入乙酸乙酯除去过量的氢氧化
钠,且加热条件下水解平衡一直正向移动,得到氢氧化铝
沉淀、醋酸钠、乙醇,由溶液IV生成沉淀V的总反应的离
子方程式为:AlO ﹣+CH COOCH CH +2H O CH COO﹣
2 3 2 3 2 3
+CH CH OH+Al(OH) ↓,
3 2 3
Al O 的质量分数为5.1%,则100kg初级石墨中氧化铝的质
2 3
量=100kg×5.1%=5.1kg,根据Al元素守恒,可知氢氧化铝
的质量= =7.8kg;
故答案为:AlO ﹣+CH COOCH CH +2H O CH COO﹣
2 3 2 3 2 3
+CH CH OH+Al(OH) ↓;7.8;
3 2 3
根据氧化铝的含量计算氧化铝质量,(5)Cu的化学性质比
石墨活泼,所以应用外接电流的阴极保护法保护Cu,故石
墨作阳极,连接电源的正极,Cu作阴极,连接电源的负极,装置图为: ,
故答案为: .
点评: 本题考查物质制备分离、阅读题目获取信息能力、化学方
程式及离子方程式书写、化学计算、电化学防护等,需要
学生具备扎实的基础及迁移运用能力,难度中等.
33.(17分)(2014•广东)H O 是一种绿色氧化还原试剂,在化学研究中应用广泛.
2 2
(1)某小组拟在同浓度Fe3+的催化下,探究H O 浓度对H O 分解反应速率的影响.限选试剂与仪器:30%
2 2 2 2
H O 、0.1mol•L﹣1 Fe (SO ) 、蒸馏水、锥形瓶、双孔塞、水槽、胶管、玻璃导管、量筒、秒表、恒温水浴槽、
2 2 2 4 3
注射器
①写出本实验H O 分解反应方程式并标明电子转移的方向和数目:
2 2
②设计实验方案:在不同H O 浓度下,测定 相同时间内产生氧气的体积多少,或生成相同体积的氧气所需时间
2 2
的多少 (要求所测得的数据能直接体现反应速率大小).
③设计实验装置,完成如1图所示的装置示意图.
④参照下表格式,拟定实验表格,完整体现实验方案(列出所选试剂体积、需记录的待测物理量和所拟定的数据;
数据用字母表示).
实验序号 V[0.1mol•L﹣1 Fe (SO ) /mL …
2 4 3
物理量
]
1 a …
2 a …
(2)利用图2(a)和2(b)中的信息,按图2(c)装置(连能的A、B瓶中已充有NO 气体)进行实验.可观
2
察到B瓶中气体颜色比A瓶中的 深 (填“深”或“浅”),其原因是 2NO
2
(红棕色)⇋ N
2
O
4
(无色),△ H < 0
是放热反应,且双氧水的分解反应也是放热反应.当右边双氧水分解时放出的热量会使 B 瓶升温,使瓶中反应朝
逆反应方向移动,即向生成 NO 移动,故 B 瓶颜色更深 .
2考点: 真题集萃;测定某些化学反应的速率;探究温度、压强对
化学反应速率的影响;性质实验方案的设计.
菁优网版权所有
专题: 实验设计题.
分析: (1)①过氧化氢在硫酸铁作催化剂条件下分解生成水与氧
气,反应中过氧化氢既作氧化剂又做还原剂;
②反应速率表示单位时间内物质的量浓度变化量,测定不
同浓度的过氧化氢对反应速率的影响,需要测定相同时间
内产生氧气的体积多少,或生成相同体积的氧气所需时间
的多少;
③利用排水量气法收集一定体积的氧气,用盛满水的量筒
倒立于盛水的水槽中,并用导管与图1连接;
④测定相同时间内产生氧气的体积多少,保证催化剂的浓
度应相同,故加入双氧水溶液体积与水的总体积不变,通
过改变二者体积,根据相同时间内生成氧气的体积说明不
同H O 浓度对反应速率影响;
2 2
(2)由图a可知,1mol过氧化氢总能量高于1mol水与
0.5mol氧气总能量,故过氧化氢分解是放热反应,由图b可
知,2mol二氧化氮的能量高于1mol四氧化二氮的能量,故
二氧化氮转化为四氧化二氮的反应为放热反应,所以图c
中,右侧烧杯的温度高于左侧,升高温度使2NO (红棕
2
色)⇋N
2
O
4
(无色)△H<0,向逆反应方向移动.
解答: 解:(1)①过氧化氢在硫酸铁作催化剂条件下分解生成水
与氧气,反应中过氧化氢既作氧化剂又做还原剂,标出电
子转移数目及方向为: ,
故答案为: ;
②反应速率表示单位时间内物质的量浓度变化量,测定不
同浓度的过氧化氢对反应速率的影响,需要测定相同时间
内产生氧气的体积多少,或生成相同体积的氧气所需时间
的多少,
故答案为:相同时间内产生氧气的体积多少,或生成相同
体积的氧气所需时间的多少;
③利用排水量气法收集一定体积的氧气,用盛满水的量筒
倒立于盛水的水槽中,并用导管与图1连接,装置图为:
,
故答案为: ;
④测定相同时间内产生氧气的体积多少,保证催化剂的浓
度应相同,故加入双氧水溶液体积与水的总体积不变,通
过改变二者体积,根据相同时间内生成氧气的体积说明不
同H O 浓度对反应速率影响,实验方案为:
2 2
实验序号 V[0.1mol•L﹣1 V(30% V(蒸馏水)
Fe 2 (SO 4 ) 3 /mLH 2 O 2 )/mL mL
1 a b c
]2 a c b
故答案为:
实验序号 V[0.1mol•L﹣1 V(30% V(蒸馏水)
Fe 2 (SO 4 ) 3 /mLH 2 O 2 )/mL mL
1 a b c
2 a ] c b
;
(2)由图a可知,1mol过氧化氢总能量高于1mol水与
0.5mol氧气总能量,故过氧化氢分解是放热反应,由图b可
知,2mol二氧化氮的能量高于1mol四氧化二氮的能量,故
二氧化氮转化为四氧化二氮的反应为放热反应,所以图c
中,右侧烧杯的温度高于左侧,升高温度使2NO (红棕
2
色)⇋N
2
O
4
(无色)△H<0,向逆反应方向移动,即向生成
NO 移动,故B瓶颜色更深,
2
故答案为:深;2NO
2
(红棕色)⇋N
2
O
4
(无色),△H<0
是放热反应,且双氧水的分解反应也是放热反应.当右边
双氧水分解时放出的热量会使B瓶升温,使瓶中反应朝逆
反应方向移动,即向生成NO 移动,故B瓶颜色更深.
2
点评: 本题考查氧化还原反应、反应速率影响因素实验、化学平
衡移动等,侧重对学生综合能力的考查,需要学生具备扎
实的基础,注意利用控制变量法测定外界条件对反应速率
的影响,难度中等.