文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
专题 08 常见的酸和碱
考点01 溶液的酸碱性和pH
考点02 酸及其性质
考点03 碱及其性质
考点04 中和反应
考点01 溶液的酸碱性和pH
1.(2024·河北·中考真题)某兴趣小组探究土壤酸碱性对植物生长的影响时,测得常温下四种不同土壤的
pH如下,其中显碱性的是( )
A. B. C. D.
2.(2024·天津·中考真题)下列食物的近似pH分别是:苹果为2.9~3.3,蕃茄为4.0~5.0,牛奶为6.3~
6.6,玉米粥为6.8~8.0。胃酸过多的人空腹时最适宜吃的食物是( )
A.苹果 B.蕃茄 C.牛奶 D.玉米粥
3.(2024·云南·中考真题)几种经济作物适宜生长的土壤pH范围如表所示。某地土壤pH为4.6,该地最
适宜种植的经济作物是( )
作物 杨梅 茶树 柑橘 樱桃
pH 4.0-5.0 5.0-5.5 5.5-6.5 6.5-7.5
A.杨梅 B.茶树 C.柑橘 D.樱桃
4.(2024·四川成都·中考真题)人体内一些液体的正常pH范围,如图。相关说法正确的是( )
人体内的一些液体的正常pH范围
血浆 7.35~7.45
唾液 6.6~7.1
胃液 0.9~1.5
乳汁 6.6~7.6
胆汁 7.1~7.3
胰液 7.5~8.0
A.血浆和乳汁均显酸性 B.胆汁比胰液的碱性强
C.可将pH试纸放入口腔测唾液的PH D.饮用苏打水可以缓解胃酸过多症状
5.(2023·江苏盐城·中考真题)苹果汁中滴入紫色石蕊溶液变红,苹果汁的 可能为( )
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.4 B.7 C.11 D.13
6.(2023·上海·中考真题)二氧化碳通入水中形成的溶液,pH可能为( )
A.4 B.7 C.10 D.13
7.(2023·青海西宁·中考真题)某同学用 pH试纸测得生活中一些物质的 pH(常温)如下:
物
番茄汁 厕所清洁剂 蒸馏水 炉具清洁剂
质
pH 4 2 7 13
其中酸性最强的是( )
A.番茄汁 B.厕所清洁剂 C.蒸馏水 D.炉具清洁剂
8.(2023·江苏常州·中考真题)“和谐”号动车保洁时先用洗车液清洗,然后用水冲洗至中性,最后洗车
工人会用pH试纸检测是否清洗合格。下列关于pH试纸的说法正确的是( )
A.可以粗略测定溶液酸碱度
B.试纸使用前要用水先湿润
C.将试纸投入待测液中测定
D.若pH=7说明洗车液残留
9.(2023·辽宁盘锦·中考真题)下列植物适宜在弱碱性土壤中种植的是( )
植物 茶树 小麦 棉花 甘草
适宜种植的土壤的pH 5.0~5.5 6.0~7.0 6.0~6.8 7.2~8.5
A.茶树 B.小麦 C.棉花 D.甘草
10.(2023·山东临沂·中考真题)某学校兴趣小组在“探究土壤酸碱性对植物生长的影响”的实践活动
中,测得土壤样品呈酸性,其测得结果可能是( )
A. B. C. D.
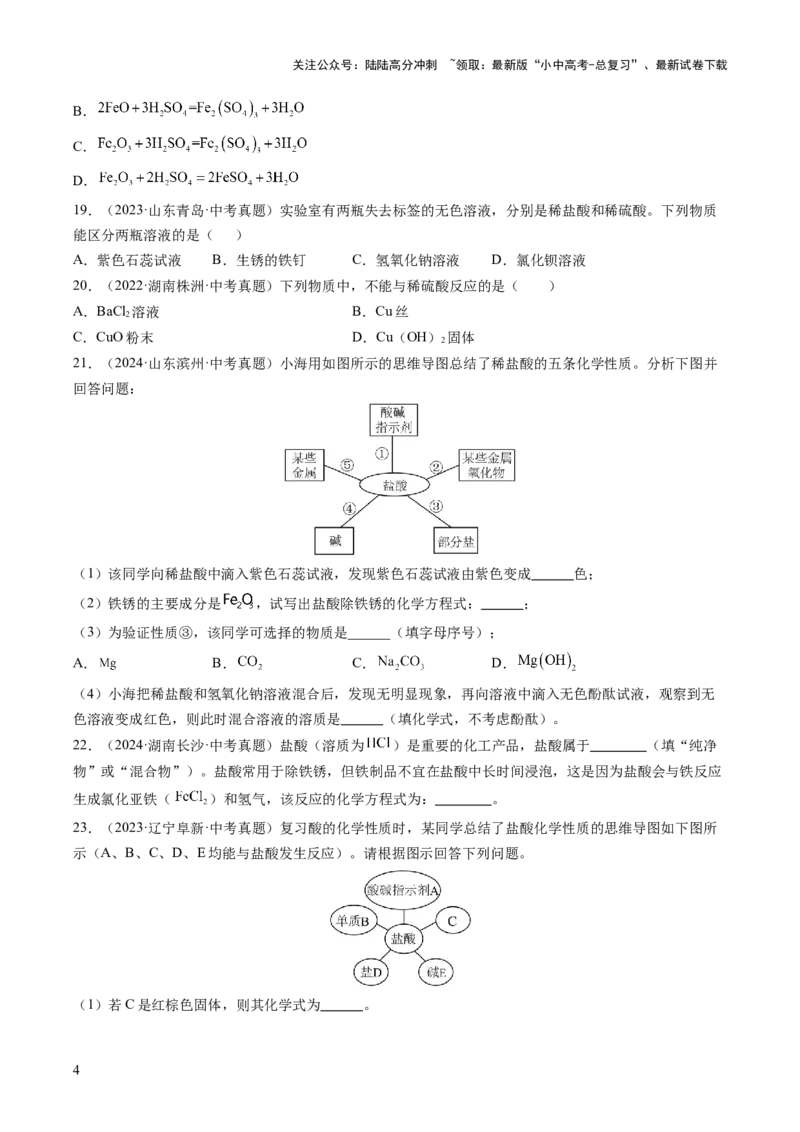
11.(2022·山东淄博·中考真题)生活中常见物质的pH如下图,下列说法正确的是( )
A.西红柿的酸性强于柠檬汁
B.洁厕净与碱液不能混合使用
C.用润湿的pH试纸测定雨水的pH
D.新鲜牛奶储存一段时间后味道变酸,pH变大
12.(2022·上海·中考真题)室温时某中性溶液的pH为( )
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.1 B.3 C.7 D.10
考点02 酸及其性质
13.(2024·重庆·中考真题)盐酸、硫酸是常见的酸。下列关于它们的说法不正确的是( )
A.两者的水溶液都能导电 B.两者的水溶液都能使紫色石蕊溶液变红
C.将水沿烧杯内壁缓慢注入浓硫酸中进行稀释 D.打开浓盐酸瓶盖观察到的白雾是盐酸小液滴
14.(2024·陕西·中考真题)下图实验进行一段时间后,观察到烧杯B内溶液已变为无色,则下列有关说
法正确的是( )
A.烧杯B内溶液无色说明溶液呈中性
B.烧杯A内溶液的质量变大
C.烧杯B内溶液颜色的变化是因为氢氧化钠溶液吸收了空气中的二氧化碳
D.上述实验能说明分子在不停地运动
15.(2023·江苏常州·中考真题)一瓶未开封的浓盐酸,部分标签如图所示。下列说法正确的是( )
盐酸(化学纯)
含HCl 37%
密度1.18g·mL-1
容量500mL
A.可加热浓缩成98%的浓盐酸
B.整瓶含有185gHCl溶质
C.可加水稀释成5%的稀盐酸
D.打开瓶盖冒出白色烟雾
16.(2023·辽宁阜新·中考真题)将盛放浓盐酸和浓硫酸的试剂瓶敞口放置在空气中一段时间(不考虑水
分蒸发),下列说法中正确的是( )
A.酸性都增强、pH都变小 B.溶质的质量分数都减小
C.溶液的质量都增加 D.溶质的质量都减小
17.(2023·吉林·中考真题)用硫酸进行下列实验,存在错误的做法是( )
A.干燥:用浓硫酸作为某些气体的干燥剂
B.稀释:将10g溶质质量分数为98%的浓硫酸稀释成10%的稀硫酸添加入90g的水
C.制备:用稀硫酸与锌粒反应来制取氢气
D.除锈:用适量的稀硫酸除去铁钉表面的铁锈
18.(2023·上海·中考真题)用稀硫酸除铁锈,反应的化学方程式书写正确的是( )
A.
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
B.
C.
D.
19.(2023·山东青岛·中考真题)实验室有两瓶失去标签的无色溶液,分别是稀盐酸和稀硫酸。下列物质
能区分两瓶溶液的是( )
A.紫色石蕊试液 B.生锈的铁钉 C.氢氧化钠溶液 D.氯化钡溶液
20.(2022·湖南株洲·中考真题)下列物质中,不能与稀硫酸反应的是( )
A.BaCl 溶液 B.Cu丝
2
C.CuO粉末 D.Cu(OH) 固体
2
21.(2024·山东滨州·中考真题)小海用如图所示的思维导图总结了稀盐酸的五条化学性质。分析下图并
回答问题:
(1)该同学向稀盐酸中滴入紫色石蕊试液,发现紫色石蕊试液由紫色变成 色;
(2)铁锈的主要成分是 ,试写出盐酸除铁锈的化学方程式: ;
(3)为验证性质③,该同学可选择的物质是______(填字母序号);
A. B. C. D.
(4)小海把稀盐酸和氢氧化钠溶液混合后,发现无明显现象,再向溶液中滴入无色酚酞试液,观察到无
色溶液变成红色,则此时混合溶液的溶质是 (填化学式,不考虑酚酞)。
22.(2024·湖南长沙·中考真题)盐酸(溶质为 )是重要的化工产品,盐酸属于 (填“纯净
物”或“混合物”)。盐酸常用于除铁锈,但铁制品不宜在盐酸中长时间浸泡,这是因为盐酸会与铁反应
生成氯化亚铁( )和氢气,该反应的化学方程式为: 。
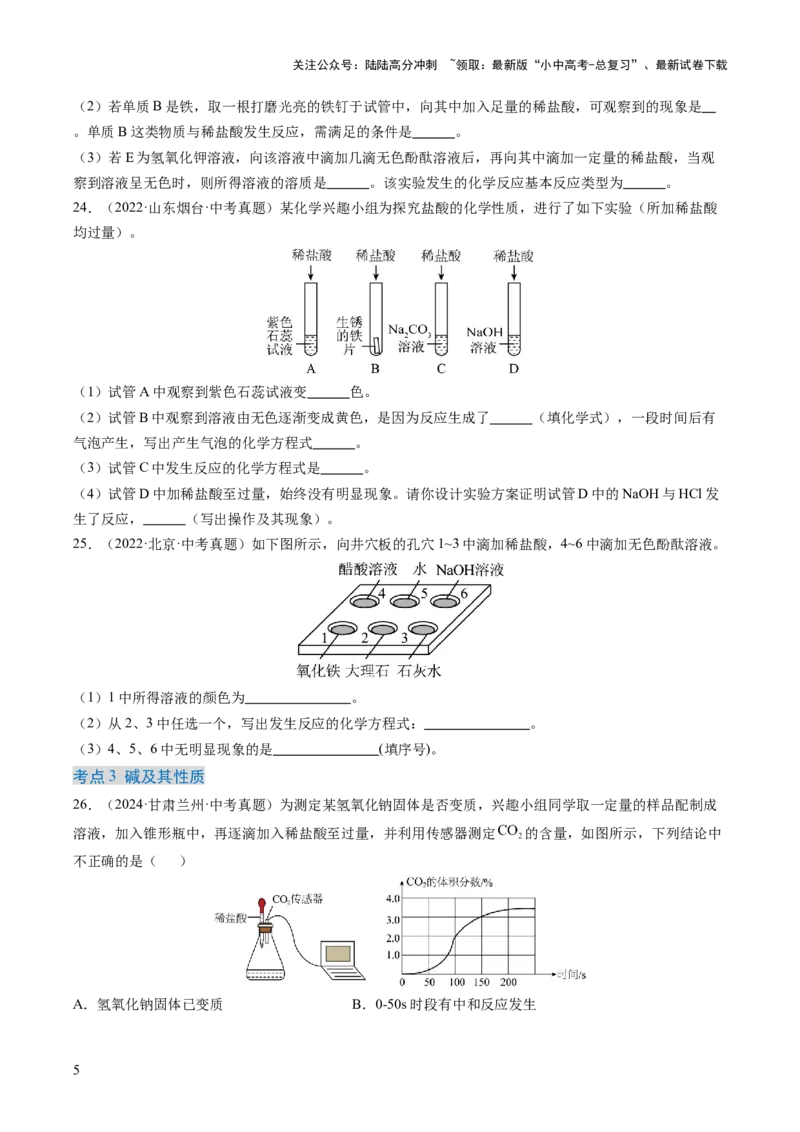
23.(2023·辽宁阜新·中考真题)复习酸的化学性质时,某同学总结了盐酸化学性质的思维导图如下图所
示(A、B、C、D、E均能与盐酸发生反应)。请根据图示回答下列问题。
(1)若C是红棕色固体,则其化学式为 。
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2)若单质B是铁,取一根打磨光亮的铁钉于试管中,向其中加入足量的稀盐酸,可观察到的现象是
。单质B这类物质与稀盐酸发生反应,需满足的条件是 。
(3)若E为氢氧化钾溶液,向该溶液中滴加几滴无色酚酞溶液后,再向其中滴加一定量的稀盐酸,当观
察到溶液呈无色时,则所得溶液的溶质是 。该实验发生的化学反应基本反应类型为 。
24.(2022·山东烟台·中考真题)某化学兴趣小组为探究盐酸的化学性质,进行了如下实验(所加稀盐酸
均过量)。
(1)试管A中观察到紫色石蕊试液变 色。
(2)试管B中观察到溶液由无色逐渐变成黄色,是因为反应生成了 (填化学式),一段时间后有
气泡产生,写出产生气泡的化学方程式 。
(3)试管C中发生反应的化学方程式是 。
(4)试管D中加稀盐酸至过量,始终没有明显现象。请你设计实验方案证明试管D中的NaOH与HCl发
生了反应, (写出操作及其现象)。
25.(2022·北京·中考真题)如下图所示,向井穴板的孔穴1~3中滴加稀盐酸,4~6中滴加无色酚酞溶液。
(1)1中所得溶液的颜色为 。
(2)从2、3中任选一个,写出发生反应的化学方程式: 。
(3)4、5、6中无明显现象的是 (填序号)。
考点3 碱及其性质
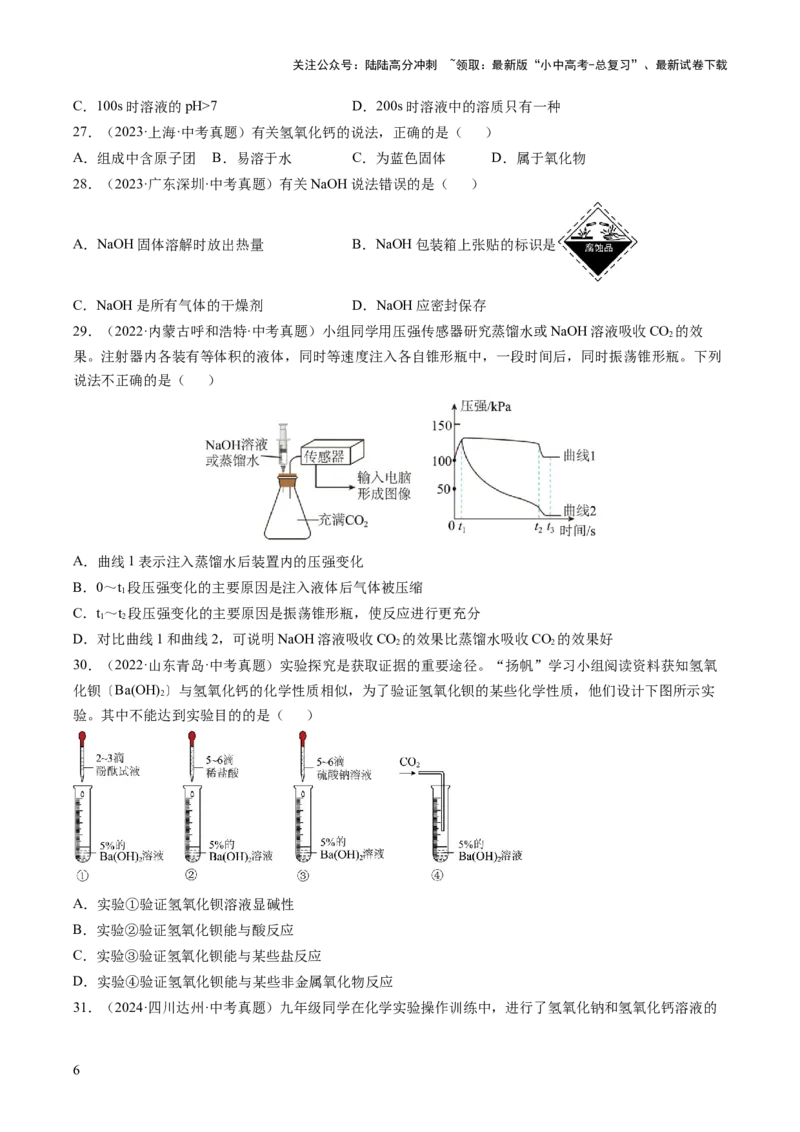
26.(2024·甘肃兰州·中考真题)为测定某氢氧化钠固体是否变质,兴趣小组同学取一定量的样品配制成
溶液,加入锥形瓶中,再逐滴加入稀盐酸至过量,并利用传感器测定 的含量,如图所示,下列结论中
不正确的是( )
A.氢氧化钠固体已变质 B.0-50s时段有中和反应发生
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C.100s时溶液的pH>7 D.200s时溶液中的溶质只有一种
27.(2023·上海·中考真题)有关氢氧化钙的说法,正确的是( )
A.组成中含原子团 B.易溶于水 C.为蓝色固体 D.属于氧化物
28.(2023·广东深圳·中考真题)有关NaOH说法错误的是( )
A.NaOH固体溶解时放出热量 B.NaOH包装箱上张贴的标识是
C.NaOH是所有气体的干燥剂 D.NaOH应密封保存
29.(2022·内蒙古呼和浩特·中考真题)小组同学用压强传感器研究蒸馏水或NaOH溶液吸收CO 的效
2
果。注射器内各装有等体积的液体,同时等速度注入各自锥形瓶中,一段时间后,同时振荡锥形瓶。下列
说法不正确的是( )
A.曲线1表示注入蒸馏水后装置内的压强变化
B.0~t 段压强变化的主要原因是注入液体后气体被压缩
1
C.t~t 段压强变化的主要原因是振荡锥形瓶,使反应进行更充分
1 2
D.对比曲线1和曲线2,可说明NaOH溶液吸收CO 的效果比蒸馏水吸收CO 的效果好
2 2
30.(2022·山东青岛·中考真题)实验探究是获取证据的重要途径。“扬帆”学习小组阅读资料获知氢氧
化钡〔Ba(OH) 〕与氢氧化钙的化学性质相似,为了验证氢氧化钡的某些化学性质,他们设计下图所示实
2
验。其中不能达到实验目的的是( )
A.实验①验证氢氧化钡溶液显碱性
B.实验②验证氢氧化钡能与酸反应
C.实验③验证氢氧化钡能与某些盐反应
D.实验④验证氢氧化钡能与某些非金属氧化物反应
31.(2024·四川达州·中考真题)九年级同学在化学实验操作训练中,进行了氢氧化钠和氢氧化钙溶液的
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
鉴别实验。为进一步探究氢氧化钠的化学性质,做了以下实验:
(1)A试管中的现象是 。
为探究B试管中反应后溶液中溶质的成分,同学们进行了以下探究。
【猜想与假设】
(2)猜想一:NaSO
2 4
猜想二:NaSO 、HSO
2 4 2 4
猜想三: 。
【设计并进行实验】
(3)完成并记录以下实验:
实验步骤 实验现象 实验结论
①取少量B试管中反应后的溶液,滴加碳酸钠溶液 无明显现象 猜想二不成立
②另取少量B试管中反应后的溶液,滴加硝酸镁溶液 。 猜想一不成立,猜想三成立
为探究氢氧化钠溶液与稀硫酸反应过程中pH的变化,甲、乙两组同学按图2所示装置进行实验,测定出
溶液pH变化如图3所示。
(4)甲组实验pH变化对应的曲线是 (填“I”或“Ⅱ”)。若取M点对应溶液滴加紫色石蕊试
液,现象是 。
(5)氢氧化钠溶液久置在空气中会变质,其原因是 (用化学方程式表示);向部分变质的
氢氧化钠溶液中加入适量 溶液可除去杂质。
32.(2024·黑龙江牡丹江·中考真题)兴趣小组对一瓶久置的 固体的变质情况进行了实验探究。
【提出问题】 变质了吗?
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【作出猜想】①没有变质 ②已经变质
(1)请用化学方程式表示 能变质的原因 。
任务一 定性实验 探究该 固体是否变质
【实验活动1】
(2)兴趣小组设计方案进行如下实验
实验方案 实验现象 实验结论
猜想②成立
取少量该 固体样品完全溶于水,加入过量稀盐酸
依据是 (用化学方程式表示)
【反思评价】有的同学提出此实验无法确定该 固体变质程度。
任务二 定量实验 探究该 固体变质程度
【实验活动2】
(3)兴趣小组利用控制变量的方法进行实验,实验数据如下表所示。
实验 分别向左右容器内加入下 温度升高值/ 溶液
实验装置
序号 列物质
1 固体 31.52 13.69
固体a的数值
2 10.03 11.92
为
3 该 固体样品 15.71 m
【实验结论】
(4)小组同学分析温度升高值数据,确定该 固体变质程度是 ,请推测m的取值范围是
。
任务三计算该 固体的变质率
【实验活动3】实验步骤:称量 该 固体样品于小烧杯中备用:量取 的稀盐酸:用电
子秤称量反应前仪器和药品的质量,记录数据:将稀盐酸加入小烧杯内,待完全反应,再次称量仪器和反
应后溶液的质量,记录数据。
反应前质量/g 反应后质量/g 质量差/g
105.32 105.02 0.30
(5)兴趣小组结合实验数据,计算出该 固体的变质率为 (结果保留至1%)。
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
温馨提示:变质率=(已经变质的 的质量/未变质前 的总质量)×100%
【反思评价】兴趣小组充分认识到定量研究在化学实验中的重要作用。
【拓展延伸】
(6)生活中的管道疏通剂和炉具清洁剂成分中都含有 ,包装标签上应注明的注意事项是
(写一条)。
33.(2023·青海·中考真题)固体氢氧化钠暴露在空气中,容易吸收 而潮解,并与空气中的二氧
化碳反应而变质,写出反应的化学方程式: 。因此,氢氧化钠必须 保存。
34.(2023·山西·中考真题)以典型物质为核心,进行问题的设置与整合,是我们全面认识物质性质及应
用的有效途径小明同学在小组合作学习过程中,对氢氧化钠的相关问题,以结构图的形式进行了如下梳理
联系实际,解决问题:
(1)氢氧化钠在生活中可用来 。
(2)氢氧化钠在空气中吸水后的热量变化为 。
(3)氢氧化钠使用时必须十分小心,原因是 。
(4)检验氢氧化钠溶液的酸碱度,最简单的方法是 。
(5)向氢氧化钠溶液中滴加硫酸铜溶液,发生反应的化学方程式为 。
35.(2023·江苏宿迁·中考真题)学习小组在老师的指导下对氢氧化钠、氧氧化钙的性质进行探究。
I.探究 的性质:同学们设计如图所示实验。
(1)实验一中酚酞试液变红,说明 溶液显 性。
(2)实验二、实验三验证了 能与某些 发生反应(填物质类别)。写出实验三中发生反应的
化学方程式: 。
(3)实验四中滴入 浓溶液后观察到的现象是 。
II.探究 的性质:甲、乙两位同学分别取 ,固体于试管中,各加入 水,充分振
荡,均得到悬浊液。
(4)甲同学将盛悬浊液的试管静置后,吸取上层清液滴入盛有少量碳酸钠溶液的试管中,观察到有白色
沉淀产生,该反应的化学方程式为 。
(5)如下图所示,乙同学向盛悬浊液的试管中滴入2滴酚酞试液,振荡、静置后,观察到试管底部有固
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
体,上层清液呈红色,然后向试管中逐滴加入稀盐酸至上层清液变为无色,该过程中发生反应的实质是
;再将试管振荡、静置,上层清液又变成红色,其原因 。
36.(2022·湖北十堰·中考真题)某化学兴趣小组同学在探究碱的化学性质时,设计并完成了如下实验:
【实验探究一】
Ⅰ、向滴加有酚酞的NaOH溶液中慢慢滴入稀盐酸(如图1所示),边滴加边振荡,测得试管①中最终溶
液的pH=2。
Ⅱ、分别称取0.5g氢氧化钙粉末置于两支试管中,各滴加2mL水,振荡;再向试管②中加入2mL水、试
管③中加入2mL稀盐酸(如图2所示)。振荡并观察现象。
Ⅲ、向盛有氢氧化钠溶液的试管④中加入少量硫酸铜溶液,振荡。静置后测得上层清液的pH=12,继续向其
中滴加几滴稀盐酸(如图3所示),试管⑤中无明显现象。
(1)实验Ⅰ中,能证明盐酸和氢氧化钠发生了化学反应的实验现象是 。试管①最终溶液中含
有的溶质有(酚酞除外) 。
(2)实验Ⅱ中用水作对照实验,其目的是 。
(3)试管④中发生反应的化学方程式是 。
【分析讨论】甲同学通过“试管⑤中无明显现象”得出“盐酸不能与Cu(OH) 发生反应”的结论。乙同
2
学认为甲同学的结论不正确,于是继续开展如下探究。
【实验探究二】取试管①反应后的溶液逐滴滴入试管⑤中,直至过量,边加边振荡。
(4)实验探究二中依次观察到的现象有 。
【结论】盐酸能与Cu(OH) 发生反应。
2
【交流反思】最终试管⑤溶液中大量存在的离子有 。
考点04 中和反应
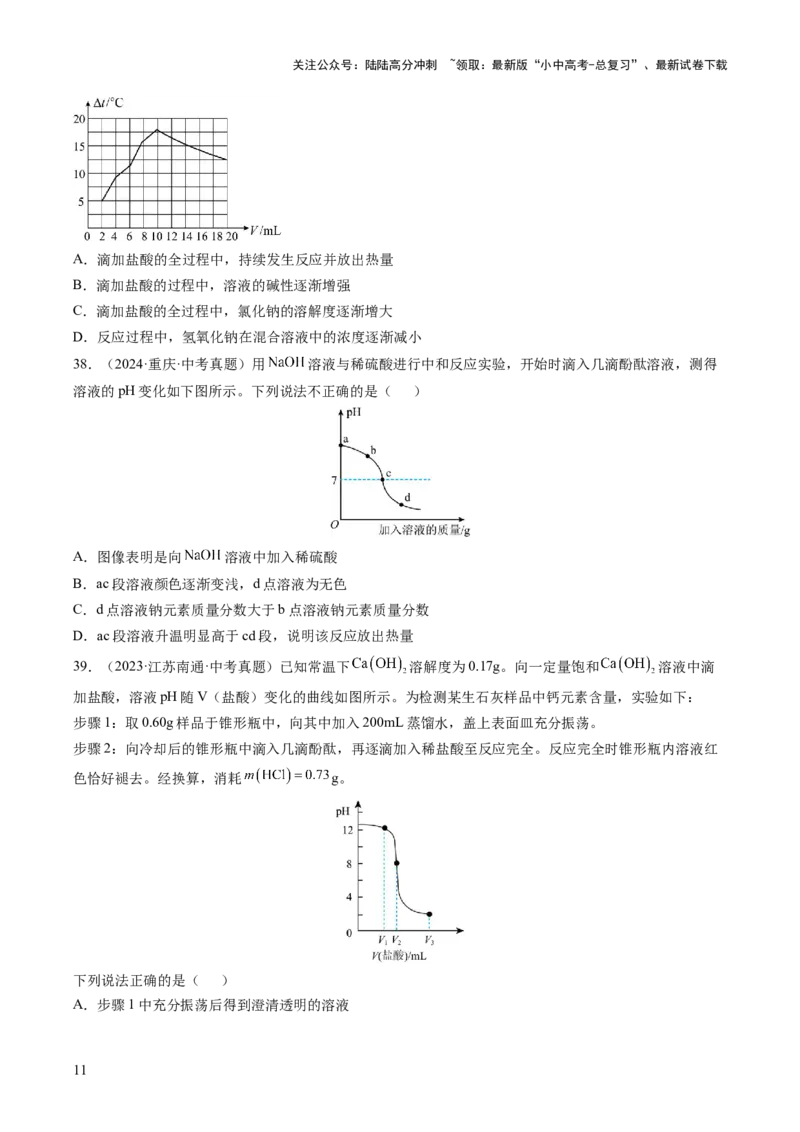
37.(2024·山西·中考真题)室温下,向一定体积10%的氢氧化钠溶液中滴加10%的盐酸,测得溶液温度
变化与加入盐酸体积的关系如表△t(为溶液实时温度与初始温度差),其中表述正确的是( )
盐酸体积V/mL 2 4 6 8 10 12 14 16 18 20
溶液温度变化△t/℃ 5.2 9.6 12.0 16.0 18.2 16.7 15.7 14.7 13.7 12.9
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.滴加盐酸的全过程中,持续发生反应并放出热量
B.滴加盐酸的过程中,溶液的碱性逐渐增强
C.滴加盐酸的全过程中,氯化钠的溶解度逐渐增大
D.反应过程中,氢氧化钠在混合溶液中的浓度逐渐减小
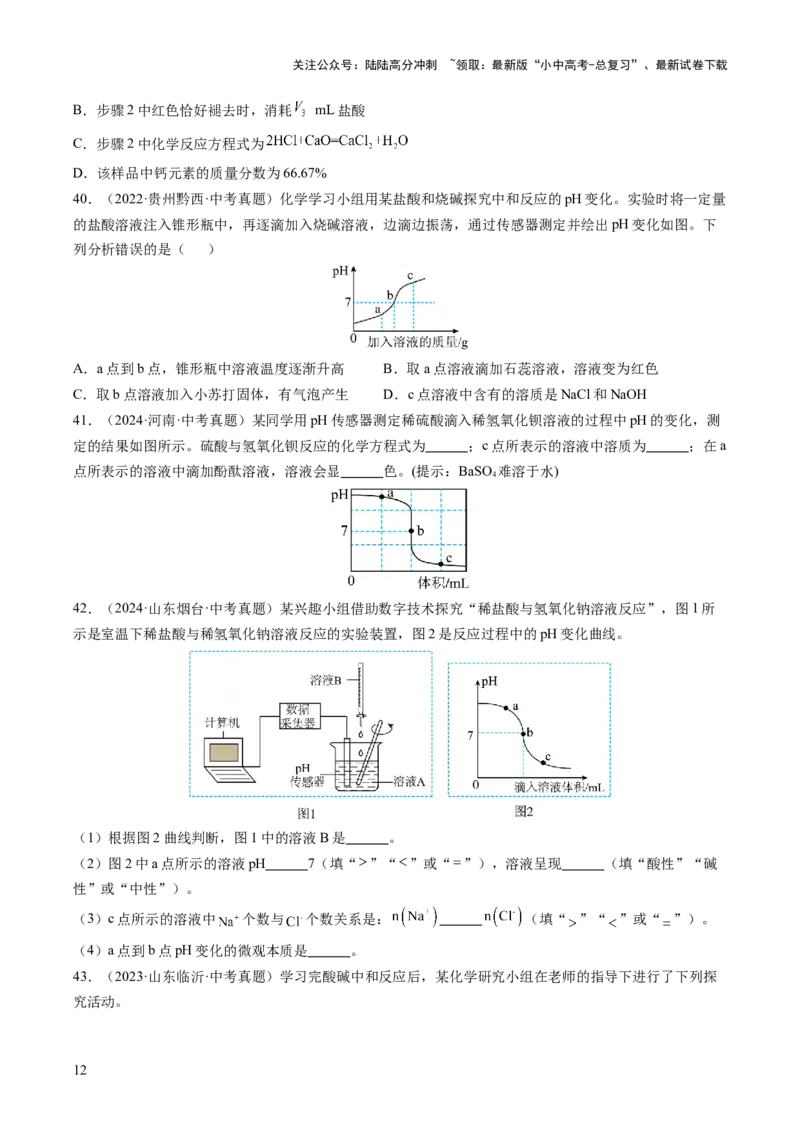
38.(2024·重庆·中考真题)用 溶液与稀硫酸进行中和反应实验,开始时滴入几滴酚酞溶液,测得
溶液的pH变化如下图所示。下列说法不正确的是( )
A.图像表明是向 溶液中加入稀硫酸
B.ac段溶液颜色逐渐变浅,d点溶液为无色
C.d点溶液钠元素质量分数大于b点溶液钠元素质量分数
D.ac段溶液升温明显高于cd段,说明该反应放出热量
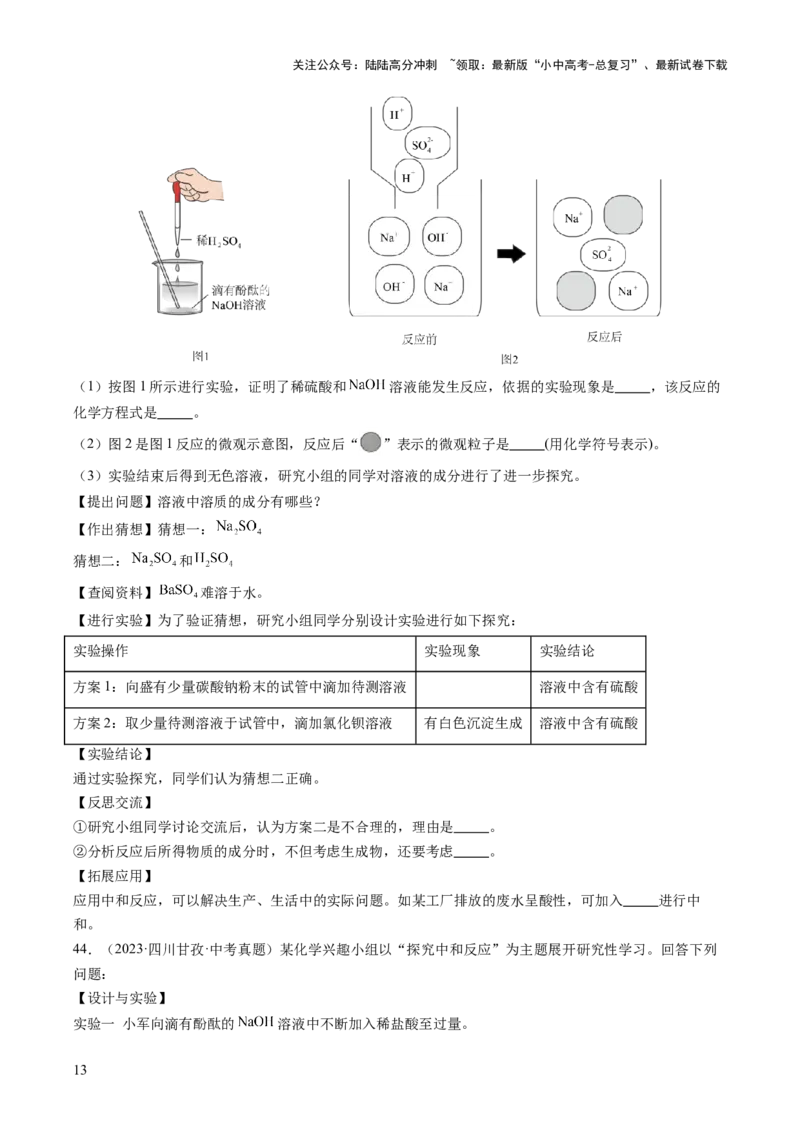
39.(2023·江苏南通·中考真题)已知常温下 溶解度为0.17g。向一定量饱和 溶液中滴
加盐酸,溶液pH随V(盐酸)变化的曲线如图所示。为检测某生石灰样品中钙元素含量,实验如下:
步骤1:取0.60g样品于锥形瓶中,向其中加入200mL蒸馏水,盖上表面皿充分振荡。
步骤2:向冷却后的锥形瓶中滴入几滴酚酞,再逐滴加入稀盐酸至反应完全。反应完全时锥形瓶内溶液红
色恰好褪去。经换算,消耗 g。
下列说法正确的是( )
A.步骤1中充分振荡后得到澄清透明的溶液
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
B.步骤2中红色恰好褪去时,消耗 mL盐酸
C.步骤2中化学反应方程式为
D.该样品中钙元素的质量分数为66.67%
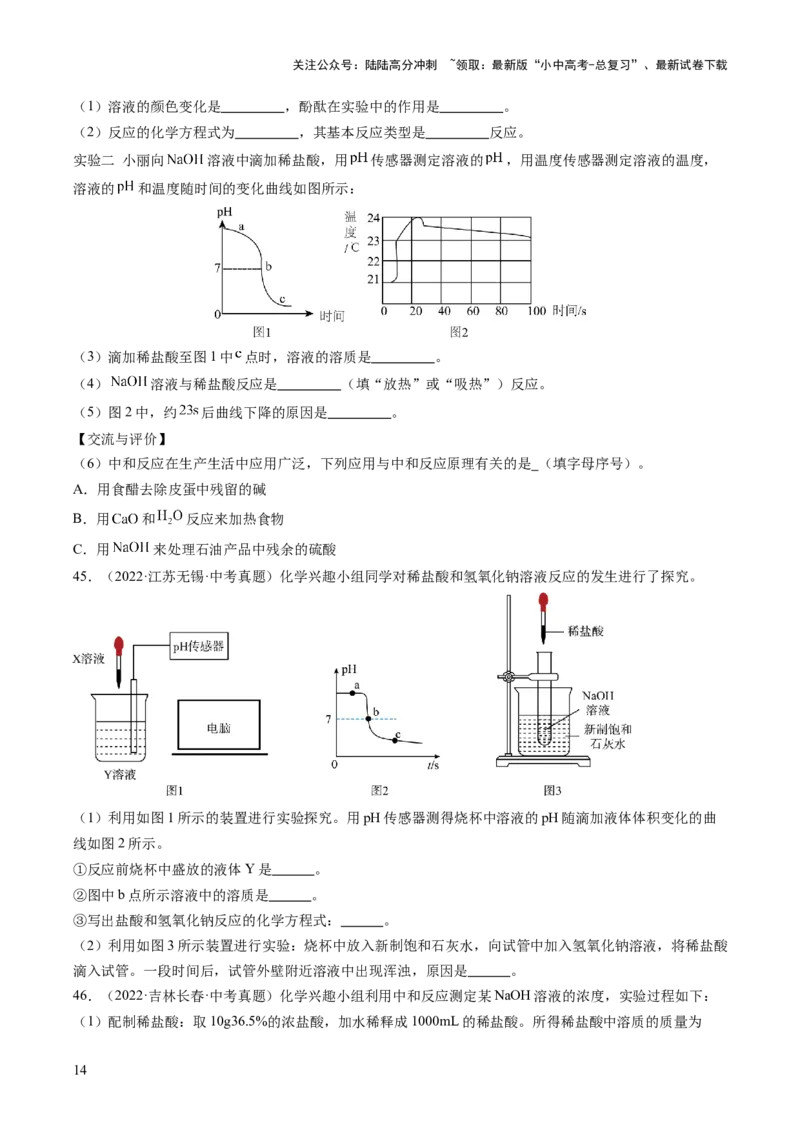
40.(2022·贵州黔西·中考真题)化学学习小组用某盐酸和烧碱探究中和反应的pH变化。实验时将一定量
的盐酸溶液注入锥形瓶中,再逐滴加入烧碱溶液,边滴边振荡,通过传感器测定并绘出pH变化如图。下
列分析错误的是( )
A.a点到b点,锥形瓶中溶液温度逐渐升高 B.取a点溶液滴加石蕊溶液,溶液变为红色
C.取b点溶液加入小苏打固体,有气泡产生 D.c点溶液中含有的溶质是NaCl和NaOH
41.(2024·河南·中考真题)某同学用pH传感器测定稀硫酸滴入稀氢氧化钡溶液的过程中pH的变化,测
定的结果如图所示。硫酸与氢氧化钡反应的化学方程式为 ;c点所表示的溶液中溶质为 ;在a
点所表示的溶液中滴加酚酞溶液,溶液会显 色。(提示:BaSO 难溶于水)
4
42.(2024·山东烟台·中考真题)某兴趣小组借助数字技术探究“稀盐酸与氢氧化钠溶液反应”,图1所
示是室温下稀盐酸与稀氢氧化钠溶液反应的实验装置,图2是反应过程中的pH变化曲线。
(1)根据图2曲线判断,图1中的溶液B是 。
(2)图2中a点所示的溶液pH 7(填“ ”“ ”或“ ”),溶液呈现 (填“酸性”“碱
性”或“中性”)。
(3)c点所示的溶液中 个数与 个数关系是: (填“ ”“ ”或“ ”)。
(4)a点到b点pH变化的微观本质是 。
43.(2023·山东临沂·中考真题)学习完酸碱中和反应后,某化学研究小组在老师的指导下进行了下列探
究活动。
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)按图1所示进行实验,证明了稀硫酸和 溶液能发生反应,依据的实验现象是 ,该反应的
化学方程式是 。
(2)图2是图1反应的微观示意图,反应后“ ”表示的微观粒子是 (用化学符号表示)。
(3)实验结束后得到无色溶液,研究小组的同学对溶液的成分进行了进一步探究。
【提出问题】溶液中溶质的成分有哪些?
【作出猜想】猜想一:
猜想二: 和
【查阅资料】 难溶于水。
【进行实验】为了验证猜想,研究小组同学分别设计实验进行如下探究:
实验操作 实验现象 实验结论
方案1:向盛有少量碳酸钠粉末的试管中滴加待测溶液 溶液中含有硫酸
方案2:取少量待测溶液于试管中,滴加氯化钡溶液 有白色沉淀生成 溶液中含有硫酸
【实验结论】
通过实验探究,同学们认为猜想二正确。
【反思交流】
①研究小组同学讨论交流后,认为方案二是不合理的,理由是 。
②分析反应后所得物质的成分时,不但考虑生成物,还要考虑 。
【拓展应用】
应用中和反应,可以解决生产、生活中的实际问题。如某工厂排放的废水呈酸性,可加入 进行中
和。
44.(2023·四川甘孜·中考真题)某化学兴趣小组以“探究中和反应”为主题展开研究性学习。回答下列
问题:
【设计与实验】
实验一 小军向滴有酚酞的 溶液中不断加入稀盐酸至过量。
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)溶液的颜色变化是 ,酚酞在实验中的作用是 。
(2)反应的化学方程式为 ,其基本反应类型是 反应。
实验二 小丽向 溶液中滴加稀盐酸,用 传感器测定溶液的 ,用温度传感器测定溶液的温度,
溶液的 和温度随时间的变化曲线如图所示:
(3)滴加稀盐酸至图1中 点时,溶液的溶质是 。
(4) 溶液与稀盐酸反应是 (填“放热”或“吸热”)反应。
(5)图2中,约 后曲线下降的原因是 。
【交流与评价】
(6)中和反应在生产生活中应用广泛,下列应用与中和反应原理有关的是 (填字母序号)。
A.用食醋去除皮蛋中残留的碱
B.用 和 反应来加热食物
C.用 来处理石油产品中残余的硫酸
45.(2022·江苏无锡·中考真题)化学兴趣小组同学对稀盐酸和氢氧化钠溶液反应的发生进行了探究。
(1)利用如图1所示的装置进行实验探究。用pH传感器测得烧杯中溶液的pH随滴加液体体积变化的曲
线如图2所示。
①反应前烧杯中盛放的液体Y是 。
②图中b点所示溶液中的溶质是 。
③写出盐酸和氢氧化钠反应的化学方程式: 。
(2)利用如图3所示装置进行实验:烧杯中放入新制饱和石灰水,向试管中加入氢氧化钠溶液,将稀盐酸
滴入试管。一段时间后,试管外壁附近溶液中出现浑浊,原因是 。
46.(2022·吉林长春·中考真题)化学兴趣小组利用中和反应测定某NaOH溶液的浓度,实验过程如下:
(1)配制稀盐酸:取10g36.5%的浓盐酸,加水稀释成1000mL的稀盐酸。所得稀盐酸中溶质的质量为
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
g:
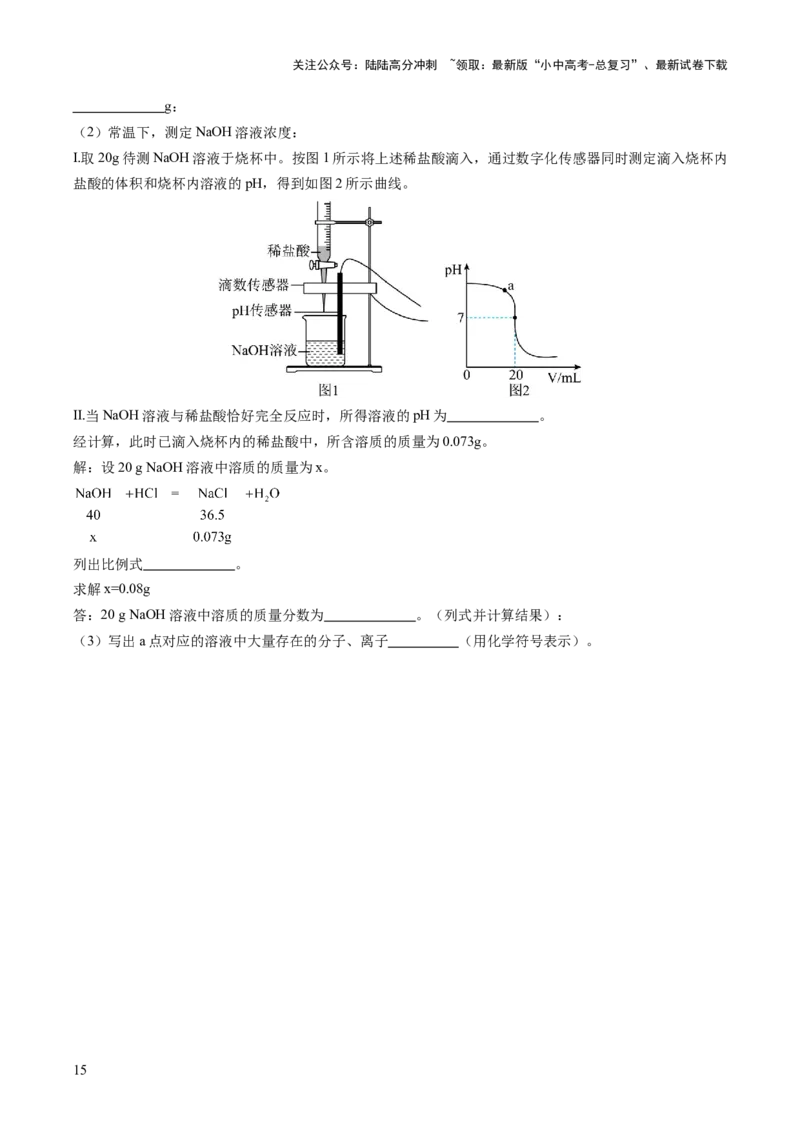
(2)常温下,测定NaOH溶液浓度:
I.取20g待测NaOH溶液于烧杯中。按图1所示将上述稀盐酸滴入,通过数字化传感器同时测定滴入烧杯内
盐酸的体积和烧杯内溶液的pH,得到如图2所示曲线。
Ⅱ.当NaOH溶液与稀盐酸恰好完全反应时,所得溶液的pH为 。
经计算,此时已滴入烧杯内的稀盐酸中,所含溶质的质量为0.073g。
解:设20 g NaOH溶液中溶质的质量为x。
列出比例式 。
求解x=0.08g
答:20 g NaOH溶液中溶质的质量分数为 。(列式并计算结果):
(3)写出a点对应的溶液中大量存在的分子、离子 (用化学符号表示)。
15