文档内容
浙江 2020 高考选科考试
化学试题
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 Si
28 S 32 Cl 35.5 K 39 Ca 40 Mn 55 Fe 56 Cu 64 Zn 65 Ag 108 I 127
Ba 137
一、选择题(本大题共 25小题,每小题 2分,共 50分。每小题列出的四个备选
项中只有一个是符合题目要求的,不选、多选、错选均不得分)
1.水溶液呈酸性的是( )
A. NaCl B. NaHSO C. HCOONa D. NaHCO
4 3
2.固液分离操作中,需要用到的仪器是( )
A. B. C. D.
3.下列物质在熔融状态下不导电的是( )
A. NaOH B. CaCl C. HCl D. K SO
2 2 4
4.下列物质对应的组成不正确的是( )
A. 干冰:CO B. 熟石灰:CaSO 2H O
2 4 2
C. 胆矾:CuSO 5H O D. 小苏打:NaHCO
4 2 3
5.下列表示不正确的是( )
A. 乙烯的结构式: B. 甲酸甲酯的结构简式:C H O
2 4 2
C. 2甲基丁烷的键线式: D. 甲基的电子式:
6.下列说法不正确的是( )
A. 天然气是不可再生能源
B. 用水煤气可合成液态碳氢化合物和含氧有机物
C. 煤的液化属于物理变化D. 火棉是含氮量高的硝化纤维
7.下列说法正确的是( )
A. 35Cl和37Cl是两种不同的元素 B. 单晶硅和石英互为同素异形体
C. HCOOH和HOCH CHO互为同系物 D. H与Na在元素周期表中处于同一
2
主族
8.下列说法不正确的是( )
A. Cl会破坏铝表面的氧化膜
B. NaHCO 的热稳定性比Na CO 强
3 2 3
C. KMnO 具有氧化性,其稀溶液可用于消毒
4
D. 钢铁在潮湿空气中生锈主要是发生了电化学腐蚀
9.下列说法不正确的是( )
A. 高压钠灯可用于道路照明
B. SiO 可用来制造光导纤维
2
C. 工业上可采用高温冶炼黄铜矿的方法获得粗铜
D. BaCO 不溶于水,可用作医疗上检查肠胃的钡餐
3
加热
10.反应MnO 4HCl(浓) MnCl Cl↑2H O中,氧化产物与还原产物的物质的
2 2 2 2
量之比是( )
A. 1:2 B. 1:1 C. 2:1 D. 4:1
11.下列有关实验说法不正确的是( )
A. 萃取Br 时,向盛有溴水的分液漏斗中加入CCl ,振荡、静置分层后,打开旋塞,先
2 4
将水层放出
B. 做焰色反应前,铂丝用稀盐酸清洗并灼烧至火焰呈无色
C. 乙醇、苯等有机溶剂易被引燃,使用时须远离明火,用毕立即塞紧瓶塞
D. 可用AgNO 溶液和稀HNO 区分NaCl、NaNO 和NaNO
3 3 2 3
12.下列说法正确的是( )A. Na O在空气中加热可得固体Na O
2 2 2
B Mg加入到过量FeCl 溶液中可得Fe
. 3
C. FeS 在沸腾炉中与O 反应主要生成SO
2 2 3
D. H O 溶液中加入少量MnO 粉末生成H 和O
2 2 2 2 2
13.能正确表示下列反应的离子方程式是( )
A. NH FeSO 溶液与少量Ba(OH) 溶液反应:SO2- Ba2 BaSO
4 2 4 2 2 4 4
通电
B. 电解MgCl 水溶液:2Cl 2H O 2OH Cl H
2 2 2 2
C. 乙酸乙酯与NaOH溶液共热:
CH COOCH CH OH ΔCH COO CH CH OH
3 2 3 3 3 2
D. CuSO 溶液中滴加稀氨水:Cu2 2OH Cu(OH)
4 2
14.下列说法不正确的是( )
A. 相同条件下等质量的甲烷、汽油、氢气完全燃烧,放出的热量依次增加
B. 油脂在碱性条件下水解生成的高级脂肪酸盐是肥皂的主要成分
C. 根据纤维在火焰上燃烧产生的气味,可以鉴别蚕丝与棉花
D. 淀粉、纤维素、蛋白质都属于高分子化合物
15.有关 的说法正确的是( )
A. 可以与氢气发生加成反应 B. 不会使溴水褪色
C. 只含二种官能团 D. 1mol该物质与足量NaOH溶液反
应,最多可消耗1mol NaOH
16.X、Y、Z、M、Q五种短周期元素,原子序数依次增大。Y元素的最高正价为4价,
Y元素与Z、M元素相邻,且与M元素同主族;化合物Z X 的电子总数为18个;Q元
2 4
素的原子最外层电子数比次外层少一个电子。下列说法不正确的是( )
A. 原子半径:Z Y M
B. 最高价氧化物对应水化物的酸性:Z Y MC. X ZZX 易溶于水,其水溶液呈碱性
2 2
D. X、Z和Q三种元素形成的化合物一定是共价化合物
17.下列说法不正确的是( )
A. 2.0107molL1的盐酸中c H 2.0107molL1
B. 将KCl溶液从常温加热至80℃,溶液的pH变小但仍保持中性
C. 常温下,NaCN溶液呈碱性,说明HCN是弱电解质
D. 常温下,pH为3的醋酸溶液中加入醋酸钠固体,溶液pH增大
18.5mL0.1molL1KI溶液与1mL0.1molL1FeCl 溶液发生反应:
3
2Fe3(aq)2I(aq)2Fe2(aq)I (aq),达到平衡。下列说法不正确的是( )
2
A. 加入苯,振荡,平衡正向移动
B. 经苯2次萃取分离后,在水溶液中加入KSCN,溶液呈血红色,表明该化学反应存在
限度
C. 加入FeSO 固体,平衡逆向移动
4
c2 Fe2+
D. 该反应的平衡常数K=
c2 Fe3+ c2 I
19.N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A. 4MnO 5HCHO12H 4Mn2 5CO 11H O,1mol4MnO 5HCHO
4 2 2 4
完全反应转移的电子数为20N
A
B. 用电解粗铜的方法精炼铜,当电路中通过的电子数为N 时,阳极应有32gCu转化为
A
Cu2
C. 常温下,pH9的CH COONa溶液中,水电离出的H数为105N
3 A
D. 1L浓度为0.100molL1的Na CO 溶液中,阴离子数为0.100N
2 3 A
20.一定条件下:2NO (g)N O (g) H 0。在测定NO 的相对分子质量时,
2 2 4 2
下列条件中,测定结果误差最小的是( )A. 温度0℃、压强50kPa B. 温度130℃、压强300kPa
C. 温度25℃、压强100kPa D. 温度130℃、压强50kPa
21.电解高浓度RCOONa(羧酸钠)的NaOH溶液,在阳极RCOO放电可得到RR(烷
烃)。下列说法不正确的是( )
通电
A. 电解总反应方程式:2RCOONa2H O RR2CO H 2NaOH
2 2 2
B. RCOO在阳极放电,发生氧化反应
C. 阴极的电极反应:2H O2e 2OH H
2 2
D. 电解CH COONa、CH CH COONa和NaOH混合溶液可得到乙烷、丙烷和丁烷
3 3 2
22.关于下列ΔH 的判断正确的是( )
CO2(aq)H(aq)HCO(aq) ΔH
3 3 1
CO2-(aq)H O(l)HCO(aq)OH(aq) ΔH
3 2 3 2
OH(aq)H(aq)H O(l) ΔH
2 3
OH(aq)CH COOH(aq)=CH COO(aq)H O(l) ΔH
3 3 2 4
A. ΔH <0 ΔH <0 B. ΔH <ΔH C. ΔH <0 ΔH >0 D.
1 2 1 2 3 4
ΔH >ΔH
3 4
23.常温下,用0.1molL1氨水滴定10mL浓度均为0.1molL1的HCl和CH COOH的
3
混合液,下列说法不正确的是( )
A. 在氨水滴定前,HCl和CH COOH的混合液中c
Cl
c
CH
COO
3 3
B. 当滴入氨水10mL时,c NH+ +cNH H O=c CH COO +cCH COOH
4 3 2 3 3
C. 当滴入氨水20mL时,cCH COOH+c H+ =cNH H O+c OH
3 3 2
D. 当溶液呈中性时,氨水滴入量大于20mL,c
NH
c
Cl
4
24.Ca SiO 是硅酸盐水泥的重要成分之一,其相关性质的说法不正确的是( )
3 5Δ
A. 可发生反应:Ca SiO 4NH Cl CaSiO 2CaCl 4NH 2H O
3 5 4 3 2 3 2
B. 具有吸水性,需要密封保存
C. 能与SO ,反应生成新盐
2
D. 与足量盐酸作用,所得固体产物主要为SiO
2
25.黄色固体X,可能含有漂白粉、FeSO 、Fe SO 、CuCl 、KI之中的几种或全
4 2 4 3 2
部。将X与足量的水作用,得到深棕色固体混合物Y和无色碱性溶液Z。下列结论合理的
是( )
A. X中含KI,可能含有CuCl
2
B. X中含有漂白粉和FeSO
4
C. X中含有CuCl ,Y中含有Fe(OH)
2 3
D. 用H SO 酸化溶液Z,若有黄绿色气体放出,说明X中含有CuCl
2 4 2
二、非选择题(本大题共 6小题,共 50分)
26.(1)气态氢化物热稳定性HF大于HCl的主要原因是__________。
(2)CaCN 是离子化合物,各原子均满足8电子稳定结构,CaCN 的电子式是_______。
2 2
(3)常温下,在水中的溶解度乙醇大于氯乙烷,原因是__________。
27.100mL0.200molL1CuSO 溶液与1.95g锌粉在量热计中充分反应。测得反应前温
4
度为20.1℃,反应后最高温度为30.1℃。
已知:反应前后,溶液的比热容均近似为4.18Jg1℃1、溶液的密度均近似为
1.00gcm3,忽略溶液体积、质量变化和金属吸收的热量。请计算:
(1)反应放出的热量Q=_____J。
(2)反应Zn(s)CuSO (aq)=ZnSO (aq)Cu(s)的ΔH=______kJmol1(列式计算)。
4 4
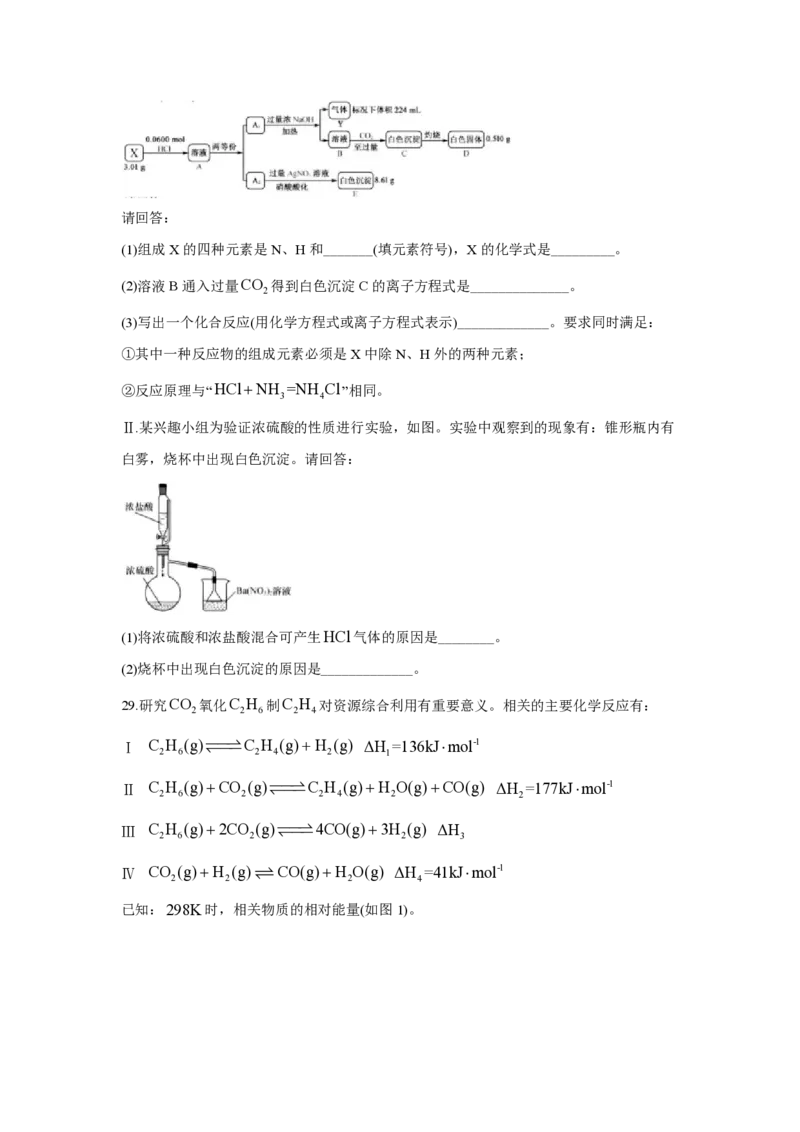
28.Ⅰ.化合物Ⅹ由四种短周期元素组成,加热X,可产生使湿润的红色石蕊试纸变蓝的气体
Y,Y为纯净物;取3.01gX,用含HCl 0.0600 mol的盐酸完全溶解得溶液A,将溶液A
分成A 和A 两等份,完成如下实验(白色沉淀C可溶于NaOH溶液):
1 2请回答:
(1)组成X的四种元素是N、H和_______(填元素符号),X的化学式是_________。
(2)溶液B通入过量CO 得到白色沉淀C的离子方程式是______________。
2
(3)写出一个化合反应(用化学方程式或离子方程式表示)_____________。要求同时满足:
①其中一种反应物的组成元素必须是X中除N、H外的两种元素;
②反应原理与“HClNH =NH Cl”相同。
3 4
Ⅱ.某兴趣小组为验证浓硫酸的性质进行实验,如图。实验中观察到的现象有:锥形瓶内有
白雾,烧杯中出现白色沉淀。请回答:
(1)将浓硫酸和浓盐酸混合可产生HCl气体的原因是________。
(2)烧杯中出现白色沉淀的原因是_____________。
29.研究CO 氧化C H 制C H 对资源综合利用有重要意义。相关的主要化学反应有:
2 2 6 2 4
Ⅰ C H (g)C H (g)H (g) ΔH =136kJmol-1
2 6 2 4 2 1
Ⅱ C H (g)CO (g)C H (g)H O(g)CO(g) ΔH =177kJmol-1
2 6 2 2 4 2 2
Ⅲ C H (g)2CO (g)4CO(g)3H (g) ΔH
2 6 2 2 3
Ⅳ CO 2 (g)H 2 (g) CO(g)H 2 O(g) ΔH 4 =41kJmol-1
已知:298K时,相关物质的相对能量(如图1)。可根据相关物质的相对能量计算反应或变化的ΔH (ΔH 随温度变化可忽略)。例如:
H O(g) H O(1) ΔH=-286kJmol-1- -242kJmol-1 =-44kJmol-1。
2 2
请回答:
(1)①根据相关物质的相对能量计算ΔH =_____kJmol1。
3
②下列描述正确的是_____
A 升高温度反应Ⅰ的平衡常数增大
B 加压有利于反应Ⅰ、Ⅱ的平衡正向移动
C 反应Ⅲ有助于乙烷脱氢,有利于乙烯生成
D 恒温恒压下通水蒸气,反应Ⅳ的平衡逆向移动
③有研究表明,在催化剂存在下,反应Ⅱ分两步进行,过程如下:【C H (g)CO (g)】
2 6 2
【C H (g)H (g)CO (g)】【C H (g)CO(g)H O(g)】,且第二步速率较慢
2 4 2 2 2 4 2
(反应活化能为210kJmol1)。根据相关物质的相对能量,画出反应Ⅱ分两步进行的“能量
-反应过程图”,起点从【C H (g)CO (g)】的能量477kJmol1,开始(如图2)_____
2 6 2
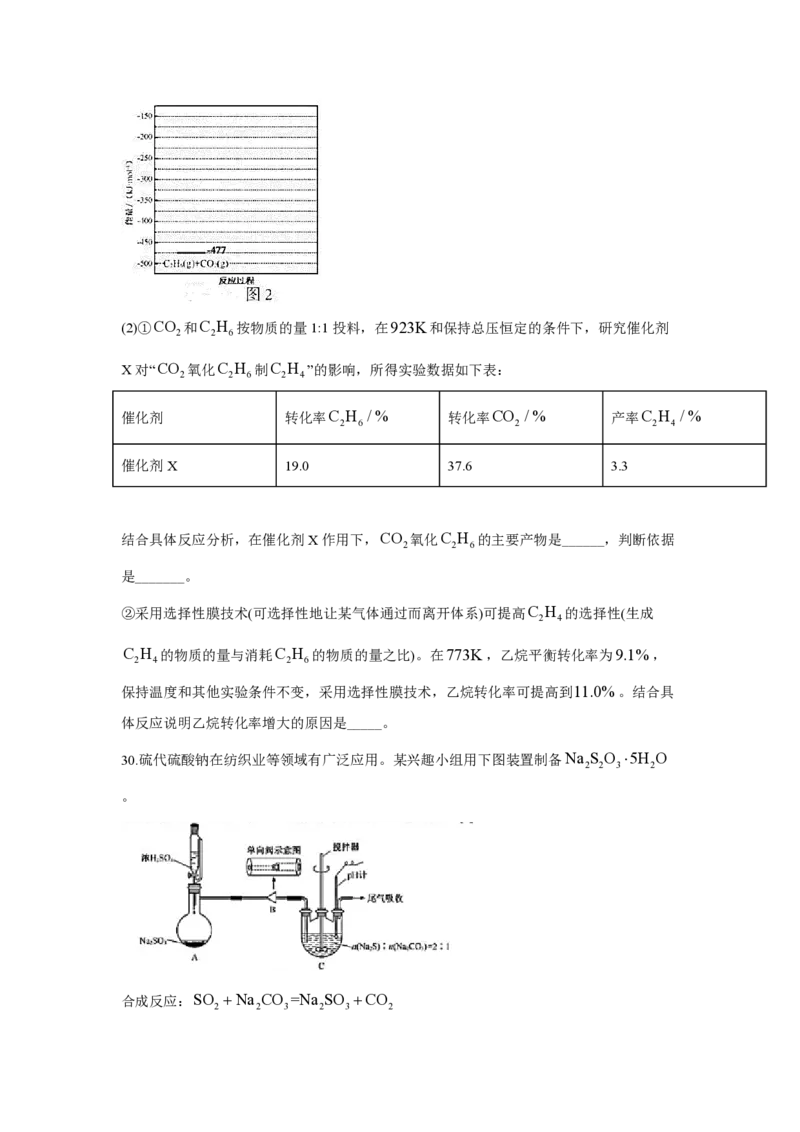
。(2)①CO 和C H 按物质的量1:1投料,在923K和保持总压恒定的条件下,研究催化剂
2 2 6
X对“CO 氧化C H 制C H ”的影响,所得实验数据如下表:
2 2 6 2 4
催化剂 转化率C H /% 转化率CO /% 产率C H /%
2 6 2 2 4
催化剂X 19.0 37.6 3.3
结合具体反应分析,在催化剂X作用下,CO 氧化C H 的主要产物是______,判断依据
2 2 6
是_______。
②采用选择性膜技术(可选择性地让某气体通过而离开体系)可提高C H 的选择性(生成
2 4
C H 的物质的量与消耗C H 的物质的量之比)。在773K,乙烷平衡转化率为9.1%,
2 4 2 6
保持温度和其他实验条件不变,采用选择性膜技术,乙烷转化率可提高到11.0%。结合具
体反应说明乙烷转化率增大的原因是_____。
30.硫代硫酸钠在纺织业等领域有广泛应用。某兴趣小组用下图装置制备Na S O 5H O
2 2 3 2
。
合成反应:SO Na CO =Na SO CO
2 2 3 2 3 22Na S3SO =2Na SO 3S Na SO S Δ Na S O
2 2 2 3 2 3 2 2 3
滴定反应:I 2Na S O 2NaINa S O
2 2 2 3 2 4 6
已知:Na S O 5H O易溶于水,难溶于乙醇,50℃开始失结晶水。
2 2 3 2
实验步骤:
Ⅰ.Na S O 制备:装置A制备的SO 经过单向阀通入装置C中的混合溶液,加热、搅
2 2 3 2
拌,至溶液pH约为7时,停止通入SO 气体,得产品混合溶液。
2
Ⅱ.产品分离提纯:产品混合溶液经蒸发浓缩、冷却结晶、过滤洗涤、干燥,得到
Na S O 5H O产品。
2 2 3 2
Ⅲ.产品纯度测定:以淀粉作指示剂,用Na S O 5H O产品配制的溶液滴定碘标准溶液
2 2 3 2
至滴定终点,计算Na S O 5H O含量。
2 2 3 2
请回答:
(1)步骤Ⅰ:单向阀的作用是______;装置C中的反应混合溶液pH过高或过低将导致产率降
低,原因是_______。
(2)步骤Ⅱ:下列说法正确的是_____。
A 快速蒸发溶液中水分,可得较大晶体颗粒
B 蒸发浓缩至溶液表面出现品晶膜时,停止加热
C 冷却结晶后的固液混合物中加入乙醇可提高产率
D 可选用冷的Na CO 溶液作洗涤剂
2 3
(3)步骤Ⅲ
①滴定前,有关滴定管的正确操作为(选出正确操作并按序排列):
检漏→蒸馏水洗涤→( )→( )→( )→( )→( )→
开始滴定。
A 烘干 B 装入滴定液至零刻度以上 C 调整滴定液液面至零刻度或零刻度以下D 用洗耳
球吹出润洗液 E 排除气泡 F 用滴定液润洗2至3次 G 记录起始读数
②装标准碘溶液的碘量瓶(带瓶塞的锥形瓶)在滴定前应盖上瓶塞,目的是______。
③滴定法测得产品中Na S O 5H O含量为100.5%,则Na S O 5H O产品中可能混
2 2 3 2 2 2 3 2有的物质是________。
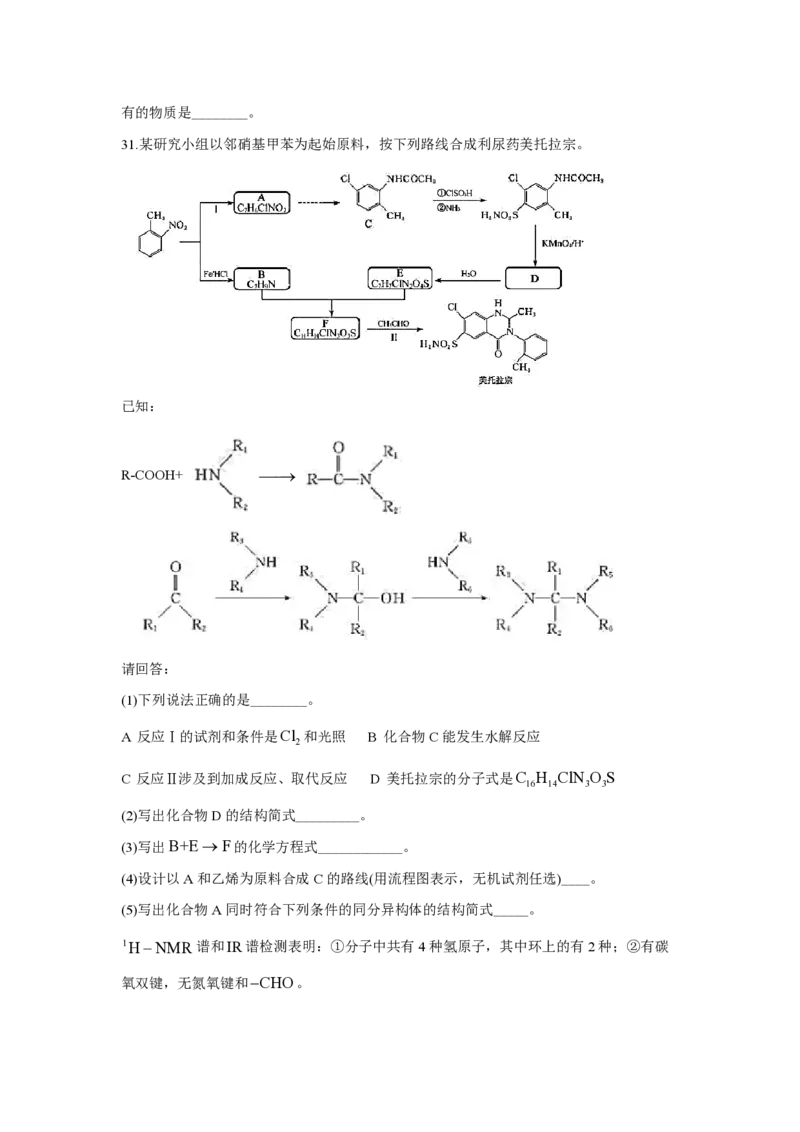
31.某研究小组以邻硝基甲苯为起始原料,按下列路线合成利尿药美托拉宗。
已知:
R-COOH+
请回答:
(1)下列说法正确的是________。
A 反应Ⅰ的试剂和条件是Cl 和光照 B 化合物C能发生水解反应
2
C 反应Ⅱ涉及到加成反应、取代反应 D 美托拉宗的分子式是C H ClN O S
16 14 3 3
(2)写出化合物D的结构简式_________。
(3)写出B+E F的化学方程式____________。
(4)设计以A和乙烯为原料合成C的路线(用流程图表示,无机试剂任选)____。
(5)写出化合物A同时符合下列条件的同分异构体的结构简式_____。
1HNMR 谱和IR谱检测表明:①分子中共有4种氢原子,其中环上的有2种;②有碳
氧双键,无氮氧键和CHO。