文档内容
2021年全国卷甲卷理综化学试卷
7.化学与人体健康及环境保护息息相关,下列叙述正确的是:
A. 食品加工时不可添加任何防腐剂。
B. 掩埋废旧电池不会造成环境污染。
C. 天然气不完全燃烧,会产生有毒气体
D. 使用含磷洗涤剂不会造成水体污染
8.N 为阿伏加德罗常数的值。下列叙述正确的是:
A
A. 8g重水(DO)中含有质子数为 10N
2 A
B.3mol的 NO与HO 完全反应转移的电子数为4N
2 2 A
C. 2g环状 S( )分子中含有S-S键数为 1N
8 A
D.1L pH 值等于4 的0.1mol/L的 KCrO溶液中含有 CrO 数为2- 0.1N
2 2 7 2 7 A
9.实验室制备下列气体的方法可行的是
气体 方法
A 氨气 加热氯化氨固体
B 二氧化氮 将铝片加到冷浓硝酸中
C 硫化氢 向硫化钠固体滴加浓硫酸
D 氧气 加热氯酸钾和二氧化锰的混合物
10.下列叙述正确的是
A. 甲醇既可以发生取代反应,也可以发生加成反应
B. 用饱和碳酸氢钠溶液可以鉴别乙酸和乙醇
C. 烷烃的沸点高低仅取决于碳原子数的多少
D. 戊二烯与环戊烷互为同分异构体。
11. W、X、Y、Z 为原子序数依次增大的短周期主族元素,Z 的最外层电子数是 W 和 X 的最外层电子数之
和,也是Y的最外层电子数的2倍。W和X的单质常温下均为气体。下列叙述正确的是
A. 原子半径Z>X>W
B. W与X只能形成一种化合物
C. Y的氧化物为碱性氧化物,不与强碱反应
D. W、X和Z可形成既含离子键又含有共价键的化合物
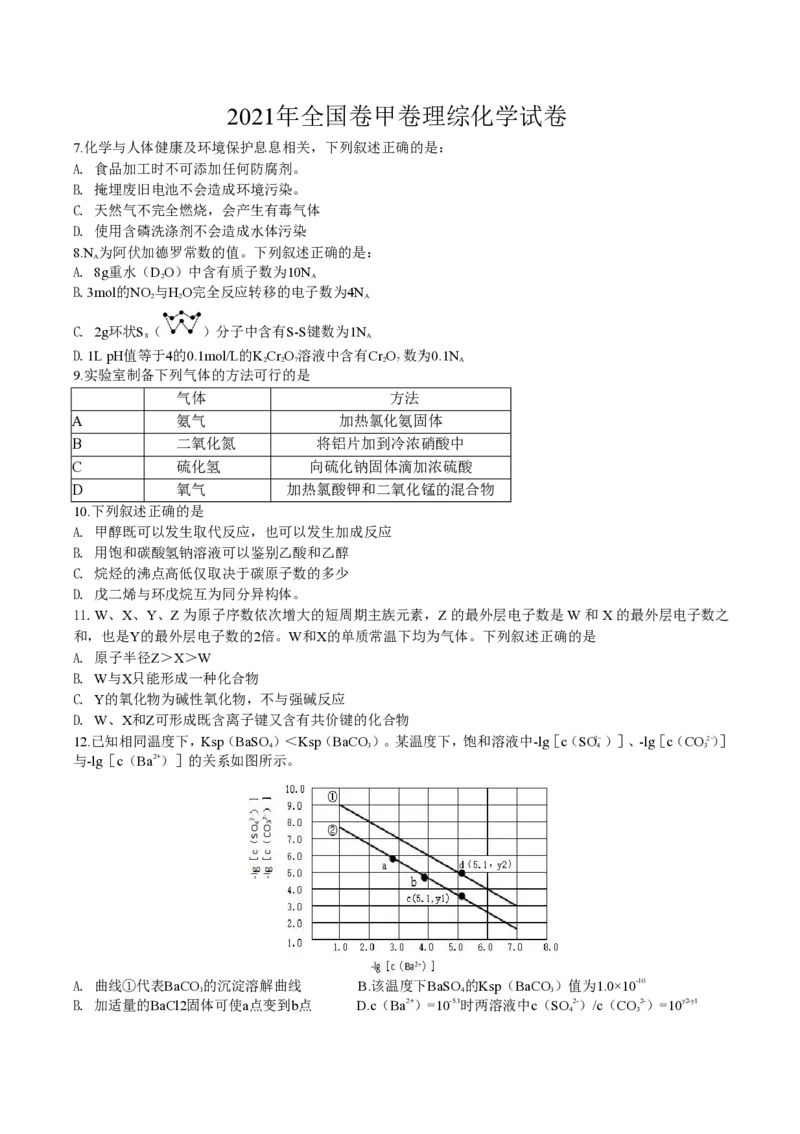
12.已知相同温度下,Ksp(BaSO)<Ksp(BaCO)。某温度下,饱和溶液中-lg[c(SO2-)]、-lg[c(CO2-)]
4 3 4 3
与-lg[c(Ba2+)]的关系如图所示。
A. 曲线①代表 BaCO的沉淀溶解曲线 B.该温度下 BaSO的Ksp(BaCO)值为1.0×10-10
3 4 3
B. 加适量的 BaCl2固体可使 a 点变到b 点 D.c(Ba2+)=10-5.1 时两溶液中c(SO2-)/c(CO2-)=10y2-y1
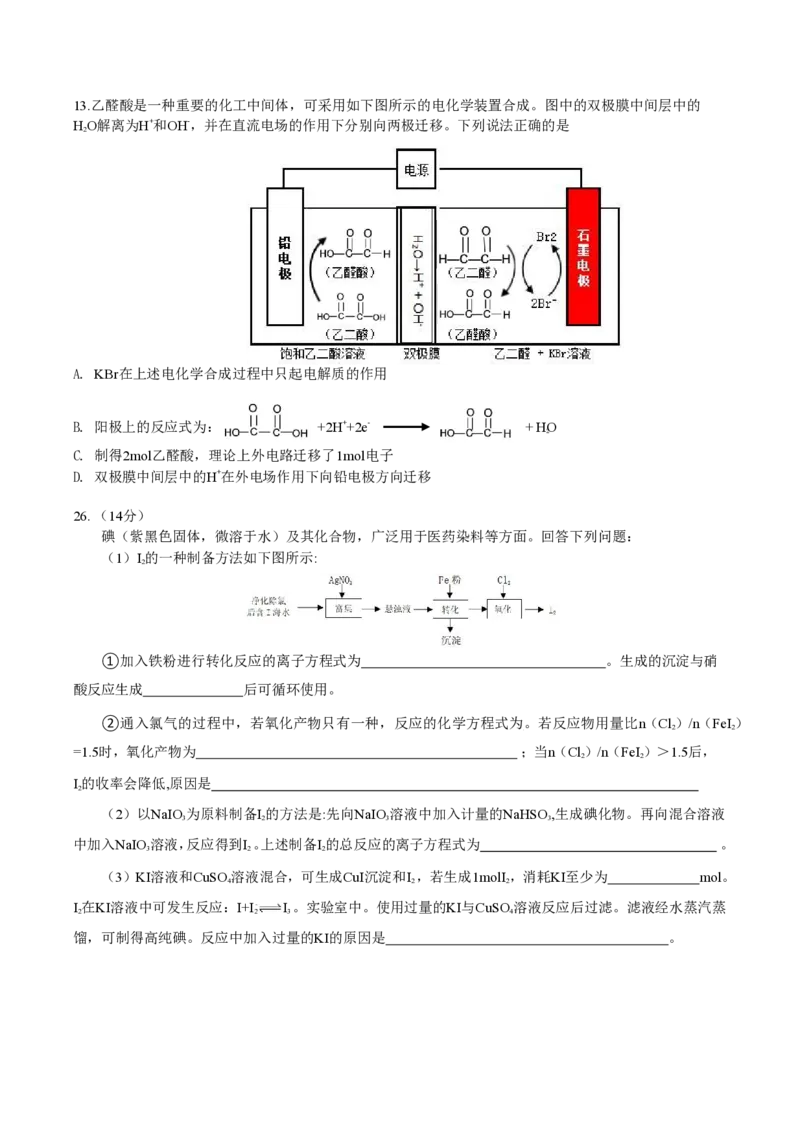
4 313.乙醛酸是一种重要的化工中间体,可采用如下图所示的电化学装置合成。图中的双极膜中间层中的
HO解离为H+和OH-,并在直流电场的作用下分别向两极迁移。下列说法正确的是
2
A. KBr在上述电化学合成过程中只起电解质的作用
B. 阳极上的反应式为: +2H++2e- + HO
2
C. 制得2mol乙醛酸,理论上外电路迁移了1mol电子
D. 双极膜中间层中的 H+在外电场作用下向铅电极方向迁移
26. (14分)
碘(紫黑色固体,微溶于水)及其化合物,广泛用于医药染料等方面。回答下列问题:
(1)I的一种制备方法如下图所示:
2
①加入铁粉进行转化反应的离子方程式为 。生成的沉淀与硝
酸反应生成 后可循环使用。
②通入氯气的过程中,若氧化产物只有一种,反应的化学方程式为 。若反应物用量比 n(Cl)/n(FeI)
2 2
=1.5时,氧化产物为 ;当n(Cl)/n(FeI)>1.5后,
2 2
I的收率会降低,原因是
2
(2)以 NaIO为原料制备 I的方法是:先向 NaIO溶液中加入计量的 NaHSO,生成碘化物。再向混合溶液
3 2 3 3
中加入 NaIO溶液,反应得到I 。上述制备 I的总反应的离子方程式为 。
3 2 2
(3)KI溶液和 CuSO溶液混合,可生成CuI 沉淀和I ,若生成 1molI,消耗KI 至少为 mol。
4 2 2
I在 KI溶液中可发生反应:I+I- I 。实-验室中。使用过量的 KI与CuSO溶液反应后过滤。滤液经水蒸汽蒸
2 2 3 4
馏,可制得高纯碘。反应中加入过量的KI的原因是 。27. (15分)
胆矾(CuSO·5HO)易溶于水,难溶于乙醇。某小组用工业废铜培烧得到的 CuO(杂质为氧化铁及泥沙)
4 2
为原料与稀硫酸反应制备胆矾,并测定其结晶水的含量。回答下列问题:
(1)制备胆矾时,用到的实验仪器除量筒、酒精灯、玻璃棒、漏斗外,还必须使用的仪器有 (填
标号)
A.烧杯 B.容量瓶 C.蒸发皿 D.移液管
(2)将CuO加入到适量稀硫酸中,加热,其主要反应的化学方程式为 。
与直接用废铜和浓硫酸反应相比,该方法的优点是 。
(3)待 CuO 完全反应后停止加热,冷却后过滤,滤液经如下实验操作:加热蒸发、冷却结晶、 、
乙醇洗涤、 ,得到胆矾。其中,控制溶液pH值为3.5~4的目的是 。
煮沸 10min的作用是 。
28.(14分)
二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。回答下列问题:
(1)二氧化碳加氢制甲醇的总反应可表示为:
CO(g)+3H=CHOH(g)+HO(g)
2 2 3 2
该反应一般认为通过如下步骤来实现:
① CO(g)+H=CO(g)+HO(g) △H=+41kJ/mol
2 2 2 1
② CO(g)+2H=CHOH(g) △H=-90kJ/mol
2 3 2
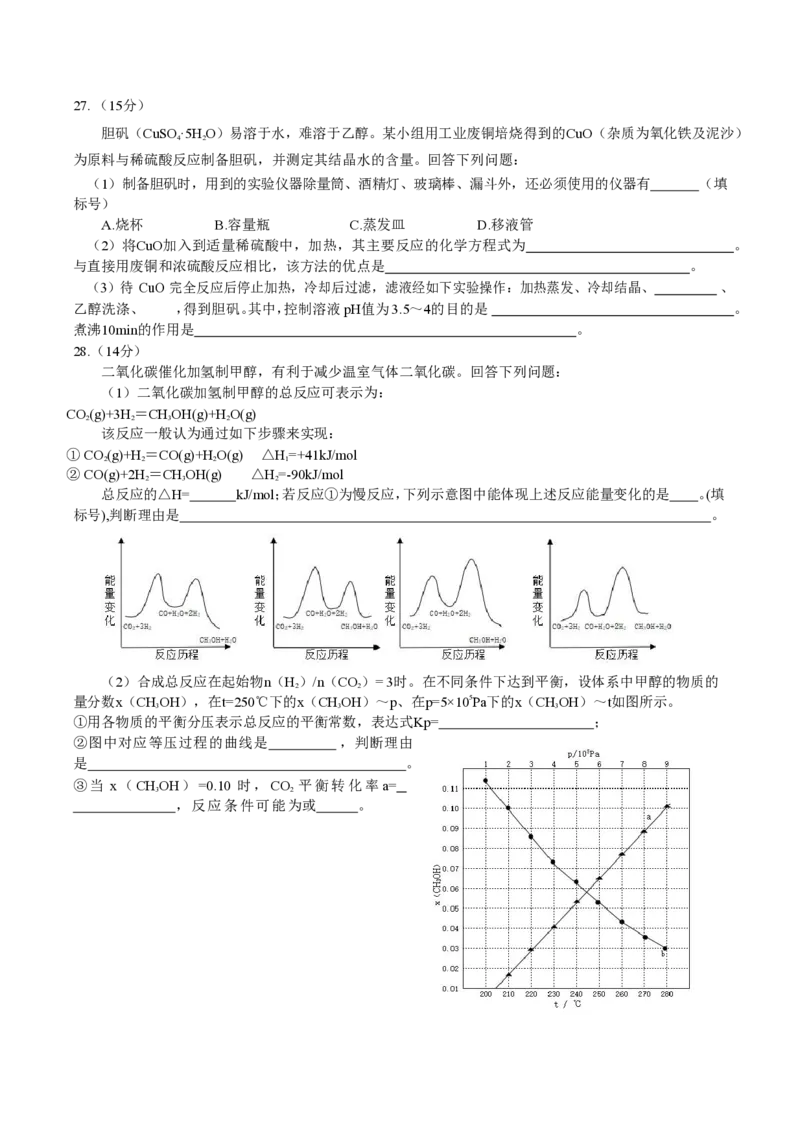
总反应的△H= kJ/mol;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是 。(填
标号),判断理由是 。
(2)合成总反应在起始物 n(H)/n(CO)= 3 时。在不同条件下达到平衡,设体系中甲醇的物质的
2 2
量分数x(CHOH),在 t=250℃下的 x(CHOH)~p、在 p=5×105Pa 下的 x(CHOH)~t如图所示。
3 3 3
①用各物质的平衡分压表示总反应的平衡常数,表达式Kp= ;
②图中对应等压过程的曲线是 ,判断理由
是 。
③ 当 x ( CHOH ) =0.10 时 , CO 平 衡 转 化 率 a=
3 2
, 反 应 条 件 可 能 为或 。36.[化学---选修五:有机化学基础](15分)
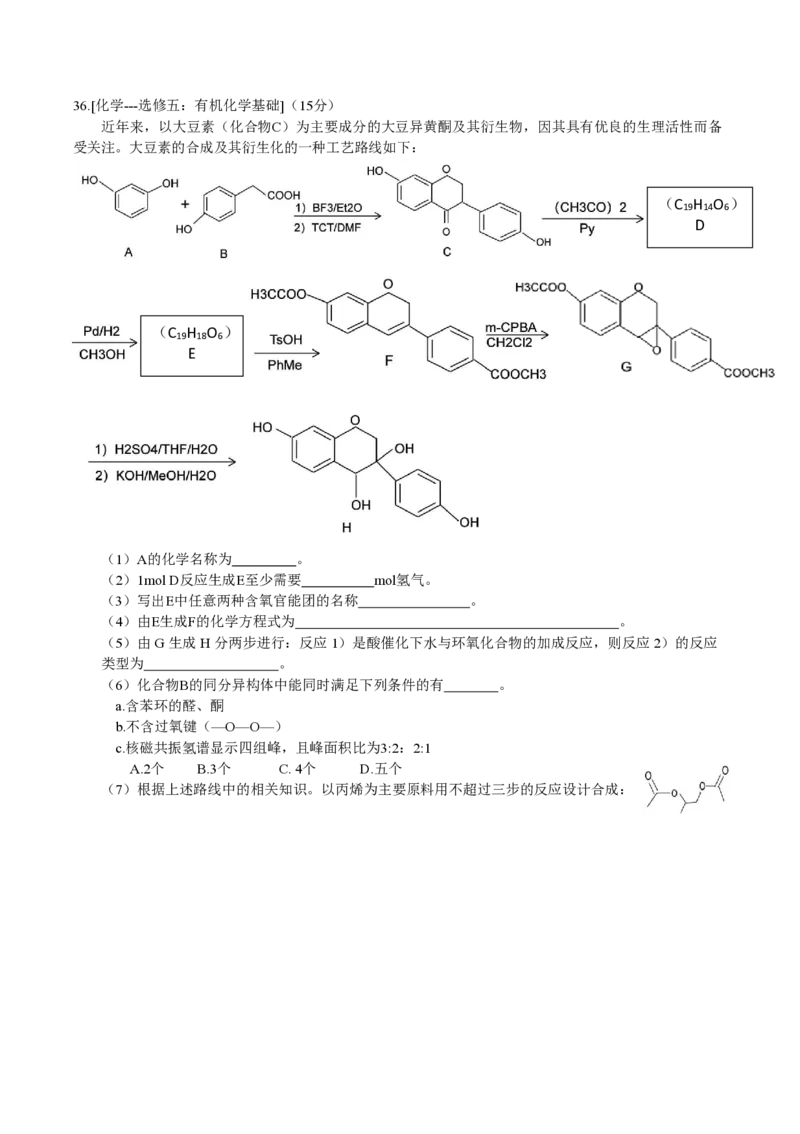
近年来,以大豆素(化合物 C)为主要成分的大豆异黄酮及其衍生物,因其具有优良的生理活性而备
受关注。大豆素的合成及其衍生化的一种工艺路线如下:
(C H O )
19 14 6
D
(C H O )
19 18 6
E
(1)A的化学名称为 。
(2)1mol D反应生成 E至少需要 mol氢气。
(3)写出E中任意两种含氧官能团的名称 。
(4)由 E生成F的化学方程式为 。
(5)由 G 生成 H 分两步进行:反应 1)是酸催化下水与环氧化合物的加成反应,则反应 2)的反应
类型为 。
(6)化合物B的同分异构体中能同时满足下列条件的有 。
a.含苯环的醛、酮
b.不含过氧键(—O—O—)
c.核磁共振氢谱显示四组峰,且峰面积比为3:2:2:1
A.2个 B.3个 C. 4个 D.五个
(7)根据上述路线中的相关知识。以丙烯为主要原料用不超过三步的反应设计合成: