文档内容
江苏省 2021 年普通高中学业水平选择性考试
化学
注意事项:
1.本试卷满分为100分,考试时间为75分钟。考试结束后,请将本试卷和答题卡一并交回。
2.答题前,请务必将自己的姓名、准考证号用0.5毫米黑色墨水的签字笔填写在试卷及答题卡
的规定位置。
3.请认真核对监考员在答题卡上所粘贴的条形码上的姓名、准考证号与本人是否相符。
4.作答选择题,必须用2B铅笔将答题卡上对应选项的方框涂满、涂黑;如需改动,请用橡皮
擦干净后,再选涂其他答案。作答非选择题,必须用0.5毫米黑色墨水的签字笔在答题卡上
的指定位置作答,在其他位置作答一律无效。
5.如需作图,必须用2B铅笔绘写清楚,线条符号等须加黑加粗。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 C1-35.5 Mn-55
Fe-56 Zn-65
一、单项选择题:共14题,每题3分,共42分。每题只有一个选项最符合题意。
1. 黑火药是中国古代四大发明之一,其爆炸反应为2KNO+S+3C=KS+N↑+3CO ↑。下列说法正确的是
3 2 2 2
A. 黑火药中含有两种单质 B. 爆炸时吸收热量
C. 反应中S作还原剂 D. 反应为置换反应
2. 反应Cl+2NaOH=NaClO+NaCl+H O可用于制备含氯消毒剂。下列说法正确的是
2 2
A. Cl 是极性分子
2
B. NaOH的电子式为
C. NaClO既含离子键又含共价键
D. Cl-与Na+具有相同的电子层结构
3. 下列由废铜屑制取CuSO ·5HO的实验原理与装置不能达到实验目的的是
4 2
A. 用装置甲除去废铜屑表面的油污 B. 用装置乙在加热的条件下溶解废铜屑
C. 用装置丙过滤得到CuSO 溶液 D. 用装置丁蒸干溶液获得CuSO ·5HO
4 4 24. 下列有关物质的性质与用途不具有对应关系的是
A. 铁粉能与O 反应,可用作食品保存的吸氧剂
2
B. 纳米Fe O 能与酸反应,可用作铁磁性材料
3 4
C. FeCl 具有氧化性,可用于腐蚀印刷电路板上的Cu
3
D. 聚合硫酸铁能水解并形成胶体,可用于净水
5. 前4周期主族元素X、Y、Z、W的原子序数依次增大,X是空气中含量最多的元素,Y的周期序数与族
序数相等,基态时Z原子3p原子轨道上有5个电子,W与Z处于同个主族。下列说法正确的是
.
A 原子半径:r(X)
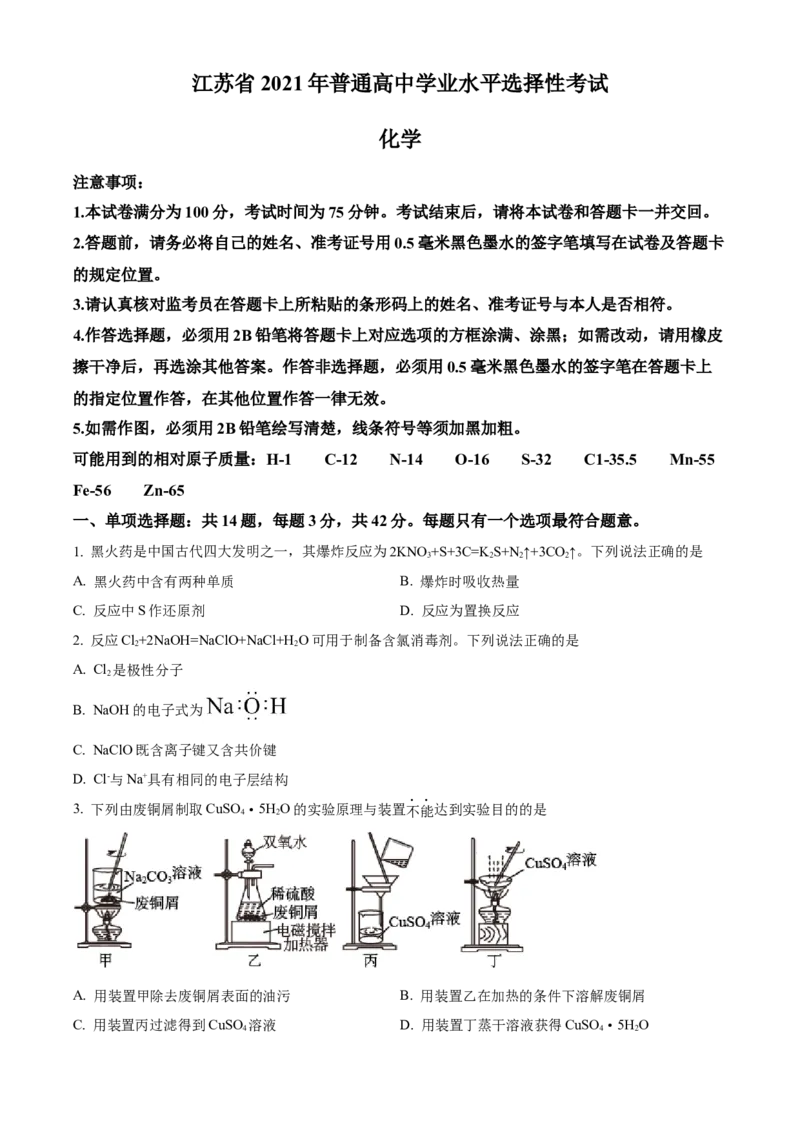
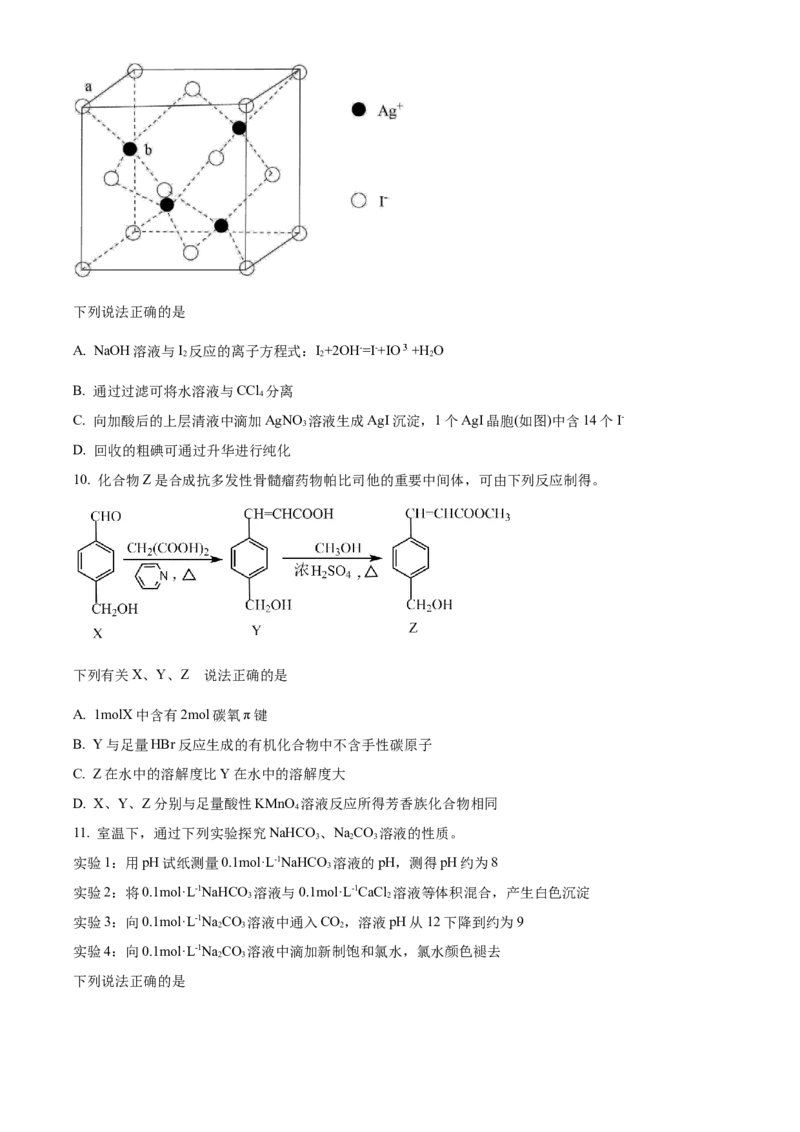
a2 2 3
B. 实验2中两溶液混合时有:c(Ca2+)·c(CO ) ×104
4 3C. 过滤后所得清液中一定存在:c(Ca2+)= 且c(Ca2+)≤
D. 滤渣中加入醋酸发生反应的离子方程式:CaCO +2H+=Ca2++CO ↑+H O
3 2 2
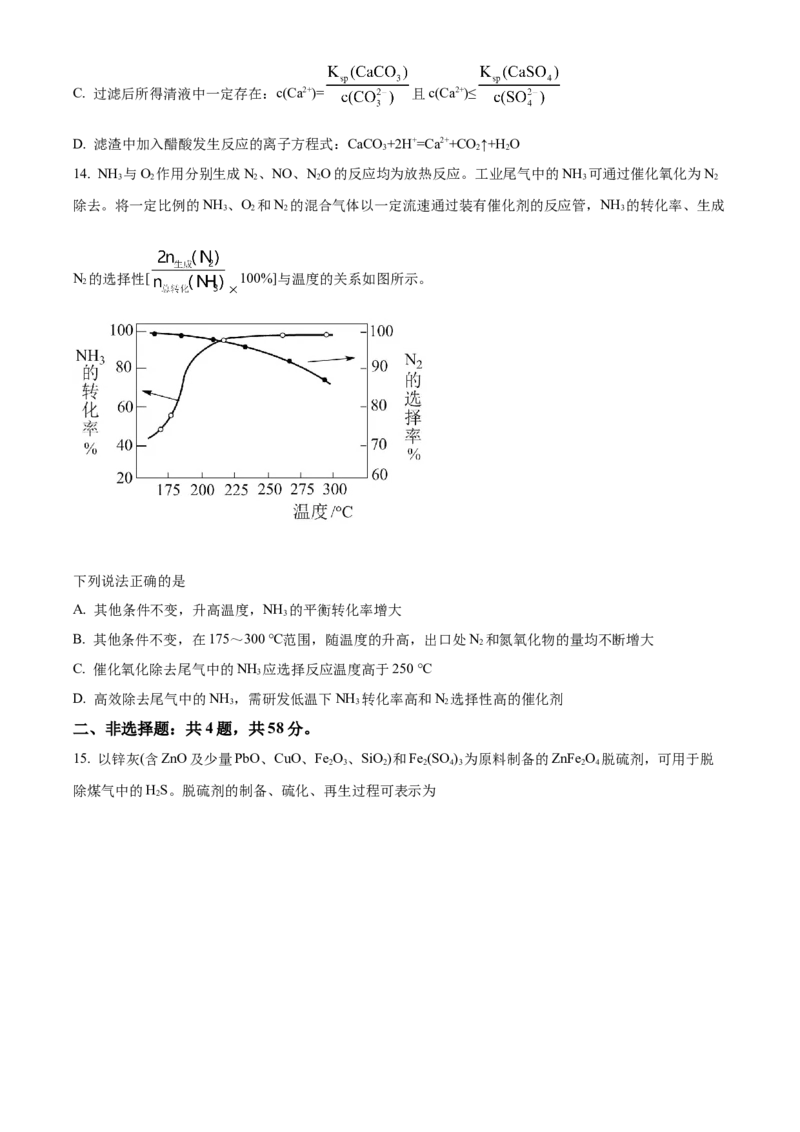
14. NH 与O 作用分别生成N、NO、NO的反应均为放热反应。工业尾气中的NH 可通过催化氧化为N
3 2 2 2 3 2
除去。将一定比例的NH 、O 和N 的混合气体以一定流速通过装有催化剂的反应管,NH 的转化率、生成
3 2 2 3
N 的选择性[ 100%]与温度的关系如图所示。
2
下列说法正确的是
A. 其他条件不变,升高温度,NH 的平衡转化率增大
3
B. 其他条件不变,在175~300 ℃范围,随温度的升高,出口处N 和氮氧化物的量均不断增大
2
C. 催化氧化除去尾气中的NH 应选择反应温度高于250 ℃
3
D. 高效除去尾气中的NH ,需研发低温下NH 转化率高和N 选择性高的催化剂
3 3 2
二、非选择题:共4题,共58分。
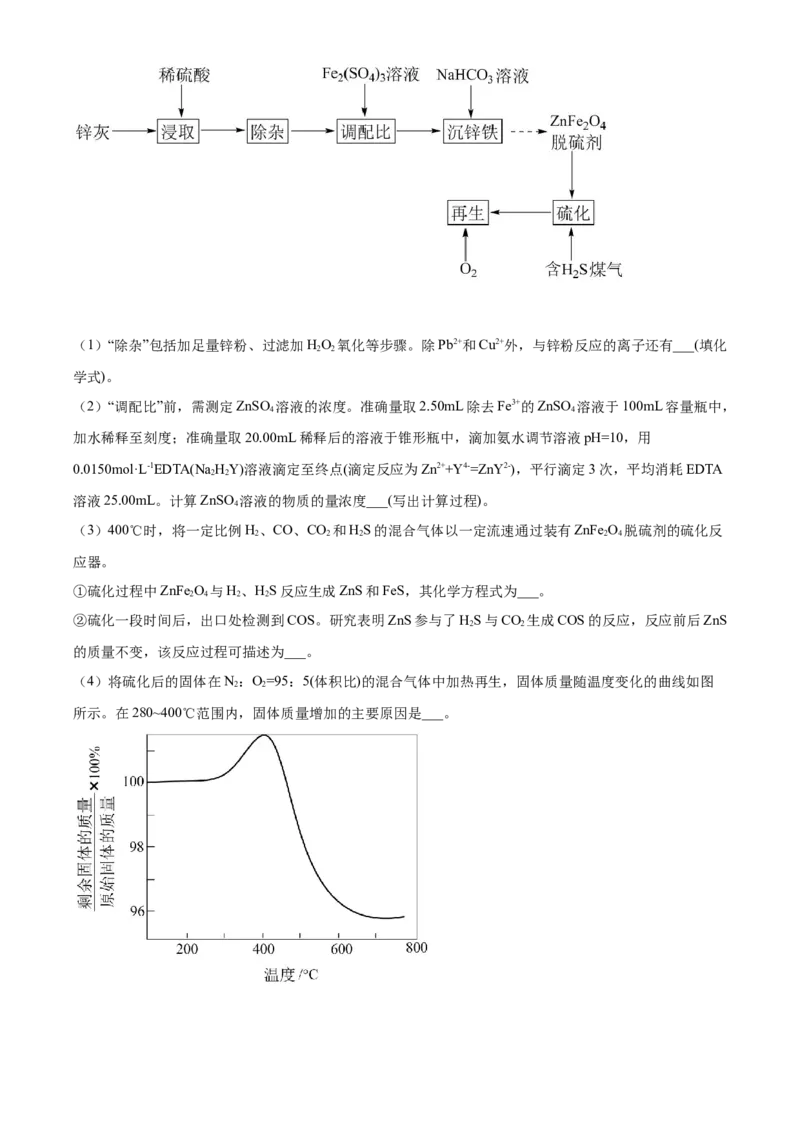
15. 以锌灰(含ZnO及少量PbO、CuO、Fe O、SiO)和Fe (SO ) 为原料制备的ZnFe O 脱硫剂,可用于脱
2 3 2 2 4 3 2 4
除煤气中的HS。脱硫剂的制备、硫化、再生过程可表示为
2(1)“除杂”包括加足量锌粉、过滤加HO 氧化等步骤。除Pb2+和Cu2+外,与锌粉反应的离子还有___(填化
2 2
学式)。
(2)“调配比”前,需测定ZnSO 溶液的浓度。准确量取2.50mL除去Fe3+的ZnSO 溶液于100mL容量瓶中,
4 4
加水稀释至刻度;准确量取20.00mL稀释后的溶液于锥形瓶中,滴加氨水调节溶液pH=10,用
0.0150mol·L-1EDTA(Na HY)溶液滴定至终点(滴定反应为Zn2++Y4-=ZnY2-),平行滴定3次,平均消耗EDTA
2 2
溶液25.00mL。计算ZnSO 溶液的物质的量浓度___(写出计算过程)。
4
(3)400℃时,将一定比例H、CO、CO 和HS的混合气体以一定流速通过装有ZnFe O 脱硫剂的硫化反
2 2 2 2 4
应器。
①硫化过程中ZnFe O 与H、HS反应生成ZnS和FeS,其化学方程式为___。
2 4 2 2
②硫化一段时间后,出口处检测到COS。研究表明ZnS参与了HS与CO 生成COS的反应,反应前后ZnS
2 2
的质量不变,该反应过程可描述为___。
(4)将硫化后的固体在N:O=95:5(体积比)的混合气体中加热再生,固体质量随温度变化的曲线如图
2 2
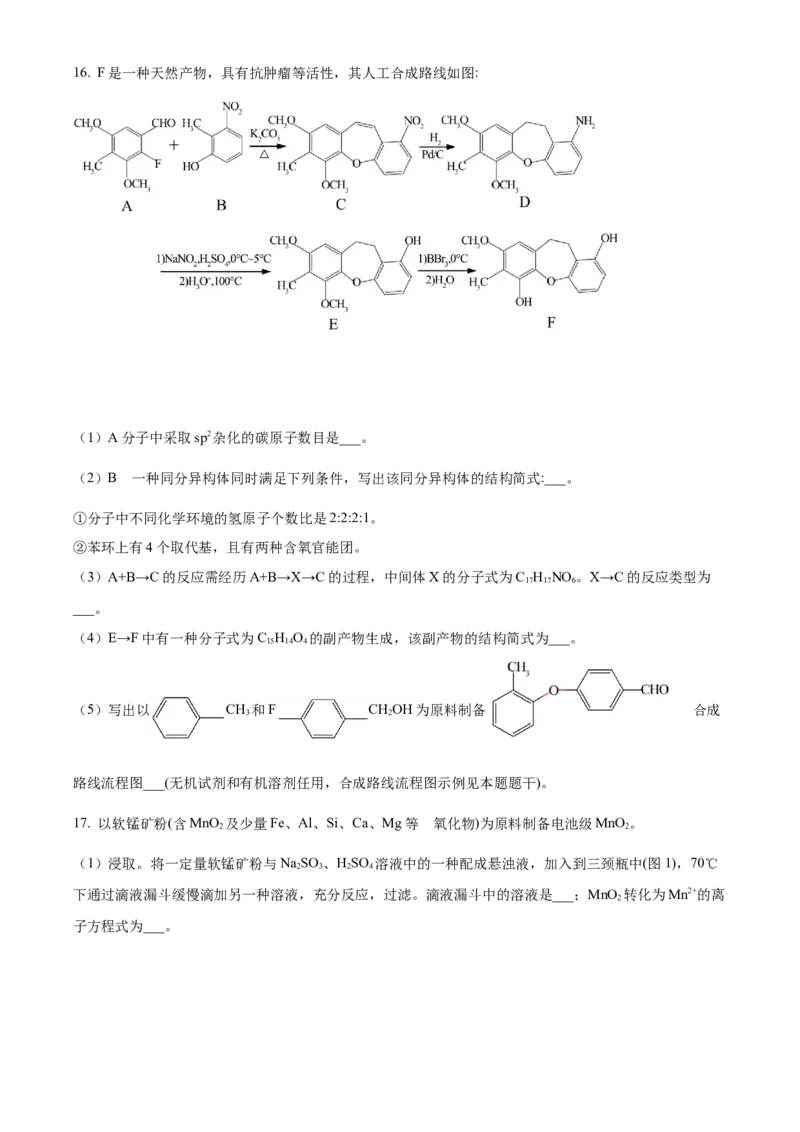
所示。在280~400℃范围内,固体质量增加的主要原因是___。16. F是一种天然产物,具有抗肿瘤等活性,其人工合成路线如图:
(1)A分子中采取sp2杂化的碳原子数目是___。
的
(2)B 一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:___。
①分子中不同化学环境的氢原子个数比是2:2:2:1。
②苯环上有4个取代基,且有两种含氧官能团。
(3)A+B→C的反应需经历A+B→X→C的过程,中间体X的分子式为C H NO 。X→C的反应类型为
17 17 6
___。
(4)E→F中有一种分子式为C H O 的副产物生成,该副产物的结构简式为___。
15 14 4
(5)写出以 CH 和F CHOH为原料制备 合成
3 2
的
路线流程图___(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
的
17. 以软锰矿粉(含MnO 及少量Fe、Al、Si、Ca、Mg等 氧化物)为原料制备电池级MnO 。
2 2
(1)浸取。将一定量软锰矿粉与NaSO 、HSO 溶液中的一种配成悬浊液,加入到三颈瓶中(图1),70℃
2 3 2 4
下通过滴液漏斗缓慢滴加另一种溶液,充分反应,过滤。滴液漏斗中的溶液是___;MnO 转化为Mn2+的离
2
子方程式为___。(2)除杂。向已经除去Fe、Al、Si的MnSO 溶液(pH约为5)中加入NH F溶液,溶液中的Ca2+、Mg2+形成
4 4
氟化物沉淀。若沉淀后上层清液中c(F-)=0.05mol·L-1,则 =___。[K (MgF )=5×10-11,
sp 2
K (CaF )=5×10-9]
sp 2
(3)制备MnCO 。在搅拌下向100mL1mol·L-1MnSO 溶液中缓慢滴加1mol·L-1NH HCO 溶液,过滤、洗涤、
3 4 4 3
干燥,得到MnCO 固体。需加入NH HCO 溶液的体积约为___。
3 4 3
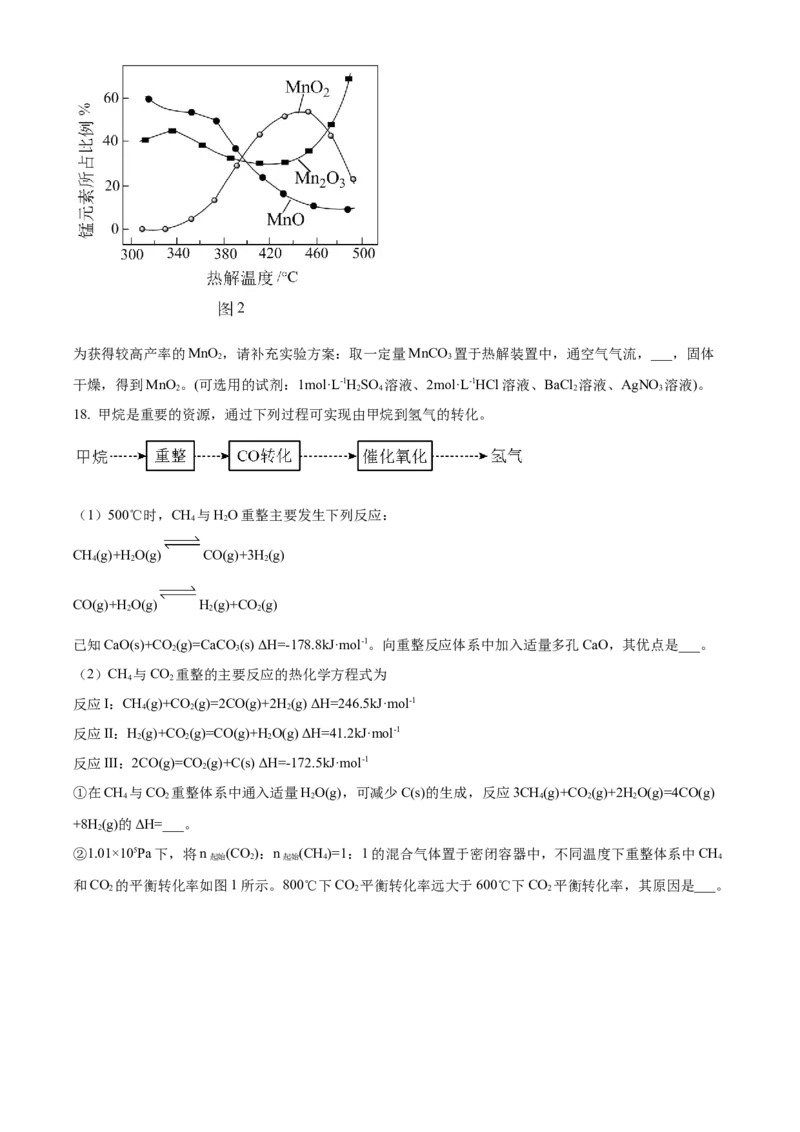
(4)制备MnO 。MnCO 经热解、酸浸等步骤可制备MnO 。MnCO 在空气气流中热解得到三种价态锰的
2 3 2 3
氧化物,锰元素所占比例( ×100%)随热解温度变化的曲线如图2所示。
已知:MnO与酸反应生成Mn2+;MnO 氧化性强于Cl,加热条件下MnO 在酸性溶液中转化为MnO 和
2 3 2 2 3 2
Mn2+。为获得较高产率的MnO ,请补充实验方案:取一定量MnCO 置于热解装置中,通空气气流,___,固体
2 3
干燥,得到MnO 。(可选用的试剂:1mol·L-1HSO 溶液、2mol·L-1HCl溶液、BaCl 溶液、AgNO 溶液)。
2 2 4 2 3
18. 甲烷是重要的资源,通过下列过程可实现由甲烷到氢气的转化。
(1)500℃时,CH 与HO重整主要发生下列反应:
4 2
CH(g)+HO(g) CO(g)+3H(g)
4 2 2
CO(g)+HO(g) H(g)+CO (g)
2 2 2
已知CaO(s)+CO (g)=CaCO (s) ΔH=-178.8kJ·mol-1。向重整反应体系中加入适量多孔CaO,其优点是___。
2 3
(2)CH 与CO 重整的主要反应的热化学方程式为
4 2
反应I:CH(g)+CO (g)=2CO(g)+2H(g) ΔH=246.5kJ·mol-1
4 2 2
反应II:H(g)+CO (g)=CO(g)+HO(g) ΔH=41.2kJ·mol-1
2 2 2
反应III:2CO(g)=CO(g)+C(s) ΔH=-172.5kJ·mol-1
2
①在CH 与CO 重整体系中通入适量HO(g),可减少C(s)的生成,反应3CH(g)+CO (g)+2HO(g)=4CO(g)
4 2 2 4 2 2
+8H (g)的ΔH=___。
2
②1.01×105Pa下,将n (CO):n (CH)=1:1的混合气体置于密闭容器中,不同温度下重整体系中CH
起始 2 起始 4 4
和CO 的平衡转化率如图1所示。800℃下CO 平衡转化率远大于600℃下CO 平衡转化率,其原因是___。
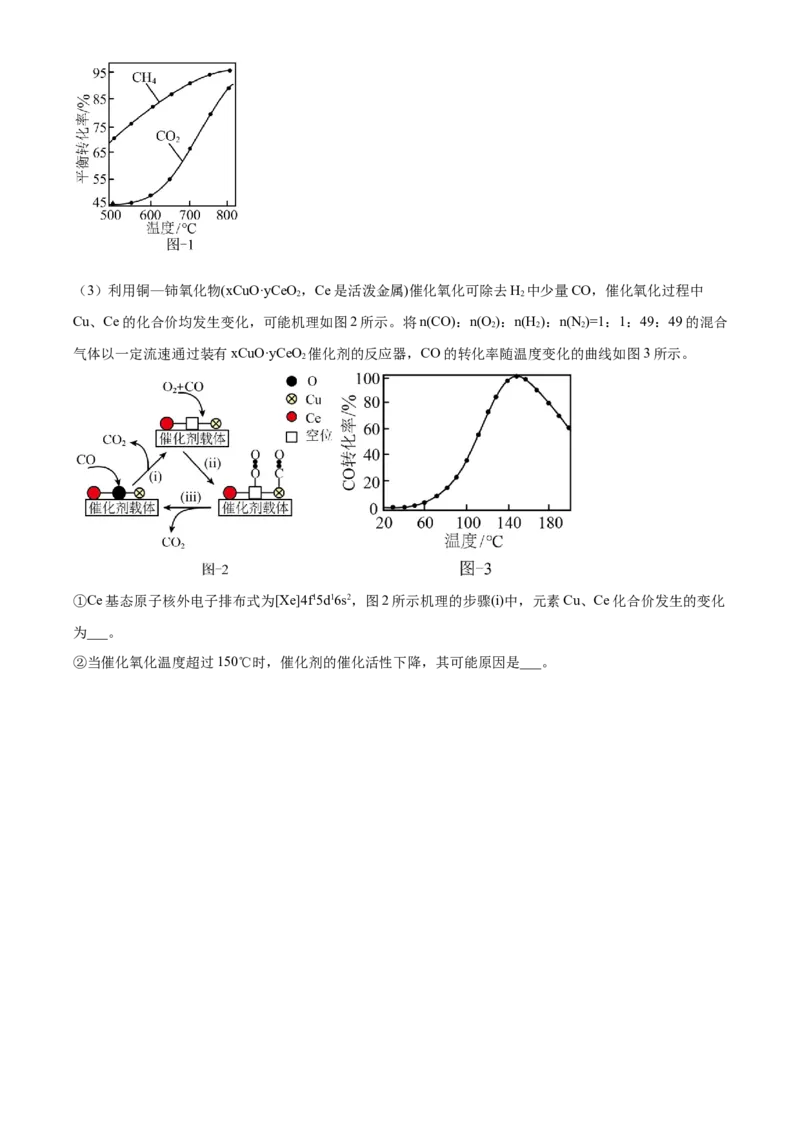
2 2 2(3)利用铜—铈氧化物(xCuO·yCeO ,Ce是活泼金属)催化氧化可除去H 中少量CO,催化氧化过程中
2 2
Cu、Ce的化合价均发生变化,可能机理如图2所示。将n(CO):n(O ):n(H ):n(N )=1:1:49:49的混合
2 2 2
气体以一定流速通过装有xCuO·yCeO 催化剂的反应器,CO的转化率随温度变化的曲线如图3所示。
2
①Ce基态原子核外电子排布式为[Xe]4f15d16s2,图2所示机理的步骤(i)中,元素Cu、Ce化合价发生的变化
为___。
②当催化氧化温度超过150℃时,催化剂的催化活性下降,其可能原因是___。