文档内容
第十五章 热学
第 01 练 分子动理论 内能
知识目标 知识点
目标一 微观量估算的两种“模型”
目标二 布朗运动与分子热运动
目标三 分子力和内能
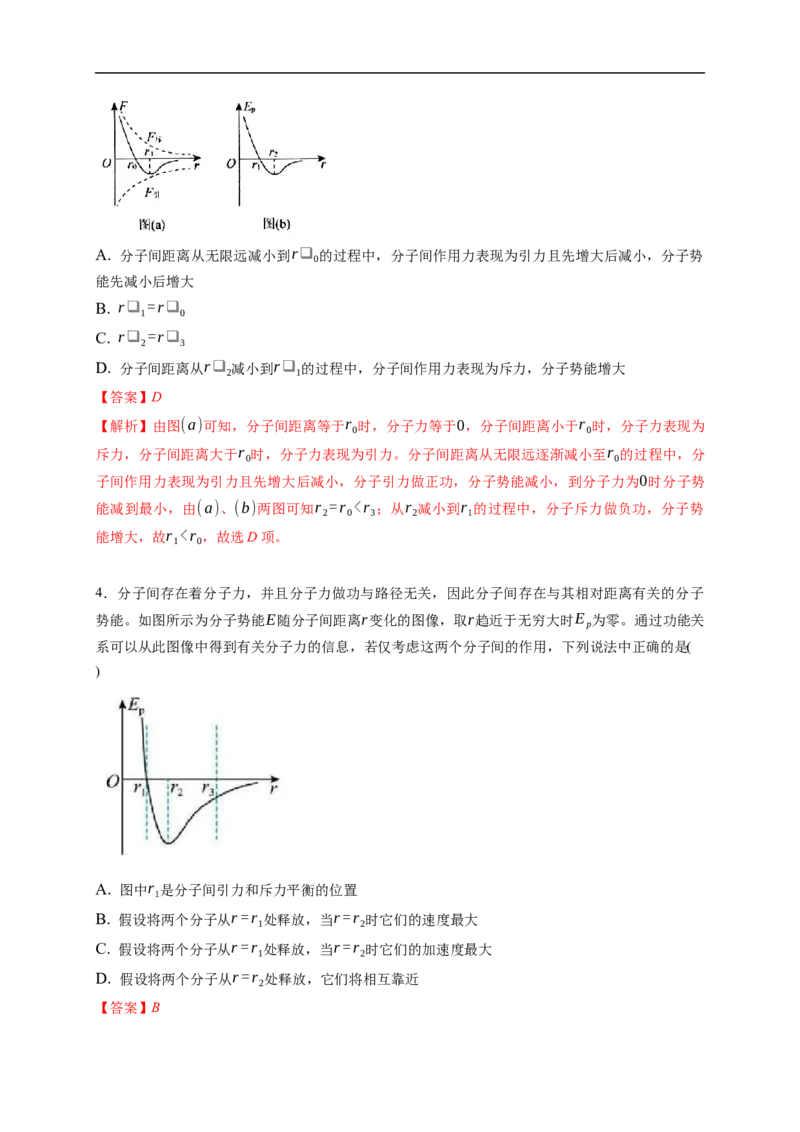
1.以下说法中正确的是( )
A. 当分子间距离增大时,分子间作用力减小,分子势能增大
B. 已知某物质的摩尔质量为M,密度为ρ,阿伏加德罗常数为N ,则该种物质的分子体积为
A
M
V =
0 ρN
A
C. 自然界一切过程能量都是守恒的,符合能量守恒定律的宏观过程都能自然发生
D. 液晶既具有液体的流动性,又具有单晶体的光学各向异性的特点
【答案】D
【解析】
【分析】
分子力做功等于分子势能的减小量;气体分子间隙远大于分子直径;宏观热现象都具有方向性;液
晶既具有液体的流动性,又具有单晶体的光学各向异性的特点。
本题考查了分子力与分子势能的关系、阿伏加德罗常数、热力学定律、液晶等,知识点多,难度小,
关键是记住基础知识。
【解答】
A.当分子间距离增大时,分子间引力和斥力同时减小,但合力不一定减小;如果分子力的合力是引
力,分子力做负功,分子势能增大;如果分子力的合力是斥力,分子力做正功,分子势能减小,故
A错误;
B.已知某物质的摩尔质量为M,密度为ρ,阿伏加德罗常数为N ,则该种物质的每个分子占据空间
A
M
的体积为:V = ;如果是气体,分子间隙远大于分子直径;分子体积未知,故B错误;
0 ρN
A
C.自然界一切过程能量都是守恒的,但根据热力学第二定律,宏观热现象具有方向性,故符合能量
守恒定律的宏观过程不一定能够发生,故C错误;
D.液晶既具有液体的流动性,又具有单晶体的光学各向异性的特点,故D正确。故选D。
2.自主学习活动中,同学们对密闭容器中的氢气性质进行讨论,下列说法中正确的是( )
A. 体积增大时,氢气分子的密集程度保持不变
B. 压强增大是因为氢气分子之间斥力增大
C. 因为氢气分子很小,所以氢气在任何情况下均可看成理想气体
D. 温度变化时,氢气分子速率分布中各速率区间的分子数占总分子数的百分比会变化
【答案】D
N
【解析】解:A、密闭容器中的氢气质量不变,分子个数不变,根据n= 0可知,当体积增大时,
V
单位体积的分子个数变少,分子的密集程度变小,故A错误;
B、气体压强产生的原因是大量气体分子对容器壁的持续的、无规则撞击,故压强增大并不是因为
分子间斥力增大,故B错误;
C、要实际气体的压强不是很高,温度不是很大,才可以近似的当成理想气体来处理,不是在任何
情况下,都可以看成理想气体的,故C错误;
D、温度是气体分子平均动能的标志,随着温度的变化时,气体分子中速率大的分子所占的比例也
随之变化,故D正确。
故选:D。
N
根据n= 0分析分子的密集程;理解压强产生的原因;实际气体在温度不太低,压强不太高的情况
V
下,遵守气体实验定律,可以看作理想气体;温度是气体分子平均动能的标志,大量气体分子的速
率呈现“中间多,两边少”的规律,温度变化时,大量分子的平均速率会变化,即分子速率分布中
各速率区间的分子数占总分子数的百分比会变化。
本题考查了理想气体、温度是分子平均动能的标志、压强的产生等知识,难度不大,多加记忆即可
作答。
3.以下说法正确的是( )
A. 当两个分子间的距离为r (平衡位置)时,分子势能最小
0
B. 布朗运动反应了花粉小颗粒内部分子的无规则运动
V
C. 一滴油酸酒精溶液体积为V,在水面上形成的单分子油膜为S,则油酸分子的直径d=
S
D. 气体的温度升高时,分子的热运动变的剧烈,分子的平均动能增加,撞击器壁时对器壁的作用
力增大,从而气体的压强一定增大
【答案】A
【解析】
【分析】
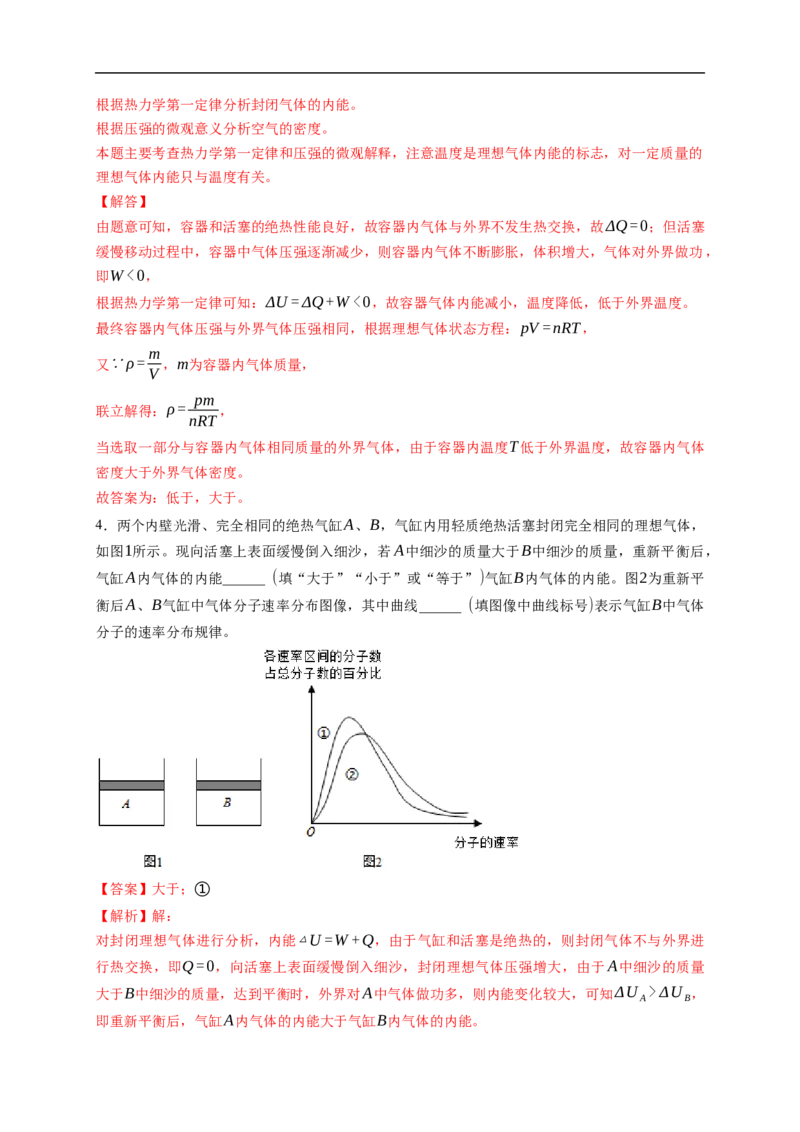
当分子间距r大于平衡距离r 时,分子力表现为引力;rΔU ,
A B
即重新平衡后,气缸A内气体的内能大于气缸B内气体的内能。理想气体内能越大,温度越高,温度是分子平均动能的标志,温度越高,分子的平均动能越大,由
图中曲线可知曲线②中分子速率大的分子数占总分子数百分比较大,即曲线②的温度较高,由前
面分析可知B气缸温度较低,故曲线①表示气缸B中气体分子的速率分布。
故答案为:大于;①。
本题考查热力学第一定律,如果物体跟外界同时发生做功和热传递的过程,那么外界对物体做的功
W加上物体从外界吸收的热量Q等于物体内能的增加。注意正确判断气体做功情况和内能的变化的
方法。根据热力学第一定律判断封闭气体的内能大小,根据内能大小判断封闭气体温度大小,根据
温度大小判断气体平均动能大小。
5.已知地球大气层的厚度h远小于地球半径R,空气平均摩尔质量为M,阿伏伽德罗常数为N ,
A
地面大气压强为p ,重力加速度大小为g.由此可估算得,(1)地球大气层空气分子总数为?(2)空
0
气分子之间的平均距离为?
【答案】
p S
解:(1)设大气层中气体的质量为m,由大气压强产生,mg=p S,即:m= 0
0 g
mN p SN 4πR2p N
分子数n= A = 0 A = 0 A
M Mg Mg
(2)假设每个分子占据一个小立方体,各小立方体紧密排列,则小立方体边长即为空气分子平均间
距,设为a,大气层中气体总体积为V,则
√V
a=3
n
而大气层的厚度h远小于地球半径R,则V =4πR2h,
√ Mgh
所以a=3
p N
0 A
【解析】(1)根据大气压力等于大气层中气体分子的总重力,求出大气层中气体的质量为m,根据
mN
n= A求出分子数.
M
(2)假设每个分子占据一个小立方体,每个小立方体紧密排列,则小立方体边长即为空气分子平均
间距,由几何知识求出空气分子平均间距.
对于气体分子间平均距离的估算,常常建立这样的模型;假设每个分子占据一个小立方体,各小立
方体紧密排列,所有小立方体体积之和等于气体的体积.